3种腔镜手术治疗老年患者输尿管上段嵌顿性结石的疗效及安全性比较
李 遄,皮江川,熊永江,刘家骥,赵 涛
(重庆医科大学附属永川医院泌尿外科,重庆 402160)
结石嵌顿在输尿管内超过8周称之为嵌顿性结石[1],这在老年人中并不少见。针对此类结石,尤其是输尿管上段结石,保守治疗及体外冲击波碎石术(extracorporeal shock wave lithotripsy,ESWL)效果不佳[2]。在临床实践中,考虑到老年患者身体机能弱、耐受性差,传统开放手术后易出现各类并发症,故临床上以各类腔镜手术等微创术式为主,目前多采用输尿管软镜碎石术(flexible ureteroscopic lithotripsy,FURL)、微创经皮肾镜取石术(minimally percutaneous nephrolithotomy,mPCNL)和后腹腔镜输尿管切开取石术(retroperitoneal laparoscopic ureterolithotomy,RLUL)等术式[3]。手术方式的选择主要与结石大小及部位相关,但在考虑患者意愿、医者技术水平、医院等级、地域等因素后,临床对不同手术方法的安全性、碎石效率、术后并发症发生情况以及住院相关费用方面仍存在一定争议。本研究回顾性分析我院2016年1月至2019年8月采用FURL、mPCNL、RLUL治疗的239例老年输尿管上段嵌顿性结石患者的临床资料,分析这3种腔镜术式的临床疗效、安全性及向基层医院普及的可行性。
1 资料与方法
1.1 临床资料
回顾性分析重庆医科大学附属永川医院2016年1月至2019年8月收治的239例老年输尿管上段嵌顿性结石患者的临床资料,按治疗方式的不同分为FURL组101例、mPCNL组62例、RLUL组76例。其中男135例,女104例;年龄65~79岁,平均(70.5±2.6)岁;结石位于左侧113例,右侧126例。患者均有不同程度腰痛、血尿、腰胀等症状,均经泌尿系彩超、腹部X射线片或CT等检查确诊为输尿管上段嵌顿性结石,所有患者均完成手术,无中转开放手术及死亡病例。3组患者年龄、性别、结石位置及结石长径比较差异无统计学意义(P>0.05),见表1。纳入标准:①泌尿系超声或CT证实结石位于输尿管上段;②影像学检查提示结石嵌顿在输尿管同一位置超过8周;③年龄大于65周岁。排除标准:①严重心肺功能障碍,手术耐受差;②存在严重的全身出血性疾病;③同侧合并长径大于4 mm的肾结石,或同侧合并输尿管中下段结石;④严重尿道或输尿管狭窄使腔内手术无法进行;⑤髋关节疾病致截石位摆放困难;⑥患侧曾行腹膜后开放性手术。
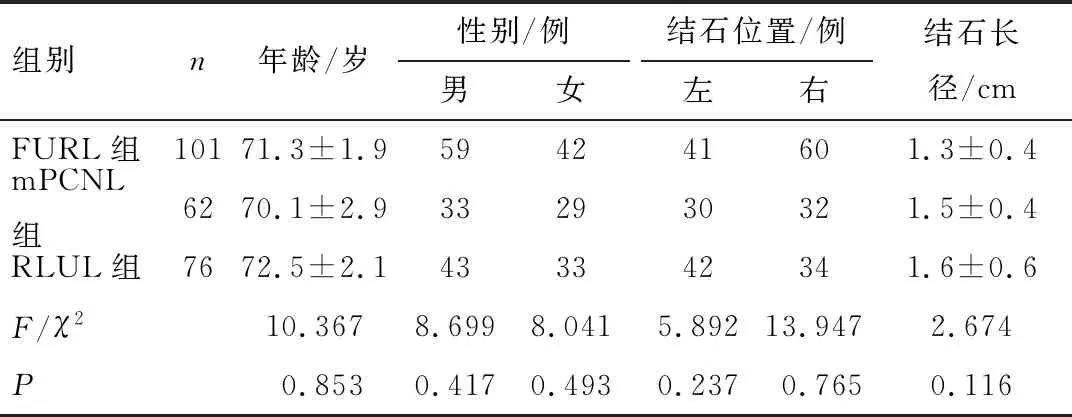
表1 3组患者临床资料比较
1.2 方法
所有患者的主要手术步骤均由同一名主刀医师完成。本研究定义麻醉成功后开始摆体位时为手术开始时间,手术结束患者恢复平卧位为手术结束时间。所有患者术后均随访6个月。
1.2.1 FURL组 全身麻醉成功后取截石位,输尿管硬镜由直视下进镜进入膀胱,置入斑马导丝,在导丝引导下缓慢上行至输尿管上段,留置导丝,退镜。沿导丝留置输尿管软镜镜鞘,输尿管软镜由镜鞘进入达结石近端,或者将结石推入肾盂,置入200 μm钬激光光纤,设置参数:能量0.4~0.6 J,频率20~24 Hz,用钬激光将结石击碎至2 mm以下,使用取石网篮尽量取净残余较大结石。退出输尿管软镜,留置斑马导丝,再退出镜鞘,放置5F双J管3~4周。对输尿管较狭窄的患者,需预留输尿管支架2周,再行软镜碎石术。
1.2.2 RLUL组 全身麻醉成功后留置导尿管。取健侧90°卧位,腰部垫高。消毒铺巾,于腋后线第12肋下作1.5 cm小切口,用大弯血管钳戳入腹膜后间隙,放入自制气囊并充气500 mL,维持1 min后取出气囊。在腋前线肋弓下1 cm处作皮肤切口,置入5 mm Trocar。于腋后线切口及腋中线髂嵴上2 cm处分别置入10 mm Trocar,封闭切口并充入CO2,压力10~12 mmHg。游离腹膜后脂肪,切开肾周筋膜,沿腰大肌向内分离找到输尿管结石,游离输尿管表面脂肪后用小刀切开输尿管,取出结石,吸尽尿液后置入F5双J管,用4-0可吸收缝线间断缝合输尿管切口2~3针。放置腹膜后引流管。双J管于4周后取出。
1.2.3 mPCNL组 全身麻醉成功后取截石位,经膀胱镜或输尿管镜逆行插入5F输尿管导管至患侧肾盂或输尿管上段。留置导尿管后改俯卧位,在超声引导下选择合适肾盏穿刺进入集合系统,置入导丝,用筋膜扩张器将穿刺通道扩张至16F/18F,留置工作鞘。插入肾镜后将工作鞘送入输尿管上段。用钬激光或气压弹道撞杆将结石击碎并冲出。常规留置16F/18F肾造瘘管3~5 d,留置双J管4周。
1.3 观察及随访指标
观察并记录3组患者手术时间、术中出血量、术后卧床时间、术后住院时间;术后心脑血管意外、肺部感染、下肢深静脉血栓形成、术后48 h内发热(腋温超过38 ℃,不含术前已有发热病例)、尿源性脓毒血症、再次出血等并发症发生率;二次手术率(含FURL组预留输尿管支架后再采用钬激光碎石、mPCNL组二期碎石、RLUL组采用输尿管镜调整输尿管支架位置、针对残余结石行ESWL等非同期有创操作);结石清除率,术后1个月复查泌尿系平片或腹部CT,无结石残留或残留结石直径≤3 mm且无临床症状视为清石成功;住院费用。
1.4 统计学方法

2 结果
2.1 手术主要结局指标比较
在手术时间上,FURL组最短,3组差异具有统计学意义(P<0.05),其中RLUL组后50例患者手术时间为(55.2±12.9)min,显著低于前26例患者的(93.5±8.3)min,差异具有统计学意义(P<0.05)。在术中出血量上,mPCNL组最大,FURL组最小,3组差异具有统计学意义(P<0.05)。在术后卧床时间与住院时间上,FURL组最短,RLUL组次之,mPCNL组最长,3组差异具有统计学意义(P<0.05)。3组结石清除率比较,差异无统计学意义(P=0.322)。FURL组二次手术率最高,达36.7%,其中35例因输尿管条件不佳预留输尿管支架2周后再行软镜碎石术,2例因结石残留行ESWL;RLUL组二次手术率最低,为2.6%,1例因结石上移至肾盂,二期行ESWL,另1例因输尿管支架下端未能插入膀胱,后期在输尿管镜下调整支架位置;mPCNL组中5例患者均因感染较重,先行经皮肾穿刺造瘘,二期再行经肾镜碎石术,3组患者二次手术率比较,差异具有统计学意义(P<0.05),见表2。
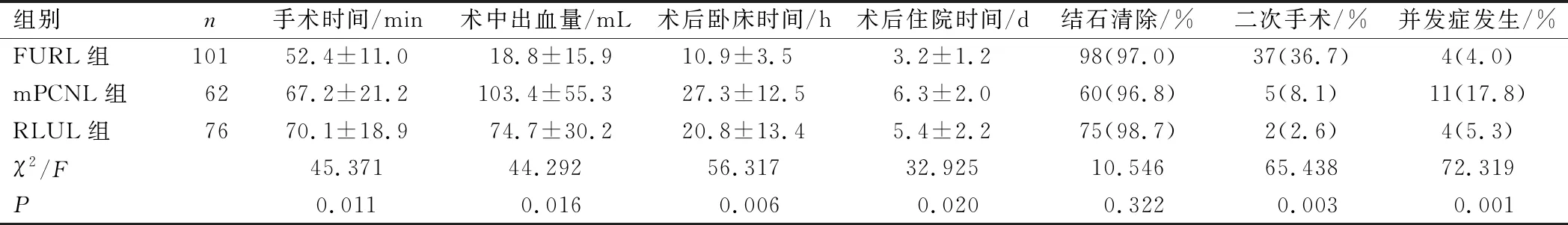
表2 患者临床疗效及并发症发生率比较
2.2 术后并发症发生情况比较
在住院期间,FURL组出现发热4例;mPCNL组出现发热5例,尿源性脓毒血症1例,心绞痛2例,肺部感染1例,下肢深静脉血栓形成1例,行超选择性肾动脉造影栓塞术1例;RLUL组出现发热2例,心绞痛1例,伤口漏尿1例。其中以上发热、尿源性脓毒血症及肺部感染患者均经抗感染治疗后症状好转;心绞痛患者在排除血栓引起的症状后予以卧床休息、服用硝酸甘油对症处理后症状好转;下肢深静脉血栓形成患者经卧床休息及抗凝溶栓后血栓消失;行超选择性肾动脉造影栓塞术治疗的患者术后恢复良好,未再出血;伤口漏尿患者在保留支架2个月后漏尿症状消失。随访期间各组均未发现输尿管狭窄病例。3组患者术后并发症发生率比较,差异具有统计学意义(P=0.001),见表2。
2.3 住院费用比较
住院期间,总费用包括与疾病相关的检查、诊断及治疗相关的费用,也包括部分患者术后并发症治疗产生的额外费用。RLUL组住院费用为(19 716.27±4 378.36)元,FURL组为(30 166.98±5 973.97)元,mPCNL组为(26 381.45±6 604.01)元,部分患者来我院就诊时携带外院相关检查结果,未再行相关检查。3组患者住院费用比较差异有统计学意义(P<0.05)。
3 讨论
腔镜微创手术治疗输尿管上段结石在临床已成为共识[4]。结石大小、位置、患者身体条件、术者技术、患者意愿等因素都对手术方式的选择产生影响[5]。ESWL作为处理输尿管结石的首选已在临床上得到广泛认可,但针对体积大、质硬、长时间嵌顿、存在炎性包裹甚至输尿管狭窄的输尿管上段结石而言,ESWL治疗成功率较低[6];范召应等[7]的研究显示,当输尿管结石直径≥10 mm时,ESWL的结石清除率仅为42%。FURL治疗输尿管中上段及肾内结石疗效明确,但对输尿管条件要求较高,患者若存在输尿管迂曲或狭窄的情况,会导致入镜困难,需一期置管扩张输尿管,二期手术,这无疑加重了患者的经济负担,延长了患者的住院时间,有时甚至无法行一期置管术[8],因此,FURL应用条件较高。mPCNL作为处理输尿管上段结石及肾结石的主要治疗方式,较容易出现出血、肾损伤、感染、手术时间长等情况[9-11]。RLUL作为泌尿外科领域微创手术的代表之一,创伤小、出血少,对输尿管条件要求不高,是上述手术方式的有效补充。针对老年患者输尿管上段嵌顿性结石,考虑到老年患者身体机能欠佳,基础疾病较多,耐受性差,应尽量选择创伤小的术式。因此,针对老年患者输尿管上段嵌顿性结石的治疗,FURL、mPCNL和RLUL三种微创手术方式的有效性、安全性以及向基层医院推广的可行性如何,是本研究探讨的重点。
输尿管软镜由于其独特的设计,能轻松进入输尿管上段、肾盂及肾盏,对术中上移至肾盂、肾盏的残石也可以一并清除,显著提高了清石效率[12]。本研究中FURL组结石清除率较高,达97.0%(98/101),手术时间短,术中出血量小,术后卧床时间及住院时间短,并发症发生率仅4.0%,说明FURL是一种高效、安全的手术方式。李壮志等[13]也认为FURL创伤极小,术后恢复快。但由于部分患者输尿管条件不佳,直接放置输尿管鞘有困难,需先留置支架扩张输尿管,导致FURL组二次手术率最高。加之软镜易损坏、耐用性差、维护成本高,导致治疗费用较高,在一定程度上限制了其在临床上的应用。同时,部分患者因经济承受能力较差、再次住院缺乏子女陪护而不愿接受输尿管软镜钬激光碎石术。此外,FURL术后输尿管狭窄需予以关注[14]。据报道,国外输尿管镜碎石术后输尿管狭窄的发生率为3%~24%[15-16],国内为2.5%[17],关于输尿管结石术后输尿管狭窄的形成,目前认为主要有两种机制:一是机械性损伤—炎症纤维化[18];二是因结石负荷大、激光作用时间长、发射能量较高、水流冲洗不畅,输尿管上皮及肌层组织在较高水温下变性、坏死,导致后期纤维化[16]。因此,术中应尽量选择高频低能模式,避免激光长时间连续激发,保持水流冲洗通畅,必要时术后留置2根D-J管,以降低术后输尿管狭窄的发生率。本研究术后随访6个月,未发现输尿管狭窄病例。
对于L3、甚至L4平面以上的输尿管上段结石,mPCNL也是一种不错的选择[19]。本研究结果显示,mPCNL结石清除率达96.8%(60/62),2例效果不佳患者均为肾盂、肾盏积水严重,结石残粒冲入下盏难以寻觅所致,说明采用mPCNL治疗L3/L4平面以上输尿管上段结石效果较好。但该术式手术时间偏长、术中出血量较大、术后卧床时间及术后住院时间长、并发症发生率相对较高,同时患者可能会出现肝、脾、胸膜、十二指肠、结肠等内脏损伤,肾静脉、腔静脉等大血管损伤,肾大出血致肾丢失,重症感染致死亡等并发症[8]。由于老年患者自身身体条件较差,基础疾病较多,心肺功能欠佳,术后卧床过久更容易导致压疮、下肢深静脉血栓形成、坠积性肺炎等并发症,一旦出现将大大增加治疗难度,增加患者住院时间以及住院费用。严重感染、尿源性脓毒血症是mPCNL术后易出现的严重并发症[20-21],发病率为0.97%~4.70%,病情凶险,病死率高。本研究中,合并有肾积脓的患者除了术前常规使用敏感抗生素外,均采用一期肾造瘘、二期碎石的方案,但仍有尿源性脓毒血症发生,这可能是由手术通道狭小、局部腔内压力高、结石核心细菌易释放、手术时间较长等因素所致,需泌尿外科医生引起高度重视;此外,本研究中mPCNL组术后并发症发生率明显较RLUL组及FURL组高,因此该术式的安全性还有待验证。
RLUL本质上是开放性输尿管切开取石术的一种改良,其适应证为较大较硬、嵌顿时间较长或合并肾盂输尿管疾病的输尿管中上段结石[22]。相较于FURL、mPCNL,RLUL最大的特点是术中能全程保持肾盂内低压状态,并能充分引流肾盂积液尤其是脓性积液,可在保持肾盂、肾盏黏膜完整性的同时减少细菌及内毒素随血液进入机体的可能,从而降低术后发生严重感染甚至尿源性脓毒血症的概率[23-24];且由于RLUL是直视下操作,没有穿刺等操作,因此损伤内脏和大血管的可能性极低[25]。本研究中RLUL组患者术中出血量少,尤其是二次手术率最低,仅有2.6%(2/76),且术后没有严重感染发生,并发症发生率仅为5.3%(4/76)。早期的RLUL组患者手术时间偏长,但随着手术技术的改进,尤其是在能快速找到结石部位,以及迅速放置输尿管支架后手术时间大大缩短,RLUL组后期的50例患者手术时间仅为(55.2±12.9)min。在术后并发症方面,RLUL组为5.3%(4/76),与FURL组相似,但低于mPCNL组。值得一提的是,本研究中有2例同时合并肾功能衰竭、肾积脓的高热患者,充分知悉各种手术风险的情况下选择RLUL,结果手术均取得成功,术后予以积极抗感染治疗后患者体温迅速恢复正常,肾功恢复良好,未出现并发症,表明RLUL是一种安全、有效的手术方式。
本研究存在一定局限性:①为回顾性非随机对照研究,可能存在选择偏移;②纳入的样本量较小,结论存在一定程度的偶然因素;③术后6个月的随访时间偏短,无法判断更长时间的复发率和远期并发症发生率;④为单中心研究,需多中心研究进一步证明结论的准确性。
综上所述,FURL、mPCNL与RLUL治疗老年患者输尿管上段嵌顿性结石都具有良好的有效性及安全性。FURL具有患者痛苦小、手术时间短、术中出血量小、术后恢复快的优势,但二次手术率高,导致总体住院时间延长,总体医疗费用较高;mPCNL手术时间偏长、术中出血量大、术后卧床时间及住院时间较长、并发症更高,但可以同期处理患侧的肾、输尿管结石;而RLUL术中出血量较小、并发症较少、一次性取石成功率高,但需要一定手术技巧,有后腹腔手术史者,由于肾、输尿管周围粘连严重,不宜选择该术式,一定程度上限制了RLUL的应用。但考虑到老年患者自身机能减退、易并发多种慢性疾病,RLUL是一种不错的选择。医生在选择手术方式时应综合评估患者的具体情况,采用合适的手术方式。
对于多数患者而言,住院费用及手术安全性为首要考虑条件。基层医院的患者经济条件相对拮据,尤其在广大县级医院及以下的医疗单位中,这种现象更为突出。RLUL在3种手术方式中优势较为突出,安全性、有效性及经济性较其余2种方式更理想,基本能够在患者初次住院期间解除患者病痛,且费用相对较低,降低了患者经济及时间成本。因此,RLUL作为一种处理老年患者输尿管上段嵌顿性结石的治疗方式向基层医院推广具有较高可行性,可减轻患者经济负担,满足群众更多样化的医疗需求。

