泌尿外科达芬奇机器人手术患者术中低体温风险预测模型的构建及应用研究
杨霞,李国宏,崔颖
(1.东南大学附属中大医院 手术室,江苏 南京 210009;2.东南大学医学院 护理系,江苏 南京 210009)
术中低体温的定义为麻醉手术期间人体核心温度低于36℃,如低体温持续,可能会增加围术期各项不良事件的发生率,如呼吸抑制、凝血异常、麻醉苏醒延迟、心肌缺血、术后寒战等,影响患者预后[1-2]。通过文献综述[3-5]发现目前国内大部分研究聚焦于术中的体温管理和术前的预保温,而规范化的术前低体温风险评估筛查研究仍较少。此外,随着达芬奇机器人在临床的推广,其已逐步成为泌尿外科的常用术式[6]。相较于传统术式,尽管机器人手术创伤小,但更长时间的手术、麻醉药物的持续使用以及能量供应的缺乏导致低体温发生率的风险更高。我院前期研究[7]结果也提示,常规体温保护措施下机器人手术低体温的发生率高达32.19%(66/205)。因此,针对机器人手术的泌尿外科患者,建立合适的低体温风险预测模型,既可以稳健的预测低体温的高风险人群从而采取专业的保温措施,也可以避免对风险较低的患者进行过度保温,节约医疗资源,对提高手术室护理质量具有重要意义。现将研究结果报告如下。
1 对象与方法
1.1 研究对象 便利抽样选取我院自2019年1月至2020年3月泌尿外科接受达芬奇机器人手术患者中发生低体温事件的72例患者列为研究组,纳入标准:年龄>18岁;全身麻醉。排除标准:精神疾病;术前有体温调节障碍相关疾病;孕期患者;大面积皮肤烧伤等皮肤保温屏障受损;术中变更麻醉方式。脱落标准:术中突发大出血、休克、呼吸心跳骤停。按照病例组和对照组样本量1∶3的配比选取此时间段达芬奇机器人术中未发生低体温的患者216例患者作为对照组。
1.2 研究方法 采用病例对照研究,由手术室护理研究人员,采用统一编制的调查问卷开展调查,内容包括性别、年龄、体质量指数(body mass index,BMI)、麻醉时间、手术时间、气腹时间、术中出血、基础体温、手术室室温、主动保温持续时间、术中输液量、CO2气腹流量。上述12个潜在危险预测因子的筛选基于既往文献学习结果、专家经验及我院低体温前期研究结果,并进行了相关资料收集。
1.3 指标定义 核心变量为术中从麻醉开始至手术结束过程中患者的鼓膜温度,两组患者统一使用同一品牌、同一型号的红外线耳温仪进行温度监测,不同患者注意更换探测帽,记录麻醉开始、手术开始、术中每隔15 min直至手术结束时的数值,每个时间点的体温连续复测记录三次并计算平均值作为最终结果,手术开始后任一记录时段出现体温<36℃则纳为低体温组。
2 结果
2.1 病例组和对照组基线特征及危险因素比较 本研究共纳入288例患者,年龄28~69岁,平均(54.7±6.35)岁,其中72例患者(25%)出现术中低体温纳入低体温组,216例患者(75%)纳入非低体温组,一般资料见表1。组间标记后,共8个变量(年龄、麻醉时间、手术时间、术中输液、基础体温、BMI、室温、主动保温持续时间)具有统计学意义,P<0.05(见表1)。
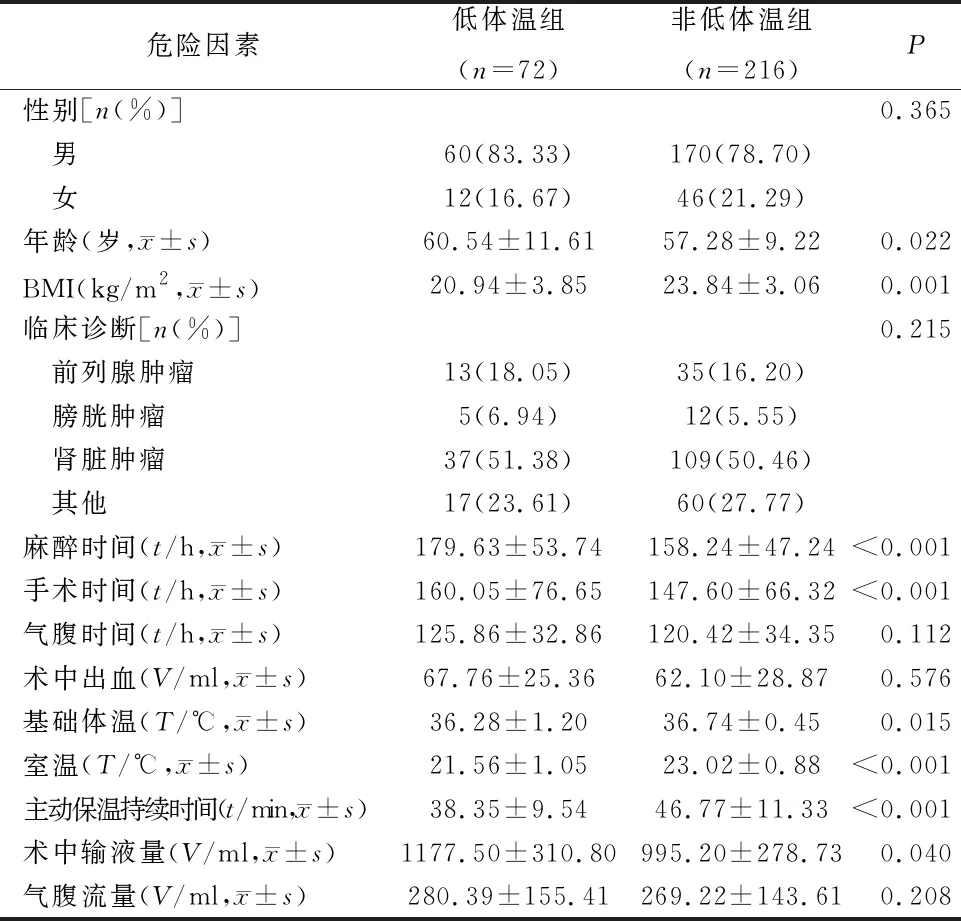
表1 两组患者一般资料和手术相关数据的比较(N=288)
2.2 达芬奇机器人手术患者术中低体温风险预测模型的建立和分析 将单因素分析有统计学意义的8个变量纳入多因素Logistic回归分析,结果显示基础体温、BMI、室温、麻醉时间、主动保温持续时间发生相关。Logit(P)=22.56-1.085×基础体温-0.669×BMI-1.182×室温+0.486×麻醉时间-0.632×主动保温持续时间(见表2)。对预测模型进行Hosmer-Lemeshow检验拟合效果,P=0.475。采用ROC曲线检验患者模型预测,以约登指数最大值为预测模型的最佳临界值,曲线下面积为0.837,灵敏度为0.766,特异度为0.829(见图1)。
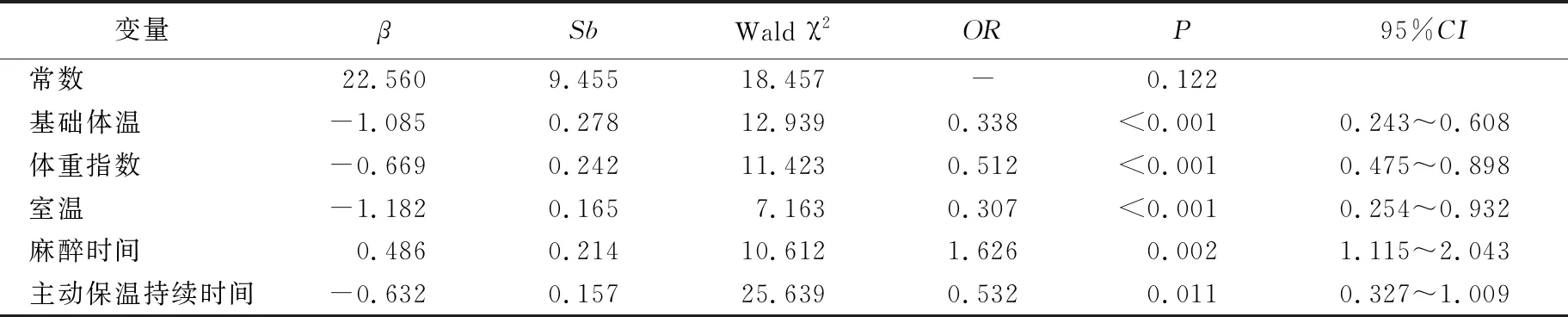
表2 术中低体温多因素Logistic回归分析(n=288)

图1 术中低体温预测的ROC曲线
2.3 达芬奇机器人手术患者术中低体温风险预测模型的临床应用效果分析 针对2020年5-12月符合纳排标准的150例患者进行预测模型应用分析,年龄30~71岁,平均(56.1±5.82)岁。实际低体温发生数为36例,模型预测低体温发生例数为29例,灵敏度为80.6%;实际未发生低体温预测数为114例,模型预测为93例,特异度为81.6%,模型总正确率为(29+93)/150=81.3%。
3 讨论
3.1 达芬奇机器人手术患者术中低体温风险预测模型建立的意义 目前为止,术中患者低体温的现象仍较为常见。患者术中核心温度过低,易导致各器官组织的代谢下降,影响血氧、脉搏、心率等生命指标[8];同时,低体温也会引起患者术中寒颤、降低舒适度,增加术中出血量和输血量,延迟麻醉苏醒和复苏时间,增加伤口感染率,间接地影响术后康复,延长住院时间,增加患者经济负担。因此,围术期合理的体温管理显得尤为重要[9]。达芬奇手术机器人由于其操作精确度高、创伤小、视野宽、灵活度高的多项技术优势,近几年已被广泛应用于泌尿外科的手术中[6],随之而来的体温管控和低体温预防的问题也亟待探讨。随着越来越多的新技术在护理工作中的应用,患者对护理质量的要求也在逐步提高,体现在治疗过程中的每个实施环节,因此护理工作的难度风险也不断增高。国内既往研究[4,10]的重点大多聚焦于术中的体温管控和监测,而缺乏术前的风险评估和预测。而低体温风险预测模型的建立的目的就是将护理人员的干预工作提前,在不良事件发生前即能高效的明确筛查出低体温的高危患者,有侧重点多方面的进行个体化的预保温;相反,针对风险程度较低、手术时间较短的患者,减少过度保温干预的措施,使护理保温干预工作更加精准化、目的导向性更明确,也有利于促进医疗资源的有效利用、减轻护理人员的工作量及优化护士满意度[11],提升优质护理。此外,低体温的规范化评估管理也可以促进护理质量的不断改进,并帮助低能级的护理人员提高术中体温精准化管理的观念意识。
3.2 达芬奇机器人手术患者术中低体温的影响因素 本研究结果显示,BMI、基础体温、室温、主动保温持续时间和麻醉时间与低体温的发生有显著相关性,其中麻醉时间为独立危险因素。在这5个显著因素的基础上,分析建立了达芬奇机器人手术患者术中低体温风险预测模型。首先体重指数一直被认为是外科术中患者发生低体温的主要危险因素,主要原因包括两点[12-13]:(1)高BMI患者的体脂率高、肌肉脂肪组织含量丰富,一方面骨骼肌作为机体产能的动力之一,在体温开始下降时增加产热,另一方面皮下脂肪组织在静止时,构成机体隔离层,具有保暖作用;(2)高BMI患者体内瘦素含量通常也较高,可增加人体代谢率、刺激交感神经产生较多热量维持核心温度。其次,基线体温较低的患者也易出现低体温,当术前体温提高时,核心部位与外周组织皮肤的温差缩小,核心热量再分布减少,有利于预防低体温。同样,手术室室温的提高也可以降低患者体表与环境之间的对流辐射,并可提高患者术中热舒适度,减缓其术中体温降低的趋势[14-15]。而主动保温持续时间,已有研究[16]指出术前即采用加温设备从体外提供热源,可有效防止术前体温过低。麻醉时间作为独立危险因素,较长的麻醉时间可以抑制强制性的血管收缩,引起血管扩张,使核心热量向外周移动,增加低体温发生率[13,17]。
3.3 达芬奇机器人手术患者术中低体温风险预测模型的应用分析 本研究采用Hosmer-Lemeshow检验模型的拟合效果,结果显示拟合优度较好。ROC曲线下面积为0.837,提示预测效果可接受。Yi等[2]对3132例全麻患者术中低体温情况进行分析,制定预测方程,ROC曲线下面积为0.759,普鹰等[11]分析264例腹腔镜手术患者情况建立术中低体温预测模型,ROC曲线下面积为0.791,均与本研究相仿。此外,本研究还选取了150例达芬奇机器人手术的患者进行模型的应用和检验,总体正确率达到了81.3%,表明此预测模型对于达芬奇机器人手术是否发生低体温的鉴别能力良好。但本研究也存在一定的局限性,如样本量相对较少,纳入患者均来自泌尿外科,后期研究可以再加入心胸外科、妇科、普外科患者进行验证。

