一种含碘涂层PVP材质导尿管的抗菌性能及生物相容性研究
伍锡栋 张俊明 李景莲 张芸 江西省医疗器械检测中心检测四室 (江西 南昌 330000)
内容提要: 目的:对含碘涂层PVP材质导尿管的样品前处理方法进行考察比较,建立其抗菌性能检测方法,为此类产品抗菌性能检测标准制定提供试验依据。方法:对GB15979-2002、GB14233.2-2015、QB/T2591-2003等标准进行重现,考察其样品与菌液接触温度的变化及与接触方式的改变对其抗菌性能的影响;采用急性全身毒性试验等评价其相关的生物相容性。结果:在静态前处理培养抗菌结果中显示25˚C的静态前处理抗菌效果更好,抗菌率为69%;在振荡法前处理中抗菌率与温度(25˚C、37˚C)和振动频率(100r/min、200r/min、300r/min)均呈正相关关系,结果显示37˚C且300r/min振荡前处理抗菌率最佳为98%;含碘涂层导尿管生理盐水浸提液对小鼠的体重增长有影响,在96h观察期内,与对照组比较,小鼠体重增长均有统计学意义(P<0.05);在24h时含碘涂层样品组小鼠体重增长率为-6.0%,与对照组比较具有显著性差异(P<0.01),且48h、72h和96h小鼠体重均缓慢增长,其增长率与对照组比较,均有统计学意义(P<0.05)。结论:该类产品与菌液接触的方式及温度均影响其抗菌性能,在检测时应考虑其实际使用的环境,模拟实际使用环境更能体现其抗菌效果;急性全身毒性试验中小鼠体重增长受到影响,这可能是由于其涂层成分浸出所引起的,提示涂层类产品在工艺上应该考虑改进涂层黏附的时效性及稳定性;该试验研究可为涂层类产品的抗菌性能标准制定及临床安全性使用提供试验依据。
导尿管相关性尿路感染(Catheter-Associated Urinary Tractinfection,CAUTI)主要是指患者留置导尿管后或者拔除导尿管48h内发生的各种病原微生物在尿路中异常繁殖所致的尿路感染性疾[1,2]。有研究报道显示,导尿管相关性尿路感染的前三致病菌为大肠埃希菌、铜绿假单胞菌和金黄色葡萄球菌[3,4]。导尿管表面形成的细菌生物膜是菌尿症和的基础,在所有的感染中生物膜机制占65%~80%[5,6]。因此,防治的关键在于阻止细菌生物膜的形成,而其中一个重要的方法就是改变导尿管的表面理化性质。
含碘涂层目前市场上还没有,是一种新型的抗菌超滑涂层导尿管,采用亲水性高分子聚合物聚乙烯吡咯烷酮(PVP)与聚维酮碘充分混合后,经过恒温技术,使碘涂层均匀的附着在导尿管上,插入尿道后,聚维酮碘会缓慢溶解释放,发挥持久抗菌效果,减少抗生素的使用,可以预防诸如大肠杆菌、绿脓杆菌等病原微生物的感染,降低临床感染率。为了较全面地检验该类导尿管的抗菌性能及生物相容性,本文对样品前处理进行优化,通过不同温度及振荡法制取供试液并对其抗菌性能进行研究评价,急性全身毒性试验等生物相容性进行研究评价,为企业的产品质量控制提供试验依据,为临床的合理使用提供参考。
1.材料与方法
1.1 一般材料
含碘涂层PVP导尿管(来源于江西益康医疗器械股份有限公司,批号20191005),金黄色葡萄球菌(CMCC26003),营养肉汤培养基,胰酪大豆琼脂培养基,胰酪大豆胨液体培养基,棉籽油,生理盐水等;恒温培养摇床,生物安全柜,生物显微镜,离心机,电子秤,恒温恒湿培养箱等。
ICR小鼠(18~22g,来源于湖南斯莱克景达实验动物有限公司,合格证号No.1107272011002858),健康家兔(>2.0kg,来源于湖南斯莱克景达实验动物有限公司,合格证号No.0001410),饲养条件为:温度18~26˚C,相对湿度40%~70%。
1.2 方法
1.2.1 抗菌性能试验
参照ISO国际标准、中华人民共和国轻工行业标准和及日本抗菌制品技术协会(Society of Industrial for Antimicrobia Articles,SIAA)等相关抗菌标准要求,在ISO846、ASTMG21-96、QB/T2591-2003及GB15979-2002基础上进行复现。用培养法(将金黄色葡萄球菌均匀涂布于大小为2.0cm×3.0cm试验上,制成菌浓度为1×104CFU/片~9×104CFU/片的试样,用灭菌镊子夹起已消毒的聚乙烯覆盖薄膜分别覆盖在样品,保证样品覆盖膜部位所铺的菌浓度不变,于带塞子的锥形瓶中25˚C、37˚C/相对湿度>90%条件下培养20min后,用生理盐水洗脱样品制取供试液,分别取0.5mL供试液于两个无菌平皿中并倾倒适量琼脂培养基,于37˚C培养箱中培养48h,计数并计算抑菌率)和振荡法(将大小为2.0cm×3.0cm的样品浸于浓度为1×104~9×104CFU/mL金黄色葡萄球菌菌液中,25˚C、37˚C/相对湿度>90%条件下不断振荡培养20min(考察转速100r/min、200r/min、300r/min的影响),分别取0.5mL供试液于两个无菌平皿中并倾倒适量琼脂培养基,于37˚C培养箱中培养48h,并平板计数计算抗菌率,试验重复3次,实验结果取平均值。抗菌率=(对照样品菌落数-被试样品菌落数)/对照样品菌落数×100%,抗菌率≥90%表示有抗菌作用。
1.2.2 急性全身毒性试验
取供试品按0.2g/mL比例浸提,浸提介质0.9%氯化钠和棉籽油。自尾静脉分别注入氯化钠注射液浸提液和氯化钠注射液,腹腔注射棉籽油浸提液和棉籽油对照液,给予容积50mL/kg,注射速度不超过0.1mL/s。给予供试液后,观察小白鼠即时反应,并于4h、24h、48h、72h和96h记录观察动物出现的毒性症状,包括开始时间、程度和持续时间。
2.结果
2.1 抗菌试验
在静态前处理培养抗菌结果中显示25˚C的静态前处理抗菌效果更好,抗菌率为69%;在振荡前处理法中抗菌率与温度和振动频率均呈正相关关系,温度越大,振动频率越大,抗菌率越好,越能体现产品的抗菌性能。结果见图1、图2、图3和表1。
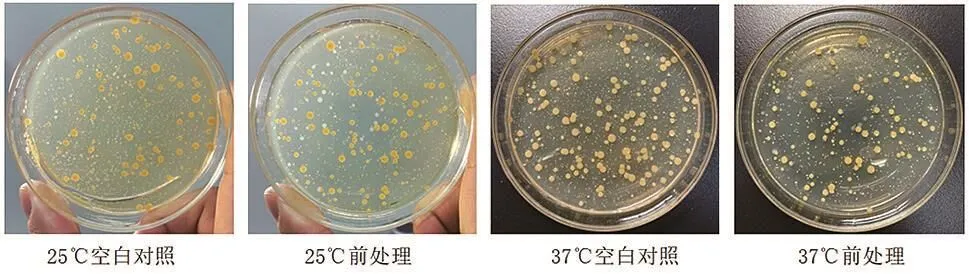
图1. 25˚C、37˚C静态前处理培养法的抗菌结果

图2. 25˚C 100r/min、200r/min、300r/min振荡法前处理培养的抗菌结果

图3. 37˚C 100r/min、200r/min、300r/min振荡法前处理培养的抗菌结果

表1. 不同前处理方法及温度改变对样品的抗菌率的影响
2.2 急性全身毒性试验
与对照组比较,小鼠体重增长均有统计学意义(P<0.05);在24h时含碘涂层样品组小鼠体重增长率为-6.0%,与对照组比较具有显著性差异(P<0.01),其余组小鼠体重增长率分别为5.7%、11.1%和17.6%,与对照组比较,均有统计学意义(P<0.05)。结果见表2、表3。
表2. 急性毒性动物体重实验结果(±s,g)
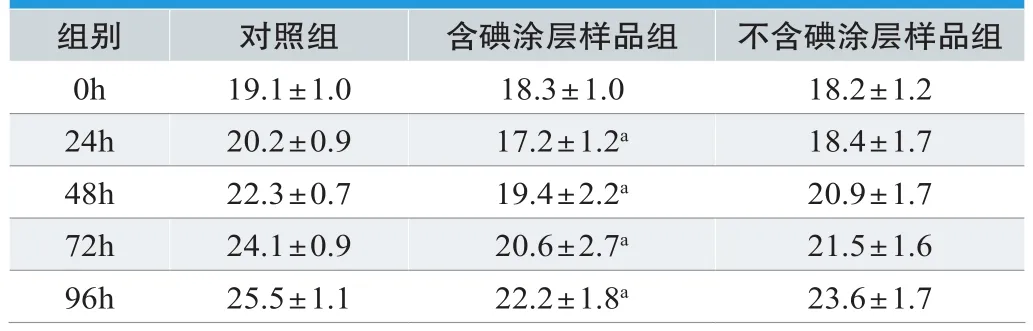
表2. 急性毒性动物体重实验结果(±s,g)
注:与对照组比较,aP<0.05
组别 对照组 含碘涂层样品组 不含碘涂层样品组0h 19.1±1.0 18.3±1.0 18.2±1.2 24h 20.2±0.9 17.2±1.2a 18.4±1.7 48h 22.3±0.7 19.4±2.2a 20.9±1.7 72h 24.1±0.9 20.6±2.7a 21.5±1.6 96h 25.5±1.1 22.2±1.8a 23.6±1.7

表3. 急性毒性动物体重增长率实验结果
3.讨论
据报道,约25%的住院患者在住院期间曾留置导尿,留置导尿是一种尿路侵入性操作,可能损伤尿路黏膜上皮,导致尿路感染的发生,且易反复发作,导管相关性尿路感染被认为是最常见的留置导尿并发症[7]。材料产品快速发展,该类产品能有效避免和减少细菌传播、交叉感染,对改善和保护人们健康生活质量具有重要意义,由于该类导尿管直接与人类接触,对其抗菌效果及生物安全性研究显得十分重要。
研究发现在静态前处理培养抗菌结果中显示,25˚C的静态前处理抗菌效果更好,抗菌率为69%,此结果提示,样品静止状态与菌接触,其抗菌效果与相对湿度有关,由于温度较低,较易使湿度保持稳定状态。在振荡前处理法中抗菌率与温度和振动频率均呈正相关关系,37˚C且300r/min振荡前处理抗菌率最佳为98%,结果提示,抗菌性能检测在样品前处理上对温度和一定频率的振动具有一定要求,使样品与菌液接触保持在一定的温度、湿度以及一定频率的振动对产品的抗菌性能检测具有很重要的影响,另一方面该方法也比较接近产品实际的使用接触环境情况,即让其充分暴露在一定浓度菌液,且给予一定频率的振动更有利于产品动态的表现抗菌性。含碘涂层导尿管生理盐水浸提液对小鼠体重增长有一定影响,可能与其涂层成分有关,加之经静脉给药敏感性高,故急性全身毒性试验反应灵敏,该结果提示,在进行该类涂层产品工艺时应考虑其涂层黏附的时效性及稳定性。该试验结果将为涂层类产品的涂层工艺改进、抗菌性能质量标准及行业检验检测标准的制定提供试验参考,同时也提示在临床使用上应注意的问题,为临床安全性使用提供试验依据。

