大剂量地塞米松联合重组人血小板生成素治疗原发免疫性血小板减少症41例
纪国超
濮阳市人民医院,河南 濮阳 457000
原发免疫性血小板减少症(primary immunologic thrombocytopenic purpura,ITP)多表现为皮肤黏膜出血,部分出血倾向严重者,可造成内脏、颅内出血,甚至导致死亡,严重威胁患者生命健康[1-2]。糖皮质激素为临床治疗ITP一线药物,起效迅速,但持续反应率低,且长期用药易发生不良反应。重组人血小板生成素(rhTPO)为临床治疗ITP二线药物,可有效提升血小板计数水平,常与一线药物联合治疗以提升临床疗效[3]。本研究应用大剂量地塞米松+rhTPO联合治疗ITP患者,观察其临床疗效,评估其对血小板的作用性、安全性,报告如下。
1 资料与方法
1.1 一般资料
选取濮阳市人民医院ITP患者82例(2019年6月至2020年9月),根据治疗方案不同分为对照组(41例)和观察组(41例)。对照组男20例,女21例,年龄(46.23±3.68)岁,年龄范围38~70岁;病程(4.02±0.56)个月,病程范围3~9个月;观察组男22例,女19例,年龄(47.51±3.05)岁,年龄范围40~72岁;病程(3.81±0.67)个月,病程范围2~8个月;两组基线资料差异无统计学意义(P>0.05),本研究符合医学伦理原则要求。
1.2 纳入及排除标准
(1)纳入标准:均确诊为ITP患者;血小板计数(PLT)符合入选标准(<30×109/L);患者或其近亲属知情同意本研究。(2)排除标准:合并肝、肾功能疾病者;合并严重糖尿病者;合并再生障碍性贫血者;合并骨髓异常增生综合征者;哺乳期或妊娠期妇女;对此类药物过敏者。
1.3 方法
对照组采用地塞米松磷酸钠注射液(国药集团荣生制药有限公司,国药准字H41020036,规格:1 mL∶5 mg)治疗,静脉滴注,40 mg/次,1次/d。
观察组在对照组基础上采用重组人血小板生成素注射液(沈阳三生制药有限责任公司,国药准字S20050048,规格:15 000 U/mL)皮下注射,1 mL/d,1次/d。两组均持续用药14 d。
1.4 疗效评估标准
治疗后临床症状基本消失,PLT恢复正常(≥100×109/L)为显效;治疗后临床症状部分缓解,PLT显著提高(>30×109/L)为有效;未达上述标准为无效。总有效率=显效率+有效率。
1.5 观察指标
(1)比较两组临床疗效。(2)比较两组治疗前后PLT水平。(3)比较两组治疗前后白细胞介素-10(IL-10)、细胞毒T淋巴细胞相关抗原4(CTLA-4)、转化生长因子-B1(TGF-β1)。(4)比较两组治疗前后T淋巴细胞亚群(CD3+、CD4+、CD8+)。(5)比较两组不良反应。
1.6 统计学方法
2 结果
2.1 临床疗效对比
两组治疗后临床疗效比较,观察组92.68%高于对照组65.85%(P<0.05),见表1。

表1 两组临床疗效比较[例(%)]
2.2 PLT对比
治疗前两组PLT对比差异无统计学意义(P>0.05),治疗后观察组高于对照组(P<0.05),见表2。
表2 两组PLT计数比较(×109/L,)
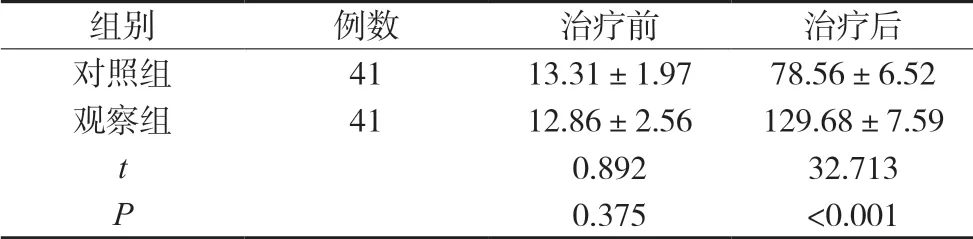
表2 两组PLT计数比较(×109/L,)
组别 例数 治疗前 治疗后对照组 41 13.31±1.97 78.56±6.52观察组 41 12.86±2.56 129.68±7.59 t 0.892 32.713 P 0.375 <0.001
2.3 IL-10、CTLA-4、TGF-β1对比
治疗前两组IL-10、CTLA-4、TGF-β1对比差异无统计学意义(P>0.05),治疗后观察组IL-10、CTLA-4、TGF-β1均高于对照组(P<0.05),见表3。
表3 两组IL-10、CTLA-4、TGF-β1比较(ng/L,)
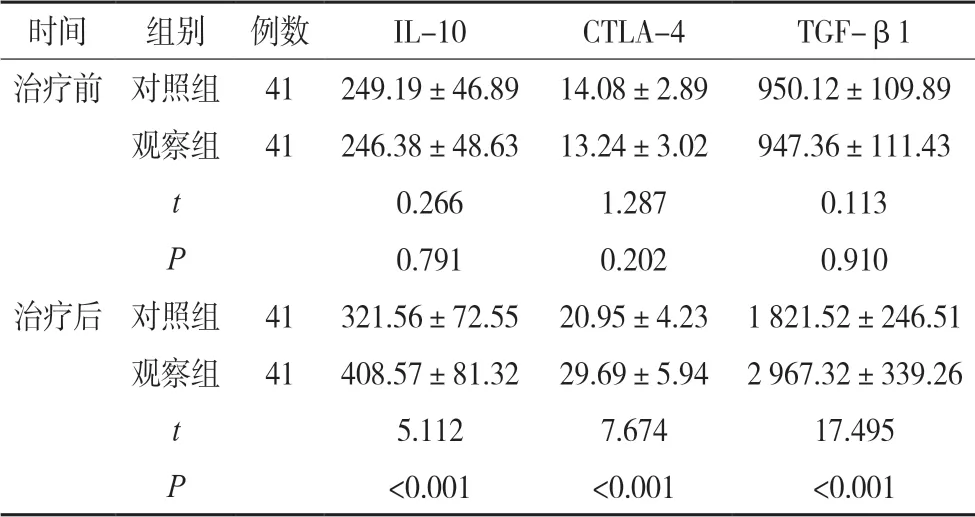
表3 两组IL-10、CTLA-4、TGF-β1比较(ng/L,)
时间 组别 例数 IL-10 CTLA-4 TGF-β1治疗前 对照组 41 249.19±46.89 14.08±2.89 950.12±109.89观察组 41 246.38±48.63 13.24±3.02 947.36±111.43 t 0.266 1.287 0.113 P 0.791 0.202 0.910治疗后 对照组 41 321.56±72.55 20.95±4.23 1 821.52±246.51观察组 41 408.57±81.32 29.69±5.94 2 967.32±339.26 t 5.112 7.674 17.495 P<0.001 <0.001 <0.001
2.4 CD3+、CD4+、CD8+对比
治疗前,两组CD3+、CD4+、CD8+对比差异无统计学意义(P>0.05),治疗后观察组CD3+、CD4+均高于对照组,CD8+低于对照组(P<0.05),见表4。
表4 两组CD3+、CD4+、CD8+比较(%,)
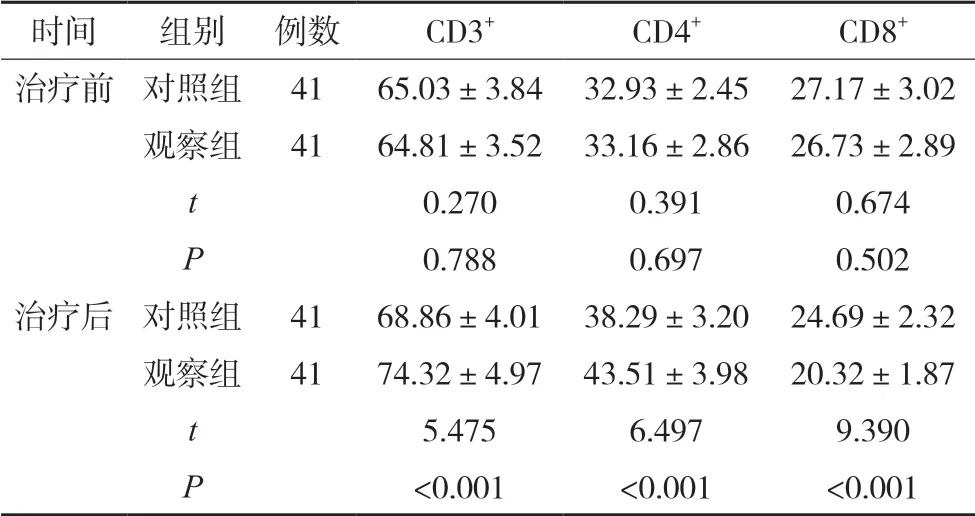
表4 两组CD3+、CD4+、CD8+比较(%,)
时间 组别 例数 CD3+ CD4+ CD8+治疗前 对照组 41 65.03±3.84 32.93±2.45 27.17±3.02观察组 41 64.81±3.52 33.16±2.86 26.73±2.89 t 0.270 0.391 0.674 P 0.788 0.697 0.502治疗后 对照组 41 68.86±4.01 38.29±3.20 24.69±2.32观察组 41 74.32±4.97 43.51±3.98 20.32±1.87 t 5.475 6.497 9.390 P<0.001 <0.001 <0.001
2.5 两组不良反应对比
治疗后两组不良反应率对比差异无统计学意义(P>0.05),见表5。

表5 两组不良反应比较[例(%)]
3 讨论
ITP具有发病机制复杂、难治愈等特点,多由免疫功能异常引起,具有一定致命性出血发生率,且尚无根治方法,因此,临床一直在探求理想有效的药物治疗方案[4]。
地塞米松属肾上腺皮质激素类药,可通过调节机体免疫系统,稳定T淋巴细胞亚群,减少血小板膜蛋白抗体繁殖,从而恢复细胞功能,短时间内迅速上调患者PLT水平;还可通过抑制单核血液细胞对血小板产生破坏,达到增加毛细血管通透性、减轻出血症状等作用。但长期使用易引发骨质疏松、胃黏膜病变等不良反应[5]。
血小板表面含有大量免疫细胞,主要包括CD3+、CD4+、CD8+,其中CD4+细胞数量减少可致B淋巴细胞繁殖,产生大量血小板抗体,导致体内血小板破损,而血小板生成素(TPO)可通过激活Janus激酶/信号转导与转录激活子(JAK/STAT)信号转导通路,调节血小板生成水平[6-7]。rhTPO是一种利用基因重组技术经提纯制作而成的全长糖基化物,为一种基因工程蛋白药物。研究发现,rhTPO与TPO相似度极高,具有332个氨基酸,可通过调节血小板各阶段生成过程,促进骨髓巨核细胞分裂,从而有效提升外周血PLT水平,增加骨髓中巨核系祖细胞,对造血干细胞的产生有积极作用[8-9]。IL-10、CTLA-4、TGF-β1为机体负性免疫调节细胞因子,由T淋巴细胞释放、合成,其水平降低时提示反应性细胞过度活化,而水平升高时则提示机体存在免疫耐受现象。本研究结果发现,治疗后观察组临床疗效高于对照组,且PLT、IL-10、CTLA-4、TGF-β1均高于对照组,CD3+、CD4+、CD8+均优于对照组(P<0.05),两组不良反应对比差异无统计学意义(P>0.05),提示联合用药可有效改善患者临床症状,增加外周血血小板计数,调节免疫细胞。
综上可知,大剂量地塞米松联合rhTPO治疗ITP患者临床疗效确切,可有效提升患者血小板计数,调节机体免疫细胞表达水平,且安全性良好。

