氯霉素分子印迹电化学传感器的制备与应用
黄象金,利健文,韦寿莲,张华生
(1.肇庆市食品检验所,广东 肇庆 526060;2.广东食品药品职业学院,广东 广州 510520;3.肇庆学院 环境与化学工程学院,广东 肇庆526061)
氯霉素(CAP)是一种广谱抗生素,被广泛应用于家禽家畜及水产品的细菌传染性疾病的预防和治疗[1]。然而过量使用会导致动物源性食品及水中残留CAP,对人体健康造成威胁[2]。许多国家已明令禁止在食用动物中使用CAP。但因CAP的抗菌效果好、价格低,在养殖业中仍存在非法使用现象,导致动物源性食品中CAP残留的检出屡见不鲜。因此对CAP残留的灵敏、准确检测尤为必要。
目前检测CAP的方法主要有高效液相色谱法[3]、气相色谱法[4]、液相色谱-质谱联用技术[5-6]、酶联免疫吸附法[7]和毛细管电泳法[8]等。上述方法普遍存在仪器昂贵,样品前处理耗时,且难以实现快速检测等局限性。电化学方法,特别是与分子印迹技术相结合后,具有较高的灵敏度和良好的选择性,是一种快速、简单、有效的分析方法。近年来,已有关于分子印迹电化学传感器用于CAP检测的研究报道,如贾真真等[9]通过电聚合法在单壁碳纳米管(SWCNTs)-纳米铜复合物修饰电极上合成CAP印迹膜,构建了对水溶液检测的CAP传感器,该方法检出限为4.8 nmol/L。Munawar等[10]开发了基于分子印迹聚合物(MIP)包覆铜纳米粒子/碳纳米管(CNTs)复合材料的电化学传感器,应用于牛奶中CAP残留的测定,检出限为10µmol/L。Borowiec等[11]构建了基于金纳米粒子掺杂石墨烯修饰玻碳电极的分子印迹传感器,对CAP的检出限为0.59 µmol/L。但有些样品中CAP含量很低,而上述电化学传感器的检出限均较高,难以满足测定要求。虽然已有CAP印迹聚合物应用报道,但该MIP主要采用单一功能单体制备,通常存在吸附容量低、选择性不高及动力学平衡慢等不足。已有研究表明双功能单体制备的印迹膜因采用了两种功能单体的组合,可增加聚合物与模板分子之间的作用力种类和识别位点数量,有效提高了MIP对模板分子的亲和力和选择性[12]。目前关于双功能单体的CAP分子印迹电化学传感器研究鲜有报道。尽管MIP在选择性方面具有优势,但其在电化学传感过程中灵敏度较低,因此各种纳米材料如贵金属[13]、石墨烯[14]、碳纳米管[9-10]及氧化物[15]等常用于修饰电极以增大电极的表面积、电子传递速率和电催化性能,从而提高电化学传感器的灵敏度。
本研究以CAP为模板分子,间氨基苯酚(MAP)和β-环糊精(β-CD)为功能单体,在纳米氧化铝(Al2O3)和羟基化多壁碳纳米管(MWCNTs)修饰金电极表面通过电聚合法制备MIP膜,构建了一种灵敏度高、特异性强的CAP分子印迹电化学传感器,成功应用于实际样品中痕量CAP的快速检测。
1 实验部分
1.1 仪器与试剂
CHI600E电化学工作站(上海辰华仪器公司);采用三电极体系,金电极(Au,直径为2mm)为工作电极,铂丝为对电极,饱和甘汞电极为参比电极;扫描电子显微镜(SEM,德国卡尔蔡司公司)。
CAP(纯度98%)、MAP(纯度98%)、β-CD(纯度96%)、壳聚糖(脱乙酰度≥95%),购于上海阿拉丁试剂有限公司;Al2O3(α相,30nm)、MWCNTs,购于南京先丰纳米材料科技有限公司;其它试剂均为分析纯,实验用水为超纯水。0.2 mol/L磷酸盐缓冲溶液(pH7.0 )由Na2HPO4和NaH2PO4配制;0.1 %壳聚糖溶液由1%(体积分数)乙酸水溶液配制。
1.2 实验方法
1.2.1 分子印迹电化学传感器的制备用Al2O3粉(0.5 µm)在湿润的麂皮上对Au电极打磨抛光后,用水冲洗干净,晾干。称取2.0 mg Al2O3(α相,30nm)于2.0 mL0.1 %壳聚糖溶液中,超声分散15min后,吸取4.0 µL Al2O3溶液滴涂在Au电极表面,在红外灯下干燥后获得Al2O3/Au电极。再取2.0 mg MWCNTs于2.0 mL0.1 %壳聚糖溶液中,超声分散15min后,吸取6.0 µL MWCNTs溶液滴涂于Al2O3/Au电极表面,在红外灯下干燥后得到MWCNTs/Al2O3/Au电极。将MWCNTs/Al2O3/Au电极置于含1.0 mmol/L CAP、2.0 mmol/L MAP和2.0 mmol/L β-CD的0.2 mol/L磷酸盐缓冲溶液(pH7.0 )中,在0.4 ~1.0 V范围内,以150mV/s速率循环伏安扫描25圈,形成CAP印迹膜。将此电极置于甲醇-盐酸溶液(8∶2,体积比)中搅拌洗脱25min,洗脱模板分子CAP,得到CAP分子印迹电化学传感器(MIP/MWCNTs/Al2O3/Au),制备过程如图1所示。在相同条件下制备了非印迹电化学传感器(NIP/MWCNTs/Al2O3/Au),除了不加模板分子CAP。
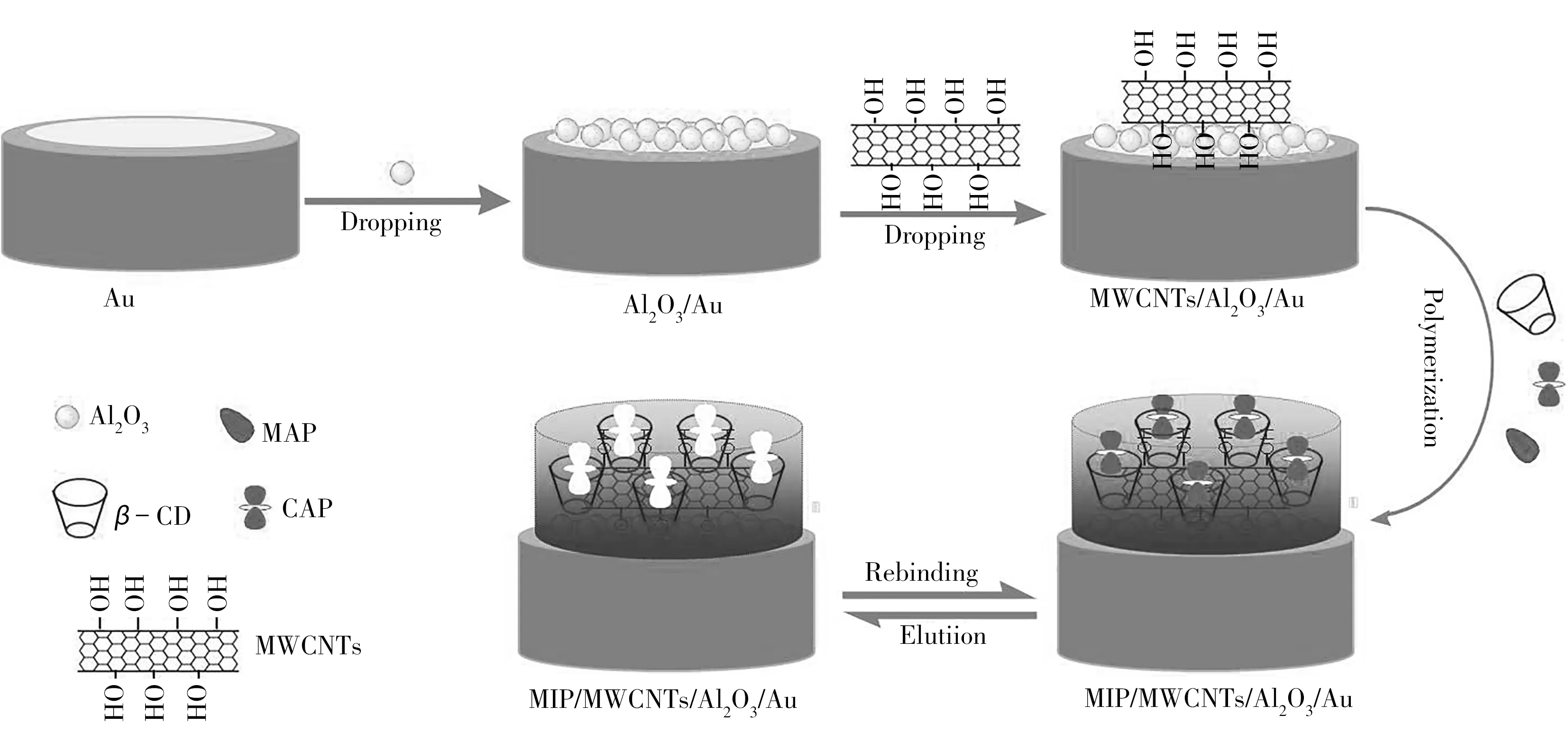
图1 分子印迹电极的制备过程Fig.1 Schematic representation for the preparation process of molecularly imprinted electrode
1.2.2 电化学测试 采用差分脉冲伏安法(DPV)和电化学阻抗法(EIS)研究了传感器在含0.1 mol/L KCl的5.0 mmol/L K3[Fe(CN)6]溶液中的电化学性能。将印迹电极置于一定浓度的CAP标准溶液中孵育10min,取出电极,用水冲洗电极表面,洗去表面非特异性吸附的物质。每次完成测试后,将电极浸入甲醇-盐酸溶液(8∶2,体积比)搅拌洗脱25min,再用少量水冲洗电极表面,晾干待用。DPV表征参数:扫描电位为-0.2 ~0.6 V,电位增量为4mV,振幅为50mV,脉冲周期为0.5 s。EIS表征参数:频率范围为0.01 ~100kHz,振幅为5mV。
1.2.3 样品前处理水样取自实验室自来水。采集时,先将管道的水流放5min,将所取水样用0.22 µm滤膜过滤后进行电化学检测。
取市售牛奶6.0 mL于离心管中,加入10mL乙酸乙酯,涡旋混合30s后,超声提取15min,以6000r/min离心10min,收集上清液。用5mL乙酸乙酯重复提取残渣,合并上清液,于40℃下氮气吹至近干。用5mL4%氯化钠溶液溶解残留物,再加入5mL正己烷涡旋30s,静置分层,弃上层正己烷液。用0.2 mol/L磷酸盐缓冲溶液(pH7.0 )定容至25mL,经0.22 µm滤膜过滤后,待测。
取市售鸡饲料2.00 g于离心管中,其余前处理步骤与上述牛奶样品处理步骤相同。
2 结果与讨论
2.1 分子印迹膜的电聚合及形貌表征
在含1.0 mmol/L CAP、2.0 mmol/L MAP和2.0 mmol/L β-CD的0.2 mol/L磷酸盐缓冲溶液(pH7.0 )中,采用循环伏安法(CV)在MWCNTs/Al2O3/Au电极表面以150mV/s速率扫描25圈进行电聚合制备MIP膜。由图2A可观察到,CAP分子印迹膜的电聚合制备过程的CV曲线仅在第1圈出现1明显的氧化峰,但无还原峰,说明电聚合MAP过程不可逆。随着聚合圈数的增加,响应电流急剧下降,最终趋于背景值,这是由于在MWCNTs/Al2O3/Au电极表面形成致密的非导电聚合膜,使得电极表面与溶液之间的电子转移受到限制。图2A插图为不含CAP的非印迹膜电聚合过程的CV曲线,与电聚合制备MIP的CV曲线基本一致,说明CAP在0.4 ~1.0 V范围内无电化学活性,在电聚合过程中其结构未发生改变。为了进一步证实MIP膜是否修饰到电极表面,采用SEM对未修饰印迹膜的MWCNTs/Al2O3/Au电极和洗脱模板分子前后的MIP/MWCNTs/Al2O3/Au电极的表面进行表征。如图2B所示,MWCNTs/Al2O3/Au电极表面呈现许多MWCNTs交错形成的网状多孔结构,这种结构既有利于电解质离子渗透和电子传递,又能有效增加电极表面积。电聚合后,MWCNTs/Al2O3/Au电极表面覆盖了一层均匀致密的聚合物膜(图2C)。而洗脱模板分子后的MIP/MWCNTs/Al2O3/Au电极表面变得相对粗糙(图2D),且印迹膜上形成与CAP尺寸大小、形状及作用位点相匹配的印迹位点,使其能选择性地吸附溶液中的CAP。

图2 MIP的电聚合制备过程的CV图(A),MWCNTs/Al2O3/Au电极(B)及洗脱模板分子前(C)后(D)的MIP/MWCNTs/Al2O3/Au电极的扫描电镜图Fig.2 CV curves of electropolymerization process for the preparation of MIP(A),SEM images of MWCNTs/Al2O3/Au electrode(B),MIP/MWCNTs/Al2O3/Au electrode before(C)and after(D)elution of template
2.2 分子印迹传感器的差分脉冲伏安法及电化学阻抗表征
采用DPV考察了不同电极在含0.1 mol/L KCl的5.0 mmol/L K3[Fe(CN)6]溶液中的电化学行为(如图3A)。裸Au电极的曲线上观察到1明显的[Fe(CN)6]3–/4–的氧化峰(曲线a)。Au电极修饰Al2O3后(曲线b),[Fe(CN)6]3-/4-的峰电流明显增加,这是因为Al2O3能增大电极表面积,有助于[Fe(CN)6]3-/4-的扩散,提高了电极的催化活性。进一步修饰MWCNTs后(曲线c),[Fe(CN)6]3-/4-的峰电流显著增加,归因于MWCNTs进一步提高了电极的导电性及表面积,促进电子传递。然而,在MWCNTs/Al2O3/Au电极表面电聚合形成印迹膜后(曲线d),[Fe(CN)6]3-/4-的氧化峰消失,这是因为电极表面形成的非导电聚合物阻止了[Fe(CN)6]3-/4-在电极表面进一步氧化。当模板分子被洗脱后,印迹电极的曲线出现明显的[Fe(CN)6]3-/4-的电流峰(曲线e),表明印迹膜上形成了大量印迹空穴,使[Fe(CN)6]3-/4-可到达电极表面发生电化学反应。将洗脱模板分子的MIP/MWCNTs/Al2O3/Au电极置于40.0 nmol/L CAP溶液中孵育10min后,[Fe(CN)6]3-/4-的峰电流下降(曲线f),原因是部分印迹空穴被CAP分子占据,减少了[Fe(CN)6]3-/4-在电极表面的扩散通道。与印迹电极相比,由于NIP膜上缺乏印迹空穴,因而NIP/MWCNTs/Al2O3/Au电极的曲线显示很弱的电流响应(曲线g)。
为进一步了解电极表面的界面特性,采用EIS对不同电极进行表征(图3B)。典型的阻抗谱一般在高频区为半圆,电子转移阻抗(Ret)等于高频区半圆的直径。从图3B可见,Au、Al2O3/Au和MWCNTs/Al2O3/Au电极的EIS曲线(曲线a~c)近似直线,说明这些电极表面的Ret非常小。当MWCNTs/Al2O3/Au电极表面修饰印迹膜(曲线d)或非印迹膜(曲线g)后,非导电的聚合膜严重阻碍了电极界面的电子转移,所以Ret急剧增大。洗脱模板分子后(曲线e),印迹电极表面留下印迹空穴,形成[Fe(CN)6]3-/4-的扩散通道,导致Ret显著减小。而吸附模板分子后的印迹电极的Ret明显增大(曲线f),说明模板分子重新堵塞了部分印迹空穴,阻碍了电子传递。这些结果与DPV表征结果相符,说明所制备的印迹传感器对CAP具有良好的印迹效应。
2.3 实验条件的优化
2.3.1 Al2O3及MWCNTs用量的优化采用DPV考察了不同用量(0、2、4、6、8µL)Al2O3修饰电极的DPV响应。结果发现,随着Al2O3用量的增加,修饰电极的峰电流增加,归因于电极经Al2O3修饰后能增大电极表面积,增多电化学反应活性位点的缘故。当Al2O3用量为4µL时,峰电流最大,继续增大Al2O3用量,电流呈下降趋势,其原因可能是Al2O3用量过多使修饰膜厚度增加,增大了传质阻力。因此选择Al2O3的最佳用量为4µL。同理,探讨了不同用量(0~8µL)MWCNTs对电流响应的影响。结果表明,当MWCNTs用量为6µL时,MWCNTs/Al2O3/Au电极上的DPV电流响应最高。因此选择MWCNTs的最佳用量为6µL。
2.3.2 功能单体的选择及模板分子与功能单体摩尔比的优化CAP分子结构上含有羰基、亚胺基、羟基、硝基等极性基团和疏水性的苯环结构,故考虑通过氢键作用和疏水作用这两种非共价键的形式组装模板分子与功能单体。氨基苯酚因其容易电聚合在不同的衬底上形成稳定的聚合物而常被选作制备MIP膜的功能单体[16]。而β-CD的疏水内腔结构使其能作为“宿主”与诸多疏水性化合物形成稳定的包合物,并被广泛用作功能单体来制备MIP膜[17]。因此分别选择MAP、MAP与β-CD作为功能单体制备了不含β-CD和含β-CD的两种印迹传感器,并研究了其对CAP的特异性识别性能,结果见图4。研究发现,以MAP和β-CD为双功能单体制备的印迹传感器的峰电流变化(ΔI1)远大于以MAP为功能单体制备的印迹传感器吸附CAP分子前后的峰电流变化(ΔI2),说明使用双功能单体制备的传感器能吸附更多CAP分子。这可能是由于MAP的羟基和氨基易与CAP分子的极性基团形成氢键,同时β-CD的内腔通过疏水作用包合CAP分子上的苯环,两种功能单体的优势互补,有助于提高MIP膜对CAP的吸附能力和选择性。因此选择MAP和β-CD为双功能单体制备印迹传感器。
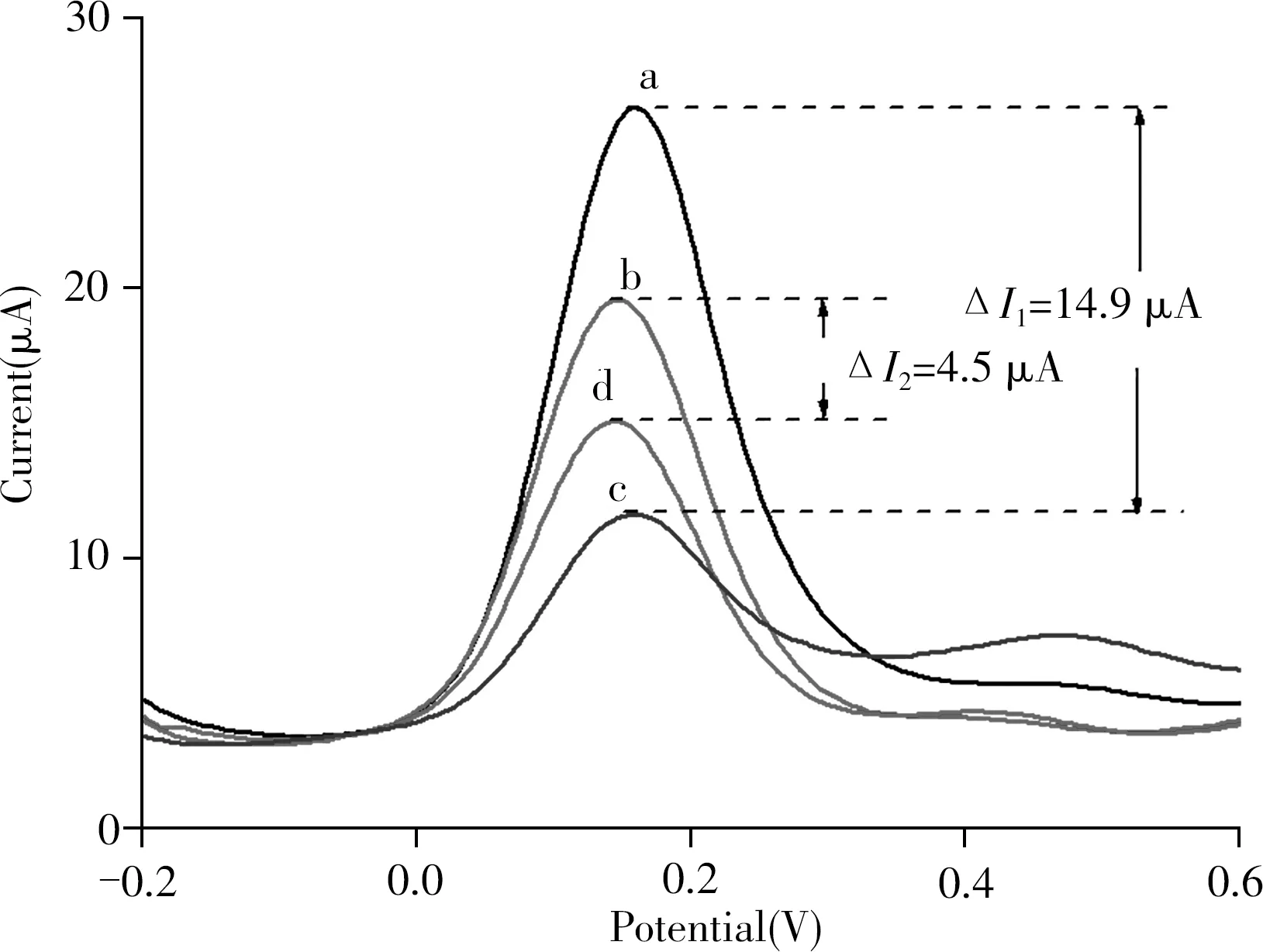
图4 使用不同单体制备的印迹电极的DPV图Fig.4 DPV curves of imprinted electrodes prepared with different monomers
模板分子与功能单体之间的比例直接影响印迹膜的印迹位点数量。若单体浓度太低,无法与模板分子充分结合,则导致形成印迹位点数量不足。相反,单体浓度过高则可能在电极表面形成覆盖部分印迹位点的聚合物,导致模板分子难以洗脱。实验固定CAP的浓度为1.0 mmol/L,研究了不同摩尔比(1∶1∶1、1∶2∶1、1∶3∶1、1∶4∶1、1∶2∶2、1∶2∶3、1∶2∶4)的CAP-MAP-β-CD制备的传感器对CAP吸附前后的峰电流变化。结果显示,模板分子与单体摩尔比为1∶2∶2时,传感器的峰电流变化最大,说明印迹膜形成识别位点较多,即CAP-MAP-β-CD的最佳摩尔比为1∶2∶2。
2.3.3 扫描圈数的优化印迹膜的厚度是影响印迹传感器识别性能的重要因素,在电聚合过程中可通过调整CV扫描圈数来控制印迹膜的厚度。扫描圈数太少,获得的聚合膜较薄,则形成的印迹位点较少,印迹膜的选择性和稳定性差。反之则会形成较厚的印迹膜,以致模板分子包埋过深,难以完全洗脱。实验通过DPV法考察了不同电聚合圈数制备的印迹电极对CAP吸附前后的电流响应变化。研究发现,当电聚合圈数为25圈时,峰电流变化达到最大值,即选择最佳电聚合圈数为25圈。
2.3.4 洗脱剂及洗脱时间的选择印迹膜上模板分子的洗脱程度与印迹孔穴的数量紧密相关,而洗脱条件需要将模板分子充分洗脱且不破坏印迹膜的结构。初步选取了甲醇、乙醇、0.5 mol/L硫酸水溶液、甲醇-乙酸(9∶1)、乙醇-乙酸(9∶1)、甲醇-盐酸(9∶1)、乙醇-盐酸(9∶1)、0.2 mol/L氢氧化钠水溶液为洗脱剂,发现甲醇-盐酸(9∶1)的洗脱效果最佳,印迹电极孵化CAP前后的峰电流变化最大。进而研究了甲醇-盐酸的体积比分别为9∶1、8∶2、7∶3、6∶4时的洗脱效果。结果显示,甲醇-盐酸(8∶2)的洗脱效果最好。同时还探究了印迹电极在甲醇-盐酸(8∶2)洗脱剂中不同洗脱时间(0、5、10、15、20、25、30min)的影响。如图5所示,随着洗脱时间的增加,电极表面的印迹空穴增多,峰值电流逐渐增大,洗脱25min后,峰电流变化很小,说明印迹膜上的模板分子已基本被洗脱。继续延长洗脱时间,除了影响实验效率外,还可能破坏印迹膜的结构。因此选择25min作为最佳洗脱时间。
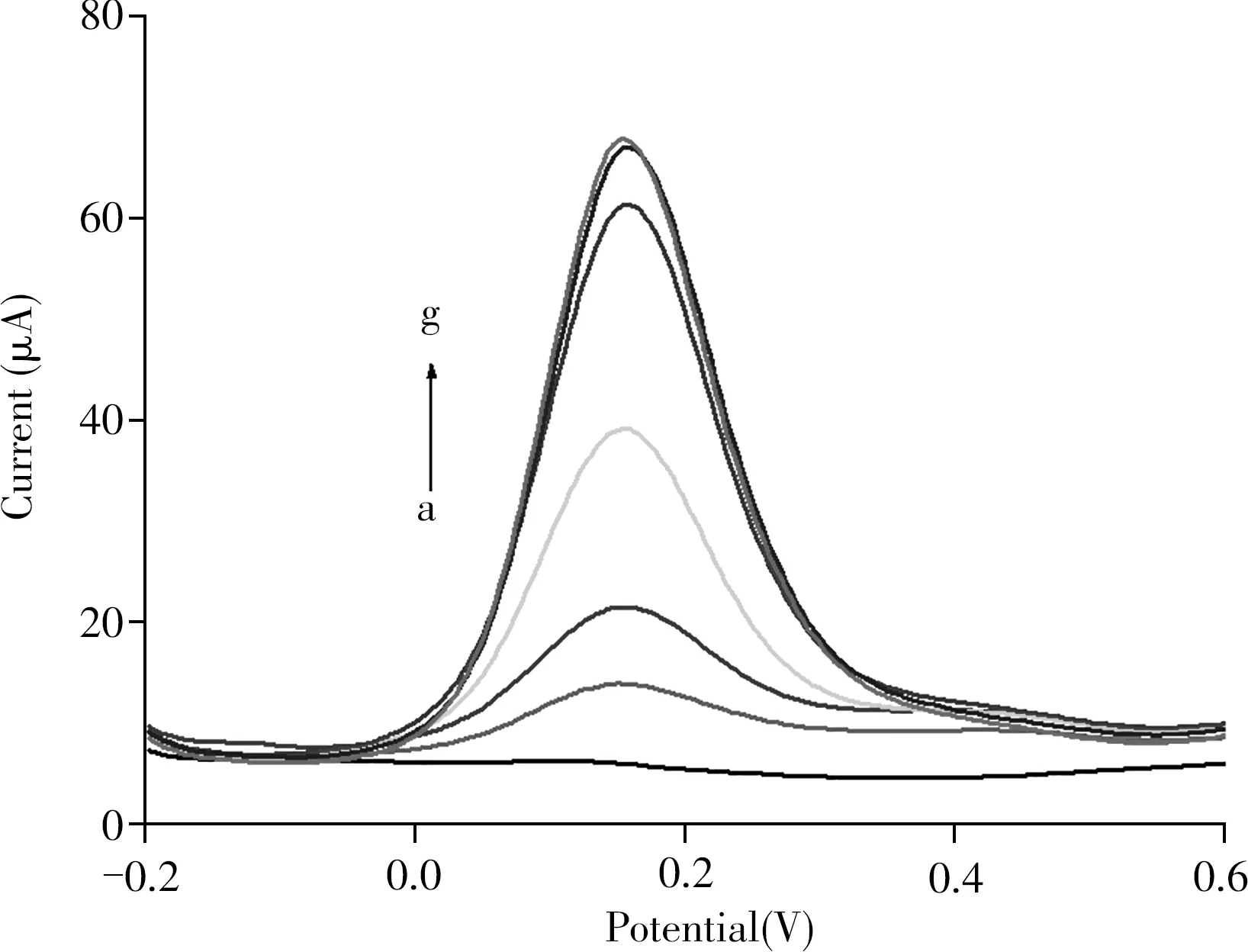
图5 MIP/MWCNTs/Al2O3/Au电极在不同洗脱时间下的DPV图Fig.5 DPV curves of MIP/MWCNTs/Al2O3/Au elec⁃trode with different elution time
2.3.5 pH值的优化溶液的pH值对模板分子在印迹电极表面的吸附效果有较大影响。因此在孵育阶段需要优化溶液的pH值,以促进CAP与印迹空穴的相互作用。本实验分别配制了含60.0 nmol/L CAP的pH分别为5.5 、6.0 、6.5 、7.0 、7.5 、8.0 的0.2 mol/L磷酸盐缓冲溶液,研究了印迹电极孵育CAP前后的峰电流变化。发现pH7.0 时,峰电流变化最大,即印迹电极对CAP的吸附量最大。pH值过低时,可能是溶液中的H+与单体MAP的氨基上的孤对电子结合,破坏了MAP与CAP之间的氢键,导致CAP容易脱离印迹膜。而pH值过高时,CAP可能发生水解[18],结构被破坏,不利于印迹膜对CAP的特异性识别。因此选择在pH7.0 的磷酸盐缓冲溶液中检测CAP。
2.3.6 孵育时间的优化模板分子在印迹膜上的孵育时间也会影响传感器的灵敏度。将洗脱模板的印迹电极置于60.0 nmol/L CAP溶液中分别孵育不同时间(0、1、2、4、6、8、10、12min)后进行DPV测试。结果显示,随着孵育时间的延长,印迹电极对CAP的吸附量逐渐增加,峰电流显著下降,超过10min后峰电流几乎不变,说明印迹膜对CAP的吸附达到饱和。由此确定最佳孵育时间为10min。
2.4 线性范围与检出限
在最佳条件下,将MIP/MWCNTs/Al2O3/Au电极置于不同浓度CAP溶液中孵育10min后,在含0.1 mol/L KCl的5.0 mmol/L K3[Fe(CN)6]溶液中进行DPV测试。如图6所示,峰电流随CAP浓度的增加而减小,归因于CAP在印迹膜上的吸附量逐渐增加,导致[Fe(CN)6]3-/4-在电极表面的扩散道减少的缘故。CAP浓度在1.0 ~60.0 nmol/L范围内与[Fe(CN)6]3-/4-的峰电流(I,µA)呈良好的线性关系,线性方程为I=-0.655 c+50.88 (r2=0.996 )。计算得到检出限(3S/b)为0.14 nmol/L,其中S为空白溶液测定8次的峰电流的标准偏差,b为校准曲线斜率的绝对值[19]。本方法的检出限低于文献报道的电化学方法(见表1),其原因主要有:①Al2O3和MWCNTs具有大的比表面积和良好的催化性能,其作为载体不仅有助于增强电流信号,而且为印迹膜的修饰提供了大的比表面积。②使用双功能单体可增加聚合物与模板分子之间的作用力种类和识别位点数量,从而提高印迹膜对模板分子的亲和力和选择性。两方面的协同作用大大提高了传感器对CAP的检测灵敏度。

表1 不同电化学方法检测CAP的性能比较Table1 Comparison of different electrochemical methods for CAP detection
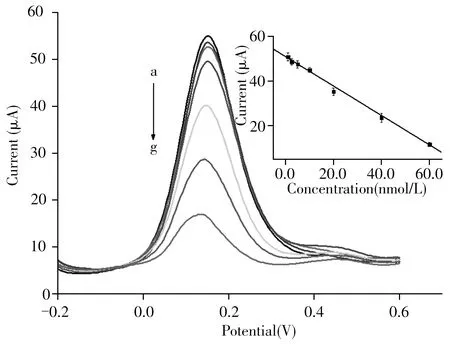
图6 孵育不同浓度CAP的MIP/MWCNTs/Al2O3/Au电极的DPV图Fig.6 DPV curves of MIP/MWCNTs/Al2O3/Au elec⁃trode incubated with different concentrations of CAP concentrations of CAP(a-g):1.0 ,2.5 ,5.0 ,10.0 ,20.0 ,40.0 ,60.0 nmol/L;insert:linear relationship between peak current and concentration of CAP
2.5 传感器的选择性
为了考察传感器对CAP的选择性,实验选择氟苯尼考、恩诺沙星和磺胺嘧啶3种常见抗菌药物作为可能干扰物进行实验。将印迹电极分别置于40nmol/L CAP和干扰物中孵育后进行DPV测定,得出印迹电极对CAP及上述3种抗菌药物吸附前后产生的相对峰电流差值分别为25.32 、13.61 、3.78 、5.94 µA(见图7)。尽管氟苯尼考的结构与CAP类似,但印迹电极表面的印迹空穴不能与之完全契合,相比于CAP进入印迹空穴的量有所减少,故峰电流变化小于CAP;而结构差异较大的恩诺沙星和磺胺嘧啶难以进入印迹空穴,所以两者的峰电流变化更小。研究表明,尽管印迹传感器对氟苯尼考有少量的特异性吸附,但对CAP的选择性更高,因此不影响传感器对CAP的检测。
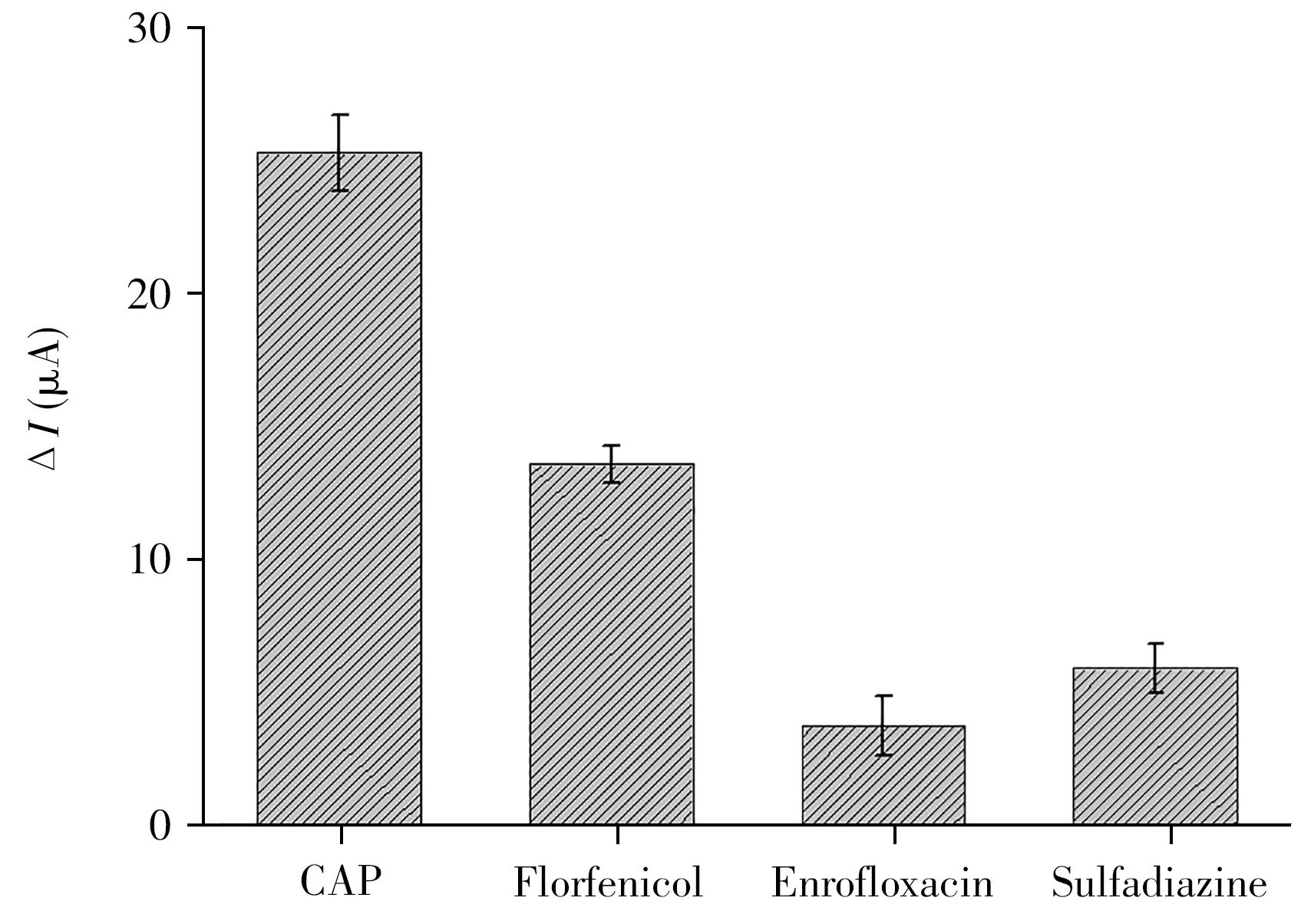
图7 MIP/MWCNTs/Al2O3/Au印迹传感器对不同药物的选择性响应Fig.7 Selectivity of MIP/MWCNTs/Al2O3/Au molecularly imprinted sensor toward different drugs
2.6 传感器的重现性与稳定性
取同一批制备的5支印迹电极于40nmol/L CAP溶液中孵育10min后,在含0.1 mol/L KCl的5.0 mmol/L K3[Fe(CN)6]溶液中进行DPV测试,计算峰电流的相对标准偏差(RSD)为3.9 %。使用同一支印迹电极对40nmol/L CAP溶液进行6次重复吸附、洗脱测试,测得RSD为3.0 %,表明此印迹电极具有良好的重现性。将印迹电极于室温保存,每天吸附40nmol/L CAP溶液后进行DPV测定,再洗脱,连续测定7d,发现第3d和第5d测得电流响应值分别为初始值的94.1%和91.2 %,第7d降至86.4 %,说明该电极在6d内的稳定性良好。
2.7 实际样品分析
将建立的方法应用于实际样品中CAP的检测,并进行加标回收实验,加标浓度分别为5.0 、10.0 、50.0 nmol/L,每个样品平行测定3次,结果见表2。自来水、鸡饲料和牛奶样品中均未检出CAP残留。CAP在3种样品中的平均回收率为88.0 %~110%,RSD小于10%。说明该方法准确、可靠,能够达到检测痕量CAP残留的要求。
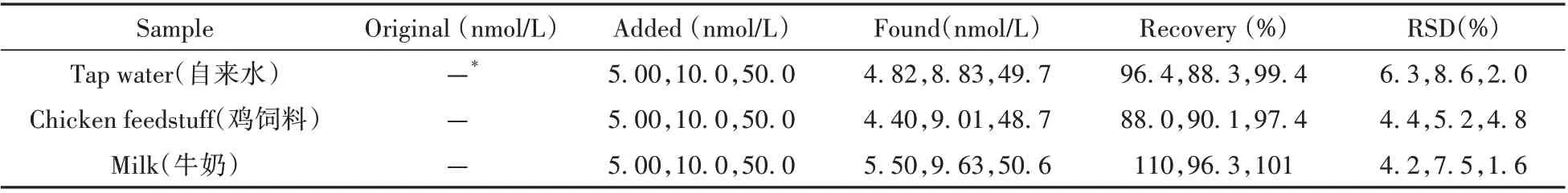
表2 样品中CAP的测定结果及其回收率Table2 Determination result of CAP and its recovery in real samples
3 结 论
本文以Al2O3和MWCNTs为载体,结合双功能单体制备的印迹膜,构建了一种用于检测痕量CAP的分子印迹电化学传感器。传感器的线性范围为1.0 ~60.0 nmol/L,检出限低至0.14 nmol/L。所构建的传感器具有良好的灵敏度、选择性、重现性及稳定性,用于实际样品中CAP的检测,结果令人满意,为实际样品中痕量CAP检测提供了一种简单、经济、有效的分析方法。

