生物等效性试验中口服托吡酯致中性粒细胞减少1 例
汪旻晖 黄 伟 沈 杰△
(1皖南医学院弋矶山医院药物临床评价中心 芜湖 241001;2合肥合源药业有限公司 合肥 230088)
托吡酯为磺酸基取代的单糖衍生物,自1995 年上市后,作为新型广谱抗癫痫药在临床上广泛使用。主要用于(单独或与其他药物联合)控制和预防癫痫和偏头痛[1],可用于治疗合并有Lennox-Gastaut 综合征的癫痫发作[2]。据文献报道和药品说明书显示,托吡酯常见不良反应多与中枢神经系统相关,如嗜睡、头晕、疲倦等[3],血液系统不良反应少见,其中中性粒细胞减少症为上市后首次判定为托吡酯相关的罕见不良反应,个别案例报道均发生于患有癫痫、偏头痛、精神分裂症等疾病的患者,且多合并使用其他药物,如苯妥英钠、乙酰唑胺、依来曲普坦、氯氮平等[4-5],在中国未见托吡酯诱发中性粒细胞减少症的案例报告。
本文报告了1 例参加托吡酯片生物等效性(bioequivalence,BE)试验的中国成年男性健康志愿者在服药后发生的严重不良事件。该试验所纳入的受试者均为无合并疾病及用药的健康人,可以认为该事件是一个在健康个体中发生的与托吡酯相关的中性粒细胞减少的独特案例。区别于具有复杂合并症状、疾病及治疗药物的情况下,描述该案例的特征可为非化疗特异性药物诱导的中性粒细胞 减少 症(idiosyncratic drug-induced neutropenia,IDIN)的早期诊疗提供一些参考。
病例资料男性,20 岁,汉族,体重指数22.3 kg/m2,签署知情同意书后进入托吡酯片BE 试验的筛选程序。该试验经皖南医学院弋矶山医院药物和器械伦理委员会审查批准,共筛选114 名志愿者,所有志愿者均签署知情同意书,48 名入选(空腹研究和餐后研究各24 名),其中45 名(包括本例)完成研究。本案例受试者在筛选过程中否认传染病史、重大疾病史、外伤史、手术史和过敏史,否认4 周内服用过改变肝药酶活性的药物,否认2 周内服用任何药物,否认3 个月内临床试验参加史、失血或献血史,否认吸烟史、饮酒史、药物滥用史,承诺遵守试验规定,包括禁烟、禁酒及饮食规定。生命体征检查、体格检查、12 导联心电图、腹部彩超、正位胸片、实验室检查、传染病筛查、尿药筛查、酒精呼气测试检查结果均为正常、阴性或异常无临床意义(no clinical significant,NCS)。于 2019 年 8 月经医师判定为符合入选标准且不符合排除标准则入组试验。首次服药当天以D-1 表示,D-4 的筛选期血常规示白细胞为6.5×109/L[参考值(4.0~10.0)×109/L],中性粒细胞绝对数为 3.2×109/L[参考值(2.0~7.5)×109/L]。D-1 分配随机号并入住Ⅰ期病房。
D1 早晨受试者进食高脂标准餐后口服托吡酯片1片(参比制剂,西安杨森制药有限公司,100 mg/片),在给药前1.5 h 至给药后72 h 采集药代动力学血液样本共17 次,3 mL/次。期间所有生命体征监测结果均正常,给药后72 h 完成生命体征检查,离开Ⅰ期病房。D19 再次入住Ⅰ期病房,D20 血常规、血生化及尿常规均为正常或NCS,白细胞为5.3×109/L,中性粒细胞绝对数为2.1×109/L。D22 早晨口服托吡酯片1 片(受试制剂,合肥合源药业有限公司,100 mg/片)。除药物类型外其余流程均同第一周期。D25 完成全部血液样本采集后进行出组安全性检查,其中体格检查、生命体征检查、12 导联心电图、腹部彩超、除血常规外的实验室检查结果均为正常或NCS,但血常规结果示白细胞3.0×109/L,中性粒细胞绝对数0.9×109/L,医师判定为异常有临床意义,要求复查。D26 血常规复查结果示白细胞2.2×109/L,中性粒细胞绝对数0.6×109/L,请血液科医师会诊,皮下注射重组人粒细胞集落刺激因子(recombinant human granulocyte colony-stimulating factor,rhG-CSF)300 μg,收治入院。研究者以“中性粒细胞减少”为医学诊断名称上报严重不良事件(serious adverse event,SAE)至相关部门。
D27 血常规示白细胞6.2×109/L,中性粒细胞绝对数3.4×109/L,已恢复至正常值范围,继续住院观察至D30 出院,住院期间血常规、心电图、各项实验室检查(包括但不限于血常规、血沉、C 反应蛋白、风湿组合、甲状腺功能、降钙素原检测等)结果均为正常或NCS,且除医疗护理外未行药物、非药物或手术治疗,无特殊不适主诉。该受试者于D33、D41和D55 回院进行安全性随访,血常规检查结果均正常。SAE 转归为症状消失且无后遗症。该受试者依从性良好,康复期间无其他不良事件发生。白细胞和中性粒细胞绝对数检查结果如图1 所示。
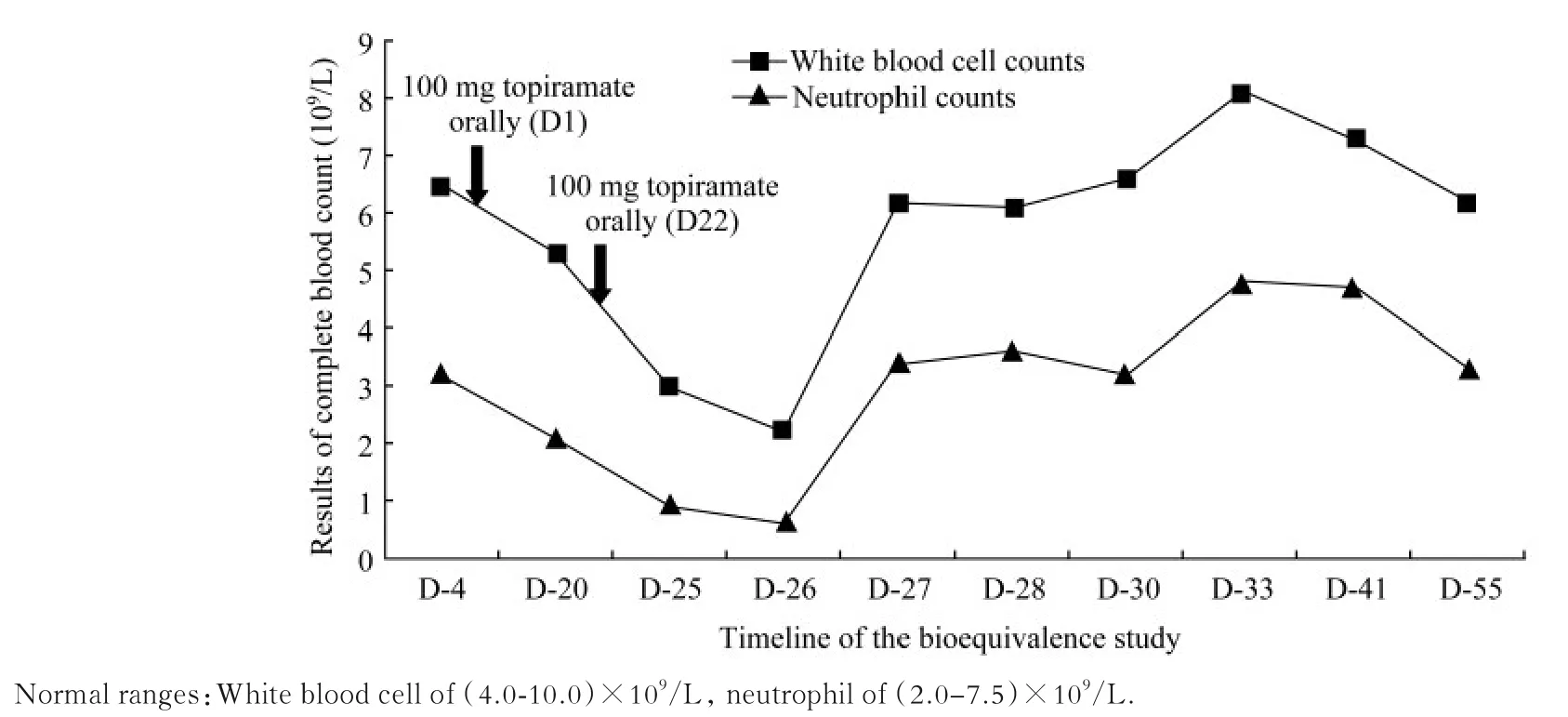
图1 受试者白细胞和中性粒细胞绝对数检查结果Fig 1 White blood cell counts and neutrophil counts of the subject
讨论中性粒细胞减少症通常定义为中性粒细胞绝对数≤1.5×109/L[6]。大多数中性粒细胞减少症的发生与药物相关,包括化疗药物导致的化疗药中性粒细胞减少症和IDIN[7]。IDIN 是一种罕见而致命的疾病,患者通常在第一次接触药物后的几周至几个月内经历严重的中性粒细胞减少,死亡率约为5%[8]。托吡酯是一种耐受良好且安全的抗癫痫药,其相关的中性粒细胞减少症被认为是十分罕见的不良反应,本案例的发生可能与个体易感因素有关。但仍需指出的是,以自发病例报告为基准计算出的发生率数据可能无法准确反映托吡酯引起中性粒细胞减少的真正频率,其原因包括实际报告数量与实际发生例次的差异,该比例数据通常较难以药物处方数为分母进行标准化处理,且大多数系统评价仅关注粒细胞缺乏症。托吡酯临床推荐剂量为100~400 mg/天,既往报道案例发生中性粒细胞减少症均处于每日服用托吡酯25~200 mg,持续30 天以上的情况下,而本案例在仅口服2 次100 mg托吡酯片且2 次口服间隔21 天清洗期的情况下即发生中性粒细胞减少症状,提示临床医师应在治疗过程中关注与托吡酯相关的血液系统不良反应,也应警惕具有血液系统不良反应的药物在低剂量治疗时出现异常情况的早期识别。
IDIN 总体发病率低,为每百万人口2.4~15.4例[8],因而阐明其确切的发生机制十分困难。托吡酯具有多种假定的作用机制[9]和广泛的临床疗效[9],因具有轻度的碳酸酐酶抑制作用,文献通常试图通过免疫过敏反应或抑制碳酸酐酶的磺酰胺/氨基磺酸盐的毒性作用,来解释托吡酯产生造血系统不良反应的潜在机制[10]。
引起中性粒细胞减少症的原因除药物外,还包括自限性病毒性疾病、先天性综合征、甚至严重的全身性疾病等[11]。中性粒细胞减少症多为轻度且具有剂量相关性,早期临床表现往往不明显,患者日常护理不易发现,直至获得重复的实验室检查异常结果后方可确认。IDIN 如不及时识别并加以治疗,后期可能导致严重的临床事件,如急性发热性疾病、败血症甚至死亡,其治疗始于立即停用任何可能引起IDIN 的药物,因而IDIN 治疗的关键环节在于需将其与其他原因造成的中性粒细胞减少症进行区分[12]。通常注射rhG-CSF 对于增加中性粒细胞绝对计数是有益的,rhG-CSF 可降低中性粒细胞减少症的发生率、病程和严重程度[13]。在本例中rhG-CSF 的有效性也得到验证。病史问询和实验室检查有助于辨明引起中性粒细胞减少的原因,病因不明的中性粒细胞减少症患者可以考虑进行骨髓穿刺和核心活检。本例患者无重大既往病史,无合并药物,否认任何放射性物质或毒素接触史,在服用托吡酯后出现中性粒细胞减少,停药后白细胞和中性粒细胞绝对数即恢复,可认为与试验用药有合理的时间顺序、符合药物已知的不良反应类型且停药后反应减轻或消失,暂无证据支持再次给药后出现反应。结合前述过程,可以推测第二次给药加速了中性粒细胞减少,因此医师判定该不良事件的发生与托吡酯的使用具有相关性,属于药物不良反应。本例中,类风湿因子、抗Smith 抗体、抗U1-RNP 抗体、抗SSA 抗体等结果阴性,降低了该患者发生系统性风湿性疾病或自身免疫性疾病的可能性[14]。红细胞沉降率和C 反应蛋白水平正常可排除潜 在 的 炎 症[15]。 人 类 免 疫 缺 陷 病 毒(human immunodeficiency virus,HIV)等抗体检测结果均为阴性,消除了传染病导致中性粒细胞减少的可能性,这是短暂性中性粒细胞减少症的常见病因之一[16]。
Ⅰ期药物临床试验和BE 研究通常是以健康人群为研究对象。本例在参与BE 试验时发生,具有一定的特殊性,包括临床无法出现的健康人服用托吡酯的情况,以及发生和处理过程得到详细记录,是首次报道的中国地区健康人中发生的托吡酯引起的中性粒细胞减少。同时也提示Ⅰ期药物临床试验研究者应高度重视健康志愿者在参加研究过程中的安全性保护,即使在低剂量、单次服药、无合并疾病和药物的情况下,也可能出现罕见或严重的不良反应。
作者贡献声明汪旻晖 论文构思和撰写,数据采集。黄伟 病例随访,内容审核。沈杰 数据分析,论文指导和修订。
利益冲突声明所有作者均声明不存在利益冲突。

