减低剂量阿扎胞苷治疗中高危MDS及MDS/MPN患者的临床疗效
龙章彪 葛 健 倪 婧 刘沁华 曾庆曙 夏瑞祥
DNA甲基化是骨髓增生异常综合征(myelodysplastic syndrome,MDS)最常见的表观遗传学改变,去甲基化治疗通过恢复抑癌基因功能,达到逆转MDS疾病进展的疗效。阿扎胞苷同时嵌入DNA与RNA实施去甲基化作用,从而发挥抗肿瘤活性。2018年批准在中国上市后,研究探索标准剂量阿扎胞苷治疗中国中高危MDS及骨髓增生异常综合征/骨髓增殖性肿瘤(myelodysplastic syndrome/myeloproliferative neoplasms,MDS/MPN)的临床疗效及不良反应,结果显示阿扎胞苷具备良好疗效及安全性。为探讨减低剂量阿扎胞苷在中高危MDS及MDS/MPN中的临床应用价值,本研究回顾性分析2018年12月至2021年1月采用减低剂量阿扎胞苷治疗中高危MDS及MDS/MPN患者的临床资料,对患者基线特征、临床疗效、生存及不良反应等进行分析,现报道如下。
1 资料与方法
1.1 一般资料 选取2018年12月至2021年1月安徽医科大学第一附属医院血液内科减低剂量阿扎胞苷治疗的中高危MDS及MDS/MPN患者,回顾性分析患者的临床资料。MDS按照维也纳标准及中国MDS诊断标准进行诊断,依据国际预后积分系统修订版(revised international prognostic scoring system,IPSS-R)进行危险度分层,24例中高危(>3.5分)的MDS患者纳入本研究。依据WHO标准,13例MDS/MPN患者纳入本研究。
1.2 方法 采取减低剂量阿扎胞苷方案:阿扎胞苷(商品名:维达莎,百济神州公司),采用60 mg/(m·d),皮下注射,共7 d,28 d为1个周期。治疗期间每2周随访1次,随访主要指标包括骨髓细胞学、血常规、血生化等疗效及安全评估。
1.3 临床疗效评价 依据MDS国际工作组制定的血液学反应和血液学改善评价标准(international working group 2006,IWG 2006)。主要评估指标为血液学反应:完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、血液学改善(hematology improved,HI)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD);总生存期(overall survival,OS);1、2年总生存率及不良反应。治疗总反应(overall response,OR)定义为CR+PR+HI,治疗无反应(non-response,NR)定义为SD+PD。OS定义为首次应用阿扎胞苷至死亡或随访终点的时间。
1.4 不良反应评价 治疗相关不良反应按照WHO药物不良反应分级标准进行判定。
1.5 随访 随访截止日期为2021年1月20日,通过住院病案首页上留存的联系方式对患者或直系亲属进行电话随访。
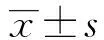
2 结果
2.1 临床基线特征 37例患者中位年龄为65.50(48.00,77.50)岁,男性23例,女性14例,中位随访时间为10.00(6.00,19.50)个月,中位美国东部肿瘤协作组(Eastern cooperative oncology group,ECOG)评分1.00(1.00,1.75)分。在MDS亚型中,8例多系发育异常(multilineage dysplasia,MLD)、2例多系发育异常伴环铁(multilineage dysplasia with ring sideroblasts,RS-MLD)、11例原始细胞增多1型(excess blasts 1,EB1)、3例原始细胞增多2型(excess blasts 2,EB2);在MDS/MPN亚型中,最常见为慢性粒单核细胞白血病(chronicmyelomonocytic leukemia,CMML)(11例),其次为环铁伴血小板增多(ring sideroblasts and thrombocytosis,RS-T)与MDS/MPN未分类(MDS/MPN unclassifiable,MDS/MPN-U)各1例。37例患者中,有10例曾接受过地西他滨或促造血治疗,27例为首次应用减低剂量阿扎胞苷治疗。37例患者中,32例在治疗前进行了二代基因测序,在基因测序的患者中,27例(84.38%)存在1个或多个基因突变,5例无突变。突变中,除1例为预后良好基因(SF3B1)外,其他均为1个或多个预后不良基因。高频突变基因包括ASXL1(11例)、TET2(9例)、SRSF2(7例)和NRAS(7例),丛集于表观遗传、RNA剪接、信号转导3个通路,其他通路突变较少。见图1。血常规的基线分析显示,患者存在显著的血细胞减低,血红蛋白、白细胞、中性粒细胞、血小板计数分别为(74.68±25.48)g/L、(14.09±28.36)×10/L、(3.43±5.50)×10/L和(74.43±75.37)×10/L。

图1 MDS及MDS/MPN测序患者基因突变热图
2.2 临床疗效 患者中位疗程为2.00(1.00,4.50)疗程,3例CR、7例PR、8例HI、8例SD、7例PD,OR率为54.05%(20/37)。见图2。亚型分析显示,MDS患者的中位疗程为2.00(1.00,3.00)疗程,3例CR、2例PR、8例HI、6例SD、5例PD,OR率为54.17%(13/24);而MDS/MPN患者的中位疗程为3.00(1.50,5.50)疗程,7例PR、2例SD、2例PD,OR率为53.85%(7/13)。见图2、3。单因素分析结果显示,OR与NR患者阿扎胞苷疗程数进行比较,差异有统计学意义(P
<0.05),而疾病类型、年龄、性别、ECOG评分、之前有无治疗、基因突变与否、白细胞计数的差异无统计学意义(P
>0.05)。见表1。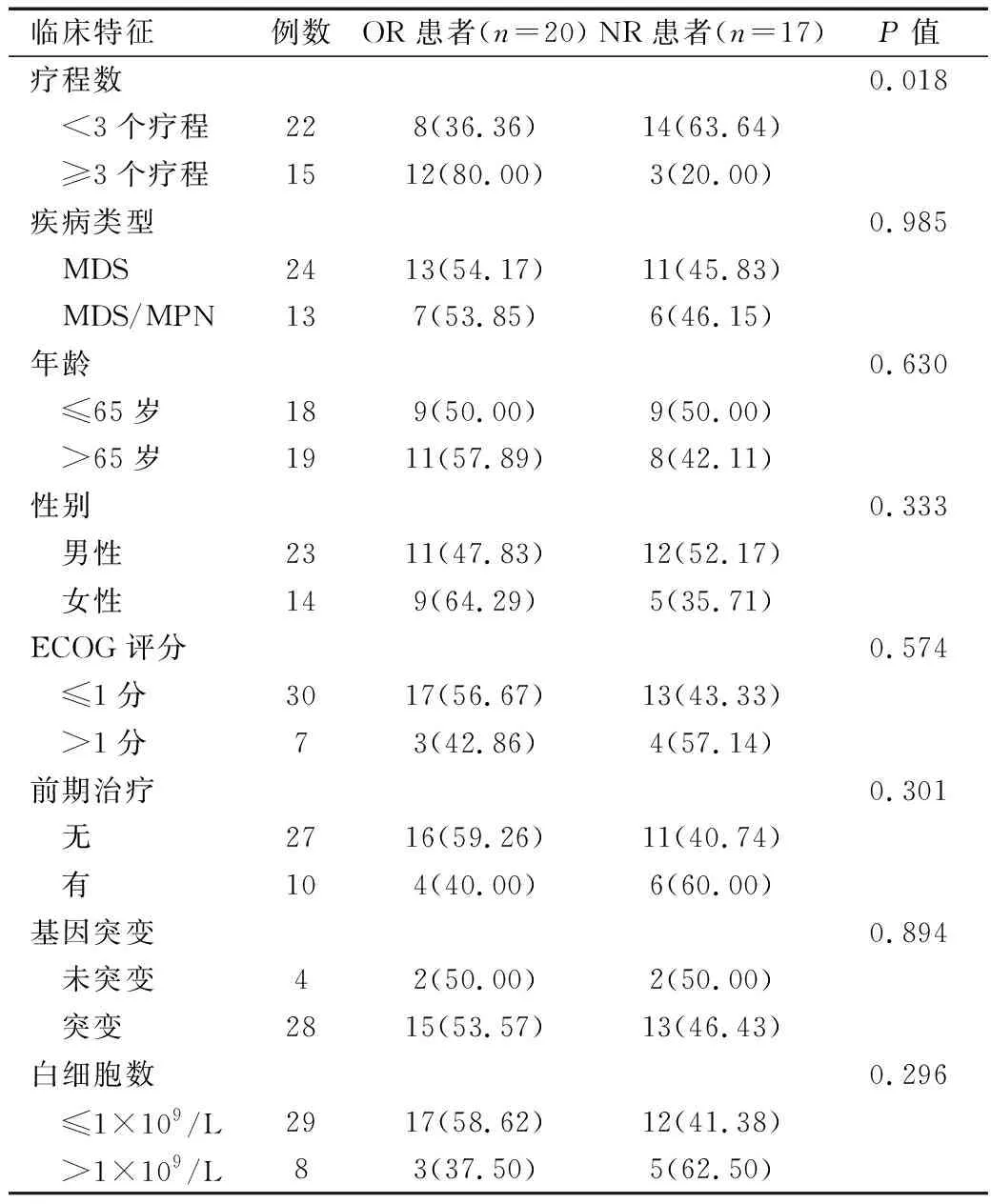
表1 MDS及MDS/MPN患者临床疗效比较[例(%)]
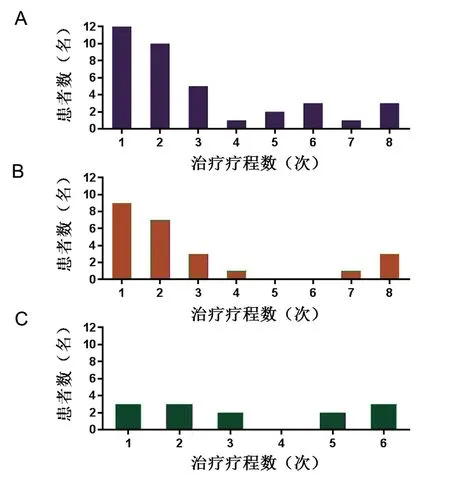
图2 阿扎胞苷治疗疗程分布注:A为全部患者疗程数;B为MDS患者疗程数;C为MDS/MPN患者疗程数
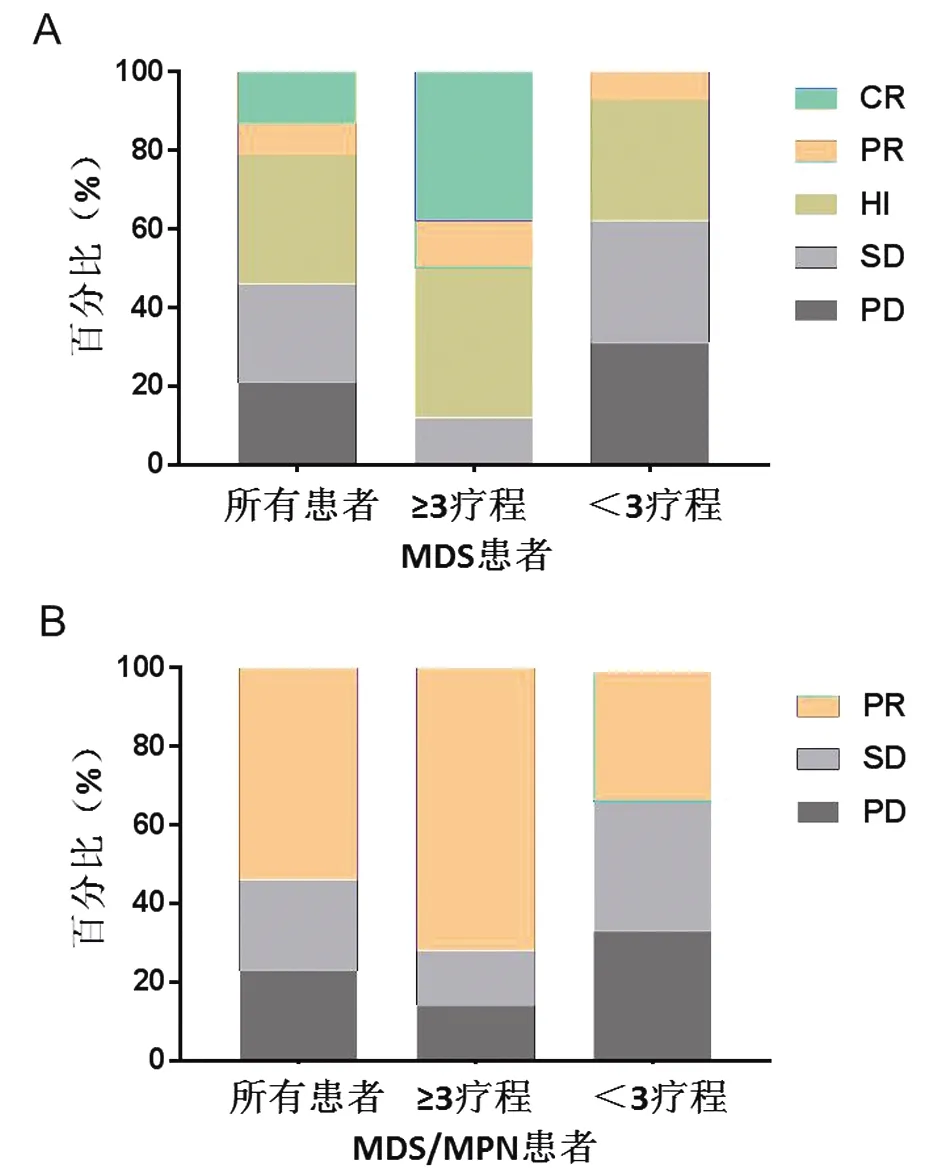
图3 不同疗程阿扎胞苷治疗后临床疗效比较注:A为MDS患者的临床疗效比较;B为MDS/MPN患者的临床疗效比较
2.3 生存分析 患者中位生存期16.00月(1、2年总生存率分别为55.04%和27.22%)。亚型生存分析显示,MDS患者中位生存期为13.50个月(1、2年总生存率分别为52.08%和16.28%),MDS/MPN患者中位生存期为15.50个月(1、2年总生存率分别为60.58%和45.43%)。阿扎胞苷治疗≥3个疗程的MDS患者中位生存期优于<3个疗程者,但差异无统计学意义(17.00个月vs
9.50个月,P
=0.643)。阿扎胞苷治疗≥3个疗程的MDS/MPN患者中位生存期优于<3个疗程者,差异无统计学意义(未达到vs
6.00个月,P
=0.713)。见图4。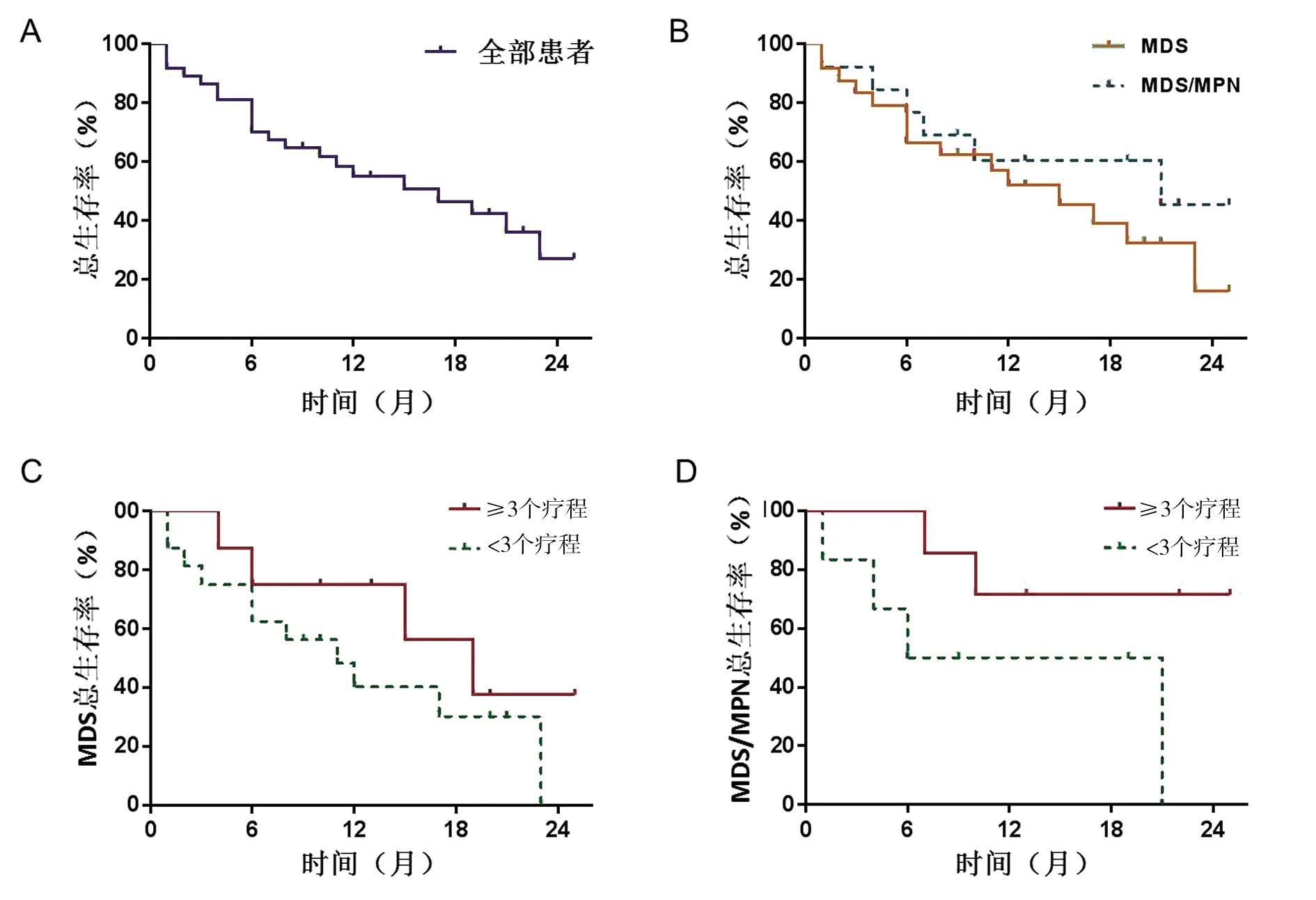
图4 减低剂量阿扎胞苷治疗MDS及MDS/MPN患者的生存曲线注:A为全部患者生存曲线;B为MDS及MDS/MPN患者生存曲线;C为阿扎胞苷治疗≥3个疗程与<3个疗程的MDS患者生存曲线;D为阿扎胞苷治疗≥3个疗程与<3个疗程的MDS/MPN患者生存曲线
2.4 不良反应 37例患者中,27例(72.97%)出现骨髓抑制,为最常见不良反应,其中Ⅲ~Ⅳ级骨髓抑制12例(32.43%)。其次为感染,6例(16.22%)患者出现肺炎,其中Ⅲ~Ⅳ级肺炎4例(10.81%);1例(2.70%)出现Ⅳ级血流感染。5例(13.51%)患者出现胃肠道反应,均为Ⅰ~Ⅱ级恶心。
3 讨论
高龄、多合并症等因素限制了造血干细胞移植在中高危MDS及MDS/MPN患者中的应用,使得多疗程去甲基化治疗成为中高危MDS及MDS/MPN重要的治疗手段。在临床实际诊疗中,仅少数患者能耐受多疗程标准剂量去甲基化治疗。因此,本研究通过减低剂量阿扎胞苷治疗中高危MDS及MDS/MPN,旨在减少治疗不良反应,使患者能够耐受多疗程治疗, 为临床治疗提供一定的参考。
本研究纳入的MDS患者包括MLD、RS-MLD、EB1及EB2;MDS/MPN中大多数为CMML,其他包括RS-T与MDS/MPN-U。患者亚型分布与MDS及MDS/MPN流行病学疾病亚型分布基本一致,无选择性偏差。分析本研究患者的临床特征,发现存在高龄及高基因突变2个特点:年龄方面,患者中位年龄65.50岁,高于中国人群临床试验的中位年龄(58岁),可能是限制患者多疗程治疗的一个客观因素;基因突变方面,在接受二代基因测序的32例患者中,84.38%的患者存在基因突变,突变频率高于国际癌症基因组联盟报道的突变频率(78%),提示肿瘤克隆的基因背景更为复杂。以上特征提示临床应用中,采取减低剂量阿扎胞苷,是提高高龄、高基因突变患者多疗程治疗耐受性的一个可行的治疗策略。
在既往真实世界研究中,标准剂量阿扎胞苷治疗MDS患者的OR率及生存逊于临床试验研究结果。国内外临床试验中阿扎胞苷治疗MDS患者OR率为88%~96%,中位生存期22~24.5个月。但在真实世界研究中,OR率为32%~54%,中位生存期多在11~16个月。可能相比较临床试验,真实世界中患者年龄更大、体能状况更差、不能耐受多疗程阿扎胞苷治疗。本研究采取减低剂量阿扎胞苷,OR率为54.05%,中位生存期15.00个月,疗效稍逊于临床试验疗效,而不劣于真实世界研究中标准剂量阿扎胞苷的疗效。表明减低剂量阿扎胞苷可使患者在临床疗效上获益。
为分析临床疗效相关因素,本研究进行了单因素分析,结果显示阿扎胞苷连续治疗≥3个疗程的患者疗效优于<3个疗程者,因此,坚持多疗程是治疗成功的重要因素。但单因素分析未发现影响临床疗效的其他因素,故未进一步多因素分析。在标准剂量阿扎胞苷治疗的研究中,临床疗效与TP53及ZRSR2基因突变呈负相关,与原始细胞数呈负相关,多项研究显示临床疗效与阿扎胞苷疗程数呈正相关,与本研究结果相一致。但本研究样本量相对较小,仍需要后续大样本量研究来探索疗效的影响因素。
本研究中,最常见不良反应为骨髓抑制,其中Ⅲ~Ⅳ级骨髓抑制达32.43%,出现Ⅲ~Ⅳ级严重不良反应比率显著低于标准剂量研究。血液学反应多出现在第1~2个疗程,与研究报道相类似。其次为感染,一些患者同时合并骨髓抑制及感染,如7例感染中,5例为Ⅲ~Ⅳ级的重症感染。提示临床应用中尤其需注意血液学毒性以及感染,及时进行促造血和抗感染治疗。其他如胃肠道等不良反应则较轻微,几乎均为Ⅰ级。本研究未出现其他研究报道的注射部位皮肤反应,可能与应用时强调有经验的护士规范操作、多部位皮下注射有关。
综上,减低剂量阿扎胞苷治疗中高危MDS及MDS/MPN患者的临床疗效不劣于标准剂量,且安全性良好。多疗程治疗可增加患者临床疗效。减低剂量阿扎胞苷可作为成人尤其是老年中高危MDS及MDS/MPN患者可选的治疗方案。

