不同原水与出厂水水质对供水管网中余氯衰减变化规律的影响
刘彩娥,王诗宇,蒋福春,张 雪,杨琛栋,林 涛
(1. 常州市金坛自来水有限公司,江苏常州 213200;2. 上海市政工程设计研究总院<集团>有限公司,上海 200092;3. 苏州自来水有限公司,江苏苏州 215002;4. 河海大学环境学院,江苏南京 210098)
在常规的饮用水处理厂中,始终将消毒作为最终处理步骤,消毒能充分灭活水中的病原微生物,且能消除与伤寒、霍乱等水传播疾病相关的风险[1],因此,使用化学氧化剂进行饮用水消毒是20世纪最主要的进步之一。
常用的消毒剂包括次氯酸钠、氯胺、二氧化氯、O3、高锰酸钾等。由于次氯酸钠具有价格便宜、制备简单、杀菌效果好、安全性能较高等优点[2],又能与铁锰反应以避免出现颜色和味道[3],其在水处理工艺中使用最广泛。
消毒剂添加后,必须确保管网水中存在足够的余氯浓度来抑制微生物的再生[4]。当管网中有为了控制病原体而存在的残留消毒剂时,潜在的消毒副产物也在增加。大部分消毒副产物是由消毒剂与天然有机质(natural organic matter,NOM)发生反应生成具有致癌性的物质[5],因此,不能忽视原水水质中NOM含量对消毒副产物的生成及余氯衰减的影响。消毒副产物种类主要分为含碳消毒副产物(carbonic disinfection by-products,C-DBPs)和含氮消毒副产物(nitrogenous disinfection by-products,N-DBPs)[6]。三卤甲烷(THMs)是最常见的C-DBPs,卤乙腈(HANs)是一类N-DBPs,则二氯乙腈(DCAN)是氯化后饮用水中最常见的一种HANs[7]。如何保障饮用水的生物安全性并控制与饮用水消毒有关的消毒副产物风险是饮用水研究中一个关键而复杂的问题[8]。不同的水源水质在消毒时产生的消毒副产物种类和浓度也千差万别,因此,研究不同的水质因素在消毒过程中的变化规律、对消毒副产物产生的影响及其对控制消毒副产物的生成具有实际意义[9]。
本文以次氯酸钠作为消毒剂,针对不同水质特点,分析了2个水质差异较大的饮用水处理厂的余氯衰减规律。通过结合其他水质指标变化以及C-DBPs、N-DBPs的生成规律,探究不同水质对余氯衰减的影响,为长距离输水的消毒技术提供支持。
1 材料与方法
1.1 试验水源
试验水源分别来自2座原水和出厂水水质差异较大的水厂,在实际水厂清水池进水管的加氯点前取得未加氯消毒的水样进行试验。2座水厂的生产工艺皆为常规的臭氧活性炭深度处理工艺,原水及出厂水在夏季某月的平均水质对比如表1所示。

表1 水厂A、B原水及出厂水夏季水质Tab.1 Raw Water and Finished Water Quality of WTP A and WTP B in Summer
1.2 试验装置与方法
1.2.1 总余氯衰减
利用局部管段反应器进行总余氯衰减试验,主体管材为离心浇铸水泥内衬的球墨铸铁管(Ф=100 mm,L=200 mm),可容纳1.5 L水样,装置如图1所示。用环氧树脂胶将黑色不透光有机玻璃圆盘(Ф=120 mm)固定在球墨铸铁管底部,顶部加盖黑色有机玻璃盖,上盖带取样口(带橡胶塞),运行装置时完全密封避光,置于磁力搅拌器上。运行时调节温度为20 ℃,将磁力转子(聚四氟乙烯圆柱带节型,6 mm×20 mm)放在装置底部,启动搅拌器对水体施加动态扰动,进行总余氯衰减模拟试验。

图1 局部管段反应器示意图Fig.1 Schematic Diagram of Partial Section of Reactor
在水厂清水池进水管前取得未加氯消毒的水样,加入次氯酸钠,实验室模拟水厂消毒工艺,并避光静置2 h以模拟清水池停留时间,最后,将消毒静置后的水倒入局部管段反应器,模拟出厂水注入市政输配水管道。根据试验要求调节不同的初始余氯浓度C0,水样倒入局部管段反应器后开始计时。每隔一定时间测量相应的C-DBPs[如余氯和三氯甲烷(TCM)]、N-DBPs(如DCAN),以及其他水质指标[如浑浊度、总有机碳(TOC)、溶解性有机氮(DON)]。选择一级衰减模型进行拟合总余氯衰减数据,如式(1)。
Ct=C0e-kt
(1)
其中:t——发生反应的时间,h;
Ct——反应发生时间t后对应的余氯浓度,mg/L;
C0——初始余氯浓度,mg/L;
k——总余氯衰减系数,h-1。
k由主体水余氯衰减系数kb、管壁余氯衰减系数kw、传质系数kf组成,关系如式(2)~式(3)[10]。
(2)
(3)
其中:kb——主体水余氯衰减系数,h-1;
kw——管壁余氯衰减系数,h-1;
kf——传质系数,m/d;
Re——雷诺数,Re=vd/u;
Sc——施密特数,Sc=u/D;
v——流速,m/s;
d——管径,m;
rh——水力半径,m,rh=d/4;
u——运动黏滞系数,20 ℃时为0.09 m2/d;
D——扩散系数,经验值为0.1×10-3m2/d。
1.2.2 主体水余氯衰减
设置静态试验,在与总余氯衰减试验容积相同的棕色密闭有机玻璃容器里进行主体水余氯衰减试验。同样选择一级模型来拟合主体水衰减数据,如式(4)。
Ct=C0e-kbt
(4)
1.2.3 管壁余氯衰减
目前,国内外还没有直接测得管壁衰减系数的方法。因此,在本试验中通过实际试验测得k和kb,由式(2)推算得到kw。
1.3 试验仪器与检测方法
各项指标检测方法如下:水样取出后立即采用便携式余氯仪(哈希,PCII)测定其中的游离氯浓度;TCM和DCAN浓度采用气相色谱仪(安捷伦7890B)测定; TOC采用TOC分析仪(岛津,TOC-VCPH)测定;水样经过0.45 μm滤膜过滤后使用差减法测定DON,计算如式(5)。
(5)
2 结果与讨论
2.1 2座水厂原水及出厂水水质分析
由表1可知,水厂A原水与出厂水的浑浊度、CODMn、TOC、细菌总数均高于水厂B。水厂B的原水浑浊度仅为水厂A的21.6%,出厂水浑浊度为水厂A的62.5%;原水CODMn仅为水厂A的31.5%,出厂水CODMn为水厂A的63.3%;原水TOC仅为水厂A的58.2%,出厂水TOC为水厂A的66.6%;原水菌落总数仅为水厂A的9.1%,水厂B的出厂水菌落总数为未检出,而水厂A月均检出12 CFU/mL。CODMn能反映水中受还原性物质污染的程度,浑浊度的高低反映水中其他物质含量。此外,TOC是表征饮用水中有机物含量的重要参数,菌落总数也是反映有机物污染程度的指标。分析可知,水厂A还原性物质及有机污染物含量更高,原水水质相差尤为明显,与水厂B水质相差较大,水厂B水质整体优于水厂A。
2.2 不同水质下的余氯衰减情况
2.2.1 总余氯衰减
我国《生活饮用水卫生标准》(GB 5749—2006)中规定,出水厂的余氯含量不低于0.3 mg/L,且不超过4 mg/L[11]。故设置了3个试验组,C0分别为1、2、3 mg/L左右。水厂A试验温度为26 ℃,各管道实测得的C0分别为1.08、1.95 mg/L和2.91 mg/L;水厂B试验温度为25 ℃,各管道实测得的C0分别为1.14、2.07 mg/L和2.86 mg/L。在不同C0条件下,局部管段器中的总余氯衰减曲线如图2所示。

图2 不同C0下的总余氯衰减及拟合曲线 (a) 水厂A;(b) 水厂BFig.2 Total Residual Chlorine Decay and Fitting Curves under Different C0 (a) WTP A; (b) WTP B
由余氯测定结果可知,随着C0依次升高,A水厂的k分别为0.360、0.161、0.086 h-1;B水厂的k分别为0.342、0.138、0.063 h-1。即总余氯衰减速率与C0呈负相关关系,且水质越差的水体总余氯衰减速率越大。研究[12]认为,余氯浓度过低时余氯会优先与水中还原性较强的物质迅速发生反应,导致余氯衰减较快;余氯浓度较高时,会导致余氯在水中同时发生2种不同速率的反应,包括快速反应和慢速反应,因此,速率会比低初始氯浓度时要慢。
通过拟合结果中2个水厂的总衰减系数(表2)可知,水厂A的C0从0.97 mg/L增至1.95 mg/L时,k减少了44.7%,当C0继续增至2.91 mg/L时,总余氯衰减速率减少了53.4%;水厂B的C0从1.14 mg/L增至2.07 mg/L时,k减少了40.3%,当C0继续增至2.86 mg/L时,总余氯衰减速率减少了45.6%。数据表明,在水质更差的水体中随着余氯浓度的升高,总余氯衰减速率的降幅变大。由于水质更差的水体中含有的与余氯发生快反应的还原性物质及有机物更多,初始氯浓度越低时,与之反应的速率越快,降幅也越大。
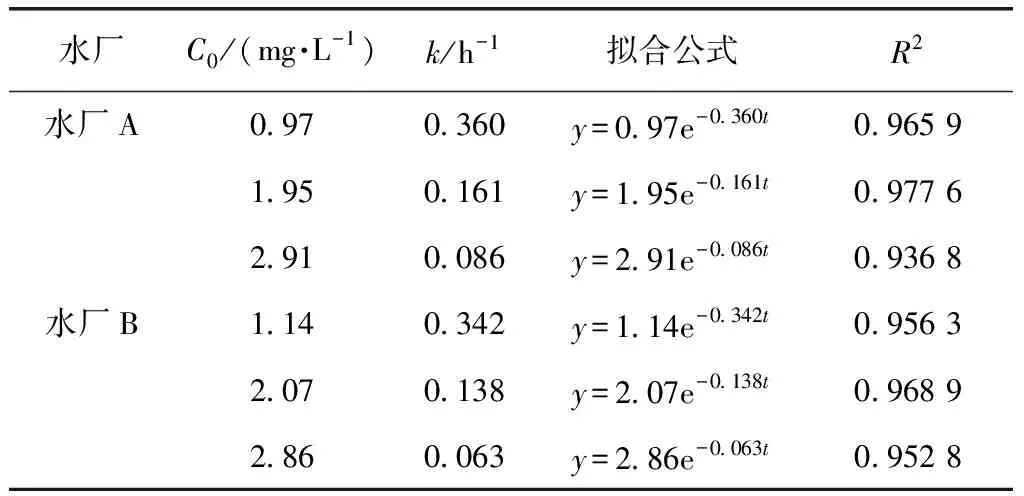
表2 水厂A、B在不同C0下的总余氯衰减拟合结果Tab.2 Fitting Results of Total Residual Chlorine Decay for WTP A and WTP B under Different C0
2.2.2 主体水及管壁余氯衰减
2个水厂的kb及kw如表3所示,可余氯衰减受主体水反应和管壁反应的双重作用。kb、kw随C0的变化规律与k一致,即衰减速率皆随着C0的增大而减小。同时,kw占比也随着余氯浓度的增大而减小,表明余氯浓度会影响管壁对余氯衰减的作用。此外,水质越差的水体kb越大,kw则与之相反。在水质好的水厂B水体中的管壁衰减速率比水质差的A水厂水体中大,表明水质也会影响管壁对余氯衰减的作用,即在水质越好的水体中,管壁反应对余氯衰减的作用就越大。由此可知,尽管主体水反应在余氯衰减中占主要作用,但余氯与管壁物质的反应及其在管壁的传质扩散作用也很重要。

表3 水厂A、B在不同C0下的主体水衰减拟合结果 及管壁衰减系数结果Tab.3 Fitting Results of Main Part and Pipe Wall Chlorine Decay for WTP A and WTP B under Different C0
2.3 C-DBPs、N-DBPs变化规律
2.3.1 DCAN变化规律
如图3所示,水质差的水厂A水体的DCAN增长速率、总生成量皆高于水质好的水厂B。在C0为2~3 mg/L水体中DCAN总生成量的相差值比1~2 mg/L水体的小,且C0约为2、3 mg/L时,水质差的水体中DCAN总生成量的相差值比水质好的水体大。由于在高浓度的投加氯下,水体中发生反应的有机物少,有机前驱物与氯的反应已较完全,对DCAN生成量的影响开始减弱,且水质好的水体有机物含量更少。因此,减弱DCAN生成量的影响程度比水质差的水体更大。

图3 不同C0下的DCAN变化规律 (a) 水厂A;(b) 水厂BFig.3 Changes of DCAN under Different C0 (a) WTP A;(b) WTP B
试验发现,在2种不同水质的水体下,DCAN生成量累积到一定程度后,均出现降低趋势(图3)。这是因为球墨铸铁材质的局部管段试验装置中存在的各种形态铁,在反应后期促进管道中生成的DCAN发生消解[13-14]。水厂A水体中的DCAN在反应发生后的4、12、34 h才开始降解; 水厂B水体中DCAN持续增加的时间较长,分别在8、30、40 h后才开始发生降解。这与其较慢的总余氯衰减速率有关,使其管道水中余氯浓度一直较高,不断与水中剩余有机物缓慢反应生成DCAN。
2.3.2 TCM变化规律
水厂A在C0逐渐升高时TCM的最终生成量分别为10.29、18.56、25.46 μg/L;水厂B在C0逐渐升高时TCM的最终生成量分别为6.31、11.21、14.48 μg/L。由图4可知,TCM生成量随着C0的增加而增加,且在反应开始时生成速率较高,而后生成速率变慢至逐渐平稳。当C0由1 mg/L增至2 mg/L左右时,水厂A和水厂B的TCM总生成量均大幅增加,分别增加了80%和77%;当C0由2 mg/L增至3 mg/L左右时,水厂A和水厂B的TCM总生成量分别增加了37%和29%。由此可知,随着氯浓度升高,水质差的水体TCM总生成量增加的幅度大于水质好的水体。在低氯浓度时,氯浓度的升高对TCM生成量的影响更显著,这与先前DCAN的变化规律一致。
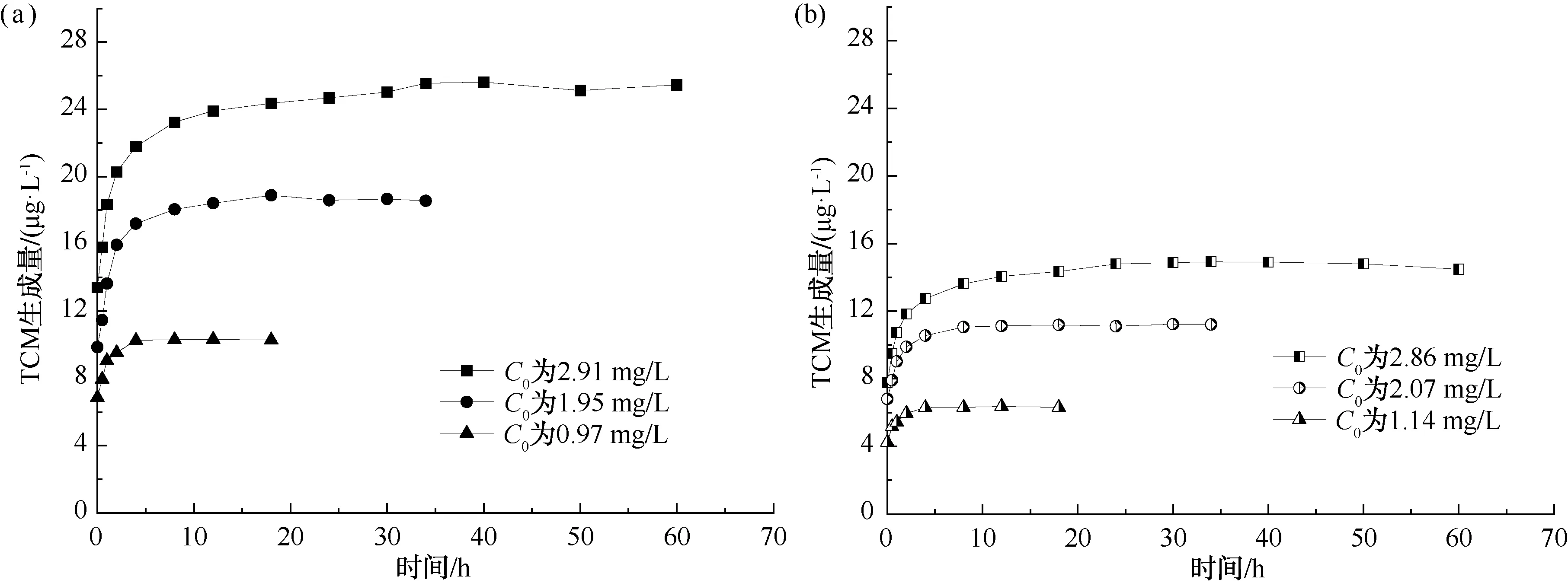
图4 不同C0下的TCM变化规律 (a) 水厂A;(b) 水厂BFig.4 Changes of TCM under Different C0 (a) WTP A;(b) WTP B
2.4 其他水质变化规律
2.4.1 浑浊度
由图5可知,2个水厂的C0对浑浊度影响都不大,3组不同C0的试验均表现为反应1 h内管内浑浊度激增,而后有所下降,随着反应进行保持不动或在一定范围内稳定波动。在反应刚开始,由于存在突然扰动的水流作用,浑浊度会突升。待水流稳定后,部分水中的颗粒物下沉,浑浊度随之下降,最后趋于稳定。此外,C0为3 mg/L左右的高浓度试验组在试验进行约12 h后,浑浊度有轻微上升的现象,且水厂B上升趋势更明显。可能是由于高浓度余氯对球墨铸铁管内壁的腐蚀作用更大,会有腐蚀产物生成并释放到水体中,使浑浊度略微升高。而水质好的水体中提供给管壁反应的余氯浓度也更充足,因此,浑浊度上升得更高。实际管道的内壁管垢及腐蚀瘤更为严重,对浑浊度影响较大,尤其在高余氯浓度时,由于氯的溶蚀作用,会导致管壁释放更多腐蚀产物至水体中,使得浑浊度上升。因此,对于使用时间较长的球墨铸铁管管网,余氯浓度不宜过高。

图5 不同C0下的浑浊度变化规律 (a) 水厂A;(b) 水厂BFig.5 Changes of Turbidity under Different C0 (a) WTP A;(b) WTP B
2.4.2 TOC与DON
TOC和DON都是表征饮用水中有机物含量的重要参数。如图6、图7所示,两个有机物指标浓度变化规律相似,C0越高,消耗水体中的有机物越多,进入管道时的TOC和DON浓度就越低。前5 h,相较于高C0组,低C0组的TOC和DON下降速率较慢,随后在一定范围内波动。高C0组在之后的变化呈先升高后稳定的趋势,其原因与浑浊度变化相同。

图6 不同C0下的TOC变化规律 (a) 水厂A;(b) 水厂BFig.6 Changes of TOC under Different C0 (a) WTP A;(b) WTP B

图7 不同C0下的DON变化规律 (a) 水厂A;(b) 水厂BFig.7 Changes of DON under Different C0 (a) WTP A;(b) WTP B
另外,Liu等[15]研究表明,水中THMs和DCAN的生成势与水中TOC和DON的值呈线性相关关系,即TOC和DON的值在一定程度上可反映水中THMs和DCAN消毒副产物的生成趋势。水厂A的TOC和DON浓度整体水平比水厂B高,这与它较大的TCM和DCAN生成量相对应,即水质差的水体由于拥有较高浓度的含氮和含碳有机物,会生成更多的TCM和DCAN。因此,TOC和DON可作为C-DBPs和N-DBPs的主要前驱物,这与宝露尔等[6]的研究相一致。
3 结论
(1)水厂A、B原水及出厂水水质相差较大,水厂A含氮和含碳有机物更多,水质更差。
(2)水厂A的C0从0.97 mg/L增至1.95 mg/L时,k减少了44.7%,当C0继续增至2.91 mg/L时,k减少了53.4%;水厂B的C0从1.14 mg/L增至2.07 mg/L时,k减少了40.3%,当C0继续增至2.86 mg/L时,k减少了45.6%。此外,不论何种水质,氯浓度与总余氯衰减速率皆呈负相关关系,且随着C0的升高,水质差的水体中k的降幅也更大。kb、kw随C0的变化规律与k一致,且水质越差kb越大,kw则与之相反;虽主体水反应在余氯衰减中占主要作用,但余氯与管壁物质的反应及其在管壁的传质扩散作用仍需重视。
(3)水质差的水厂A水体的DCAN、TCM的增长速率及总生成量皆高于水质好的水厂B。且在低氯浓度时,氯浓度的升高对2种消毒副产物生成量的影响更显著。此外,对于2种不同水质的水体,DCAN生成量累积到一定程度后,均出现降低趋势,且水厂A发生DCAN降解的时间早于水厂B,在反应发生后的4、12、34 h才开始降解,而水厂B分别在8、30、40 h后才开始发生降解。
(4)浑浊度在反应1 h内突增,而后有所下降,随反应进行保持不动或在一定范围内稳定波动。在初始浓度较高时,浑浊度、TOC和DON变化规律类似,由于高浓度余氯会对管壁产生腐蚀作用,均在一段时间后出现短暂的升高趋势,而后变得稳定。水质差的水厂A中TOC和DON浓度整体水平比水厂B高,这是导致TCM和DCAN生成量较大的原因。因此,可将TOC和DON作为C-DBPs和N-DBPs的主要前驱物。

