小儿柴胡退热栓的制备及质量标准研究*
王莉博,刘泽干,雷 攀,黄良永,叶 方,黄小凤,王淑慧,杜士明△
(1. 湖北医药学院药学院,湖北 十堰 442000; 2. 湖北医药学院附属太和医院,湖北 十堰 442000;3. 武当特色中药研究湖北省重点实验室·湖北医药学院,湖北 十堰 442000)
中药柴胡为传统解表药材,是伞形科植物柴胡Bupleurum chinense DC. 或狭叶柴胡 Bupleurum scorzonerifolium Willd. 的干燥根[1],具有解表退热、升举阳气、疏肝解郁功效,主要用于治疗感冒发热、寒热往来、胸胁胀痛、月经不调、子宫脱垂、脱肛等[2-3]。现代药理学研究表明,柴胡的主要药效成分有柴胡挥发油、柴胡皂苷等,有解热、抗炎、保肝、抗菌、抗病毒、抗肿瘤、调节免疫功能等作用。其中,柴胡挥发油是其解热作用的主要活性成分,效果确切,作用温和[4]。近年来以其为主要药效成分研发了多种新制剂[5],其中柴胡注射剂作为中药西制的代表品种,研制于20 世纪40 年代,用于治疗流行性感冒、回归热、肺结核发展期的发热等症状,但不良事件频发[6-7],国家药品监督管理局于2018 年5 月发布《关于修订柴胡注射液说明书的公告》,限制其用于儿童。本课题组在柴胡注射液制备工艺基础上进行了剂型改造,直肠(栓剂)给药成为简便、安全的替代途径。栓剂为传统给药剂型,可有效避免使用注射剂引起的局部疼痛和口服制剂的肝脏首过效应,同时能减少透皮贴剂用药的个体差异,安全性高,患者依从性好[8-9],是儿童用药较理想的剂型。基于此,本课题组采用水蒸气蒸馏法提取柴胡挥发油并通过β-环糊精进行包合,采用熔融法制备小儿柴胡退热栓,依据2015 年版《中国药典(四部)》制剂通则0107 栓剂项下质量检查要求制订其质量标准,为后续药效学研究和临床应用提供理论基础。现报道如下。
1 仪器与试药
1.1 仪器
GC-MS-TQ8040 型气相色谱-质谱联用仪(日本Shimadzu 公司);TU-1901 型紫外-可见分光光度仪(北京普析通用仪器有限责任公司);RBY-IV 型融变时限检查仪(天津天大仪器有限公司);KPL-10 子弹型栓剂模具(长沙益广制药机械有限公司);DF-101S 型恒温加热磁力搅拌器(河南予华仪器有限公司);YP1002N 型电子天平(上海菁海仪器有限公司);PTHW型电热套(郑州市煜城仪器有限公司)。
1.2 试药
柴胡饮片(湖北神农本草中药饮片有限公司,批号为20190301),经湖北医药学院附属太和医院杜士明教授鉴定为伞形科柴胡属植物北柴胡Bupleurum chinense DC. 的干燥根;正己烷、正己醛、正庚醛均为色谱纯,均购于上海麦克林试剂公司;β-环糊精(国药集团化学试剂有限公司,批号为20180613);半饱和脂肪酸甘油酯(湖北远成赛创科技有限公司,批号为20160426);甲醇(武汉市中天化工有限责任公司,批号为20181009);药用级氯化钠(陕西正一药用辅料有限公司,批号为20190910);水为纯化水(自制)。
2 方法与结果
2.1 样品制备
2.1.1 柴胡挥发油提取工艺优化
取柴胡饮片500 g,加入10%氯化钠溶液中浸泡,采用水蒸气蒸馏法提取柴胡挥发油[10](保持100 ℃左右,避免暴沸),收集初馏液,重蒸馏,得柴胡挥发油精提液250 mL,备用。取挥发油精提液1 mL,用甲醇定容至10 mL,采用紫外分光光度法[11]测定挥发油精提液的吸光度( A1),并作为评价指标,以料液比(因素A)、浸泡时间(因素B)、提取时间(因素C)为考察因素,考察影响柴胡挥发油提取率的主要因素[12],采用L9(34)正交试验优化柴胡挥发油提取工艺。详见表1 至表3。可见,各因素对挥发油提取工艺影响大小顺序为A >C >B,3 个因素对挥发油提取工艺均有显著影响。综合以上试验结果,确定最佳提取工艺为A1B2C2,即料液比为1 ∶10(g ∶mL),浸泡8 h,提取2.0 h。
2.1.2 柴胡挥发油包合工艺优化
取柴胡挥发油精提液250 mL(其吸光度记为A2),置具塞锥形瓶中,加入适量β-环糊精,在恒温水浴磁力搅拌条件下包合,室温冷却后,在2 ~8 ℃条件下静置12 h,抽滤干燥,即得柴胡挥发油包合物,将包合物置250 mL 圆底烧瓶中,加100 mL 10%氯化钠溶液溶解,采用水蒸气蒸馏法加热使之微沸,保持1 h,收集30 mL溶液,测定吸光度(A3)。计算挥发油的包合率[包合率=A3/(A2×空白回收率)×100% ]。在单因素试验结果的基础上选取环糊精用量(因素A)、包合温度(因素B)、包合时间(因素C)为考察因素[13],以包合率为考察指标,采用L9(34)正交试验优化柴胡挥发油包合工艺。结果见表1 至3。可见,柴胡挥发油包合率的3 个因素的影响强弱为A >B >C,因素A、因素B 对挥发油包合工艺有显著影响。综合以上结果,确定最佳包合工艺为A3B3C2,即β-环糊精用量为60 g,在50 ℃条件下,包合2 h。

表1 柴胡挥发油提取、包合工艺正交试验因素水平表Tab.1 Factors and levels of the orthogonal test for extraction and inclusion process of volatile oil from Bupleurum chinense

表2 柴胡挥发油提取、包合工艺正交试验设计与结果(n =9)Tab.2 Results and design of the orthogonal test for extraction and inclusion process of volatile oil from Bupleurum chinense(n =9)

表3 柴胡挥发油提取、包合工艺正交试验方差分析结果Tab.3 Analysis of variance for extraction and inclusion process of volatile oil from Bupleurum chinense by the orthogonal test
2.1.3 小儿柴胡退热栓制备
取柴胡饮片500 g,加入10 倍量10%氯化钠溶液中浸泡8.0 h,采用水蒸气蒸馏法提取柴胡挥发油(保持约100 ℃,避免暴沸),提取2.0 h,收集初馏液,重蒸馏,得柴胡挥发油精馏液250 mL。柴胡挥发油精馏液中加入β-环糊精50 g,于50 ℃恒温水浴磁力搅拌条件下包合2 h,冷却至室温后,置2 ~8 ℃条件下静置12 h,抽滤干燥得柴胡挥发油包合物。取半饱和脂肪酸甘油酯75 g,置烧杯中,于50 ℃水浴中搅拌至熔融,加入柴胡挥发油包合物,搅拌均匀,保持流体状,注入栓模中,室温放置30 min,取栓,即得小儿柴胡退热栓100 粒(每粒质量为1.14 g)。共制5 批,批号分别为202008031,202008032,202008041,202008042,202008043。
2.2 质量标准研究[14-15]
2.2.1 质量检查
性状:在黑色背景、日光条件下观察,小儿柴胡退热栓呈乳白色子弹型,色泽均匀、一致,表面光滑、完整、细腻,室温下成型性较好,无软化、变形或开裂现象。
鉴别反应:取样品5 枚,置250 mL 圆底烧瓶中,加入100 mL 10%氯化钠溶液,采用水蒸气蒸馏法蒸馏后精馏,取精馏液2 mL,加品红亚硫酸试液2 滴,摇匀,放置5 min 后,溶液显玫红色。
质量差异考察:每批次栓剂样品中随机取10 粒,精密称定每粒质量,计算总质量及平均质量,结果见表4。总体平均质量为(1.136±0.034)g,符合2015 年版《中国药典》对栓剂的质量差异限度要求。

表4 质量差异考察结果(g,n =10)Tab.4 Investigation results of quality difference(g,n =10)
融变时限考察:每批次栓剂样品中随机取3 粒,室温放置1 h 后,置温度为(37±0.5)℃融变时限检测仪中检测,结果见表5。平均融变时间为(18.2±0.47)min,符合2015 年版《中国药典》脂溶性基质栓剂在30 min内全部溶解或软化的融变时限限度要求。
小时不识月,呼作白玉盘。又疑瑶台镜,飞在青云端。仙人垂两足,桂树何团团。白兔捣药成,问言与谁餐?蟾蜍蚀圆影,大明夜已残。羿昔落九乌,天人清且安。阴精此沦惑,去去不足观。忧来其如何?凄怆摧心肝。(李白《古朗月行》)
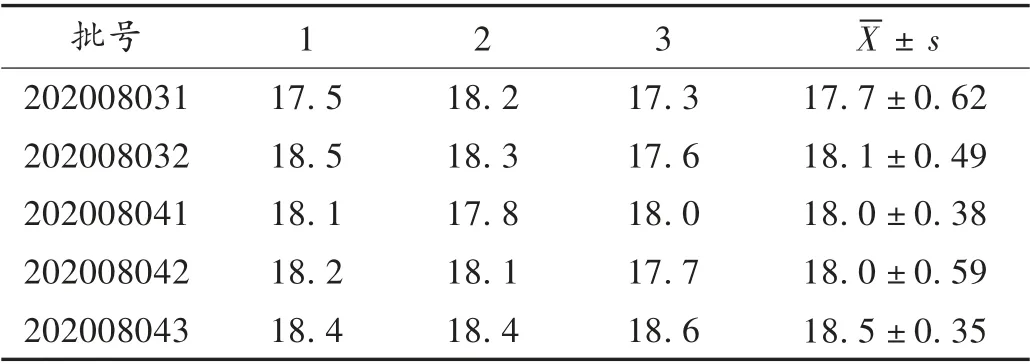
表5 融变时限考察结果(min,n =3)Tab.5 Results of time-limited melting(min,n =3)
微生物限度:依据2015 年版《中国药典》微生物检测限定方法,采用平皿法检查小儿柴胡退热栓微生物限度。结果5 批检测样品中均未检出金黄色葡萄球菌、铜绿假单胞菌等致病菌,检查结果符合非无菌产品微生物限度标准规定。
2.2.2 正己醛及正庚醛含量测定[16-17]
1)试验条件
气相色谱条件:色谱柱为SH-Rtx-Wax 毛细管色谱柱(30 m×0.25 mm,0.25 μm);载气为氦气;进样口温度为230 ℃;分流比为10 ∶1;流速为1 mL/min。程序升温,色谱柱初始温为60 ℃、保持2 min,以20 ℃/min的速率升温至140 ℃、保持3 min,再以15 ℃/min 的速率升温至180 ℃、保持4 min,最后以10 ℃/min 的速率升温至230 ℃、保持4 min。
质谱条件:接口温度为230 ℃,离子源温度为230 ℃,离子源电压为70 eV,进样量为1.0 μL,质量扫描范围m/ z 为45 ~300,溶剂峰切除时间为3 min,质谱检测起测时间为2.5 min,数据采集模式为Q3Scan。
2)溶液制备
分别称取正己醛、正庚醛对照品适量,精密称定,置10mL 容量瓶中,加入正己烷,制成含正己醛9.900mg/mL、正庚醛7.840 mg/mL 的混合对照品溶液。分别取3 批(批号为202008041,202008042,202008043)小儿柴胡退热栓各10 粒,精密称定,置250 mL 圆底烧瓶中,加入10%氯化钠溶液100 mL,加热蒸馏,收集前蒸馏液30 mL,用20 mL 正己烷分2 次萃取,合并萃取液,加入适量无水硫酸钠去除正己烷溶液中的水分,密封保存,滤过,滤液置50 mL 容量瓶中,加正己烷定容,即得供试品溶液。取10 粒空白栓,置250 mL 圆底烧瓶中,按供试品溶液制备方法制得阴性对照品溶液。
3)方法学考察
专属性试验:取混合对照品溶液、供试品溶液及阴性对照品溶液,按拟订试验条件进样。结果质谱图中基质和杂质无干扰,专属性良好,质谱条件符合要求。详见图1。

图1 质谱图Fig.1 Mass spectrum
线性关系考察:取混合对照品溶液,分别稀释成含正己醛99.00,49.50,24.75,12.38,6.19 μg/mL 和含正庚醛78.40,39.20,19.60,9.80,4.90 μg/mL 的系列混合对照品溶液,按GC-MS 检测条件分别进样1 μL。以质量浓度(X,μg/mL)为横坐标、相对峰面积( Y)为纵坐标进行线性回归,得正己醛回归方程 Y1=56 862 X1+42 431(r =0.998,n =5),正庚醛回归方 程 Y2=28361X2+75846(r =0.998,n =5)。结果表明,正己醛、正庚醛质量浓度分别在6.19 ~99.00 μg/mL 和4.90 ~78.40 μg/mL 范围内与相对峰面积线性关系良好。
检测限和定量限:取混合对照品溶液,逐级稀释,按拟订试验条件进样,记录质谱图。以信噪比(S / N)为3 ∶1 和10 ∶1 分别计算检测限和定量限。结果正己醛和正庚醛的检测限分别为1.23 μg/mL 和1.51 μg/mL,定量限分别为2.05 μg/mL 和2.51 μg/mL。
精密度试验:取正己醛和正庚醛质量浓度分别为24.75μg/mL 和19.60μg/mL 的混合对照品溶液,按拟订试验条件连续进样6 次。结果正己醛和正庚醛峰面积的RSD 分别为1.26%,0.78%(n =6),表明仪器精密度良好。
稳定性试验:取“溶液制备”项下供试品溶液(批号为202008041),按拟订试验条件分别于0,2,4,6,8 h 时进样。结果正己醛和正庚醛峰面积的RSD 分别为2.82%,1.58%(n =5),表明供试品溶液8 h 内稳定性良好。
重复性试验:取样品(批号为202008032)6 份,依法制备正己醛和正庚醛供试品溶液,平行制备6 份,按拟订试验条件连续进样。结果正己醛和正庚醛峰面积的RSD 分别为1.35%,2.32%(n =6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号为202008041)5 粒,平行6 份,分别精密加入样品原有量80%,100%,120%的正己醛、正庚醛对照品,依法制备供试品溶液,按拟订试验条件进样测定,计算回收率。结果见表6。
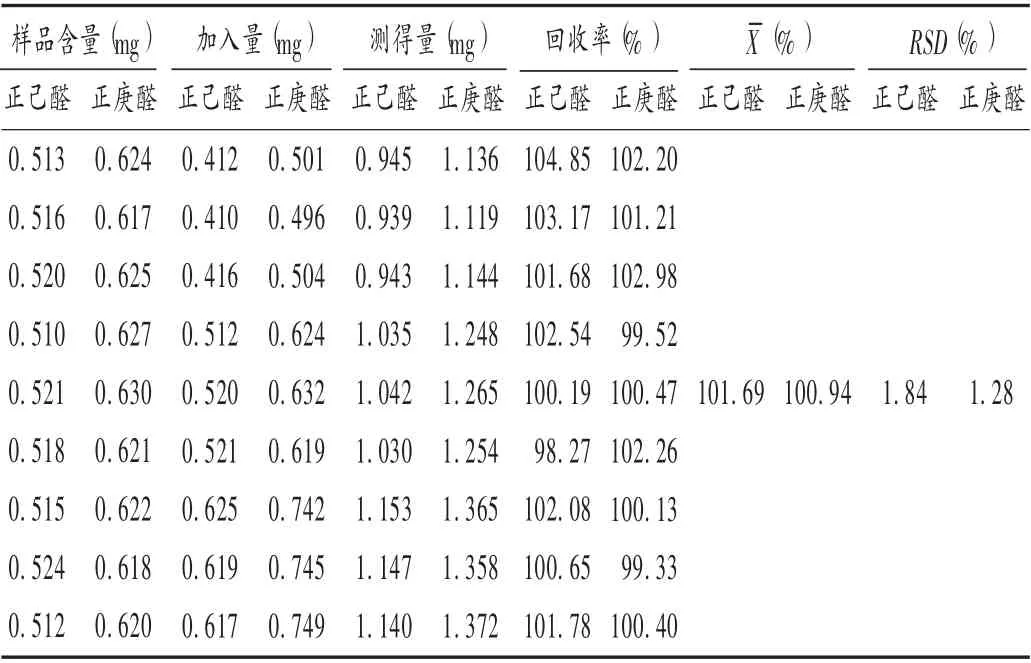
表6 加样回收试验结果(n =9)Tab.6 Results of the recovery test(n =9)
4)样品含量测定
取3 批样品各10 粒,依法制备供试品溶液,按拟订试验条件分别进样测定。结果见表7。

表7 样品含量测定结果(mg,n =3)Tab.7 Content determination of n-hexanal and n-heptanaldehyde in the sample(mg,n =3)
3 讨论
3.1 栓剂制备工艺优化
柴胡药材中的挥发油含量较低,且柴胡挥发油在室温条件下易挥发。预试验中按2015 年版《中国药典(四部)》挥发油测定“甲法”提取挥发油,并结合有机溶剂萃取方法,均无法得到纯挥发油。陈文露等[10]通过水蒸气蒸馏法得到挥发油精馏液,进一步制备柴胡注射液。本试验中主要参考此工艺以挥发油精馏液吸光度为指标,优选最佳提取工艺条件,并通过验证试验发现吸光度值较稳定,此提取工艺稳定可行;β-环糊精水溶性好,空腔尺寸适中,其包合药物后可提高有效成分在制备及储藏过程中的稳定性[18-19],因此本研究中用β-环糊精对挥发油精馏液进行包合,以包合率为指标,优选最佳包合工艺条件;而栓剂制备过程中,通过对其成型温度(40,50,60 ℃)及脱模时间(20,30,40 min)进行考察。结果显示,温度为50 ℃时栓剂成型性较好,色泽均匀,冷却30 min 后脱模的栓剂表面光滑、细腻。
3.2 栓剂含量测定指标选择
试验前期,工艺优化主要采用紫外-可见分光光度法测定柴胡挥发油吸光度,简便、易操作,但用于含量测定可能会存在一定误差。柴胡挥发油的主要有效成分为正己醛、正庚醛等,正己醛、正庚醛可能是其主要解热、抗炎有效成分[16-17],因此选择这2 种成分为指标,采用GC-MS 法测定其含量。试验结果表明,制备的栓剂性状、质量差异、融变时限等均符合2015 年版《中国药典》对栓剂质量标准的要求,GC-MS 法测定3 批样品中正己醛和正庚醛最低平均含量分别为1.015 mg 和1.145 mg,因此设定小儿柴胡退热栓中正己醛含量不得低于每粒0.081 mg,正庚醛含量不得低于每粒0.092 mg。
3.3 方法评价
本课题在中医药理论的指导下,参考相关文献,并结合现代研发技术对小儿柴胡退热栓的制备及质量标准进行研究,保证了本品的制备工艺合理、可行。但制备的小儿柴胡退热栓与已上市的其他柴胡制剂的生物等效性有待进一步研究。课题组下一步将对其药效学展开研究,以保证小儿柴胡退热栓相关研究的完整性。

