原位合成铜基金属有机框架差分脉冲伏安法快速检测肉制品中亚硝酸盐
徐艺伟,朱 丹,石吉勇,张 文,王 鑫,刘 超,李文亭,邹小波
(江苏大学食品与生物工程学院,江苏 镇江 212013)
亚硝酸盐作为食品添加剂,被广泛应用于培根、火腿和香肠等肉制品中,具有发色、防腐和增强风味的作用[1]。亚硝酸盐被人体摄入,在胃酸环境中,能够与体内的胺类物质作用,生成亚硝基化合物[2],该化合物是强致癌物质[3]。当亚硝酸盐经消化道吸收进入血液,能够将低铁血红蛋白氧化为高铁血红蛋白,降低血红蛋白运输和释放氧的功能,导致组织缺氧,形成高铁血红蛋白血症[4]。国内外对于肉制品中亚硝酸盐的含量都有严格限制,亚硝酸盐含量是肉制品卫生检疫中必检项目。因此,开发肉制品中亚硝酸盐的快速检测方法,对于保障消费者食用安全具有重要意义。
食品中亚硝酸盐检测方法主要有分光光度法[5]、色谱法[6]、毛细管电泳法[7]、电化学法等[8]。其中,电化学方法具有设备便携、操作简单、响应速度快等优势[9],在亚硝酸盐检测中具有广阔的应用前景[10]。NO-2中的氮原子化合价为正3价的中间价态,既有还原性又具备强氧化性,能够在电位作用的同时,在电极表面发生电子转移[11]。在低电位作用时,NO-2可以获得电子,发生还原反应生成NO;在高电位作用时,NO-2将失去电子,发生氧化反应生成NO2[12]。依据电子转移所产生的电流信号,可实现NO-2浓度的测定[13]。基于NO-2的反应原理,在电极表面修饰具有催化NO-2氧化或还原的功能性材料,可有效增强电流信号,提高传感器的灵敏度[14]。辣根过氧化物酶可催化NO-2氧化,常被用于开发电化学传感器[15]。然而,由于酶的生物属性,这些传感器的性能往往受到酶活性和稳定性的限制[16]。
金属-有机骨架材料(metal-organic frameworks,MOFs)是金属离子与有机配体通过自组装形成的具有三维结构的晶体材料[17]。近年来,MOFs材料被发现具有模拟酶活性[18],与天然酶相比具备许多独特优势,如催化性能稳定、不易失活、成本低廉、易保存等[19]。MOFs材料的合成方法主要包括水热法、机械法、扩散法、微波辅助法以及电化学法等[20]。其中电化学合成法能够在电极表面原位生成目标产物[21],无需使用黏合剂固定,方便用于电化学传感器的构建[22]。
本实验通过电化学法原位合成铜基金属有机框架(Cu-based metal organic frameworks,Cu-MOFs),制备用于肉制品中亚硝酸盐检测的电化学传感器。首先,采用电沉积方法在玻碳电极(glassy carbon electrode,GCE)表面修饰1 层致密且均匀的铜膜;然后,利用碱性氧化作用,将电极表面的铜转化为Cu(OH)2;最后,使用交联剂将Cu(OH)2转化为Cu-MOFs。电化学原位合成方法制备Cu-MOFs具有反应速度快、反应条件温和、化学试剂消耗少等优势。Cu-MOFs能够催化NO-2氧化,可有效增强NO-2的电流信号。
1 材料与方法
1.1 材料与试剂
硫酸铜、硫酸铵、过硫酸铵、氢氧化钠、无水乙醇、1,3,5-苯三甲酸(1,3,5-benzenetricarboxylic acid,H3BTC)、磷酸钠、磷酸氢二钠、铁氰化钾、三水亚铁氰化钾等试剂(均为分析纯) 国药集团化学试剂有限公司;亚硝酸盐标准溶液(质量浓度100 mg/L) 上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
CHI600D电化学工作站、GCE(直径3 mm)、Ag/AgCl电极、铂丝电极 上海辰华仪器有限公司;JSM-7001F场发射扫描电子显微镜 日本Jeol公司;BSA224S-CW分析天平 德国Sartorius公司;微量移液器 德国Eppendorf公司;KQ-100KDE型超声清洗器昆山市超声仪器有限公司。
1.3 方法
1.3.1 电化学传感器制备
电极预处理:将GCE依次用粒径为1.00、0.30、0.05 μm的氧化铝粉末,在抛光绒布上抛光呈镜面,然后在无水乙醇和去离子水中分别超声处理5 min清除残留的氧化铝,并用氮气吹干备用。
电沉积制备Cu/GCE[23]:分别称取0.000 1 mol的硫酸铜和0.005 mol的硫酸铵放入同一烧杯中,加入10 mL的水溶解,配制电解质溶液。将预处理的GCE作为工作电极,浸入10 mL已经配制好的电解质溶液中,在-0.3 V(vsAg/AgCl)的恒电位中保持400 s。在该过程中,溶液中的铜离子在电位作用时被还原为铜单质而沉积在电极表面,形成1 层均匀、致密且附着性好的铜膜,由此获得Cu/GCE。
Cu/GCE转变为Cu(OH)2/GCE[24]:将Cu/GCE浸入浓度3 mol/L的氢氧化钠溶液,并施加0.2 mA的恒定电流保持180 s。在该过程中,电极表面的铜在碱性氧化作用中转变为Cu(OH)2,获得Cu(OH)2/GCE。
Cu(OH)2/GCE转变为Cu-MOFs/GCE[25]:称取0.1 g的H3BTC与4.7 mL无水乙醇和1.8 mL的去离子水混合,超声处理5 min,配制交联剂溶液。将Cu(OH)2/GCE浸入到交联剂溶液中保持240 s,电极表面的Cu(OH)2在交联剂H3BTC的作用中转变为Cu-MOFs,获得Cu-MOFs/GCE。
1.3.2 电化学检测NO-2
通过差分脉冲伏安法(differential pulse voltammetry,DPV),以0.1 mol/L的磷酸缓冲溶液(pH 7)为电解质,获得NO2-的电流信号[26]。DPV参数:初始电位0.3 V,终止电位1.2 V,步进电位5 mV,振幅0.05 V,脉冲宽度0.05 s,采样宽度0.016 7 s,脉冲周期0.05 s。
采用循环伏安(cyclic voltammetry,CV)法分别设置不同的扫描速率(20、40、60、80、100 mV/s),观察NO-2在Cu-MOFs/GCE表面的电化学行为。CV电位范围为0.3~1.2 V,NO2-的浓度为100 μmol/L,电解质为0.1 mol/L的磷酸缓冲溶液(pH 7)。
1.3.3 电极的选择性和稳定性
选择食品中常见的离子(包括Na+、K+、Ca2+、作为干扰物质代表。分别取上述离子1 mmol/L加入到100 μmol/L的NO-2溶液中,使用Cu-MOFs/GCE,通过DPV法获得伏安曲线,以NO-2的氧化峰电流强度为指标,评估Cu-MOFs/GCE的选择性及抗干扰能力。
为了考察Cu-MOFs/GCE的稳定性,将制备的Cu-MOFs/GCE置于密闭环境中,在25 ℃左右的室温保存,并使用该电极对100 μmol/L的NO-2进行检测,连续7 d记录每天获得的伏安曲线。
1.3.4 肉制品检测
购买培根、火腿肠、酱牛肉和猪肉脯共4 种常见肉制品作为待测样品。首先,使用料理机分别将每种样品搅碎混匀;其次,准确称量5 g样品放入锥形瓶中,加入80 mL水并超声30 min,超声过程中每隔3 min摇晃锥形瓶,使固态样品完全分散;然后,将锥形瓶置于75 ℃的水浴锅中,水浴加热5 min,冷却至室温后,将样品转移至100 mL容量瓶中,并加入纯水定容至刻度;接着,将样品溶液用滤纸过滤,滤液10 000 r/min离心15 min,取上清液备用;最后,将上清液用水系一次性针头微孔滤膜过滤,使用C18柱纯化,获得样品提取液。通过建立的电化学方法,使用Cu-MOF为工作电极,测定样品提取液中亚硝酸盐含量。
1.4 数据处理
通过Microsoft Excel统计并分析实验数据,并将数据信息输入Origin软件绘制图片。
2 结果与分析
2.1 修饰电极的形貌表征
电极修饰流程如图1所示。首先,通过电化学还原电解液中的铜离子生成铜单质,沉积在电极表面,电极表面会形成1 层黄色的铜膜;然后,利用碱性氧化作用,将电极表面的铜转化为Cu(OH)2,可以看到电极表面由黄色变为蓝色;最后,使用交联剂H3BTC将Cu(OH)2转化为Cu-MOFs,可以观察到电极表面由蓝色变为蓝绿色。电极表面各修饰阶段发生的化学反应依次为:
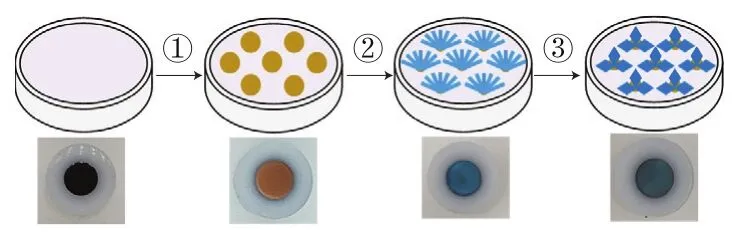
图1 修饰电极的制备过程及其电极表面图像Fig. 1 Flow chart for the preparation of the modified electrode and image of the electrode surface at each step
① Cu2++2e→Cu
② Cu+2OH--2e→Cu(OH)2
③ 3Cu(OH)2+2H3BTC→Cu3(BTC)2+6H2O
通过扫描电镜观察电极表面修饰的Cu、Cu(OH)2和Cu-MOFs的微观结构,结果如图2所示。采用电沉积在电极表面修饰的铜呈颗粒状;经碱性氧化处理,在铜粒子基底上生成的Cu(OH)2呈纳米带状,纳米带相互交错随机排列;利用交联剂H3BTC将Cu(OH)2转化为Cu-MOFs,生成的Cu-MOFs呈八面体结构。上述结果直观证明了Cu-MOFs在电极表面被成功制备。

图2 电极表面修饰的Cu(a)、Cu(OH)2(b)、Cu-MOFs(c、d)扫描电镜图Fig. 2 SEM images of modified Cu (a), Cu(OH)2 (b), Cu-MOFs (c, d)on the electrode surface
2.2 修饰电极对NO-2的电催化性能分析
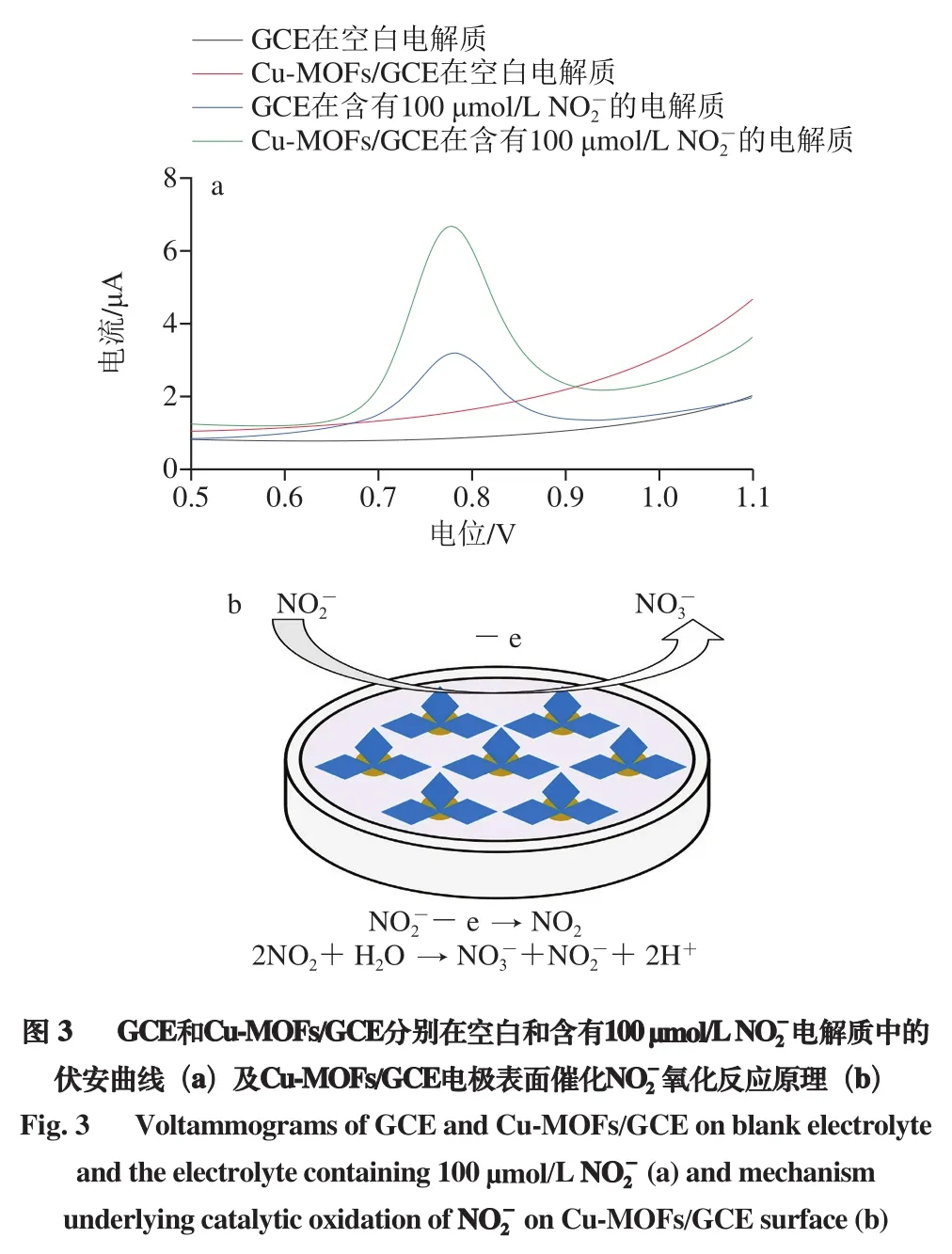
采用DPV法收集NO-2在电极表面电化学行为的相关数据,结果如图3a所示。在空白的电解液中,GCE和Cu-MOFs/GCE获得的伏安曲线均无明显的氧化峰。当电解液有NO-2存在,GCE和Cu-MOFs/GCE获得的伏安曲线均在0.8 V左右处出现一个明显的氧化峰,其原因为NO-2在工作电极表面发生氧化反应。NO-2在电位作用时,失去电子生成NO2,NO2又发生均相的歧化反应生成NO-3和NO-2。在含有100 μmol/L的NO-2的电解液中,GCE获得的峰电流为2.02 μA,Cu-MOFs/GCE获得的峰电流为4.76 μA,Cu-MOFs/GCE获得的NO-2氧化峰电流是传统GCE的2.36 倍。以上结果表明,电极表面修饰的Cu-MOFs能够催化NO-2氧化反应,增强电极的响应信号,有利于提高NO-2检测的灵敏度。
为了进一步考察NO-2在Cu-MOFs/GCE电极表面的电化学行为,采用CV技术分别设置不同的扫描速率(20、40、60、80、100 mV/s),观察NO-2氧化峰电流随扫描速率的变化。从图4可知,Cu-MOFs/GCE在NO-2的电解质中获得的峰电流强度随扫描速率逐渐增加,峰电流强度与CV扫描速率呈良好的线性关系(R2=0.98),说明NO-2在电极表面的电化学氧化反应是表面控制过程[27]。
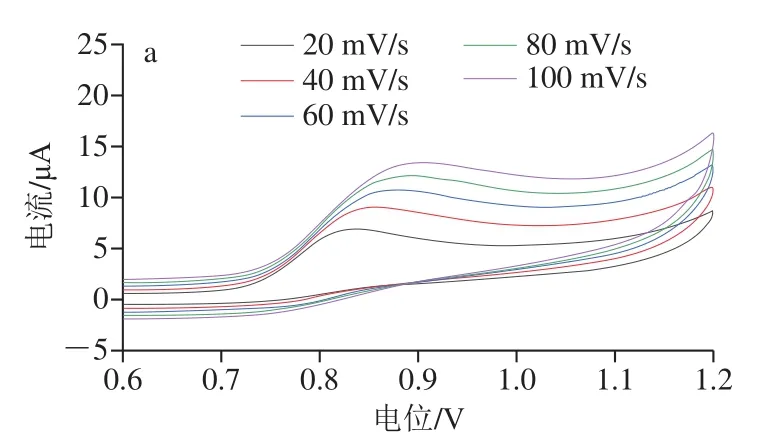
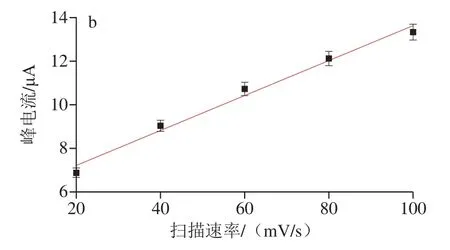
图4 不同扫描速率时Cu-MOFs/GCE在含有100 μmol/L NO-2的电解质中的循环伏安曲线(a)及对应的线性拟合曲线(b)Fig. 4 Cyclic voltammograms (a) of Cu-MOFs/GCE in the electrolyte containing 100 μmol/L NO-2 at different scan rates and resulting calibration curve (b)
2.3 Cu-MOFs/GCE的标准曲线和检测限
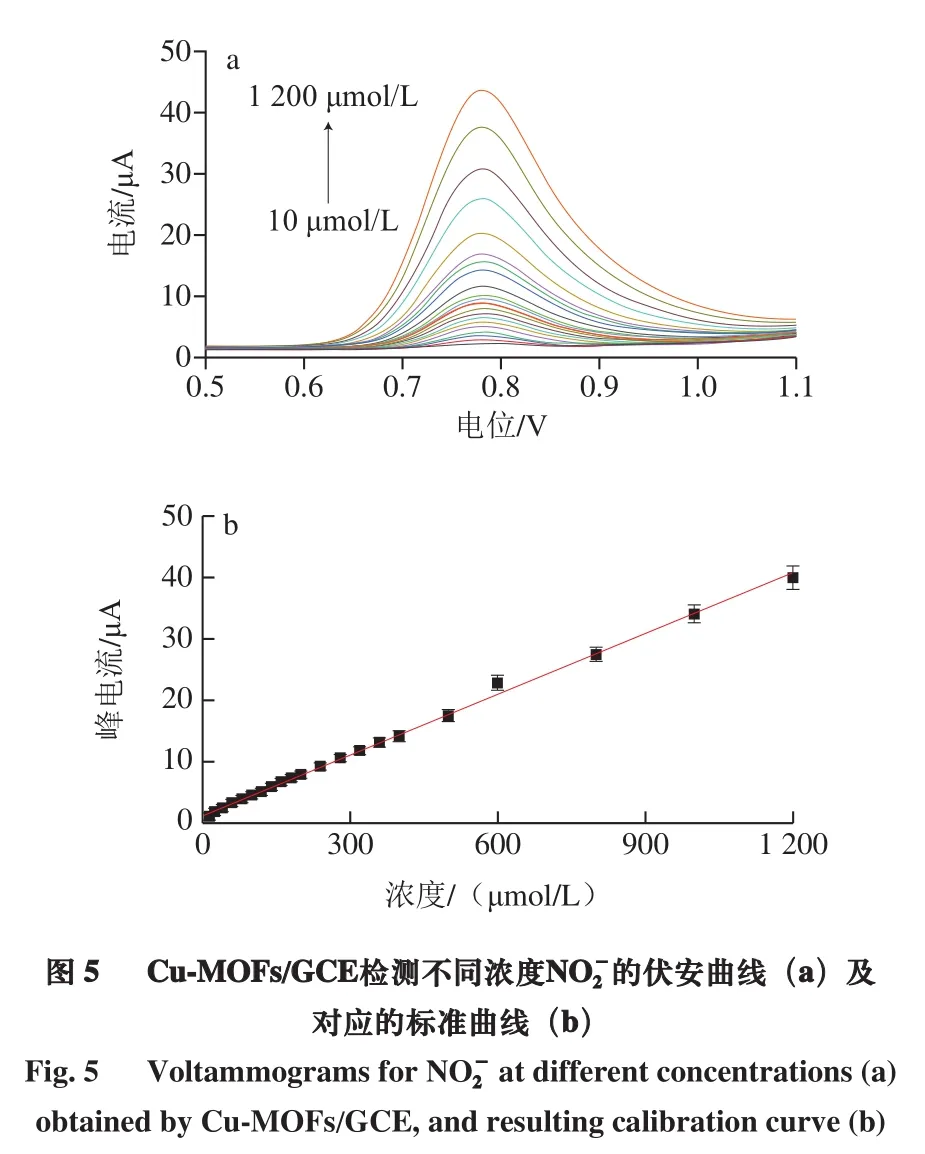
为了得到Cu-MOFs/GCE的线性工作范围数据,通过DPV法获得不同浓度NO-2的响应信号。图5a为Cu-MOFs/GCE检测10、20、30、40、60、80、100、120、140、160、180、200、240、280、320、360、400、500、600、800、1 000、1 200 μmol/L NO-2获得的伏安曲线,0.8 V处的氧化峰电流强度随NO-2浓度增大而逐渐增加。以峰电流强度为纵坐标,NO-2浓度为横坐标,建立如图5b所示的标准曲线,在浓度10~1 200 μmol/L范围内,Cu-MOFs/GCE的峰电流强度与NO-2浓度呈良好的线性关系,线性回归方程为:y=0.033x+1.182,R2=0.99。依据3 倍信噪比计算,Cu-MOFs/GCE对NO-2的检测限为1.57 μmol/L。与已报道的NO-2电化学传感器相比[28-30],Cu-MOFs/GCE具有检测限低、灵敏度高、线性范围宽、制备简单等优势。
2.4 Cu-MOFs/GCE的选择性和稳定性
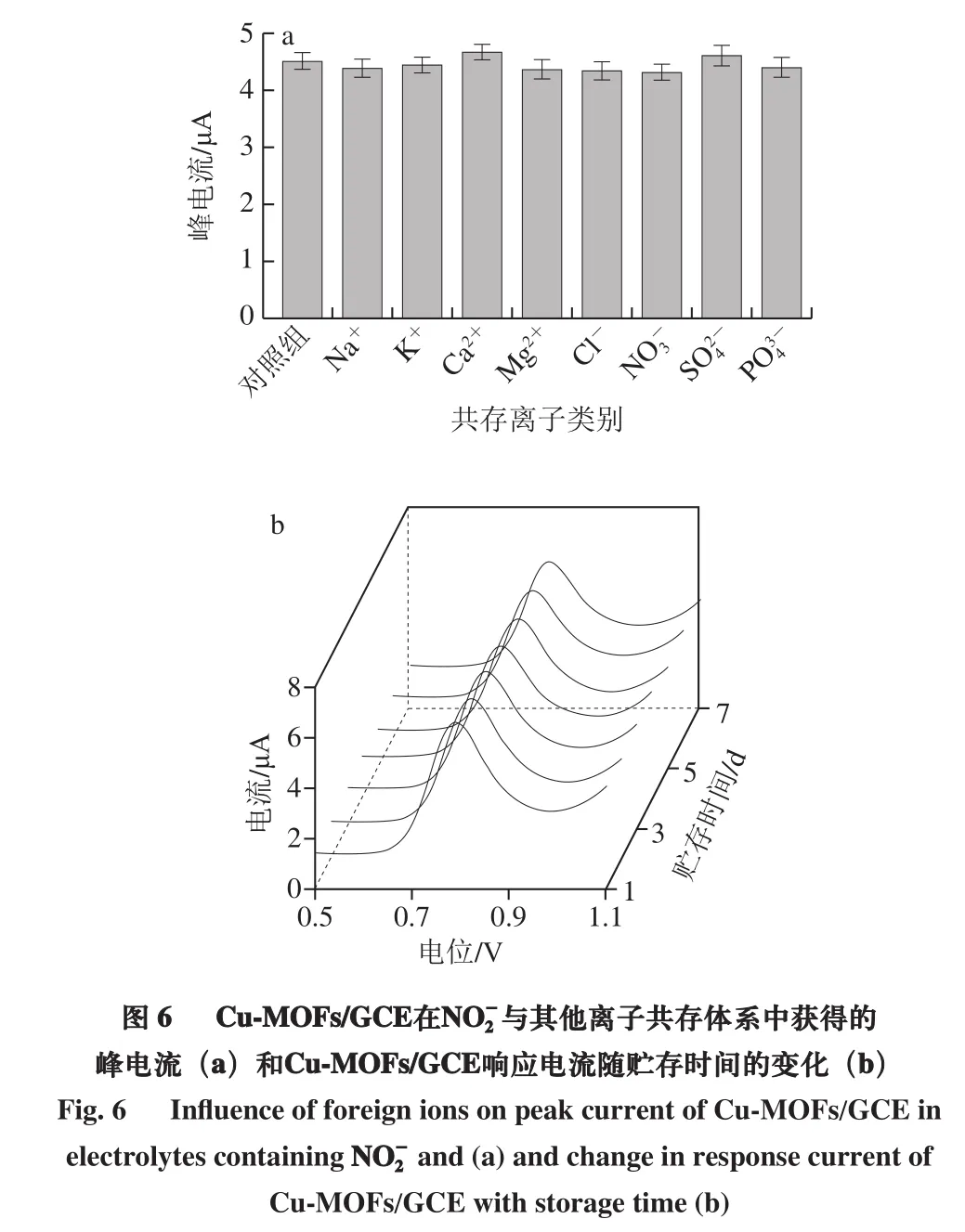
在食品亚硝酸盐检测中,NO2-常与其他离子共存,因此需要对Cu-MOFs/GCE的选择性进行研究。选择食品中常见的离子包括Na+、K+、Ca2+、Mg2+、Cl-、作为干扰物质代表。图6a结果显示,在NO-2溶液中添加这些离子,NO-2的氧化峰电流没有明显变化(小于5%),说明Cu-MOFs/GCE具有良好的选择性。
为了考察Cu-MOFs/GCE的稳定性,采用DPV法连续记录Cu-MOFs/GCE对100 μmol/L NO-2的响应电流。图6b结果显示,Cu-MOFs/GCE获得的电流信号随使用时间延长有下降趋势,这可能是因为Cu-MOFs/GCE在贮存过程的电极表面发生钝化。经统计分析,在连续测量7 d后,Cu-MOFs/GCE的电流信号比初始电流响应值仅降低了10%左右,说明制备的Cu-MOFs/GCE具有较好的稳定性。
2.5 肉制品中亚硝酸盐的检测
采用电化学DPV法,以Cu-MOFs/GCE作为工作电极,采集肉制品样品提取液中亚硝酸盐的响应信号,并结合多次标准加入法,获得亚硝酸盐浓度信息。结合样品前处理方法,Cu-MOFs/GCE对肉制品中亚硝酸盐的检测限为2.17 mg/kg,远低于GB 2760—2014《食品添加剂使用标准》规定的最大残留量30 mg/kg,因此该传感器能够满足国标限量标准的检测要求。基于样品提取液中亚硝酸盐浓度,计算得到肉制品中亚硝酸盐含量如表1所示,结果表明检测的肉制品中以NaNO2计的亚硝酸盐含量均低于GB 2760—2014规定的最大残留量。为了验证检测结果的准确性,同时采用GB 5009.33—2016《食品中亚硝酸盐与硝酸盐的测定》规定的第二法(分光光度-盐酸萘乙二胺法)对样品中的亚硝酸盐进行测定,结果显示这2 种方法获得的检测结果基本一致,相对误差均低于10%。上述试验结果说明,基于Cu-MOFs/GCE的电化学方法,在肉制品亚硝酸盐测定中具有较好的准确性。
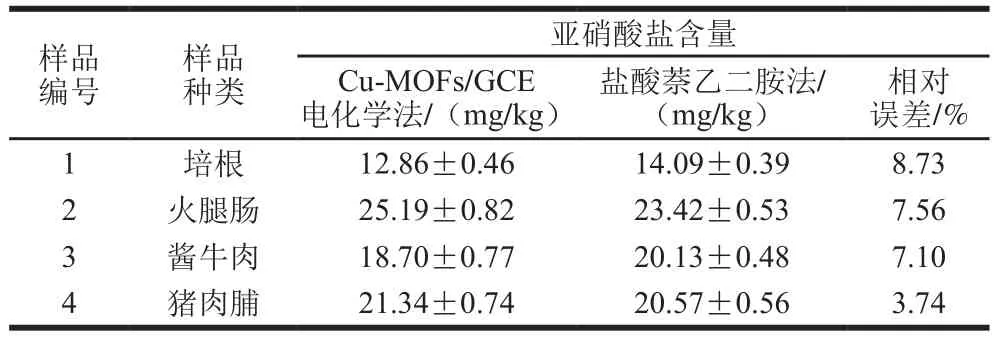
表1 肉制品中亚硝酸盐检测结果Table 1 Results of nitrite determination in different meat products
3 结 论
通过电化学法在电极表面原位合成Cu-MOFs,制备了用于肉制品中亚硝酸盐检测的电化学传感器。电极表面修饰的Cu-MOFs对电化学氧化NO-2反应具有催化作用,能够增强电极对NO-2的响应信号。以Cu-MOFs/GCE为工作电极,通过DPV法对NO-2进行测定,线性工作范围为10~1 200 μmol/L,检测限为1.57 μmol/L,且该修饰电极具有良好的选择性和稳定性。使用Cu-MOFs/GCE检测肉制品中亚硝酸盐,结果显示该电极获得的检测结果与盐酸萘乙二胺法的结果基本一致,相对误差低于10%,证明该修饰电极可以用于肉制品中亚硝酸盐的检测。本实验构建了基于Cu-MOFs的电化学传感器,建立了肉制品中亚硝酸盐的快速检测方法,为食品亚硝酸盐检测提供了新思路。

