GnRHa联合GH治疗中枢性性早熟或快速进展型青春期女孩有效性及安全性研究
黄秒,董国庆,苏月月
(南方医科大学附属深圳妇幼保健院 儿科,广东 深圳 518028)
0 引言
中枢性性早熟(CPP)主要是指因下丘脑-垂体-性腺轴功能提前启动而促使女孩8岁前,男孩9岁前即出现内外生殖器官快速发育以及第二性征出现[1]。临床上将8岁开始出现性发育,且性发育进程快速,从一个发育分期进展至下一分期的时间<6个月称之为快速进展型青春期[2]。无论是CPP亦或是快速进展型青春期均可能因生长的提前加速、骨龄远超同龄、骨骺预后时间减短等引起女孩成人身高异常,继而出现低矮身材以及相应心理问题或社会行为异常。由此可见,早期有效治疗CPP或快速进展型青春期女孩显得尤为重要,亦是临床重点关注的问题之一。目前,临床上针对上述女孩的主要治疗目标为抑制性发育进程,延长骨骼的成熟时间,最终实现成人身高的改善,在最大程度上减少或避免心理、行为问题的发生[3]。目前,临床上主要是通过促性腺激素释放激素激动剂(GnRHa)对CPP及快速进展型青春期女孩进行治疗,可帮助女孩达到或接近于遗传靶身高,同时不会对生殖系统产生严重影响[4]。然而,随着近年来人们生活水平的不断提高以及健康意识的逐渐加强,单纯的GnRHa治疗成年终身高改善并不理想。鉴于此,本文通过研究GnRHa联合GH治疗CPP或快速进展型青春期女孩有效性及安全性,旨在为临床用药方案的选择提供思路支持,现作以下报道。
1 资料与方法
1.1 一般资料
将深圳市妇幼保健院从2018年6月至2019年12月收治的CPP或快速进展型青春期女孩128例纳入研究。将其按照治疗方式的差异分为GnRHa治疗组45例,GnRHa联合GH治疗组40例,未治疗组43例。CPP诊断标准如下[5]:①8岁之前出现第二性征;②线性生长加速,且年生长速率高于正常儿童;③骨龄超过实际年龄1岁;④HPGA功能启动,血清促性腺激素以及性激素超过青春期水平。快速进展性青春期诊断标准如下:8岁后即出现第二性征,性发育进程迅速,从一个发育分期进展至下一分期的时间<6个月。入选标准:①所有受试者均符合上述相关诊断标准;②入院前尚未接受过相关治疗;③无GnRHa或(和)GH治疗禁忌证者;④所有研究对象符合(年龄>6岁;骨龄≤11.5岁;且骨龄>实际年龄1岁)。剔除标准:①心、肝、肾等重要脏器发生严重病变者;②高度过敏体质者;③合并严重感染性疾病,免疫性疾病,恶性肿瘤,血液系统疾病者;④明确诊断为其他病因导致的生长发育异常者;⑤合并糖尿病者;⑥乙肝病毒检测抗-HBC、HBSAG以及Hbeag阳性者;⑦研究过程中因各种原因退出或失访者。本研究与《赫尔辛基宣言》相关要求相符。
1.2 方法
GnRHa治疗组予以单纯GnRHa治疗,即肌内注射醋酸曲普瑞林(辉凌制药FERRING生成,批准文号:国药准字H20140123),28d/次,首次剂量为100μg/kg,维持剂量为80μg/kg,最大剂量不得超过3.75mg,持续治疗3年。GnRHa联合GH治疗组则在GnRHa治疗组的基础上增用GH治疗:重组人生长激素注射液(赛增)(长春金赛药业有限责任公司,批准文号:国药准字S20050025,规格30IU/10mg/3mL/瓶),用药次数为1次/Qn,给药时间为睡前30min。对照组为未治疗组,指未予以上药物干预,仅通过调节生活方式,6月随访一次患者。
1.3 观察指标
所有研究对象由专门内分泌科医生进行随访登记。
(1)随访记录:①体格检查。身高、体重、腰围、臀围、生长速率、Tanner分期指标;②实验室检查。血常规、血生化、糖代谢指标、甲状腺功能、乙型肝炎病毒检测、性腺功能相关激素;③影像学。B超(子宫及卵巢)、骨龄、MR检查(下丘脑及垂体)。
(2)骨龄使用Greulich和Pyle Atlas(GP图谱)测量,精度为±0.1cm。
(3)遗传靶身高(Tht,父亲身高+母亲身高/2-5cm)、以身高计算年龄(HA)、根据骨龄(BH)计算出的身高预测的成年时的身高(PAH),年生长速率(GV),身高标准差值(HtSDS)=(身高-平均身高相同人口)/同一人口身高的标准偏差。
(4)分析三组患者治疗前、治疗第1年、治疗第2年、治疗第3年时的预测成年终身高(PAH)、骨龄(BA)的身高标准差积分(HtSDSBA)、生长速率(GV)。以及GnRHa治疗组与GnRHa联合GH治疗组不良反应发生情况。
1.4 统计学处理
数据处理软件为SPSS 22.0,计数/计量资料以%/()表示,开展χ2/t检验。多组间计量资料的分析采用方差分析,计算F值,P<0.05预示差异有统计学意义。
2 结果
2.1 GnRHa治疗组治疗前后PAH、BA、HtSDSBA、GV评价
GnRHa治疗组治疗后2年PAH(160.42±4.18)cm明显高于初始PAH(157.61±3.96)cm,且治疗第1年、治疗第3年的HtSDSBA明显高于治疗前,治疗第2年、治疗第3年的GV相较于治疗第1年明显降低(均P<0.05),见表1。
表1 GnRHa治疗组治疗前后PAH、BA、HtSDSBA、GV评价()

表1 GnRHa治疗组治疗前后PAH、BA、HtSDSBA、GV评价()
2.2 GnRHa联合GH治疗组治疗前后PAH、BA、HtSDSBA、GV评价
GnRHa联合GH治疗组HtSDSBA在治疗前后第1年和第3年的身高SDS升高;治疗后2年PAH(157.13±4.76)cm,明显高于治疗前的(154.62±3.42)cm;治疗第1年、治疗第2年、治疗第3年GV均高于治疗前(均P<0.05),见表2。
表2 GnRHa联合GH治疗组治疗前后PAH、BA、HtSDSBA、GV评价()
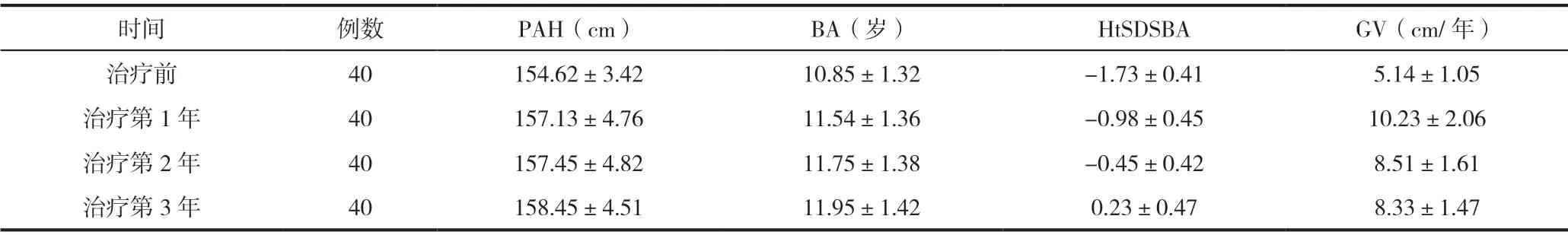
表2 GnRHa联合GH治疗组治疗前后PAH、BA、HtSDSBA、GV评价()
2.3 无治疗组不同时间点PAH、BA、HtSDSBA、GV评价
HtSDSBA在第1年和第3年的身高SDS比较无明显差异;2年后PAH(153.12±2.14)cm明显低于初始PAH(156.23±4.15)cm;GV在治疗第1年为(8.12±2.34)cm、第2年(5.32±4.23)cm、第3年(4.54±2.53)cm,差异有统计学意义(P<0.05),见表3。
表3 对照组不同时间点PAH、BA、HtSDSBA、GV评价()
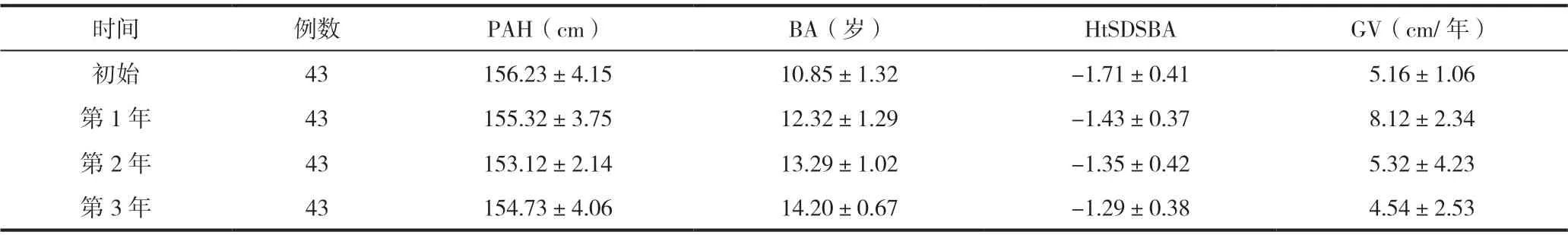
表3 对照组不同时间点PAH、BA、HtSDSBA、GV评价()
2.4 GnRHa治疗组与GnRHa联合GH治疗组不良反应发生情况分析
GnRHa治疗组未见明显不良反应,GnRHa联合GH治疗组仅出现2例亚临床甲低,且在1年后恢复正常。
3 讨论
迄今为止,关于CPP或快速进展型青春期的具体发病机制尚未完全阐明,目前普遍认为可能和环境激素、饮食、不良生活习惯以及营养状态等多种因素密切相关[6-7]。现阶段,全球范围内针对CPP或快速进展型青春期女孩的治疗以GnRHa为主,其主要是通过取代促性腺激素释放激素第六位、第十位点的氨基酸获得的一种化合物,相较于GnRH具有较长的半衰期以及更显著的受体结合能力,因此可发挥较强的垂体分泌促性腺激素作用,目前临床上应用较为广泛的曲普瑞林以及亮丙瑞林制剂药效是天然GnRHa的15~200倍。相关研究报道显示[8-9],GnRHa治疗CPP或快速进展型青春期不会对患者的甚至功能产生影响,且在停药后下丘脑-垂体-性腺轴功能会在短时间内恢复正常,同时会提高腺激素以及雌激素的表达水平,进一步促进子宫、卵巢发育恢复正常。然而,另有相关研究报道指出[10-11],部分患者在接受GnRHa治疗的患者可能出现血管运动性症状以及骨密度下降等一系列毒副作用,继而对整体疗效产生负面影响。
本研究发现,在接受GnRHa治疗的CPP女孩中,而PAH高于初始PAH,其中GnRHa联合GH治疗显示身高增加明显,证实了GnRHa联合GH治疗的有效性。既往研究发现,GnRHa联合GH应用于CPP患者中,可明显改善患者预测成年身高、年生长速度以及HtSDSBA[12]。考虑原因可能在于:GnRHa是目前临床上用以治疗CPP或快速进展型青春期的首选药物,其可持续作用在垂体中的GnRH受体,从而对卵泡刺激素以及血清促黄体生成素分泌产生抑制作用,进一步导致下丘脑-垂体-性腺轴功能遭受抑制,继而促使性激素分泌的下降,延长骨龄成熟时间以及骨生长时间,避免骨骺的过早融合,最终达到改善身高的目的[13-15]。而生长激素属于腺垂体细胞分泌的蛋白质,亦是肽类激素之一,对神经组织之外的所有其他组织的生长均有一定的积极促进作用,同时有助于刺激机体代谢过程以及蛋白质合成,且有效促进骨骼的线性生长,进一步达到改善患者骨骼发育状态的目的[16-18]。两药联合应用可发挥一定的协同互补作用,最终达到提高临床治疗效果,改善患者预后的目的。这在既往相关研究报道中得以佐证[19]:GnRHa联合GH治疗可有效弥补GnRHa限制骨生长的不足,继而获取更为理想的效果。此外,GnRHa治疗组未见明显不良反应,GnRHa联合GH治疗组仅出现2例亚临床甲低,且在1年后恢复正常。这提示了GnRHa联合GH应用于CPP或快速进展型青春期患者的治疗中,具有较好的安全性。这与陈秋莉的研究报道相似[20]:GnRHa联合GH应用于CPP女童的治疗中,未出现明显不良反应,且各项实验室指标水平均无异常。
综上所述,对于年龄>6岁;骨龄≤11.5岁;且骨龄>实际年龄1岁CPP或快速进展型青春期女孩应用GnRHa联合GH治疗成年身高改善效果显著,且具有较好的安全性,临床推广应用价值较高。

