三维可视化穿刺置管辅助经椎间孔入路经皮内窥镜下腰椎椎间盘切除术治疗腰椎椎间盘突出症
缪 伟,施建东*,茅旭平,张 文,叶晓健
1.南京中医药大学附属张家港医院骨科,苏州 215600
2.苏州大学骨科研究所,苏州 215006
3.上海交通大学医学院附属同仁医院骨科,上海 200336
腰椎椎间盘突出症(LDH)是脊柱外科常见病、多发病,因突出髓核压迫神经根导致腰腿痛[1-3]。经皮内窥镜技术治疗LDH是当前研究和临床应用的热点,技术发展迅速[4-6]。经椎间孔入路经皮内窥镜下腰椎椎间盘切除术(PETD)因手术创伤小、疗效佳、术后恢复快等优点[7-8],在国内外得到广泛开展。由于不同个体存在身高、年龄、脊柱形态、横突大小、关节突增生程度、椎间隙高度、脊柱退行性变程度等差异,导致PETD术中穿刺置管难度较大,良好的穿刺置管技术是顺利完成手术的关键点和难点。针对这一难点,现有研究[9-12]虽然较多,但仍缺乏有效的指导性技术。为了提高PETD术中穿刺置管的准确性,本研究组提出术前在三维可视化技术辅助下模拟置管,参考模拟结果行PETD,为优化临床治疗提供参考,现报告如下。
1 资料与方法
1.1 一般资料
纳入标准:①年龄18 ~ 75岁,具有典型的腰痛伴下肢放射痛,经询问病史、查体、影像学检查明确诊断为L3/L4或L4/L5单节段LDH;②经至少3个月的规范非手术治疗无效;③明显影响生活、工作;④无明显手术禁忌证。排除标准:①腰椎峡部裂或滑脱、严重椎管狭窄;②因腰椎感染、肿瘤、结核等致相应症状;③患有精神类疾病;④既往脊柱手术史;⑤更换手术方案。根据上述标准,纳入2017年1月—2019年9月于南京中医药大学附属张家港医院接受PETD治疗的42例单节段LDH患者临床资料,按入院顺序编号,单号为观察组,双号为对照组。观察组20例,其中男13例、女7例,年龄为19 ~ 73(47.34±6.15)岁,L3/L44例,L4/L516例;对照组22例,其中男13例、女9例,年龄为21 ~ 73(48.25±6.78)岁,L3/L44例,L4/L518例。2组一般资料差异无统计学意义(P> 0.05),具有可比性。本研究获南京中医药大学附属张家港医院伦理委员会批准(2016批056)。2组手术均由同一组医师完成。
1.2 手术方法
观察组患者采用硬膜外麻醉或全身麻醉,取俯卧位,腹部垫空,C形臂X线机透视定位手术节段及穿刺点,常规消毒、铺巾。该组患者术前俯卧于俯卧位垫上进行腰椎横断位CT扫描,影像学数据以dicom格式存储并导入Mimics 15.0软件(Materialise公司,比利时),建立腰椎模型,利用Mimics软件模拟PETD术中置管,计算机模拟从神经根压迫侧置入直径为7.5 mm的工作套管至责任椎间盘相邻下位椎体上缘中点。如模拟置入过程中无骨质阻挡则直接测量工作套管在矢状面、冠状面及横断面的角度(图1);如置管过程中有关节突骨质阻挡,则需模拟切除部分下位椎体上关节突后再测量工作套管各角度,同时通过软件测算出需切除关节突的体积和表面积(图2)。C形臂X线机引导下采用18号穿刺针经皮穿刺,根据术前模拟置管数据进入责任节段椎间隙黄韧带后方,适当调整穿刺方向。从穿刺点一直穿到责任椎间盘相邻下位椎体上缘中点,通过正侧位透视确认穿刺针到达与模拟置管同样位置,然后在穿刺针中穿入定位导丝,以导丝为中心做1个约7 mm纵行切口,依次放置导杆、逐级扩张导管,根据术前规划及术中情况决定是否使用环锯磨除部分上关节突及磨除程度,随后放置工作通道及内窥镜系统,采用射频刀头进行局部止血,用抓钳将突出的椎间盘组织完全摘除,探查神经根完全松解、硬膜囊搏动有力后,再次用射频刀头进行髓核及纤维环成形,退出内窥镜系统,缝合伤口,敷贴覆盖。
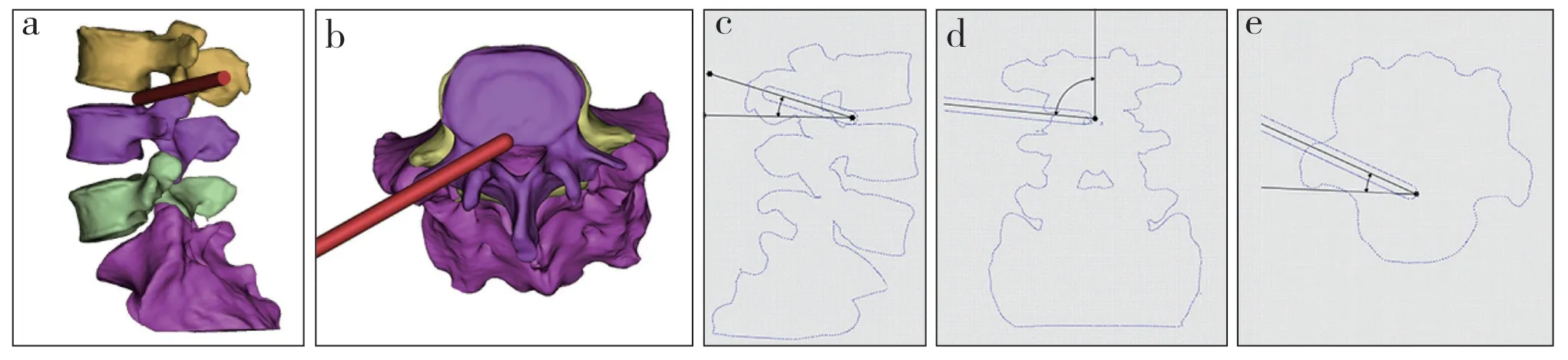
图1 模拟置管时无骨质阻挡Fig. 1 Simulated catheter placement without bone obstruction

图2 模拟置管时上关节突阻挡Fig. 2 Superior articular process obstruction during simulated catheter placement
对照组术前未采用可视化置管规划,采用常规方法穿刺进针。术中根据C形臂X线机透视图像及术者手感调整穿刺方向及判断是否使用环锯磨除部分关节突,其余操作同观察组。
1.3 观察指标
记录2组穿刺置管时间(从开始穿刺至成功放置工作通道的总时间)、术中透视次数及并发症发生情况。术前、术后1周、术后3个月及末次随访时采用疼痛视觉模拟量表(VAS)评分[13]、Oswestry功能障碍指数(ODI)[14]、日本骨科学会(JOA)评分[15]评估疼痛程度及腰椎功能。
1.4 统计学处理
采用SPSS 19.0软件对数据进行统计分析,计量资料以±s表示,组间比较采用两独立样本t检验,同组手术前后比较采用配对t检验;以P< 0.05为差异有统计学意义。
2 结 果
所有手术顺利完成,所有患者随访(8.19±2.23)个月。观察组穿刺置管时间、术中透视次数与对照组相比明显减少,差异均有统计学意义(P< 0.05,表1)。2组术后各时间点VAS评分、ODI、JOA评分较术前显著改善,差异均有统计学意义(P< 0.05,表1);术后各时间点组间比较差异无统计学意义(P> 0.05,表1)。2组均未发生感染、硬膜囊撕裂、神经根损伤、腹腔脏器损伤、出血等并发症。2组各发生1例因神经根减压不彻底术后遗留部分腰腿痛,经非手术治疗基本恢复;对照组1例因穿刺置管过程中敲击打磨下的关节突小骨片卡压神经根致腰腿痛较术前加重,止痛、脱水等非手术治疗无效,复查CT示L4/L5椎间盘平面小骨片卡压神经根(图3),行开放手术取出卡压神经根的骨块,并行后路减压植骨融合内固定术治疗后腰腿痛症状消失。
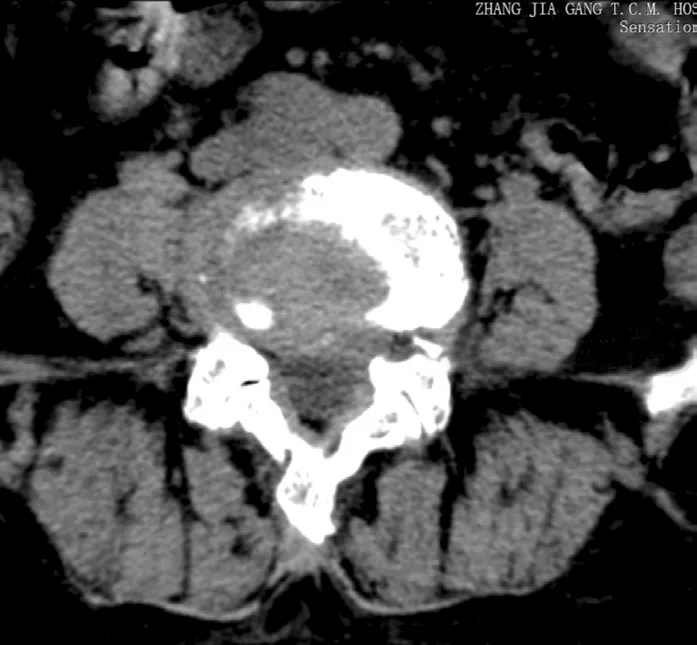
图3 游离骨块卡压神经根Fig. 3 Nerve root entrapment with free bone mass

表1 2组统计数据Tab. 1 Statistical data of 2 groups
3 讨 论
LDH严重影响患者生活和工作,部分患者采用非手术治疗,如牵引、药物、针灸、物理治疗等[16-18],效果良好,但部分患者仍需手术治疗。传统的开放手术效果确切,但创伤大、恢复慢、可能造成邻椎病及脊柱潜在不稳等原因使患者较难接受。随着微创理念普及、人们对健康要求的提高,脊柱微创手术已深入人心。经皮内窥镜技术可在直视下摘除突出髓核达到神经根直接减压的目的,且不破坏脊柱稳定结构,治疗LDH疗效显著,具有创伤小、手术时间短、出血量少、术后疼痛轻、恢复快等优势[19-21]。但经皮内窥镜技术对术者的经验及技术要求较高,术中穿刺置管的位置对于能否顺利摘除突出髓核起重要作用。目前,穿刺置管的辅助技术报道较多,包括体表金属网格辅助定位技术[22]、超声定位技术[23]、导航技术[24]、三维打印技术[25]等。网格定位技术局限于二维,精度较差,空间定位困难;超声技术仍处于发展阶段,尚未成熟,且对操作者技术要求高;导航技术及三维打印技术虽然更为直观、准确,但价格昂贵,不利于临床广泛推广应用。穿刺定位技术可提高术中穿刺准确性、缩短手术时间,但目前仍缺乏全面的解剖学基础研究和简便的指导性技术,难以做到术前准确评估穿刺置管角度及穿刺的难易程度。本研究组在前期采用PETD治疗LDH经验的基础上,提出采用三维可视化技术术前模拟置管辅助PETD,在术前更好地了解个体解剖特点的情况下结合模拟置管数据做术前规划。
技术要点:①穿刺置管至椎间盘后缘中点是能保证内窥镜系统进入,且视野及操作范围足够的理想位置。②经椎间孔脊柱内窥镜系统(TESSYS)要求置管不宜超过横突腹侧,否则容易损伤横突前下方的行走神经根及腹腔脏器,因此,横突最外下点是参考极点。③本研究组采用的TESSYS通道直径为7.5 mm,半径为3.8 mm,若以轴线为中心用环锯打磨上关节突的最大半径为3.8 mm,因此以3.8 mm为界限打磨上关节突会出现4种情况。零接触,无需打磨上关节突,可直接置管进入;≤3.8 mm,正常打磨;> 3.8 mm,需要反复调整轴线位置打磨,操作困难;超越上关节突,需要同时打磨上下关节突,可能会损伤脊柱稳定性,若骨质较硬可能会导致置管失败。对照组1例患者因术前未行三维可视化置管规划,缺乏需打磨关节突大小的数据,并且患者关节突骨质较硬,术中盲目敲击关节突致较大块骨块掉落卡压神经根,出现明显腰腿痛症状。术前采用三维可视化置管技术模拟置管,可明确工作通道在各方向的倾斜角度及是否需要打磨关节突及打磨程度,术前即可了解穿刺的难易程度。当术前规划明确需要打磨关节,术中穿刺到达关节突后可直接打磨,无须再花费时间反复调整穿刺针。当术前规划提示无需打磨关节突时,术中通过调整穿刺针位置即可置管成功,避免了盲目打磨关节突,减少了损伤,节约了时间。同时,术前规划可减少不必要的术中透视,降低了医患术中的辐射暴露。有研究[26]表明,超剂量的辐射暴露会增加多种疾病的发生率,如甲状腺癌、皮肤红斑、白血病等,同时也会损伤视网膜[27],并会增加生育期人群后代畸形的风险[28],且选择采用PETD治疗的生育年龄LDH患者不在少数[29],这是医师必须关注的问题。
本研究结果显示,2组手术疗效无明显差异,但三维可视化置管技术辅助PETD可明显缩短术中穿刺置管时间、减少术中透视次数,能更好拟订并及时调整手术方案,利于术中做到更精准、快速置管,更少的辐射暴露,具有良好的临床应用价值。通过对前期手术中一定数量样本进行测量及临床验证,本研究组发现,椎间孔相关解剖结构,包括横突大小、椎间隙高度、关节突角及关节突增生程度,对置管难易程度均有影响,但因样本量限制,对目前测量数据进行统计分析无法得出完全趋势性的结论,需要在后期工作中进一步挖掘。

