深海真菌Neoroussoella sp.固体发酵物中次生代谢产物及其生物活性研究
钟晋谦,陈玉婵,陈闪冲,刘昭明,刘洪新,章卫民*,严寒静
1广东药科大学中药学院,广州 510006;2广东省科学院微生物研究所 华南应用微生物国家重点实验室 广东省菌种保藏与应用重点实验室,广州 510070
海洋微生物长期处于高盐、高压、低温、低光照及寡营养等极端环境下,进化出了与陆生生物不同的代谢系统及防御机制,因而产生的次生代谢产物具有高度的复杂性和多样性。海洋微生物源天然产物种类极其丰富,几乎涵盖了所有天然产物的结构类型,并具有广泛的生物活性,是新型天然药物先导化合物的重要来源。对海洋微生物次生代谢产物进行研究,将能够发现化学结构新颖、生物活性显著的先导化合物,为新药研究与开发提供重要的模式结构和药物前体[1-4]。
本课题组前期对我国南海(114°34′52″E,13°57′27″N)4 314 m深处沉积物中的真菌进行了分离鉴定,获得了一株新型的海洋真菌Neoroussoellasp.。查阅文献发现,目前国内外尚未有关于其次生代谢产物研究的报道。通过对小量液体发酵获得的粗提物进行HPLC-MS分析,发现其代谢产物十分丰富。基于此,我们利用正相硅胶柱、凝胶柱和高效液相色谱等多种色谱技术对该真菌进行了系统的化学成分研究。
1 材料与方法
1.1 仪器与试剂
核磁共振波谱仪(AVANCE III型500 MHz和AVANCE III型600 MHz,瑞士Bruker公司);高效液相色谱仪(1220 Infinity II制备型,美国Agilent Technologies公司);高效液相色谱仪(LC-20A半制备型,日本岛津公司);YMC-pack ODS-AQ制备柱(250 mm × 10 mm,5 μm);Phenomenex ACE 5 C18-PFP制备柱(250 mm × 10 mm,5 μm);Phenomenex MD(2)-RH制备柱(250 mm × 10 mm,5 μm);Phenomenex Chiral MJ(2)制备柱(250 mm × 10 mm,5 μm);S-chirial A制备柱(250 mm × 10 mm,5 μm);Chiralpak IC制备柱(250 mm × 10 mm,5 μm);旋转蒸发仪(OSB-2100型,日本东京理化器械株式会社);大容量普通摇床(PZ1000B旋转式,武汉瑞华仪器设备有限公司);柱色谱硅胶(200~300目,山东青岛海洋化工厂);Sephadex LH-20(18~110 μm,瑞典Amersham Bioscience公司);薄层层析硅胶板(HSGF254,烟台江友硅胶开发有限公司);石油醚、乙酸乙酯、二氯甲烷、甲醇(分析纯,广州化学试剂厂);甲醇、乙腈、正己烷、异丙醇(色谱纯,美国BCR公司)。
1.2 菌株鉴定
菌株FS526分离自我国南海(114°34′52″E,13°57′27″N)4 314 m深处的沉积物,通过液氮冻融法提取菌株的基因组DNA,采用引物ITS1扩增其rDNA ITS区,并对产物进行测序;测序结果提交GenBank,登录号为MW255342。序列blast结果显示,菌株FS526与Neoroussoellasp.AP-2019(登录号为MN556318.1)的相似度为96.93%。下载相关种属ITS区序列,连同FS526序列,以Neoconiothyriumvitcola(登录号为MN556318.1)为外群,运用MEGA5.0通过邻近法构建系统发育树(图1)。在发育树中,菌株FS526与若干Neoroussoella属的种类聚为一个分支,彼此间遗传距离很小。通过系统学分析确定FS526为Neoroussoellasp.,菌种保藏于广东省微生物研究所。将该菌株接种于装有PDA培养基(含3%海盐)斜面上27 ℃培养好后,置于4 ℃冰箱保藏。
1.3 发酵培养
在无菌条件下,将活化后的Neoroussoellasp.菌体接种至装有马铃薯葡萄糖培养液(PDB)的锥形瓶中,在28 ℃、120 rpm的条件下振荡培养5天,获得种子液。将适量种子液转接到装有9 g海盐、250 g大米、300 mL水的3 L锥形瓶中,制作成大米固体培养基。室温下静置培养30天,共发酵大米5 kg。
1.4 分离纯化
发酵结束后,培养基用乙酸乙酯提取3次,合并全部提取液,经旋蒸浓缩后得到棕红色提取物。浸膏进行硅胶柱层析(200~300目),以石油醚-乙酸乙酯(体积比10∶1→1∶1)和二氯甲烷-甲醇(体积比10∶1→0∶1)溶剂系统进行梯度洗脱,并用薄层色谱(TLC)检测;合并相似组分,得到12个组分Fr.1~12。
Fr.5经Sephadex LH-20凝胶(二氯甲烷-甲醇体系,体积比为50∶50)得到3个亚组分Fr.5.1~Fr.5.3。Fr.5.3经硅胶柱(200~300目,石油醚-乙酸乙酯体系,体积比为10∶1→1∶1,梯度洗脱)得到5个组分Fr.5.3.1~Fr.5.3.5;其中Fr.5.3.1为化合物10(4.1 mg)。Fr.5.3.3经Phenomenex Chiral MJ(2)制备柱(正己烷-异丙醇体系,体积比为80∶20,2 mL/min)得到Fr.5.3.3.1~Fr.5.3.3.4。Fr.5.3.3.4经硅胶柱(200~300目,石油醚-乙酸乙酯体系,体积比为5∶1,等度洗脱)得到化合物13(14.4 mg)。Fr.5.3.3.1经Phenomenex Chiral MJ(2)制备柱(正己烷-异丙醇体系,体积比为50∶50,2 mL/min)得到化合物6(0.7 mg)。
Fr.6经Sephadex LH-20凝胶(二氯甲烷-甲醇体系,体积比为50∶50)得到4个亚组分Fr.6.1~Fr.6.4。Fr.6.2经Chiralpak IC制备柱(正己烷-异丙醇体系,体积比50∶50,2 mL/min)得到6个组分Fr.6.2.1~Fr.6.2.6。Fr.6.2.3经Chiralpak IC制备柱(乙腈-水体系,体积比50∶50,2 mL/min)纯化得到化合物3(11.1 mg),Fr.6.2.6经Chiralpak IC制备柱(乙腈-水体系,体积比50∶50,2 mL/min)纯化得到化合物1(9.0 mg)。Fr.6.3经Chiralpak IC制备柱(正己烷-异丙醇体系,体积比50∶50,2 mL/min)得到8个组分Fr.6.3.1~Fr.6.3.8。Fr.6.3.1经两次Sephadex LH-20凝胶(二氯甲烷-甲醇体系,体积比为50∶50)后,再经Chiralpak IC制备柱(正己烷-异丙醇体系,体积比80∶20,2 mL/min)纯化得到化合物4(6.9 mg),Fr.6.3.3经Sephadex LH-20凝胶(二氯甲烷-甲醇体系,体积比为50∶50)与YMC-pack ODS-AQ制备柱(乙腈-水体系,体积比70∶30,2 mL/min),得到化合物11(4.4 mg)。Fr.6.3.6经Chiralpak IC制备柱(乙腈-水体系,体积比50∶50,2 mL/min)纯化,得到化合物2(4.9 mg)。Fr.6.4经硅胶柱(200~300目,石油醚-乙酸乙酯体系,体积比为8∶1→1∶1,梯度洗脱)分离,得到6个组分Fr.6.4.1~Fr.6.4.6。Fr.6.4.1经硅胶柱(200~300目,石油醚-乙酸乙酯体系,体积比为8∶1→7∶1,梯度洗脱)与YMC-pack ODS-AQ制备柱(甲醇-水体系,体积比50∶50,2 mL/min)纯化,得到化合物14(1.9 mg)和组分Fr.6.4.1.1与Fr.6.4.1.2。Fr.6.4.1.1通过Phenomenex Chiral MJ(2)制备柱(正己烷-异丙醇体系,体积比为60∶40,2 mL/min)纯化得到化合物15(0.6 mg)。Fr.6.4.1.2通过Phenomenex Chiral MJ(2)制备柱(正己烷-异丙醇体系,体积比为75∶25,2 mL/min)与Phenomenex MD(2)-RH制备柱(乙腈-水体系,体积比为40∶60,2 mL/min)纯化,得到化合物12(1.1 mg)。Fr.6.4.2经硅胶柱(200~300目,石油醚-乙酸乙酯体系,体积比为7∶1→5∶1,梯度洗脱)与MC-pack ODS-AQ制备柱(甲醇-水体系,体积比75∶25,2 mL/min)纯化,得到化合物7(10.5 mg)。
Fr.8经正相硅胶柱(200~300目)层析,溶剂系统为石油醚-乙酸乙酯,体积比为20∶1→2∶1,梯度洗脱,得到3个亚组分Fr.8.1~8.3。Fr.8.3经Chiralpak IC制备柱(正己烷-异丙醇体系,体积比60∶40,2 mL/min)得到化合物9(25.1 mg)与粗组分Fr.8.3.1~Fr.8.3.6,Fr.8.3.3经Chiralpak IC制备柱(甲醇-水体系,体积比50∶50,2 mL/min)纯化,得到化合物8(21.5 mg)和5(9.8 mg)。
2 结果与分析
2.1 结构鉴定
化合物1白色固体;分子式C24H26O8。1H NMR(600 MHz,CD3OD)δ:6.38(1H,t,J= 1.2 Hz,H-14),6.30(1H,d,J= 5.3 Hz,H-22),6.15(1H,d,J= 1.6 Hz,H-2),4.20(1H,q,J= 7.1 Hz,H-9),3.73(1H,d,J= 10.0 Hz,H-11),3.39(1H,dd,J= 9.9,5.4 Hz,H-21),3.26(1H,d,J= 4.7 Hz,H-24β),2.91(1H,ddd,J= 13.0,4.7,2.7 Hz,H-5),2.83(1H,d,J= 4.7 Hz,H-24α),2.07(1H,dd,J= 14.6,4.6 Hz,H-6β),1.66(3H,s,H-17),1.66(3H,s,H-18),1.58(1H,dd,J= 14.6,13.1 Hz,H-6α),1.35(3H,s,H-23),1.30(3H,d,J= 7.1 Hz,H-20),1.22(3H,d,J= 1.5 Hz,H-19);13C NMR(150 MHz,CD3OD)δ:214.0(C-10),206.2(C-13),178.5(C-8),164.6(C-1),153.9(C-3),143.4(C-15),131.2(C-14),118.7(C-2),100.7(C-22),84.5(C-16),75.4(C-9),60.9(C-4),55.3(C-24),50.9(C-12),49.5(C-11),47.1(C-21),44.9(C-7),34.2(C-5),29.3(C-6),27.0(C-18),26.9(C-17),26.4(C-23),18.2(C-20),17.5(C-19)。上述数据与文献报道[5]基本一致,故鉴定化合物1为amestolkolide B。
化合物2无色油状;分子式C27H32O8。1H NMR(600 MHz,CDCl3)δ:11.06(1H,s,4′-OH),7.15(1H,d,J= 10.2 Hz,H-1),6.51(1H,s,H-5′),6.16(1H,d,J= 1.7 Hz,H-7′),5.99(1H,d,J= 10.2 Hz,H-2),4.72(1H,m,H-8′),4.17(1H,dd,J= 8.9,2.9 Hz,H-7),2.96(1H,dd,J= 15.5,5.0 Hz,H-11β),2.61(1H,m,H-11α),2.26(2H,overlapped,H-6α,H-9),2.18(1H,overlapped,H-5),2.17(3H,s,7′-Ac),1.85(1H,ddd,J= 14.4,14.0,3.0 Hz,H-6β),1.49(3H,d,J= 6.6 Hz,H-9′),1.36(3H,s,H-15),1.27(3H,s,H-12),1.17(3H,s,H-14),1.15(3H,s,H-13);13C NMR(150 MHz,CDCl3)δ:203.9(C-3),170.8(7′-Ac),168.9(C-10′),162.5(C-4′),159.8(C-6′),156.2(C-1),136.0(C-2′),127.7(C-2),112.4(C-3′),106.5(C-5′),102.5(C-1′),79.9(C-8),76.2(C-8′),72.1(C-7),64.3(C-7′),44.9(C-4),42.6(C-5),42.1(C-9),38.6(C-10),27.8(C-14),27.6(C-15),26.8(C-6),21.7(C-11),21.6(C-12),21.5(C-13),20.9(7′-Ac),16.6(C-9′)。上述数据与文献报道[6]基本一致,故鉴定化合物2为thailandolide B。
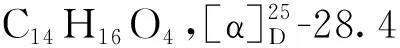
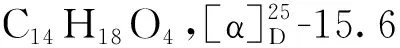
化合物5红棕色晶体;分子式C12H12O5。1H NMR(600 MHz,CD3OD)δ:6.37(1H,s,H-4),6.31(1H,d,J= 2.2 Hz,H-7),6.30(1H,d,J= 2.0 Hz,H-5),4.15(1H,m,H-2′),2.58(2H,m,H-1′),1.26(3H,d,J= 6.3 Hz,H-3′);13C NMR(150 MHz,CD3OD)δ:167.8(C-1),167.5(C-8),164.9(C-6),156.1(C-3),141.2(C-10),107.0(C-4),103.7(C-7),102.7(C-5),99.8(C-9),66.2(C-2′),43.8(C-1′),23.3(C-3′)。上述数据与文献报道[8]基本一致,故鉴定化合物5为de-O-methyldiaporthin。
化合物6红棕色固体;分子式C10H12O3。1H NMR(500 MHz,CDCl3)δ:7.08(2H,d,J= 8.5 Hz,H-2,6),6.77(2H,d,J= 8.5 Hz,H-3,5),4.23(2H,t,J= 7.1 Hz,H-8),2.86(2H,t,J= 7.1 Hz,H-7),2.04(3H,s,H-2′);13C NMR(125 MHz,CDCl3)δ:171.2(C-1′),154.4(C-4),130.2(C-1),130.1(C-2,6),115.5(C-3,5),65.3(C-8),34.4(C-7),21.1(C-2′)。上述数据与文献报道[9]基本一致,故鉴定化合物6为4-(2-乙氧基乙基)苯酚。
化合物7绿色晶体;分子式C11H10O6。1H NMR(600 MHz,CD3OD)δ:7.26(1H,s,H-3),6.52(1H,s,H-7),4.99(1H,q,J= 6.6 Hz,H-9),1.50(3H,d,J= 6.5 Hz,H-10);13C NMR(150 MHz,CD3OD)δ:166.7(C-1),158.2(C-8),155.9(C-6),139.4(C-3),132.5(C-5),120.7(C-4a),119.8(C-4),102.4(C-7),97.4(C-8a),66.5(C-9),22.0(C-10)。上述数据与文献报道[10]基本一致,故鉴定化合物7为5,6,8-三羟基-4-(1′-羟乙基)异香豆素。
化合物8无色晶体;分子式C11H10O5。1H NMR(600 MHz,CD3OD)δ:7.36(1H,d,J= 0.9 Hz,H-3),6.60(1H,d,J= 2.1 Hz,H-5),6.36(1H,d,J=2.1 Hz,H-7),4.88(1H,m,H-9),1.50(3H,d,J= 6.4 Hz,H-10);13C NMR(150 MHz,CD3OD)δ:167.5(C-1),167.2(C-6),165.5(C-8),142.7(C-3),130.0(C-4a),123.4(C-4),103.1(C-7),102.4(C-5),100.4(C-8a),65.2(C-9),23.2(C-10)。上述数据与文献报道[11]基本一致,故鉴定化合物8为sescandelin。
化合物9红棕色固体;分子式C11H12O4。1H NMR(600 MHz,CD3OD)δ:6.56(1H,d,J= 2.1 Hz,H-4),6.34(1H,d,J= 2.2 Hz,H-6),4.61(2H,s,H-9),3.92(3H,s,H-10),2.41(3H,s,H-8);13C NMR(150 MHz,CD3OD)δ:155.0(C-5),154.4(C-2),146.3(C-7),139.1(C-7a),132.0(C-3a),115.9(C-3),97.4(C-4),97.2(C-6),56.6(C-10),55.3(C-9),12.0(C-8)。上述数据与文献报道[12]基本一致,故鉴定化合物9为penicifuran A。
化合物10红棕色固体;分子式C11H12O4。1H NMR(500 MHz,CDCl3)δ:7.70(1H,m,7-OH),5.20(2H,s,H-3),3.76(3H,s,H-9),2.20(3H,s,H-8),2.14(3H,s,H-10);13C NMR(125 MHz,CDCl3)δ:173.2(C-1),164.0(C-5),154.0(C-7),143.6(C-3a),118.7(C-6),116.6(C-4),106.3(C-7a),70.2(C-3),60.4(C-9),11.5(C-8),8.7(C-10)。上述数据与文献报道[13]基本一致,故鉴定化合物10为7-羟基-5-甲氧基-4,6-二甲基邻苯二甲酯。
化合物11黄色油状;分子式C10H16O3。1H NMR(600 MHz,CDCl3)δ:4.96(1H,t,J= 7.5 Hz,H-7),2.98(1H,qd,J= 7.7,5.1 Hz,H-2),2.62(1H,td,J= 8.2,5.1 Hz,H-3),2.14(1H,d,J= 15.2 Hz,H-6β),1.89(1H,d,J= 8.0 Hz,H-6α),1.87(1H,M,H-4),1.27(3H,d,J= 7.4 Hz,H-8),1.25(3H,s,H-10),1.05(3H,d,J= 7.0 Hz,H-9);13C NMR(150 MHz,CDCl3)δ:186.2(C-1),81.4(C-7),79.7(C-5),51.4(C-3),58.0(C-6),45.3(C-4),36.3(C-2),25.8(C-10),19.0(C-8),8.5(C-9)。上述数据与文献报道[14]基本一致,故鉴定化合物11为pestalotiolactone A。
化合物12黄色固体;分子式C10H12O4。1H NMR(600 MHz,CDCl3)δ:5.96(1H,s,H-3),3.83(3H,s,H-8),2.68(3H,s,H-10),2.01(3H,s,H-7);13C NMR(150 MHz,CDCl3)δ:203.4(C-9),163.6(C-2),163.4(C-6),163.4(C-4),106.2(C-5),104.9(C-1),91.4(C-3),55.7(C-8),32.9(C-10),7.1(C-7)。上述数据与文献报道[15]基本一致,故鉴定化合物12为2′,4′-二羟基-6′-甲氧基-3′-甲基苯乙酮。
化合物13黄色晶体;分子式C10H12O4。1H NMR(500 MHz,CD3OD)δ:6.03(1H,s,H-5),3.84(3H,s,H-7),2.65(3H,s,H-10),1.93(3H,s,H-8);13C NMR(125 MHz,CD3OD)δ:205.1(C-9),165.3(C-4),163.60(C-6),162.3(C-2),106.0(C-3),104.6(C-1),90.9(C-5),55.9(C-10),33.0(C-7),7.2(C-8)。上述数据与文献报道[16]基本一致,故鉴定化合物13为1-(2,4-二羟基-6-甲氧基-3-甲基苯基)乙酮。
化合物14白色固体;分子式C8H10O2。1H NMR(600 MHz,CD3OD)δ:6.14(2H,s,H-4,6),2.15(3H,d,J= 0.9 Hz,H-8),1.99(3H,s,H-7);13C NMR(150 MHz,CD3OD)δ:157.1(C-1,3),136.8(C-5),109.0(C-2),108.3(C-4,6),21.3(C-8),8.2(C-7)。上述数据与文献报道[17]基本一致,故鉴定化合物14为2,5-二甲基间苯二酚。
化合物15白色固体;分子式C7H8O2。1H NMR(600 MHz,CD3OD)δ:6.12(2H,d,J= 2.3 Hz,H-4,6),6.07(1H,t,J= 2.3 Hz,H-2),2.18(3H,d,J= 0.7 Hz,H-7);13C NMR(150 MHz,CD3OD)δ:158.9(C-1,3),140.7(C-5),108.1(C-4,6),100.2(C-2),21.1(C-7)。上述数据与文献报道[18]基本一致,故鉴定化合物15为1,3-二羟基甲苯。
2.2 生物活性测试
采用SRB法[19]以人神经癌细胞(SF-268)、人乳腺癌细胞(MCF-7)、人肝癌细胞(HepG-2)为供试细胞株、阿霉素作为阳性对照分离得到的化合物进行细胞毒活性评价(表1),结果显示化合物1表现出一定的细胞毒活性,对三株细胞株的IC50值为41.44~77.89 μM,而其余化合物无明显的细胞毒活性。
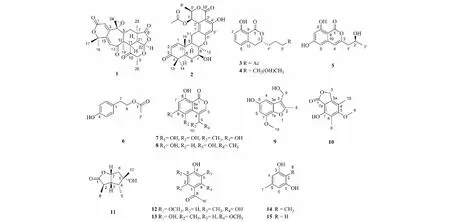
图2 化合物1~15的结构式Fig.2 Structures of compounds 1-15
此外,采用DPPH法[20]以DPPH自由基清除率为指标、Vc作为阳性对照,对分离得到的化合物进行抗氧化活性评价。实验结果显示化合物7有较强的抗氧化活性,其IC50值为14.95 μM,接近阳性对照Vc的IC50值13.93 μM,其余化合物则无明显抗氧化活性(表1)。
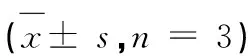
表1 化合物1和7的细胞毒活性与抗氧化活性评价
3 讨论
Neoroussoella是Liu等[21]在2014年首次发现并描述的一个真菌新属。目前分离鉴定的Neoroussoella属真菌主要来源于植物,存在于竹子、草本植物以及棕榈树中,而海洋来源的报道较少,集中在地中海流域,且来源均为海底植物[22-24]。本研究使用的FS526菌株为南海深海沉积物中分离得到。经文献调研表明,该属真菌未见次生代谢产物的研究报道。
本研究首次从深海真菌Neoroussoellasp.FS526的固体发酵产物中分离鉴定了15个单体化合物,其结构类型多样,包括杂萜2个、异香豆素5个、苯并呋喃2个、单萜1个、苯酚衍生物5个,所有化合物均为首次从Neoroussoella属真菌中分离得到。从这些化合物的结构类型上推测,苯酚及其衍生物是该真菌主要的特征性次生代谢产物,该类型化合物主要由聚酮生源合成途径产生。化合物1有C-9位构型不同的结构类似物,该结构类型的S构型被Stierle等[25]从Penicillium属真菌中首次发现,并命名为berkeleyacetal C,该化合物对非小细胞肺癌细胞系有抑制作用。之后Sun等[26]从PenicilliumpurpurogenumMHZ 111中也发现了berkeleyacetal C。随后,Chen等[5]从TalaromycesamestolkiaeYX1中分离纯化到C-9位R构型的新结构类似物,并命名为amestolkolide B。对berkeleyacetal C和amestolkolide B两种不同构型的单体化合物进行活性测试,结果均显示有较强的NO产生抑制活性,但未发现明显的细胞毒活性[5,26]。而本研究的生物活性测试结果显示化合物1具有较弱的细胞毒活性。此外,异香豆素化合物7具有较强的抗氧化活性,其IC50值接近阳性对照Vc,值得进一步研究。本研究结果丰富了Neoroussoella属真菌的化学成分,为今后进一步开展其他生物活性研究提供了物质基础。

