自制施源器固定器在宫颈癌三维近距离放射治疗中的应用
陈仁金,杨蕾,谭龙婧,杨波,石翔翔
西南医科大学附属医院 肿瘤科,四川 泸州 646000
引言
宫颈癌是妇科常见恶性肿瘤之一,在全世界的发病率与死亡率居女性恶性肿瘤第4位[1]。我国宫颈癌的年发病例数为9.89万,年死亡例数为3.05万[2]。外照射结合近距离放射治疗是局部晚期宫颈癌根治性放疗的标准模式,而施源器是宫颈癌近距离治疗不可缺少的工具[3‐6]。图像引导近距离治疗(Image‐Guided Brachytherapy,IGBT)是近年来宫颈癌近距离治疗模式的重大突破,其靶区概念从传统的A点处方剂量演变成了三维的剂量体积直方图(Dose Volume Histogram,DVH)参数,通过靶区勾画、施源器重建、剂量优化,使宫颈癌的治疗取得了更好的效果并降低了并发症的发生[7‐12]。但在实施IGBT的过程中,转运患者、患者疼痛等因素可能导致施源器在体内发生移位,而近距离治疗的物理剂量分布遵循平方反比定律,施源器移位将影响实际治疗的剂量精度,造成肿瘤局部剂量缺失或危及器官(Organ at Risk,OAR)受量增加等严重后果。该试验的目的是通过评估在宫颈癌患者IGBT中使用自制施源器固定器的安全性和可行性,通过比较施源器位置变化情况评估施源器固定器的应用价值,为实现IGBT精确治疗提供参考。
1 材料和方法
1.1 自制施源器固定器
在转移床板的一端设置施源器固定器,包括设置在床体上用于调节固定立柱子高度和位置的架体,固定立柱包括套设在架体上的连接杆和设置在连接杆端部的安装部分,安装部分内设有用于套插施源器的转动装置,施源器上位于转动装置的两端套设有锁紧螺母。该施源器固定装置对施源器的位置和角度进行有效的固定,防止在转运和治疗过程中,施源器出现位移等情况,见图1。
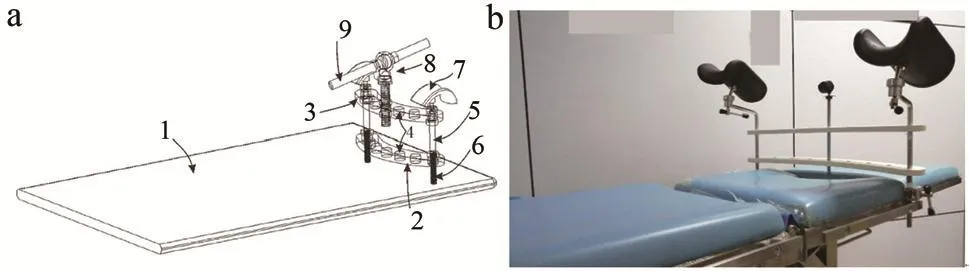
图1 施源器固定装置结构
1.2 仪器设备
Lightspeed螺旋CT模拟定位机(美国通用公司);Oncentra V4.3后装治疗计划系统(荷兰核通公司);Micro‐selectron型高剂量率后装机(荷兰核通公司);标准Fletcher三管施源器(荷兰核通公司)。
1.3 患者资料
选取2017年1—12月在该院治疗的宫颈癌根治性放疗患者40例,年龄43~68岁,平均年龄54.63岁,病理类型为鳞癌,分期Ⅱ~Ⅳ(2009年国际妇产科联盟分期)。该试验通过医院伦理委员会批准,所有患者均已签署知情同意书。要求入组患者:东部肿瘤协作组状态评分达到0~1分,无明显禁忌症,妇检结果显示患者的阴道伸展性适合施源器放置。所有患者分为试验组(n=20,使用自制固定器)和对照组(n=20,使用胶带常规固定),计划于外照射结束后行5次IGBT(单次物理剂量为6 Gy)。
1.4 IGBT定位
患者均先置入尿管排空膀胱,医师完成施源器放置后进行施源器固定:试验组患者使用自制装置固定,对照组患者使用胶带常规固定。将患者推入CT模拟定位室,向膀胱注入150 mL生理盐水,使用CT模拟机进行定位扫描,层间距2.5 mm,扫描范围上起宫腔管顶端上3 cm水平,下至坐骨结节下2 cm,扫描结束后将患者推入准备室等待治疗。为保障患者安全和避免施源器发生移动,整个转运过程均使用专用转运床。
1.5 计划制作和执行
所有患者的靶区勾画工作均由同一高年资医师根据欧洲放射治疗与肿瘤协会妇科协作组推荐方案在Oncentra后装计划系统中完成,要求如下:
(1)靶区:高危临床靶区(High Risk Clinical Target Volume,CTVhr)包括可见的肿瘤病灶和全部宫颈区域,中危临床靶区(Intermediate Risk Clinical Target Volume,CTVir)包括CTVhr及不同安全边界防止潜在的传播,即CTVhr在前后方向外扩5 mm(考虑CTVhr前后方向为膀胱和直肠等正常组织限制),在上下左右方向外扩10 mm。
(2)OARs:包括膀胱、直肠、小肠和乙状结肠。物理师制作并依据CTVhr‐D90(即90%体积CTVhr所接受的最小剂量)为6 Gy和QAR‐D2cc(即2 cm3正常组织所接受的最小剂量)小于处方剂量80%等限制要求来优化近距离放疗计划,根据DVH图评估靶区和OARs的剂量情况。结合外照射联合IGBT,要求最终CTVhr‐D90等效生物剂量(Biologically Equivalent Dose,BED)到达80~90 Gy,膀胱D2cc‐BED小于90 Gy,直肠、小肠和乙状结肠D2cc‐BED小于 75 Gy[13‐14]。
计划经医师审核确定后,传至治疗室进行近距离治疗。考虑到在制作评估计划期间膀胱容积的变化,在实际治疗前将患者膀胱排空后再次注入生理盐水150 mL,即与定位扫描时保持一致。待治疗结束后以相同条件再次进行CT扫描定位,前后两次图像扫描时间间隔应在2 h以内。
1.6 评价指标
1.6.1 施源器位移变化
将治疗前后两次扫描图像传入Oncentra计划系统以宫腔管的顶点和基点在三维坐标系中的坐标作为参考点进行融合(当参考点位移>5 mm判定为施源器发生位移),评估施源器在患者左右(LR)、上下(SI)和前后(AP)等方向的位移情况。
1.6.2 评估不良反应和近期疗效
患者在治疗期间每周至少1次血常规和妇检,按照美国国立癌症研究所通用毒性标准5.0版(Common Terminology Criteria for Adverse Events,CTCAE V5.0) 将不良反应分为0~V度(无、轻度、中度、重度、威胁生命、死亡)。
按照实体瘤治疗效果评价标准1.1版(Response Evaluation Criteria In Solid Tumors,RECIST V1.1)评价局部治疗效果:① 完全缓解(Complete Response,CR):肿瘤病灶完全消失;② 部分缓解(Partial Response,PR):肿瘤病灶和基线水平比较,直径减少大于等于30%;③ 疾病进展(Progressive Disease,PD):肿瘤病灶和基线水平比较,直径增加大于等于20%;除外,必须满足病灶直径和的绝对值增加至少5 mm(出现一个或多个新病灶也视为疾病进展);④ 病情稳定(Stable Disease,SD):肿瘤病灶直径变化程度介于PR和PD两者之间,即肿瘤病灶直径减小程度没达到PR,增加程度也没达到PD水平。治疗有效率即为(CR+PR)/总人数×100%。
1.7 统计学方法
2 结果
试验组20名患者均完成5次IGBT,共计100次;对照组1名患者仅完成4次IGBT,其余19名患者完成5次IGBT,共计99次。
2.1 施源器位移情况
在LR、SI和AP方向,测量试验组宫腔管施源器的顶点和基点位移情况共600次,发生位移共计66次,位移率11%;测量对照组宫腔管施源器的位移情况共594次,发生位移共计100次,位移率16.8%;两组比较位移率差异有统计学差异(χ2=8.490,P=0.004)。试验组宫腔管施源器顶点在LR和SI方向移位度均显著小于对照组(t=‐2.056,‐2.114,P<0.05),试验组宫腔管施源器基点在LR和SI方向移位度均显著小于对照组(t=‐2.510,‐2.403,P<0.05)。所有患者施源器位移情况,见表1。
表1 两组患者施源器位移情况比较(mm,±s)
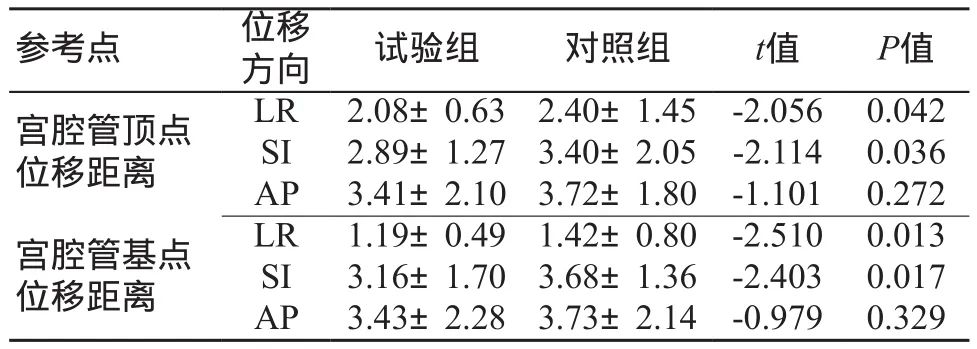
表1 两组患者施源器位移情况比较(mm,±s)
注:LR为患者左右方向,SI为患者头脚方向,AP为患者腹背方向。
参考点 位移方向 试验组 对照组 t值 P值宫腔管顶点位移距离LR 1.19±0.49 1.42±0.80 ‐2.510 0.013 SI 3.16±1.70 3.68±1.36 ‐2.403 0.017 AP 3.43±2.28 3.73±2.14 ‐0.979 0.329 LR 2.08±0.63 2.40±1.45 ‐2.056 0.042 SI 2.89±1.27 3.40±2.05 ‐2.114 0.036 AP 3.41±2.10 3.72±1.80 ‐1.101 0.272宫腔管基点位移距离
2.2 不良反应
在治疗期间患者均接受顺铂同步化疗,故不良反应较相近,试验组和对照组具体的不良反应发生率比较无统计学差异,见表2。
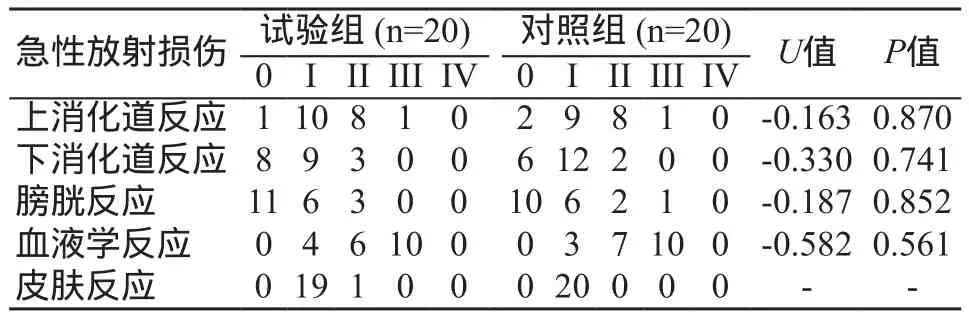
表2 两组患者急性放射损伤对比(例)
2.3 近期疗效比较
患者在治疗结束后1个月行查体和盆腔核磁共振等进行复查,结合查体和影像学资料:试验组CR+PR共计19人,治疗有效率为95%(19/20),而对照组CR+PR共计18人,治疗有效率为90%(18/20),两组的治疗有效率差异不具有统计学差异(χ2=‐0.427,P=0.669)。
3 讨论
在西部欠发达地区,由于宫颈病变筛查工作尚不完善,大部分的宫颈癌患者确诊时已发展为浸润癌,导致其发病率和死亡率均居高不下。宫颈癌目前的治疗模式以综合治疗为主,主要包括手术、放疗和化疗等,其中放疗作为局部治疗手段已广泛应用于各期宫颈癌的治疗中,并且为无法行根治性外科手术切除的中晚期宫颈癌患者提供了治愈的可能,腔内近距离治疗联合体外照射已成为中晚期宫颈癌标准的治疗模式[15‐18]。随着现代影像技术的发展与普及,CT、MRI等三维成像引导技术逐步应用于宫颈癌的近距离治疗中,大大改善了传统二维后装治疗可能存在的靶区遗漏缺点[19]。由于需要将患者在施源器置入后需要推入CT模拟定位机室进行定位,在转移过程中以及治疗过程中若有施源器移位会直接造成治疗计划无法准确实施,并造成靶区及OAR受量不准确,可能会造成肿瘤局部剂量缺失及OAR受量增加的风险[20]。因此,针对宫颈癌近距离治疗中施源器是否移位的研究具有重要意义。
当在转运患者中、或出现患者躁动或阴道收缩时,若施源器未行有效固定,可能出现位移甚至脱出的情况。施源器移位不但会影响靶区吸收剂量,也会对OAR的受量带来较大的改变,特别那些是位置靠近子宫的器官,如膀胱、直肠、乙状结肠等。施源器移位所引起的吸收剂量的改变,很可能导致靶区的吸收剂量过高或不足,同时也会可能造成OAR的吸收剂量过高,进而增加了放射性膀胱炎和放射性直肠炎等并发症的发生率。在李菲等[21]的研究中,经应用自制T型固定带固定,使得施源器各方向位移均得到较好的控制。而在该研究中,通过使用自制施源器固定器,使得施源器在三维方向位移均得到较好的控制,尤其是左右、上下方向位移度均显著少于对照组,施源器固定器有效控制了施源器的位移。De Leeuw等[22]对MRI引导下脉冲式三维近距离治疗宫颈癌时施源器移位对靶区、OAR受量变化也进行了相关研究。而在该研究中,通过使用固定器有效地保持了施源器的一致性,较好地杜绝了因施源器移位而造成的靶区及OAR剂量变化。通过比较两组患者,发现试验组近期治疗有效率与对照组不存在统计学意义的差异,与文献报道相当,均达到90%左右[23‐25];而所有患者均接受内外联合放射治疗和同步化疗,所表现的急性期不良反应近似。
入组患者的远期疗效以及不良反应还有待进一步观察,同时需要更多病例入组来得出更符合临床实际的参数结果。在使用固定器过程中需两人熟练操作,协助完成,一人控制施源器,另一人进行固定。该固定器为一般性设计和制作,以后在此基础上将尝试开发智能化和适配多类型施源器的固定装置。综上所述,对于接受IGBT的宫颈癌患者,通过应用自制施源器固定器,较好地降低了施源器移位率和位移程度,保持了治疗过程中剂量分布的一致性,可以在临床推广使用。

