卵巢甲状腺肿2例
1.郑州大学附属洛阳中心医院影像科(河南 洛阳 471000)
2.郑州大学附属洛阳中心医院超声科(河南 洛阳 471000)
周津如1 杨奇奇1 陈秀杰1 王 华2 行艳艳2 董志辉1,*
卵巢甲状腺肿(struma ovarii,SO)是一种罕见的单胚层卵巢畸胎瘤,SO占卵巢畸胎瘤的2.7%,占所有卵巢肿瘤的0.5%。SO多为良性,仅不到5%为恶性[1]。临床及影像表现不典型,术前极易误诊。现报道我院病理学确诊的2例SO。
1 临床资料
女,66岁,主因“体检发现盆腔占位”入院,平素体健,偶有小腹胀痛。实验室检查无明显异常。超声所见:右侧附件区子宫后方囊实性包块,以囊性为主。CDFI:实性部分少许血流信号。超声考虑:右侧卵巢囊腺瘤。CT所见:子宫右上方圆形稍高密度肿块,囊性部分CT值约60HU,病灶右缘见不规则低密度区,增强扫描不规则低密度区较平扫边界清晰,旁边可见点线样明显强化,肿块囊性部分未见强化。CT考虑:右侧卵巢占位,性质待定。
女,69岁,主因“下腹间断疼痛2年,加重1个月”入院,实验室检查无明显异常。超声所见:盆腔内不规则囊实性包块,内回声不均质,病灶与邻近结构分界不清。CDFI:实性部分中量血流信号。超声考虑:卵巢畸胎瘤。CT所见:子宫与直肠陷凹内见形态不规则囊实性肿块,病灶边缘及分隔见多发线样钙化影,内实性成分呈略高密度,增强后囊性部分未见强化,实性成分明显强化。CT考虑:卵巢畸胎瘤,恶性可能性大。
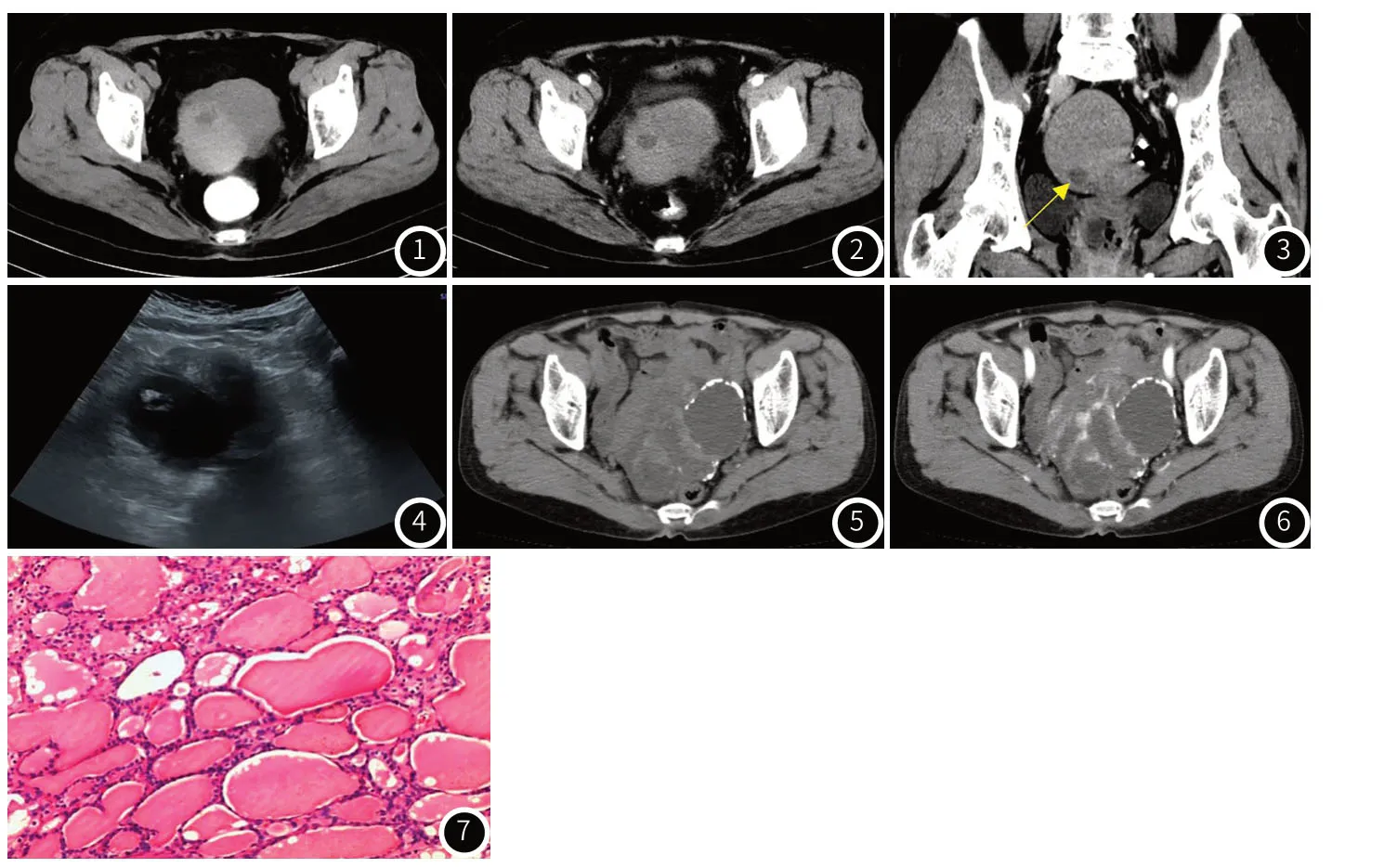
图1~3 子宫右上方圆形稍高密度肿块,病灶右缘见不均匀低密度区,增强扫描低密度区较平扫边界清晰,冠状位重组肿块右下方见点线状明显强化影,余囊性部分未见强化。图4 超声示病灶内大部分为囊性成分,大囊内见囊实性结节。图5~6 盆腔内囊实性不规则肿块,病灶边缘及内部多发线样钙化影,肿块内部实性成分呈略高密度,增强后囊性部分未见强化,实性成分明显强化。图7 病理诊断:卵巢甲状腺肿(HE×200)。
2 讨论
SO好发于23~71岁女性,以育龄期女性为主[1],本文中两例均为绝经后女性。患者可能会经历腹痛、腹胀、部分触诊时可摸到下腹部肿块,但在多达40%的病例中无临床症状[2]。SO通常表现为单侧附件区囊实性肿块,双侧较少见。在CT图像上,肿瘤多呈囊实性改变,以囊性成分为主,根据囊的多少可以分为单囊病灶和多囊病灶。单囊病灶密度多均匀,以稍高密度为主,约66.7%病例囊腔内CT值大于50HU[2],本文第一例囊性病灶CT值为60HU。高密度囊腔为SO在CT平扫中最具特征的表现,其可能由于滤泡内富含的甲状腺素有很强的X线衰减能力,并非真正的密度增加,故高密度囊腔在超声声像图中表现为无回声或低回声。囊性SO内部也存在不规则结节样小突起,由于CT软组织分辨率较低,很难区分高密度囊腔内软组织结节,超声却可以清晰显示囊内实性成分。所以两者结合可以提高单囊SO诊断的准确率[3]。多囊病灶是SO最主要的表现形式,肿瘤与周围结构分界清晰或模糊,其内密度极不均匀,囊内可见分隔及钙化,肿块内沿着增厚间隔或囊壁的钙化也是特征之一,文献报道其出现率在54%[4]。增强扫描囊内实性成分明显强化,部分甚至出现“甲状腺样强化”。其可能与含有成熟甲状腺组织、纤维基质、丰富的血管有关[3]。另外,约17%患者可出现胸腔、腹腔积液,并伴有CA125的升高,但没有腹腔和大网膜的转移[5]。
SO需要与囊性畸胎瘤、卵巢囊腺瘤或囊腺癌、子宫内膜异位症、输卵管-卵巢脓肿及转移瘤进行鉴别。囊性畸胎瘤一般含有脂肪成分,而SO一般少见脂肪。不含脂肪的畸胎瘤实性成分CT值一般低于SO。卵巢囊腺瘤表面光滑,囊壁较薄,囊腔密度低且均匀,无明显实性成分或含有少量实性成分,由于SO富含甲状腺球蛋白等成分,在MRI上可呈现T1高信号[6],也可与囊腺瘤鉴别。卵巢癌囊壁及分隔厚薄不均,软组织可见不规则壁结节,增强后强化程度低于甲状腺肿。但是卵巢癌可以表现出非常复杂的特征,有些会出现类似于甲状腺肿的花边型结构,此外,当卵巢囊腺癌出现出血时,表现为与SO中胶体相似的特征,鉴别仍然比较困难。子宫内膜异位症囊肿也可以出现密度不均匀囊实性肿块,但患者多有痛经病史,且由于病灶反复出血机化,导致与周围组织粘连分界不清。输卵管-卵巢脓肿具有典型的疼痛、发热和高白细胞增多症的临床症状,与SO无症状的临床表现不同。转移瘤通常表现为双侧附件区肿块,并伴有腹盆腔大量积液和腹膜转移征象,临床往往可以找到其原发肿瘤。文献报道95%的SO是良性的,临床上对良性和恶性卵巢肿瘤所进行的手术是完全不同的,所以术前正确诊断对于保留育龄期妇女的生育能力有重要意义。

