正交试验优选制洋金花的炮制工艺研究
夏永严 李娅 秦昆明 杨超 蔡宝昌 金俊杰

【摘 要】 目的:对制洋金花的炮制工艺进行优化。方法:以东莨菪碱含量和水分含量的综合评分为指标,采用正交试验考察生姜打汁后加水量(A)、闷润时间(B)、炒制温度(C)、炒制时间(D)4项指标,确定制洋金花的最佳炮制工艺。结果:筛选出制洋金花的最佳工艺参数为生姜打汁后加水量(A)3倍,闷润时间(B)40 min,炒制温度(C)270~300 ℃、炒制时间(D)5 min,炮制后的制洋金花有酒香气和微姜味。结论:优选得到的制洋金花炮制工艺稳定可行,为更好地控制制洋金花的质量提供科学依据。
【关键词】 制洋金花;炮制工艺;东莨菪碱;正交试验
【中图分类号】R283 【文献标志码】 A 【文章编号】1007-8517(2021)09-0058-05
Abstract:Objective To study the processing technology of Fried Daturae Flos by orthogonal experiment. Methods Taking scopolamine and water content as the evaluation indexes, the effects of ginger water added(A), wetting time(B), frying temperature(C) and frying time(D) on the processing technology were investigated by orthogonal experiment. Finally determine the best processing technology for Fried Daturae Flos. Results The optimum technological parameters for fried Daturae Flos are 3 times of ginger water added(A), 40 min of wetting time(B), 270~300 ℃ of frying temperature(C) and 5 min of frying time(D). The processed Daturae Flos smell has aroma of wine and slight ginger. Conclusion The optimal process of fried Daturae Flos is stable and feasible, which can provide scientific basis for better control of its quality.
Keywords:Fried Daturae flos; Processing Technology; Scopolamine; Orthogonal Experiment
洋金花Daturae flos为茄科植物白花曼陀罗Datura metel L.干燥花,性味辛温、有毒[1]。研究表明洋金花具有麻醉人体中枢神经系统作用,伍玉哲等[2]对87例临床患者进行镇痛研究表明洋金花制剂镇痛明显,故洋金花以“中药麻醉”临床功效而被广泛使用[3]。洋金花具有毒性,内服急性中毒报道6例[4],多由误服或用量过度所导致,在内服用量上需谨慎[5]。对于洋金花在临床使用有明显镇痛效果,表明其具有临床使用价值,但因其本身具有毒性或临床使用量不精确,临床上解决方法:一方面可以通过控制临床用量,减少其毒性反应出现,另一方面对洋金花进行炮制,达到减毒增效和提高其内在质量稳定性的效果。对制洋金花的炮制工艺进行研究,获得稳定的炮制工艺参数,形成质量均一稳定的制洋金花,有助于制洋金花的临床使用安全有效。
制洋金花只有《上海市中药饮片炮制规范》[6]收载:将生洋金花用生姜汁拌匀,待吸透,略润,切成1~2 mm细丝,置锅内,炒干,趁热喷洒白酒,拌匀,稍闷,晾干(每生洋金花100 kg,用生姜25 kg打汁,60°白酒12.5 kg)。目前,《藥典》规定洋金花含量测定成分为东莨菪碱[1],未有相关文献对制洋金花的炮制工艺优化报道,对于炮制工艺中“将生洋金花用生姜汁拌匀”中生姜汁加水量及之后进行的闷润时间和“置锅内,炒干”中的炒制温度和炒制时间未有明确的参数,为将其更好地用于临床,本课题组对其进行最佳炮制工艺探索。
1 仪器与试药
1.1 仪器 LC-20AT型高效液相色谱仪(SPD-M20A二极管阵列检测器)(日本岛津公司)、BP211D型万分之一电子天平(北京赛多利斯仪器系统有限公司)、FN1004N型十万分之一电子天平(北京赛多利斯仪器系统有限公司)、PHS-3C精密数显台式酸度计PH计(上海雷磁仪器有限公司)、RE-52型旋转蒸发仪(BUCHI)、KQ5200DE型数控超声波清洗器(昆山市超声仪器有限公司)、XL-10B型500g密封型摇摆式高速粉碎机(广州市旭朗机械设备有限公司)、SHZ-D(III)型循环水式真空泵(巩义市予华仪器有限责任公司)、榨汁机JYZ-D57(九阳)。
1.2 试药 洋金花(产地安徽)和生姜(产地山东),购自南京海源中药饮片公司,并经南京海源中药饮片有限公司首席质量官执业中药师丁斐鉴定,洋金花Daturae flos为茄科植物白花曼陀罗Datura metel L.干燥花。氢溴酸东莨菪碱对照品(成都普菲德生物技术有限公司,批号18113008,纯度≥98%)。磷酸钠、十二烷基硫酸钠、磷酸、盐酸、浓氨水、三氯甲烷均为分析纯,乙腈为色谱纯,水为纯化水。
2 方法与结果
2.1 制洋金花中东莨菪碱含量测定方法的建立[1]
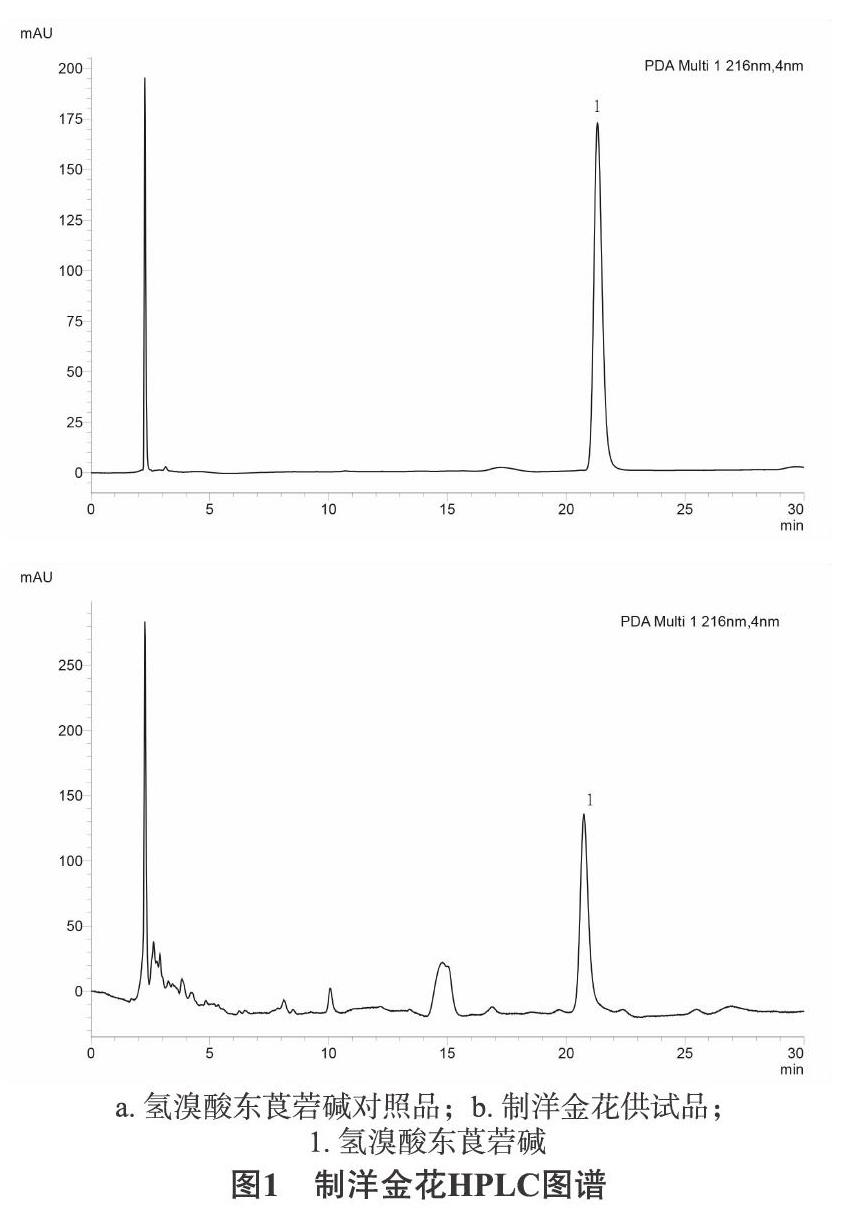
2.1.1 色谱条件 YMC-Pack ODS-A色谱柱(4.6 mm×250 mm,5 μm);流动相:乙腈-0.07 mol/L磷酸钠溶液(含0.0175 mol/L十二烷基硫酸钠,用磷酸调节pH值至6.0)(50∶[KG-*3/5]100)为流动相;流速:1 mL·min-1;检测波长为216 nm;柱温:30 ℃;进样量:10 μL。氢溴酸东莨菪碱对照品和供试品的HPLC图谱如图1所示。
2.1.2 对照品溶液的制备 取氢溴酸东莨菪碱对照品适量,精密称定,加“2.1.1项下”流动相制成每1 mL含0.679 mg的溶液,即得(东莨菪碱重量=氢溴酸东莨菪碱重量/1.445)。
2.1.3 供试品溶液的制备 取制洋金花样品粉末(过三号筛)约1 g,精密称定,置锥形瓶中,加入2 mol/L盐酸溶液10 mL,超声处理(功率250 W,频率40 kHz)30 min,放冷,滤过,滤渣和滤器用2 mol/L盐酸溶液10 mL分数次洗涤,合并滤液和洗液,用浓氨试液调节pH值至9,用三氯甲烷振摇提取4次,每次10 mL,合并三氯甲烷液,回收溶剂至干,残渣用流动相溶解,转移至5 mL量瓶中,加“2.1.1项下”流动相至刻度,摇匀,滤过,取续滤液,即得。
2.1.4 线性关系考察 精密吸取对照品溶液0.2、0.4、0.6、0.8、1 mL各置于1 mL容量瓶中,加“2.1.1项下”流动相定容至刻度,摇匀,制得13.58、27.16、40.74、54.32、67.90 μg/mL。分别吸取对照品溶液各10 μL,按“2.1.1”项下色谱条件进样,记录峰面积值。将所得峰面积(Y)与对照品的浓度(X)进行线性回归,得氢溴酸东莨菪碱回归方程、相关系数(R)及线性范围为Y=12071X+148,R=0.9999,135.8~679 μg/mL。
2.1.5 精密度试验 取“2.1.2”项下对照品溶液10 μL,按“2.1.1”项下色谱条件进样,连续进样6次,记录氢溴酸东莨菪碱峰面积和保留时间值,并计算RSD值,面积和保留时间RSD值分别为1.18%、0.66%,说明该方法精密度良好。
2.1.6 稳定性试验 于0、2、4、8、12、24 h精密吸取按“2.1.3”项下制备的供试品溶液10 μL,按“2.1.1”项下色谱条件进样分析,记录氢溴酸东莨菪碱峰面积和保留时间值,计算 RSD值,面积和保留时间RSD值分别为1.77%、1.00%,说明供试品溶液在24 h内具有较好的稳定性。
2.1.7 重复性试验 制洋金花样品粉末混合均匀分成6份,按“2.1.3”项下方法制备得供试品溶液,分别吸取10 μL,按“2.1.1”项下色谱条件进样,记录氢溴酸东莨菪碱含量和保留时间值,并计算RSD值,氢溴酸东莨菪碱平均含量0.15%,含量和保留时间RSD值分别为1.35%、0.72%,说明该方法重复性良好。
2.1.8 加样回收率试验 制洋金花样品粉末9份,每份0.5 g,各加入对照品溶液0.9、0.9、0.9、1.1、1.1、1.1、1.3、1.3、1.3 mL,按“2.1.3”项下方法制备供试品溶液,在三氯甲烷溶解蒸干后的残渣中用流动相溶解,转移至5 mL量瓶中,加“2.1.1项下”流动相至刻度。按“2.1.1”项下色谱条件进样,记录峰面积值,计算回收率以及RSD值,氢溴酸东莨菪碱平均回收率为103.76%,RSD为1.40%,说明该方法具有良好的准确度,具体见表1。
2.2 制洋金花炮制工艺单因素考察
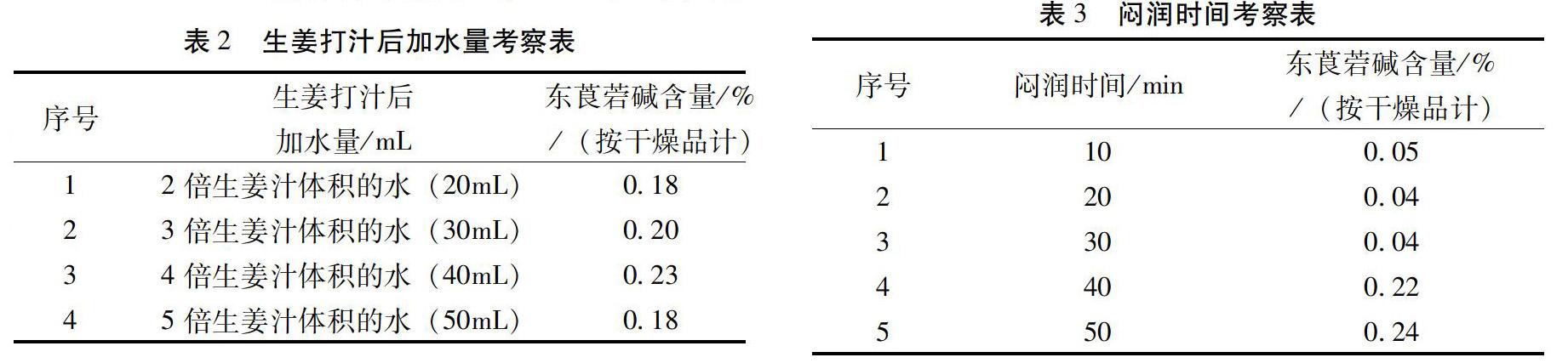
2.2.1 生姜加水量考察 取50 g洋金花样品,生姜用量12.5 g,榨汁机打汁后得到生姜汁10 mL,加水量见生姜打汁后加水量考察表,25 ℃下闷润30 min后切碎,炒制温度190~220 ℃(500 W),炒制时间5 min,样品的温度降到29~30 ℃时,喷洒60°白酒6.25 g,25 ℃下闷润30 min后晾干。按“2.1”项测定东莨菪碱含量。生姜打汁后加水量考察见表2。由表2可知,生姜打汁后加水量为2倍生姜汁体积的水(20 mL)、3倍生姜汁体积的水(30 mL)、4倍生姜汁体积的水(40 mL)时,东莨菪碱含量较高。
2.2.2 闷润时间考察 取50 g洋金花樣品,生姜用量12.5 g,榨汁机打汁后得到生姜汁10 mL,加3倍生姜汁体积的水(30 mL),25 ℃下闷润后切碎,闷润时间见闷润时间考察表,炒制温度190~220 ℃(500 W),炒制时间5 min,样品的温度降到29~30 ℃时,喷洒60°白酒6.25 g,25 ℃下闷润30 min后晾干。按“2.1”项测定东莨菪碱含量。闷润时间考察见表3。由表3可知,闷润时间为30 min、40 min、50 min时,东莨菪碱含量较高。
2.2.3 炒制温度考察 取50 g洋金花样品,生姜用量12.5 g,榨汁机打汁后得到生姜汁10 mL,加3倍生姜汁体积的水(30 mL),25 ℃下闷润30 min后切碎,炒制温度见炒制温度考察表,炒制时间5 min,样品的温度降到29~30 ℃时,喷洒60°白酒6.25 g,25 ℃下闷润30 min后晾干。按“2.1”项测定东莨菪碱含量。炒制温度考察见表4。由表4可知,炒制温度为100~130 ℃、190~220 ℃、270~300 ℃时,东莨菪碱含量较高。[KH*1]
2.2.4 炒制时间的考察 取50 g洋金花样品,生姜用量12.5 g,榨汁机打汁后得到生姜汁10 mL,加3倍生姜汁体积的水(30 mL),25 ℃下闷润30 min后切碎,炒制温度190~220 ℃(500 W),炒制时间见炒制时间考察表,样品的温度降到29~30 ℃时,喷洒60°白酒6.25 g,25 ℃下闷润30 min后晾干。按“2.1”项测定东莨菪碱含量。炒制时间考察见表5。由表5可知,炒制时间为5 min、6 min、7 min时,东莨菪碱含量较高。
2.3 制洋金花炮制工艺正交试验
2.3.1 正交试验设计 根据单因素试验的结果,取洋金花样品选择生姜打汁后加水量(A)、闷润时间(B)、炒制温度(C)、炒制时间(D)为考察因素,以东莨菪碱含量和水分含量评价为指标,进行正交设计安排实验,因素水平见表6。
2.3.2 正交试验结果 采用L9(34 )表安排试验,以东莨菪碱含量和水分含量评价为指标,制洋金花中水分测定方法见2015版《中国药典》通则0832第二法[7]。以综合加权评分法来评价,评分方法为东莨菪碱含量占80%,水分含量占20%。东莨菪碱含量和水分含量的满分均为10分,综合评价=东莨菪碱含量/最大的东莨菪碱含量×10×80%+水分含量评价/最大的水分含量评价×10×20%。水分含量评价标准如表7,实验结果见表8,方差分析见表9。
由方差分析可知,生姜加水量对于制洋金花的炮制工艺具有显著性影响,其影响因素重要性为:生姜打汁后加水量>炒制时间>炒制温度>闷润时间。根据正交试验结果,第5组实验综合评价最高,其中东莨菪碱含量和水分含量评价均为最高值,所以选择第5组实验方法为最优炮制工艺,即取50 g洋金花样品,用生姜12.5 g打汁后加3倍生姜汁体积的水(30 mL),25 ℃下闷润40 min后切碎,在270~300 ℃下炒制5 min,29~30 ℃下喷洒6.25 g的60°白酒后,25 ℃下闷30 min,晾干。
2.3.3 验证试验 采用确定的最优炮制工艺条件,取洋金花样品进行3次平行试验,计算东莨菪碱含量和水分,3次测定结果均优于正交试验各工艺结果,说明制洋金花的炮制工艺合理可行,结果见表10。
3 讨论
生姜加水量范围选择,润透洋金花药材考察得出,低于2倍生姜汁体积的水(20 mL),洋金花药材没有润湿完全,高于5倍生姜汁体积的水(50 mL),洋金花药材过于润湿,有滴水现象。对炮制工艺中的喷洒60°白酒进行考察,选取药材温度和喷洒60°白酒后的药材闷润时间进行考察,药材温度过高时喷洒过白酒的药材进行闷润,白酒挥发快,本项炮制工艺消耗时间短,结果酒味淡;药材温度过低时喷洒过白酒药材闷润后,白酒挥发慢,本项炮制工艺消耗时间长,结果酒味浓。本项炮制工艺优选药材温度降到29~30 ℃时,喷洒60°白酒,25 ℃下闷润30 min后晾干,使炮制后的饮片有酒香气,同时本项炮制工艺用时短,展示出本项炮制工艺效率。
在制洋金花的單因素考察中选取东莨菪碱含量为指标,但在炮制过程中发现虽然水分在上海市中药饮片炮制规范[6]中没有明确规定,但其会影响贮藏时间、外观等方面,在正交试验中以水分为评价指标,以2015版《中国药典》对洋金花水分[1]规定的不超过11%为上限,下限不低于5%,制洋金花炒制后表面太干燥,水分含量太少,外观变形难识别,造成其性状鉴别难度。
洋金花作为一种毒性药材,临床上多有不良反应报道,本项研究对制洋金花进行炮制工艺研究,运用正交试验对制洋金花的炮制工艺研究,为其他研究工作者提供制洋金花的炮制工艺参考,提高制洋金花的内在质量稳定性,同时在建立药材内在质量稳定性的情况下,才有药材功效和毒性的稳定性。优化制洋金花的炮制工艺有利于其质量控制和临床用药安全,下一步将开展制洋金花的毒性试验研究,同时查找出制洋金花中的毒性标记物成分。
参考文献
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:267.
[2]伍玉哲,高珺.洋金花制剂在手术麻醉中的疗效分析[J].中药药理与临床,2015,31(1):339-340.
[3]周化春.洋金花的药理作用及临床应用研究[J].中医临床研究,2017,9(9):129-130.
[4]黄诺嘉.毒性中药洋金花急性中毒6例报告[J].中国药事,2007,21(2):141-142.
[5]井佳楠,吕邵娃,王秋红,等.洋金花化学成分和药理作用及临床应用研究进展[J].中草药,2016,47(19):3513-3521.
[6]上海市食品药品监督局.上海市中药饮片炮制规范[M].上海:上海科学技术出版社,2008:338-339.
[7]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:103.
(收稿日期:2020-10-19 编辑:程鹏飞)

