宫腔镜下电切术与刮宫术治疗子宫内膜息肉患者的临床效果观察
陈丽华
(无锡市惠山区第二人民医院妇产科,江苏无锡 214001)
子宫内膜息肉 (endometrial polyps,EP)是临床妇科常见的女性疾病,主要是因为子宫内膜结缔组织或局部血管异常增生,导致子宫腔内出现单个或多个突出的局限性肿物。据相关流行病学研究调查结果显示,在我国妇科疾病中,子宫内膜息肉的患病率占24%~25%[1]。子宫内膜息肉的数量、大小及位置与对患者造成的影响关系密切,较小、单发的息肉常无明显临床表现,而较大、多发的息肉会严重破坏子宫内膜环境,使宫腔形态改变,导致子宫功能受损,从而进一步导致各种妇科疾病的发生[2]。因此,对于持续存在的子宫内膜息肉,应尽早进行干预治疗,以避免严重不良后果的发生。近年来,随着现代医学技术的不断发展,宫腔镜被广泛应用于临床子宫内膜息肉的诊断和治疗中。在宫腔镜直视下进行息肉清除可有效减轻卵巢和子宫功能受到的损伤。电切术与刮宫术是子宫内膜息肉治疗的常用术式,刮宫术操作简单,但易发生息肉刮除不彻底等情况,从而导致复发率升高;而电切术通过电切环切除息肉,可直达子宫浅肌层以下2.5 mm,切除更彻底,减少了复发风险,在一定程度上较刮宫术更具优势[3]。基于此,本次研究就宫腔镜下电切术与宫腔镜下刮宫术应用于子宫内膜息肉的效果进行了对比,详细报告如下。
1 资料与方法
1.1 一般资料 选取无锡市惠山区第二人民医院2019年5月至2020年1月收治的54例子宫内膜息肉患者为研究对象,根据随机数表法将其分为两组:电切组与刮宫组,每组各27例。电切组患者年龄20~42岁,平均年龄 (31.13±8.44)岁;病程1~7年,平均病程 (3.25±1.64)年。刮宫组患者年龄21~41 岁,平均年龄 (30.94±8.32)岁;病程1~8年,平均病程 (3.31±1.67)年。两组患者的一般资料比较,差异无统计学意义 (P>0.05),可进行对比研究。本研究经无锡市惠山区第二人民医院医学伦理委员会批准。患者及家属均知情并签署知情同意书。子宫内膜息肉临床诊断标准[4]:①阴道超声检查是诊断子宫内膜息肉的首选,超声下可看到边界清楚的高回声结节,部分可显示为子宫内膜厚度增厚,此种情况一般会显示回声不均但有局部增强;②宫腔镜联合病理检查是诊断子宫内膜息肉的金标准,镜下可见单个或多个尺寸不等的有蒂柔软突出肿物。纳入标准:①临床确诊为子宫内膜息肉的患者;②初次进行宫腔镜下治疗的患者;③可耐受宫腔镜手术的患者。排除标准:①存在其他子宫疾病的患者;②存在生殖道感染的患者;③存在凝血功能障碍的患者;④存在手术禁忌证的患 者。
1.2 方法 术前完善两组患者各项相关术前检查及妇科检查等。刮宫组患者均采用宫腔镜下刮宫术方案治疗,具体操作:患者取膀胱截石位,予行静脉麻醉,麻醉成功后,进行扩张子宫颈的操作,完全暴露手术视野,然后使用宫腔镜检查患者子宫腔,定位病灶,明确息肉的数量及大小,选择合适的刮匙并实施刮宫手术治疗,治疗结束后再次使用宫腔镜观察宫腔内情况及息肉是否刮净。电切组患者均采用宫腔镜下电切术方案治疗,具体操作:体位、麻醉与宫腔镜检查操作同刮宫组。经宫腔镜定位病灶后,使用电切环从宫底至宫颈外口,依次定位并切除息肉根部,切割深度至子宫内膜基底下2~3 mm,并对出血部位进行电凝止 血。
1.3 观察标准 ①分析比较两组患者的手术情况:包括手术时间、术中出血量及住院时间;②分析比较两组患者的并发症发生情况:对患者进行随访,观察其3个月内并发症发生情况,如持续腹痛、感染、宫腔黏连等;③分析比较两组患者的病灶情况:对患者进行术后随访,了解其12个月内子宫内膜息肉的复发情况。
1.4 统计学分析 本次研究采用SPSS 20.0版统计学软件对数据资料进行分析处理。计量数据资料均以 ()表达,以t进行检验;计数数据资料均以[例 (%)]表达,以χ2进行检验。P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者的手术情况比较 两组患者的手术时间及住院时间比较,差异无统计学意义 (P>0.05)。但是电切组患者术中出血量少于刮宫组,组间比较差异有统计学意义 (P<0.05),见表1。
表1 两组患者的手术情况比较 ()

表1 两组患者的手术情况比较 ()
组别 例数 手术时间 (min)术中出血量 (mL)住院时间(d)电切组 27 23.17±7.33 3.10±0.62 3.26±0.77刮宫组 27 23.64±6.74 4.63±0.79 3.24±0.79 t值 1.017 5.610 0.873 P值 >0.05 <0.05 >0.05
2.2 两组患者的并发症发生情况比较 电切组患者的并发症发生率为7.41%,明显少于刮宫组的14.81%,组间比较差异有统计学意义 (P<0.05),见表2。
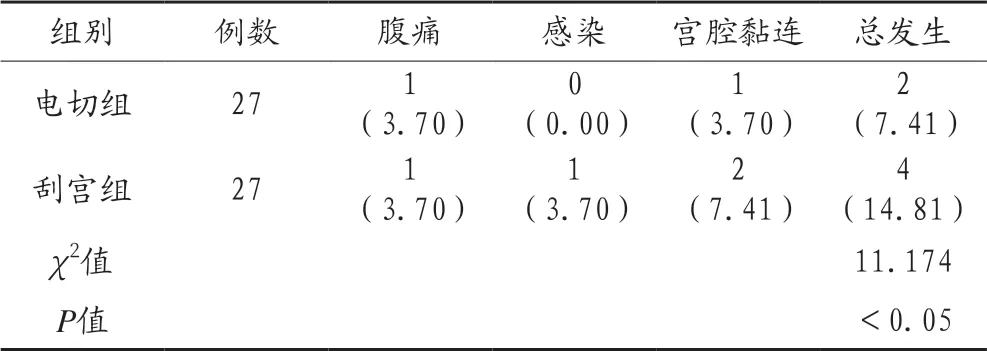
表2 两组患者的并发症发生情况比较[例 (%)]
2.3 两组患者的术后复发情况比较 电切组患者12个月内病灶复发率为7.41%,明显低于刮宫组的25.93%,组间比较差异有统计学意义 (P<0.05),见表3。
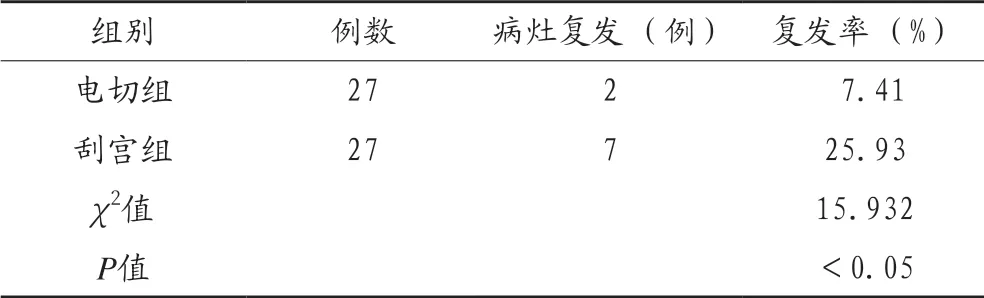
表3 两组患者的术后复发情况比较
3 讨论
子宫内膜息肉 是位于子宫内膜基底层的一种局限性增生,由间质、厚壁血管及腺体等组成,其发病原因尚不明确。大多患者的子宫内膜息肉较小,无明显临床症状表现,部分患者息肉较大,可表现为经期延长、不规则阴道流血等。在不孕妇女中,子宫内膜息肉的发生率为2.8%~3.9%[5],这说明子宫内膜息肉对于女性生殖功能具有一定影响。虽然95%以上的子宫内膜息肉为良性病变,但若不予及时有效的治疗与干预,随着年龄增长及病情进展也可发展为瘤样增生,甚至发生癌变,因此,选择合适有效的治疗手段对子宫内膜息肉患者的康复至关重要[6-7]。
宫腔镜是临床应用较为广泛的一种微创技术,是一套将光源、传导、成像技术整合在一起的设备系统,医生可通过宫腔镜直接观察患者的宫腔内情况及病灶情况,并在直视下进行治疗或检查,大大减少了误诊、误治率,提高了疾病检出率和准确性,具有操作时间短、出血少、恢复快等优点[8]。目前,宫腔镜下电切术与刮宫术是子宫内膜息肉治疗的两种主要手段。电切术是经宫腔镜定位后,用电切环将电能通过不同的转化方式,以热效应对息肉部位及其周围内膜进行破坏切除,该种术式在保证手术效果更好的同时还能减少并发症发生率。但电切术的手术过程中需注意电切环的切割深度及范围,若切割过浅、范围过小则易发生息肉残留和病灶复发,而切割过深、范围过大则易损伤子宫内膜,甚至可能造成穿孔,对患者未来的妊娠也可能造成一定的潜在影响[9-10]。刮宫术操作方式相对简单,但是该方法存在术后阴道出血发生率较大,且术后病灶复发率相对较高,而治疗后的妊娠率较低等缺点[11]。
本次研究结果中,电切组与刮宫组患者的手术时间及住院时间比较,差异无统计学意义 (P>0.05),但是电切组患者术中出血量、并发症发生率、12个月内病灶复发率均明显低于刮宫组,组间比较差异有统计学意义 (P<0.05)。关于两组病灶复发率的差异,通过对两组手术方法的机制进行研究分析,认为可能是由于宫腔镜下电切术能够对病灶周围的组织及潜在的、尚未明显突出的子宫内膜息肉进行彻底清除,治疗更加彻底,因此减少了病灶复发。同时,电切术在手术过程中通过电凝止血的方式,在减少术中出血量的同时,也保证了手术安全性,从而降低了患者并发症的发生率。
综上所述,宫腔镜下电切术可有效切除子宫内膜息肉,相较于刮宫术的效果更理想,可以明显减少术中出血量,并发症发生率更低,病灶复发情况更少,值得推广应用。

