多相复合富锂锰基材料的合成及性能
赵 珊,徐 星*,石 斌,杜春雨
(1. 贵州梅岭电源有限公司,特种化学电源国家重点实验室,贵州 遵义 563003;2. 哈尔滨工业大学化工与化学学院,黑龙江 哈尔滨 150001)
正极材料是决定锂离子电池能量密度、使用寿命及成本等指标的关键因素。 现有的商业化锂离子电池正极材料中,LiCoO2、LiMn2O4、LiFePO4和LiCoxNiyMnzO2的实际比容量普遍低于200 mAh/g,不能够满足人们对高能量密度锂离子电池的需求。 富锂锰基正极材料xLi2MnO3(1-x)LiMO2(M=Ni、Co 和Mn)具有接近300 mAh/g 的高比容量,是实现锂离子电池400 Wh/kg 高比能量的良好选择,颇有发展前景。 制备困难、倍率性能差、首次库仑效率低及容量衰减快等问题,严重制约了富锂锰基正极材料的应用进程。
富锂锰基正极材料的合成方法主要有:共沉淀法、高温固相法、溶胶-凝胶法、熔盐法和水热法等[1-4]。 高温固相法采用机械手段混合原料,但原料微观分布不均匀,且煅烧温度高、能耗大,锂损失严重,易形成杂相。 溶胶-凝胶法设备简单,合成温度低,可制得高纯度材料,但合成周期长,工艺较复杂。 熔盐法采用低共熔混合盐辅助合成单晶材料,但工艺复杂,成本高。 水热法制备的材料元素分布均匀,且易于调控材料形貌,但元素比例难以控制,反应周期长,工业化难度较大。 共沉淀法具有元素分布均匀、制备工艺简单、周期短和成本低等优点,在三元正极材料的工业生产中应用广泛,但共沉淀反应涉及多相反应过程,反应时需要精确地控制体系的pH 值、温度、络合剂浓度、搅拌速度、固液比及反应液的进料速率等参数。 由于影响因素多,且各参数间存在相互耦合作用,合成工艺的控制困难,始终难以批量合成具有良好球形形貌和电化学性能的富锂锰基正极材料。
针对高性能富锂锰基正极材料的制备难题,本文作者在前期研究的基础上,采用共沉淀-高温固相法制备高性能富锂锰基三元正极材料,并通过XRD、SEM、X 射线能量色散谱(EDS)等对材料的形貌、组成、结构进行分析,对扣式半电池的电化学性能进行测试。
1 实验
1.1 材料合成
采用共沉淀-高温固相法合成富锂锰基三元正极材料。先用碳酸盐共沉淀法合成Mn0.66Ni0.17Co0.17CO3碳酸盐前驱体。 按n(Mn)∶n(Ni)∶n(Co)= 4 ∶1 ∶1配制MnSO4·H2O(南京产,AR)、NiSO4·6H2O(南京产,AR)和CoSO4·7H2O(汕头产,AR)的混合溶液,总浓度为2.0 mol/L;称量并配制2.0 mol/L Na2CO3(汕头产,AR)溶液作为沉淀剂,2.0 mol/L(NH4)2SO4(汕头产,AR)溶液作为络合剂,0.6 mol/L 氨水(天津产,AR)溶液作为反应底液。 用BT100-2J 蠕动泵(英国产)控制反应条件,持续搅拌的六口玻璃反应釜中缓慢加入金属盐溶液、络合剂溶液和沉淀剂溶液,并用pH 复合电极连接HI504 型在线数字pH 控制仪(意大利产),控制反应体系的pH 值为7.49~7.53。 以750 r/min 的转速连续搅拌,反应12 h,继而经过洗涤(蒸馏水常温洗涤5 次)、过滤,再在80℃下真空(真空度为-0.1 MPa,下同)干燥12 h,最终得到粉末状的富锂锰基材料碳酸盐前驱体Mn0.66Ni0.17Co0.17CO3。
高温固相法分为预烧和高温混锂烧结两步。 将碳酸盐前驱体在空气气氛中、600 ℃下热解为CO2和金属氧化物MO(M=Ni、Co 和Mn),预烧8 h。 预烧后的金属氧化物MO与LiOH 充分混合,再在氧气条件下于920 ℃高温混锂烧结20 h,生成Li1.2Mn0.54Ni0.13Co0.13O2富锂锰基正极材料。
1.2 材料分析
用Panalytical Empyrean X 射线衍射仪(荷兰产)测试材料的晶体结构,CuKα,波长为0.154 056 nm,管压50 kV,管流100 mA,扫描速度为4(°)/min,步长0.04°。 用Merlin Compact 场发射环境扫描电子显微镜(德国产)观察和分析材料的微观形貌及粒径分布,加速电压为20 kV。 用PARSTAT2273 型电化学工作站(美国产)进行电化学阻抗谱(EIS)测试,频率为10-2~105Hz。 形貌和元素分布分析通过配备EDS 的FEI Helios Nanolab600i 场发射扫描电子显微镜(美国产)进行,工作电压为10~30 kV。
1.3 电池组装
将正极材料、导电炭黑(Timcal 公司)和聚偏氟乙烯(PVDF,法国产)按8 ∶1 ∶1的质量比制备成浆料,用专用刮刀将浆料均匀涂覆在16 μm 厚的铝箔(佛山产,99.7%)上,涂层厚度为120 μm。 之后,在120 ℃下真空干燥24 h 以上。 在氩气保护的手套箱中组装CR2025 型扣式电池,所用电解液为1 mol/L LiPF6/EC+DMC(体积比1 ∶1,苏州产),隔膜为2325型聚丙烯薄膜(美国产),负极为金属锂片(天津产,99.9%)。
1.4 电化学性能测试
用CT-4000-mA 测试系统(深圳产)对扣式电池进行电化学性能测试,温度为室温25 ℃,电压为2.0~4.6 V。 装配后的电池首先静置10 h,使电解液充分浸润极片,再在30 mA/g(0.1C)的电流下充放电3 次,进行活化。 倍率性能测试分别采用30~1 000 mA/g 的电流,每种电流下循环5 次;循环性能测试采用30 mA/g 和300 mA/g 的电流。
2 结果与讨论
2.1 合成产物的结构和形貌
前驱体材料和富锂锰基三元正极材料的XRD 图见图1。
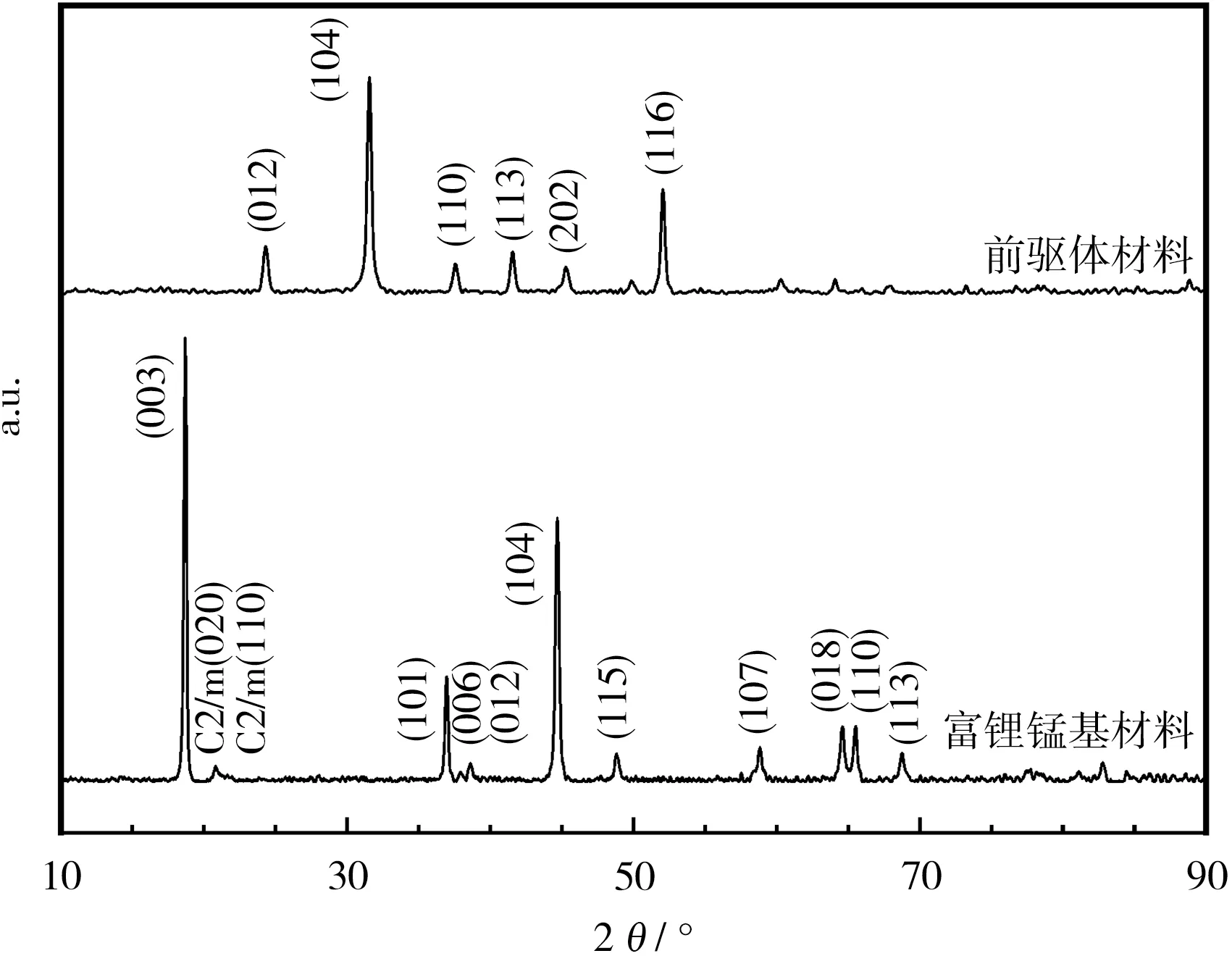
图1 前驱体及富锂锰基正极材料的XRD 图Fig.1 XRD patterns of the precursors and Li-rich Mn based cathode material
从图1 可知,前驱体材料的XRD 图与MnCO3(PDF:86-0172)的物相衍射峰对应,富锂锰基三元正极材料的衍射峰与六方层状结构LiNiO2(PDF:09-0063)和单斜结构Li2MnO3(PDF:27-1252)的衍射峰对应,所有衍射峰的峰形尖锐且峰强度高,说明材料结晶度良好。 在20°~25°出现了一系列较小的衍射峰,是单斜结构的Li2MnO3相的超晶格结构衍射峰,归属于Li2MnO3相中Li 和Mn 在小范围内有序排列而形成的超点阵。 衍射峰(006)和(012)、(018)和(110)的双峰明显分裂,说明材料的层状结构较好。 图1 中存在微弱的与尖晶石结构LiMn2O4相对应的衍射峰,可能是因为预烧后材料中存在少量Mn3O4,在混锂烧结过程中与氢氧化锂发生反应,生成了尖晶石结构LiMn2O4所致。 陆地等[5]研究表明,在富锂锰基正极材料中引入具有三维Li+传输通道的尖晶石结构,有利于提升材料的倍率性能。 XRD 分析结果表明,采用共沉淀-高温固相法合成的富锂锰基三元正极材料,具有结晶度良好的六方层状-单斜层状-立方尖晶石复合结构。
图2 为通过共沉淀法合成的富锂锰基材料碳酸盐前驱体的SEM 图。

图2 600 ℃预烧前后富锂锰基材料碳酸盐前驱体的SEM 图Fig.2 SEM photographs of carbonate precursors of Li-rich Mn based material before and after calcination at 600 ℃
从图2(a)可知,富锂锰基材料前驱体二次颗粒为球形,具有良好的单分散粒度分布,最大粒径为25.80 μm、最小粒径为11.14 μm、平均粒径为18.62 μm;从图2(b)可知,前驱体二次颗粒由纳米一次颗粒紧密团聚而成。
从图2(c)、(d)可知,预烧后前驱体材料由碳酸盐分解成CO2和金属氧化物MO,但球形形貌和粒度分布均没有发生明显的变化。
920 ℃混锂烧结后的富锂锰基正极材料的SEM 图和EDS 面扫描分析图分别见图3、图4。

图3 富锂锰基正极材料的SEM 图Fig.3 SEM photographs of Li-rich Mn based cathode material

图4 富锂锰基正极材料的X 射线EDS 面扫描分析Fig.4 Surface scan analysis of X-ray energy dispersive spectroscopy(EDS) of Li-rich Mn based cathode material
从图3 可知,与前驱体材料相比,在高温固相嵌锂反应后,富锂锰基材料二次颗粒的球形形貌和粒径均匀度未发生明显的变化,但一次颗粒的形貌却明显改变,粒径增大且棱角更明显,说明高温烧结过程中,前驱体与LiOH 发生了固相反应并重结晶。 一次颗粒粒径的增大,有利于降低材料的比表面积和减少在电池中的电极/电解液界面,从而减少充放电过程中副反应的发生,减缓活性物质的溶解,使材料具有更好的电化学性能。
从图4 可知,材料中的Ni、Co 和Mn 元素分布均匀,X 射线EDS 面扫分析结果显示,碳酸盐前驱体材料中Mn、Co 和Ni 的摩尔分数分别是67.64%、16.28%和16.08%;混锂烧结后的富锂锰基三元正极材料中,Mn、Co 和Ni 的摩尔分数是70.05%、16.06%和13.89%,与共沉淀反应过程中加入的Mn、Co 和Ni 的物质的量比4 ∶1 ∶1相符。
为深入研究富锂锰基三元正极材料二次颗粒内部的过渡金属元素分布情况,将材料二次颗粒破碎,并进行横断面EDS 元素线扫描分析,结果如图5 所示。

图5 富锂锰基正极材料半球颗粒的EDS 元素线扫描分布Fig.5 Element line scan distribution of EDS in hemispherical particles of Li-rich Mn based cathode material
从图5 可知,在富锂锰基三元正极材料二次颗粒内部,Mn、Co 和Ni 等3 种元素从球面到球心分布均匀,说明采用共沉淀-高温固相合成法,能获得具有良好球形形貌、元素分布均匀的富锂锰基三元正极材料。
2.2 电化学性能分析
富锂锰基三元正极材料在电流为30 mA/g 时的首次充放电曲线见图6(a);倍率性能测试结果见图6(b)。

图6 富锂锰基正极材料的首次充放电曲线和倍率性能Fig.6 Initial charge-discharge curves and rate capability of Lirich Mn based cathode material
从图6(a)可知,富锂锰基三元正极材料在2.0 ~4.6V的首次充电曲线主要分为两个部分:4.5 V 以下的部分,曲线斜率相对较大,呈S 形,主要对应的是层状结构中Li+的脱出,并伴随着Ni2+和Co3+的氧化,在此电压下,Li2MnO3为电化学惰性,不参与充电反应;在4.5 V 及以上的部分,呈一个平缓的长平台,主要对应富锂相Li2MnO3的活化过程,Li+从Li2MnO3中脱出,并伴随着晶格中O2-的氧化,近似于净脱出Li2O。 富锂锰基三元正极材料的首次库仑效率低,原因是在4.5 V 及以上时,Li2MnO3得到活化,脱出Li2O 生成MnO2,在随后的放电过程中,Li+回嵌到MnO2中,生成LiMnO2,无法恢复到原来的Li2MnO3相。 920 ℃烧结温度下制备的富锂锰基三元正极材料首次放电比容量达到了234.5 mAh/g,首次库仑效率为73.6%。
从图6(b)可知,随着充放电电流的逐步增大,材料的充放电比容量降低,原因是大电流条件下电池的极化增强,导致实际充放电电压区间缩小,富锂锰基三元正极材料的氧化还原反应不完全。
富锂锰基三元正极材料的循环性能测试结果见图7。
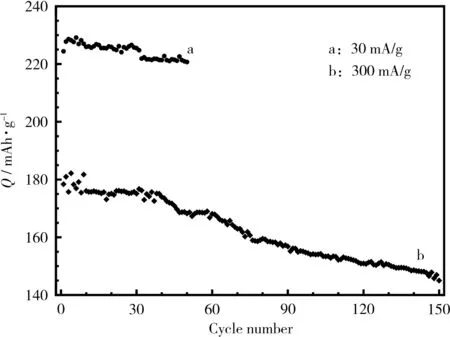
图7 富锂锰基正极材料在电流为30 mA/g 和300 mA/g 时的循环性能Fig.7 Cycle performance of Li-rich Mn based cathode material at the current of 30 mA/g and 300 mA/g
从图7 可知,以30 mA/g 循环,材料在前3 次的活化过程中放电比容量呈现逐渐上升的趋势,达到最高值后开始缓慢下降,第50 次循环时,富锂锰基三元正极材料的容量保持率为96.5%。 富锂锰基三元正极材料以300 mA/g 循环150次,容量保持率为81.4%。
EIS 分析可了解富锂材料的界面阻抗状态。 电池经过3次和150 次循环,富锂锰基正极材料的EIS 见图8。
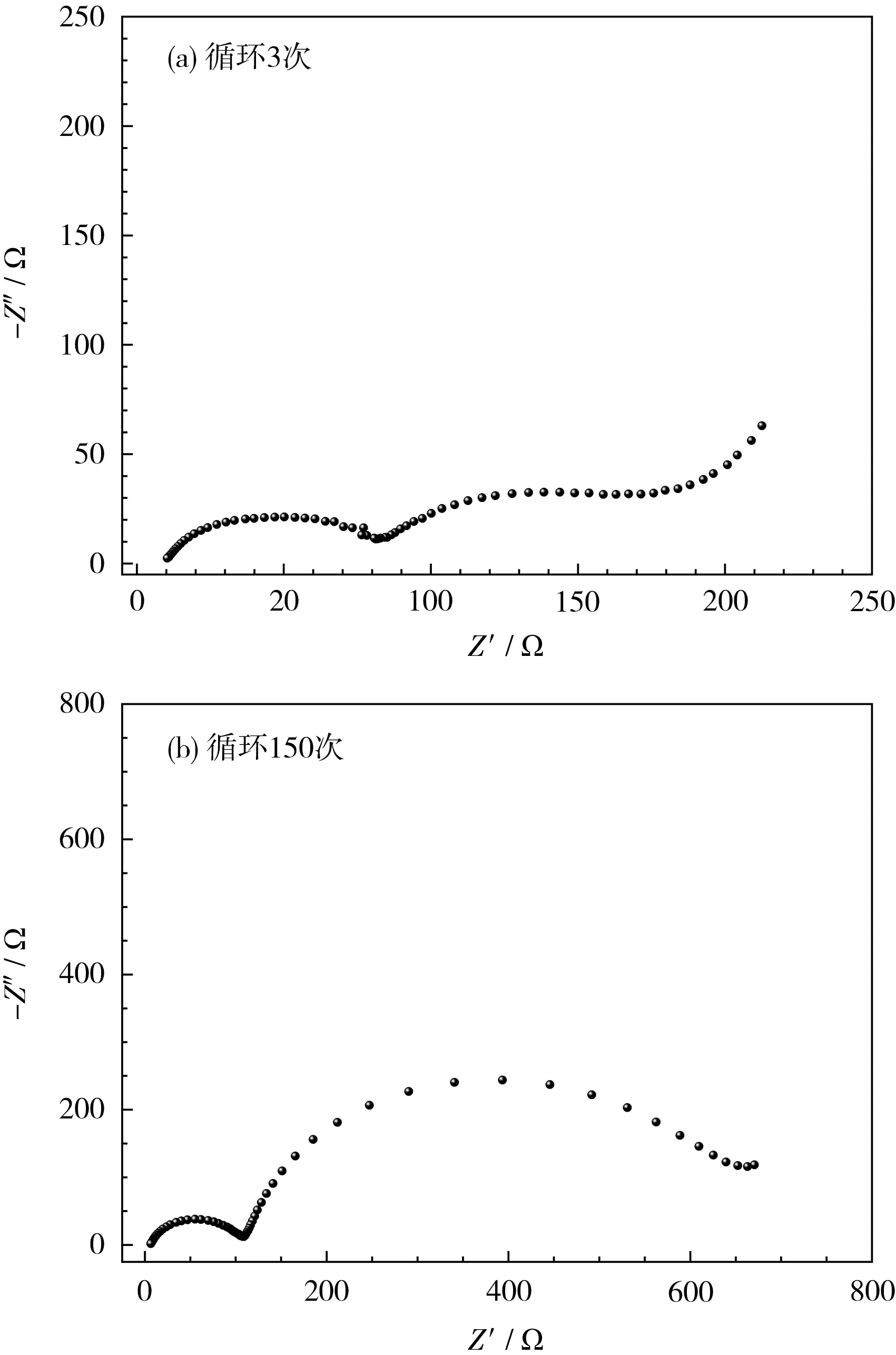
图8 循环3 次和150 次后富锂锰基正极材料的EISFig.8 Electrochemical impedance spectroscopy(EIS) of Li-rich Mn based cathode material after 3 and 150 cycles
图8 中的曲线包含两个半圆弧和一条倾斜的直线,其中低频区的直线代表Li+在固体电极材料中的Warburg 扩散阻抗(W);中频区的半圆弧代表电荷传递阻抗(Rct);高频区的半圆弧代表电极/电解液界面膜阻抗(Rsf)[6]。 在300 mA/g电流下经过150 次循环,富锂正极材料的Rsf和Rct发生了不同程度的增大,尤其是Rct大幅增加,与材料经过150 次循环的容量衰减较大一致。 循环过程中,材料的电极和电解液界面发生副反应,使得界面膜增厚、Rsf增加。 同时,富锂锰基三元正极材料随着循环的深入,逐步发生不可逆相变过程,不仅会导致活性相的损失,还会极大地影响传荷过程,导致Rct增加、容量衰减。
3 结论
本文作者在前期研究的基础上,采用共沉淀-高温固相法合成了Li1.2Mn0.54Ni0.13Co0.13O2富锂锰基三元正极材料。
对前驱体和混锂烧结后的富锂锰基三元正极材料进行XRD 分析,发现前驱体的XRD 图与MnCO3的衍射峰相对应;烧结后的富锂锰基三元正极材料,主要与六方层状结构和单斜结构的衍射峰相对应,同时,衍射图中存在微弱的与尖晶石结构LiMn2O4相对应的衍射峰,说明制备出了具有六方层状-单斜层状-立方尖晶石复合结构的富锂锰基三元正极材料。
EDS 分析结果表明,合成的富锂锰基三元正极材料中,Mn、Co 和Ni 的摩尔分数分别为70.05%、16.06%和13.89%,符合n(Mn)∶n(Ni)∶n(Co)= 4 ∶1 ∶1。
电化学性能测试结果表明,先将碳酸盐前驱体在600 ℃下预烧(空气条件下),再在920 ℃下烧结(氧气条件下),所得材料在2.0~4.6 V 下的首次放电比容量为234.5 mAh/g,首次循环的库仑效率为73.6%;以30 mA/g 的电流循环50次,容量保持率为96.5%。

