嗜酸性肉芽肿性多血管炎5例临床特征分析
韩李周,郑红,靳双周
(焦作市人民医院 呼吸与危重症医学科,河南 焦作 454002)
嗜酸性肉芽肿性多血管炎(eosinophilic granulomatosis with polyangiitis,EGPA)是抗中性粒细胞胞质抗体(anti-neutrophil cytoplasmic antibodies,ANCA)相关性血管炎的一种,也称为Churg-Strauss综合征(ChurgStrauss syndrome,CSS)或变应性肉芽肿性血管炎(allergic granulomatosis and angiitis,AGA)。由于该病发病率很低,且常以喘息、咳嗽等哮喘样症状为首发表现,按支气管哮喘正规诊治,症状控制不良,易被误诊为重症哮喘或“难治性哮喘”。近年来,随着诊断意识的提高与检验、病理技术的发展,EGPA逐渐被呼吸科医生所熟悉。诱导痰细胞分类检测常用于慢性咳嗽的诊治或支气管哮喘的分型管理,临床上若发现痰中嗜酸性粒细胞百分比异常升高,常能为诊断提供线索。本文结合诱导痰细胞分类检测,探讨EGPA的临床、影像和病理特点,以提高诊治水平。
1 资料和方法
1.1 资料来源选取2015年10月至2020年9月焦作市人民医院呼吸与危重症医学科确诊的5例EGPA患者。
1.2 诊断标准EGPA诊断符合1990 年美国风湿病学会分类标准[1]。即:(1)哮喘样症状;(2)外周血嗜酸性粒细胞增多>10%;(3)单发性或多发性单神经病变或多神经病变;(4)游走性或一过性肺浸润影;(5)鼻窦炎;(6)病理提示血管外嗜酸性粒细胞浸润。符合4条及4条以上可确诊。仅有肺部和呼吸系统受累(包括耳鼻喉)者为局限型EGPA,有至少2个及以上器官受累者则为全身型EGPA[2]。
1.3 诱导痰留取、痰液处理及检测方法
1.3.1痰液留取 参考《咳嗽的诊断与治疗指南(2015)》[3],超声雾化吸入30~50 g·L-1高渗盐水诱导患者咳痰。30~50 g·L-1高渗盐水配制方法:取100 g·L-1氯化钠(扬州中宝药业股份有限公司,国药准字H32021123)3 mL,加灭菌注射用水(石家庄四药有限公司,国药准字H20153113)7 ml混合即得30 g·L-1高渗盐水。40、50 g·L-1高渗盐水配制方法以此类推。(1)诱导前10 min吸入沙丁胺醇(葛兰素史克制药苏州有限公司,国药准字J20160074)400 μg。(2)清水漱口、擤鼻。(3)30 g·L-1高渗盐水雾化吸入15 min,用力咳痰至培养皿。(4)若患者无痰或痰量不足换用40 g·L-1高渗盐水继续雾化8 min。(5)若患者仍无痰或痰量不足则换用50 g·L-1高渗盐水继续雾化7 min。(6)雾化期间若患者咳出足量合格痰标本或雾化总时间达30 min时终止雾化。
1.3.2痰液处理及检测 痰液咳出后需立即处理,4 ℃存放不超过3 h。取黏稠、密度大的痰栓或痰块放入EP管中,加入4倍体积1 g·L-1二硫苏糖醇(美国Sigma公司,货号V900830-5G)充分混合,裂解10~15 min,37 ℃水浴和水平温和震荡可提高裂解效果,48 μm滤纸过滤掉黏液和碎片,常温2 500 r·min-1离心10 min,弃上清液。沉渣经细胞涂片瑞氏姬姆萨染色,计数分类400个炎症细胞。
1.4 观察指标通过医院病历系统收集患者临床症状及血常规、ANCA、血清总IgE、诱导痰细胞分类、G试验、动脉血气分析、肺功能、胸部CT等结果。
2 结果
2.1 一般情况5例患者中男3例,女2例,年龄40~77岁,局限型2例,全身型3例。出现肺部症状至确诊4个月~50 a,住院2~4次确诊。初诊为支气管哮喘3例,先诊断为支气管哮喘、后诊断为变应性支气管肺曲霉病(allergic bronchopulmonary aspergillosis,ABPA )1例,肺炎1例。
2.2 临床表现5例均有喘息、胸闷、咳嗽、咳痰等呼吸道症状,2例发热。5例耳鼻喉及其他情况:多发性副鼻窦炎4例,左侧上颌窦局灶性炎1例,变应性鼻炎3例,左侧真菌性上颌窦炎、上颌窦息肉、双侧分泌性中耳炎1例;1例消化系统受累表现为食管炎、胃炎、十二指肠炎、胃食管反流病;1例冠心病、腹茧症;肌电图证实周围神经受累2例(表1中病例3、4)。
2.3 实验室检查见表1。

表1 5例EGPA患者实验室检查结果
2.4 肺功能、心脏彩超及其他检查病例1、2曾接受肺功能检查,激发试验均阳性。3例心脏彩超提示左、右室舒张功能减低。5例尿常规均正常。4例红细胞沉降率(erythrocyte sedimentation rate,ESR)、C反应蛋白(C-reactive protein,CRP)不同程度升高。
2.5 胸部及鼻窦CT胸部CT 1例表现为两肺多发细支气管炎及轻度支气管扩张;1例表现为两肺多发斑片淡薄渗出影、磨玻璃影;1例表现为两肺多发片状实变渗出影、结节影、磨玻璃影;1例表现为游走性浸润影、间质性病变及条索影;1例表现为小片状渗出影、支气管周围炎、支气管壁增厚。鼻窦CT 4例表现为多发副窦炎,其中1例合并真菌性上颌窦炎;1例左侧上颌窦局灶性炎。见图1~5。
2.6 病理结果病例1、2气管镜肺活检及黏膜活检病理提示肺组织间质小血管周围淋巴细胞及嗜酸性粒细胞浸润,支气管黏膜下小血管周围亦可见嗜酸性粒细胞浸润,未见嗜酸性坏死性肉芽肿。病例2亦接受胃镜检查。病例3气管镜刷片、灌洗液真菌1-3-β-D葡聚糖检测(GM试验)及真菌培养均排除真菌感染或过敏。病例4、5未取得病理证据。

注:A为轻度支气管扩张、细支气管炎;B为手术证实左侧真菌性上颌窦炎。图1 病例1 CT图

注:A、B为两肺多发斑片淡薄渗出影、磨玻璃影。图2 病例2 CT图

注:A、B为双肺多发片状、结节状渗出影。图3 病例3 CT图
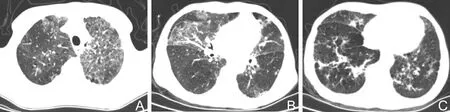
注:对比外院CT,A、B、C右上肺团块状实变影消失,双肺可见磨玻璃影、渗出影、纤维条索影。图4 病例4 CT图

注:A、B为左上肺小片状渗出影,双下肺支气管周围炎症、支气管壁增厚。图5 病例5 CT图
2.7 治疗与随访糖皮质激素联合环磷酰胺等免疫抑制剂治疗3例,单纯激素治疗2例。出院后10~15 d门诊随访1次,门诊或电话随访50 d~2 a,胸部病变基本吸收。
3 讨论
EGPA与显微镜下多血管炎(microscopic polyangitis,MPA)、肉芽肿性多血管炎(granulomatosis with polyangiitis,GPA)同属于ANCA相关性血管炎(ANCA associated vasculitis,AAV)。与MPA和GPA不同,EGPA常表现为哮喘、外周血嗜酸性粒细胞升高且常伴变应性鼻炎、慢性鼻窦炎,易误诊为重症哮喘或“难治性哮喘”[4]。本研究患者均有“哮喘样”症状,或伴发热,初诊均误诊。除呼吸系统受累,非对称性以轴索损害为主的周围神经病变也是EGPA的常见表现[5]。本研究2例肌电图证实周围神经受累,少数可出现脑梗死或缺血、脑出血、蛛网膜下腔出血、颈髓受累等中枢神经系统受累表现[6]。肾脏受累常表现为镜下血尿和蛋白尿,少数出现急进性肾小球肾炎[7]。本研究5例均未见尿常规异常。还可出现皮肤、消化系统、心脏等多系统损害。如肢体、颜面或躯干部出现丘疹、风团或紫癜,不能解释的腹痛、腹泻或大便隐血阳性,不能解释的心包积液[8],甚至出现急性冠状动脉综合征样表现[9]。有些患者可出现趾(指)端坏疽。
EGPA常为核周型抗中性粒细胞胞质抗体(perinuclear pattern anti-neutrophil cytoplasmic antibodies,pANCA)阳性或抗髓过氧化物酶抗体(MPO-ANCA)阳性,但国内几家教学医院较大样本的研究显示,EGPA中ANCA的阳性率只有10.0%~41.9%[10-14]。本研究5例患者中ANCA阳性3例,病例1、2 ANCA阴性,取得气管镜活检病理支持。ANCA阳性者更易出现肾脏受累,ANCA阴性者更易出现心脏受累[13]。EGPA自然病程可分为前驱期、组织嗜酸性粒细胞浸润期和血管炎期,ANCA阳性与阴性是否代表疾病的不同分期,或者代表不同的发病模式或疾病亚型,如阳性表示ANCA介导为主的器官损害,阴性表示嗜酸性粒细胞介导为主的器官损害,尚需进一步研究。病例4出现不典型ANCA(atypical ANCA,aANCA)阳性,aANCA与炎症性肠病、自身免疫性肝病有关[15],EGPA中鲜有报道,需进一步追踪观察。
诱导痰细胞及炎症介质检测是近年兴起的评价气道炎症的非侵袭性方法,可重复性强,安全性高,操作简便[16]。哮喘患者诱导痰中嗜酸性粒细胞百分比>3%,被称为嗜酸性粒细胞性哮喘[17]。文献报道重症哮喘患者诱导痰嗜酸性粒细胞百分比中位值为21.7%[18]。慢性咳嗽患者诱导痰嗜酸性粒细胞百分比≥2.5%是诊断嗜酸性粒细胞性支气管炎(eosinophilic bronchitis,EB)的要点之一[3]。目前尚无公认的EGPA诱导痰嗜酸性粒细胞百分比界值。通过有限的病例观察,本研究发现EGPA患者诱导痰嗜酸性粒细胞百分比常升高,但范围波动较大,当百分比>30%要谨慎诊断嗜酸性粒细胞性哮喘、EB,需鉴别EGPA、ABPA、嗜酸性粒细胞性肺炎等疾病。总之,诱导痰嗜酸性粒细胞升高是诊断EGPA的重要线索之一。
胸部影像异常是与哮喘鉴别的另一要点。无合并症的哮喘除部分可见轻度支气管壁增厚、局灶性或弥漫性透过度增加外,胸部影像常相对正常。EGPA胸部CT表现多样,可发现磨玻璃样阴影至气腔实变影,双肺外周为主的多发斑片状非节段性实变阴影、结节样阴影、网状阴影、细支气管炎等,不同特征的影像病变常多发并存[8,19]。胸部影像的另一特点是浸润影呈游走性,需与ABPA鉴别,ABPA易出现中心型支气管扩张,而EGPA少见。本研究胸部CT表现与文献报道相似,但这些影像特点并不具有特异性,可疑病例仍需结合其他临床特征细心甄别。
EGPA肺脏病理可见血管周的过敏性肉芽肿、血管炎、嗜酸性粒细胞肺炎和不同程度的哮喘性支气管炎[20]。对于肺部病理无嗜酸性坏死性肉芽肿表现,而有肺泡腔、间质及血管腔大量嗜酸性粒细胞浸润者,不能排除诊断[4],需进一步鉴别其他嗜酸性粒细胞相关肺病,也可依据临床情况选择肺外活检,如鼻黏膜活检、皮肤活检等。
EGPA治疗主要根据存在影响预后因素的多少而决定。目前评估预后的标准主要参考5因子评分评价体系:(1)胃肠道受累;(2)心脏受累;(3)肾功能不全(血肌酐>150 μmol·L-1);(4)年龄>65岁;(5)缺乏耳鼻喉部位受累的证据。每项计1分,总分5分,分数越高,预后越差。0分:可使用糖皮质激素控制症状;≥1分:建议激素和免疫抑制剂联合治疗。治疗分诱导缓解和维持治疗2个阶段。诱导缓解治疗用药主要包括激素和(或)环磷酰胺等免疫抑制剂,维持治疗推荐使用硫唑嘌呤或甲氨蝶呤。两阶段疗程尚未统一,需根据临床情况决定,维持治疗推荐时间为疾病达到缓解后至少24个月[2,21]。另外,生物靶向药物如抗IL-5单克隆抗体、抗IgE人源化单克隆抗体、抗CD-20单克隆抗体、TNF-α拮抗剂等也可根据不同的临床情况选用[22]。
总之,应重视“难治性哮喘”患者血常规及诱导痰嗜酸性粒细胞异常升高、胸部CT浸润影等常规检验检查提示的信息,结合ANCA、肌电图、组织病理等有助于提高EGPA的诊断率。

