钠与溶液反应实质的探究
尹尧

【摘 要】钠与溶液反应实质课本上解释是先与水电离的氢离子反应,我们通过实验,证明钠是与溶剂水本身反应。钠和溶液的反应是人教版化学必修1第三章第一节中的重要实验,这个实验不仅在本章非常重要,在整個高中阶段也非常重要,是每年高考试题的热点。同时,钠与溶液反应的实质对学生而言也是一个比较困扰的问题。因此,我们设计了以下实验对其进行探究。
【关键词】钠与溶液;实验;反应
一、问题的提出
在一些权威的教辅资料(如教材完全解读)上明确说明:当钠与酸、水溶液反应时,是在和溶液中的氢离子反应。故氢离子的浓度越高,其反应越剧烈。从所学的知识可知,氧化性:铜离子>氢离子。如果钠与溶液反应的实质是在和溶液中的氢离子反应,那么钠和硫酸铜溶液反应应优先置换出铜单质。而书本上说明:钠与硫酸铜溶液反应不能够置换出单质铜,而是会优先和水反应生成氢氧化钠,生成的氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀。这两种说法与所学知识存在矛盾。故此次实验,我们要探究钠与溶液反应的实质:是在和水本身反应还是在和水中的氢离子反应。
二、实验仪器与药品
实验仪器:烧杯、玻璃棒、滤纸、表面皿、试管架、量筒、胶头滴管、镊子、小刀
药品:盐酸、氢氧化钠、蒸馏水、钠单质
三、实验步骤
(一)钠与酸碱溶液反应实质探究
1.钠与不同浓度的盐酸溶液反应:在四只烧杯中分别加入50ml的蒸馏水、0.01mol/L HCl、0.1mol/L HCl、1mol/L HCl,然后再将四块大小相同的钠一起投入水中,观察其实验现象;
2.钠与不同浓度的氢氧化钠溶液的反应:在四只烧杯中分别加入50ml的蒸馏水、0.01mol/L NaOH、0.1mol/L NaOH、1mol/L NaOH,然后再将四块大小相同的钠一起投入水中;
3.钠与不同浓度的盐酸、氢氧化钠溶液反应在五只烧杯中分别加入0.1mol/L HCl、1mol/L HCl 、50ml的蒸馏水、0.1mol/L NaOH、1mol/L NaOH,然后再将四块大小相同的钠一起投入水中。
(二)钠与硫酸铜溶液反应实质探究
钠与不同浓度硫酸铜反应:在四只烧杯中分别加入50ml 0.01mol/L CuSO4、0.1mol/L CuSO4、1mol/L CuSO4,然后再将四块大小相同的钠一起投入水中。
四、实验数据
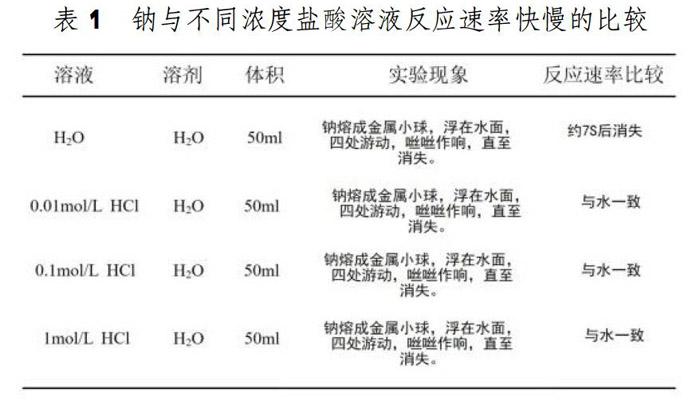
(一)钠与不同浓度盐酸溶液反应速率快慢的比较
从教材完全解读可以知道,钠与水反应的实质是与氢离子的反应,氢离子的浓度越大,反应速率越快,反应越剧烈,所以随盐酸浓度的增加,其反应速率越快。但实验结果却出乎意料,从表1中可以看出,钠与不同浓度的盐酸反应的反应速率并无明显的差别,几乎一致。我们大胆的猜测钠与溶液反应并不是钠与溶液的氢离子反应,而是钠直接与溶剂水反应。为了论证我们的猜想,我们将钠分别置于不同浓度的氢氧化钠溶液反应。
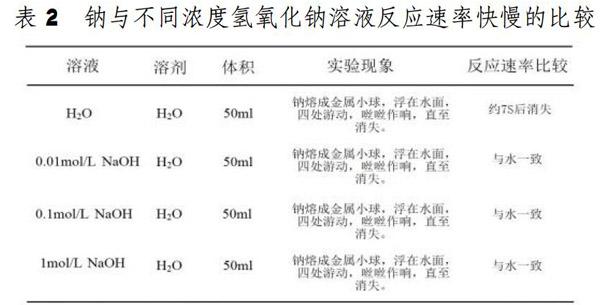
(二)钠与不同浓度氢氧化钠溶液反应速率快慢的比较
由水离子积常数可知:氢氧化钠溶液的溶度越大,水电离出来的氢离子浓度越小,钠与其反应的速率应越慢。但从表2可以看出,钠与不同浓度的氢氧化钠反应速率基本一致。由此进一步论证了钠不是与溶液中的氢离子反应,而是在与溶剂水本身反应。我们决定再将酸、水、碱放在一起进行比较,来更明显准确的证明我的猜想。
(三)钠与不同浓度盐酸、氢氧化钠溶液反应速率快慢的比较
由水离子积常数可知:酸、碱溶液中氢离子浓度差高达10^8,然而从表3中可以看出,其反应速率仍没有明显差别。通过上面的一系列实验,可证明:钠不是在与溶液中的氢离子反应,而是在与溶剂本身反应。
(四)钠与硫酸铜反应的探究
从表4中可以看出,其实验结果与教材上描述一致,钠并没有置换出单质铜,而是与溶剂水反应后生成的氢氧化钠使得铜离子沉淀,生成氢氧化铜,钠与水反应放出的热使得硫酸铜分解生成黑色的氧化铜粉末。
钠与1mol/L的硫酸铜反应比我们预料中的剧烈。我们猜测是因为铜离子浓度较高时,钠与水反应生成的氢氧化钠使得铜离子迅速沉淀,溶液中迅速出现了大量氢氧化铜固体沉淀,由于固体导热较慢,钠与水反应放出的热放不出去,液体表面温度迅速升高,达到了氢气的燃点,故在硫酸铜溶液浓度为1mol/L时出现钠燃烧、爆炸的现象。
五、结束语
钠与溶液反应的实质是在和溶剂水本身反应,而不是在和水电离出来的氢离子反应。无论溶质是酸、是碱还是硫酸铜,都不会影响钠与水反应的速率。
由此能够说明:教辅资料中的观点:钠与酸反应剧烈程度大于水、钠与酸反应的实质是与酸中的氢离子反应有误。
六、反思与评价
(一)天气对实验的影响
我们发现在雨天或是雨后,空气过于潮湿,钠与空气中的水分有较为明显的反应,即钠表面有气泡冒出,如图1所示。因此在空气湿度比较大时,不宜进行实验。
(二)将钠转移到反应容器内遭遇的困境
如果用镊子一个一个的夹取钠,那么每个钠进入烧杯内的反应时间不一致,就无法比较反应的快慢。所以我们采用玻璃棒赶钠的方法,能够一次将所有钠同时赶到反应容器内。但在后面的实验发现当天气有点潮湿时,用玻璃棒赶钠的方法不适用,因此我们想了用针头固定钠,再将其放入溶液中的办法。
(三)个人问题
由于我是第一次接触实验室里的正规化学实验,不同于家中的“随手玩玩” 实验室中操作要求规范严谨,所以在操作过程中犯了很多错误,比如切钠时多次不能剥离钠的氧化层、配制溶液时胶头滴管使用方式不正确等等。
评价:
科学探索就是如此,在不断的探索和尝试中追寻真理。科学容许犯错,正是在不断的犯错过程中不断地接近事物的本质。在严谨规范的实验操作中,我在不断地犯错,也在不断地规范、不断地进步。相比于考试时遭遇的理论上的实验操作知识,就是死记硬背,考试时也能得分。然而实际操作不能是死记硬背,而要灵活多变,实践时会遭遇种种困难,都需要扎实的基础、发散的思维才能摸索出解决困难的方法。所以,或许在实验规范要求、实验效果上,我不能算是成功的,但是在学习实验技能、培养科学素养上,我绝对是获益匪浅。正是这种持之以恒、敢于专研的能力,使得我在学习中不断进步。(实验指导老师:汪莉芬)
【参考文献】
[1]陶都,毛芳芳,刘梦琴,刘文静,任晶.实验教学中化学核心素养培养的探讨——以“钠与水反应”为例[J].山东化工,2020,49(09):200-201.
[2]王秀芬.高中化学实验中的几点思考[J].课程教育研究,2020(01):178.
[3]丁培桓.生活化视角下的高中化学实验学习分析[J].学周刊,2019(06):68-69.

