依鲁替尼治疗复发性难治性弥漫大B细胞淋巴瘤的疗效和安全性评估
任亮亮,王馨悦,孔 飞,赵 洋,张明智,李 玲
(1.郑州大学第一附属医院肿瘤科,河南 郑州 450052; 2.郑州大学医学院,河南 郑州 450052)
淋巴瘤是较为常见的血液系统肿瘤,具有较大的异质性[1-2]。弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL)是最常见的非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)亚型[3],在国内约占NHL的50.7%[4]。根据其细胞起源为:活化的B细胞样、生发中心B细胞样(germinal center B-cell-like lymphoma,GCB)及原发纵隔B细胞样淋巴瘤[5]。
对于大多数新诊断的DLBCL患者来说,利妥昔单抗联合环磷酰胺+多柔比星+长春新碱+泼尼松方案治疗后可达到完全缓解(complete remission,CR)[6],但不同病例生存率仍存在很大差异[7]。虽然近几年嵌合抗原受体T细胞免疫疗法(chimeric antigen receptor T-cell immunotherapy,CAR-T)为这些患者带来了希望,但仍有部分患者无法从中获益[8]。对于复发性难治性DLBCL患者来说,其治疗方案有限[9],故寻找潜在治疗方案来改善其预后就显得尤为重要[10]。
布鲁顿酪氨酸激酶(Bruton’s tyrosine kinase,BTK)作为B细胞受体途径的关键激酶,对于B细胞成熟和激活至关重要[11-12]。而依鲁替尼是一种有效的,可口服的BTK的不可逆有效抑制剂,并于2013年、2014年在套细胞淋巴瘤和慢性淋巴细胞白血病中获批适应证[13]。Young等[14]在文献中提到依鲁替尼对活化的B细胞样DLBCL肿瘤具有选择性毒性。Jiang等[15]同样认为口服依鲁替尼已成为非GCB亚型的进一步治疗手段。
目前关于依鲁替尼在复发性难治性DLBCL的临床研究相对较少,因此本研究通过回顾性研究,探讨依鲁替尼在治疗复发性难治性DLBCL中的疗效评价和安全性评估。
1 资料与方法
1.1 研究对象2018年6月至2020年6月郑州大学第一附属医院收治的34例应用依鲁替尼的复发性难治性DLBCL患者。男20例,女14例;年龄30~89岁,其中>60岁17例,≤60岁17例;ECOG评分<2分16例,≥2分18例;EB病毒RNA阴性29例,阳性5例;Ki-67指数<50% 2例,≥50% 32例;乳酸脱氢酶正常14例,升高20例;血β2微球蛋白正常22例,升高12例;B症状:有19例,无15例;依鲁替尼±利妥昔单抗治疗25例,依鲁替尼+来那度胺±利妥昔单抗治疗9例。纳入标准:原发灶均由高年资病理科医师确诊其病理组织学类型为DLBCL;经标准二线或二线以上方案治疗后失败或复发;至少具备一个可测量的病灶;既往未接受过BTK抑制剂治疗。排除标准:孕期及哺乳期女性。所有患者均口服依鲁替尼1个月以上。本研究经郑州大学第一附属医院伦理委员会审查批准,研究对象或其家属均知情同意并签署知情同意书。
1.2 治疗方法所有患者均给予依鲁替尼口服,140 mg×4片,共560 mg,每天1次,均持续口服直至疾病进展(progressive disease,PD)或死亡。若患者不可耐受,可将依鲁替尼减量至420 mg/次,每天1次,或暂停用药,暂停用药时间<1周。每周建议复查血、尿常规,肝、肾功能。
34例复发性难治性DLBCL患者。其中25例接受了依鲁替尼±利妥昔单抗方案治疗。此次治疗是否应用利妥昔单抗则取决于该患者在前期治疗中是否用足8个周期,应用不足者补足给予8个周期。利妥昔单抗按照体表面积375 mg/m2计算后,用生理盐水或体积分数5%葡萄糖溶液稀释,稀释后浓度为1 mg/mL,于每个治疗周期第1天静脉滴注至患者体内,密切关注患者输液反应及过敏反应并积极对症处理。21 d为1个周期,每2个周期进行1次疗效评价。
余9例接受依鲁替尼+来那度胺±利妥昔单抗治疗,9例患者持续口服来那度胺,10 mg/次,每天1次,口服3周停服1周。依鲁替尼和利妥昔单抗应用原则同上。
1.3 随访及观察指标采用电话随访,随访截止日期为2020年6月。每2个治疗周期进行疗效评估,根据WHO近期疗效评价标准将近期疗效分为CR、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)、PD。以CR+PR计算客观缓解率(objective response rate,ORR),以CR+PR+SD计算疾病控制率(disease control rate,DCR)。远期疗效评估指标为疾病无进展生存时间(progression-free survival,PFS)和总生存时间(overall survival,OS)。PFS是指首次服用依鲁替尼至PD或死亡的时间。OS则为首次服用依鲁替尼至任何原因死亡或末次随访的时间。
1.4 统计学处理采用SPSS 24.0进行统计学数据处理,采用Kaplan-Meier法绘制生存曲线,采用Cox回归模型分析影响复发性难治性DLBCL患者PFS及OS的因素,检验水准α=0.05。
2 结果
2.1 近期疗效34例复发性难治性DLBCL患者中,5例患者达到CR(14.7%),2例患者达到PR(5.9%),9例患者达到SD(26.4%),ORR为20.6%,DCR为47.1%。
2.2 远期疗效34例复发性难治性DLBCL患者中位PFS为13.000个月(95%CI:7.282~18.718),中位OS为14.000个月(95%CI:7.990~20.010)。34例患者的PFS和OS生存曲线见图1。
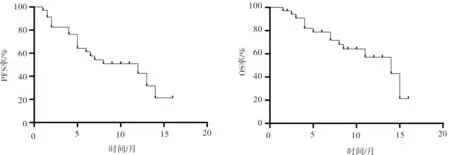
图1 34例复发性难治性DLBCL患者的PFS(左)、OS(右)生存曲线
2.3 不良反应34例复发性难治性DLBCL患者在治疗过程中出现的不良反应主要为Ⅰ、Ⅱ度,Ⅲ、Ⅳ度较为少见。依鲁替尼±利妥昔单抗患者皮疹、食欲下降较为常见,依鲁替尼+来那度胺±利妥昔单抗患者恶心、乏力较为常见。其中依鲁替尼±利妥昔单抗组内有1例患者出现较重的泌尿系出血情况,给予停服依鲁替尼同时给予止血药物应用,3 d后患者血尿消失,给予观察2 d后继续口服依鲁替尼并动态观察。见表1。
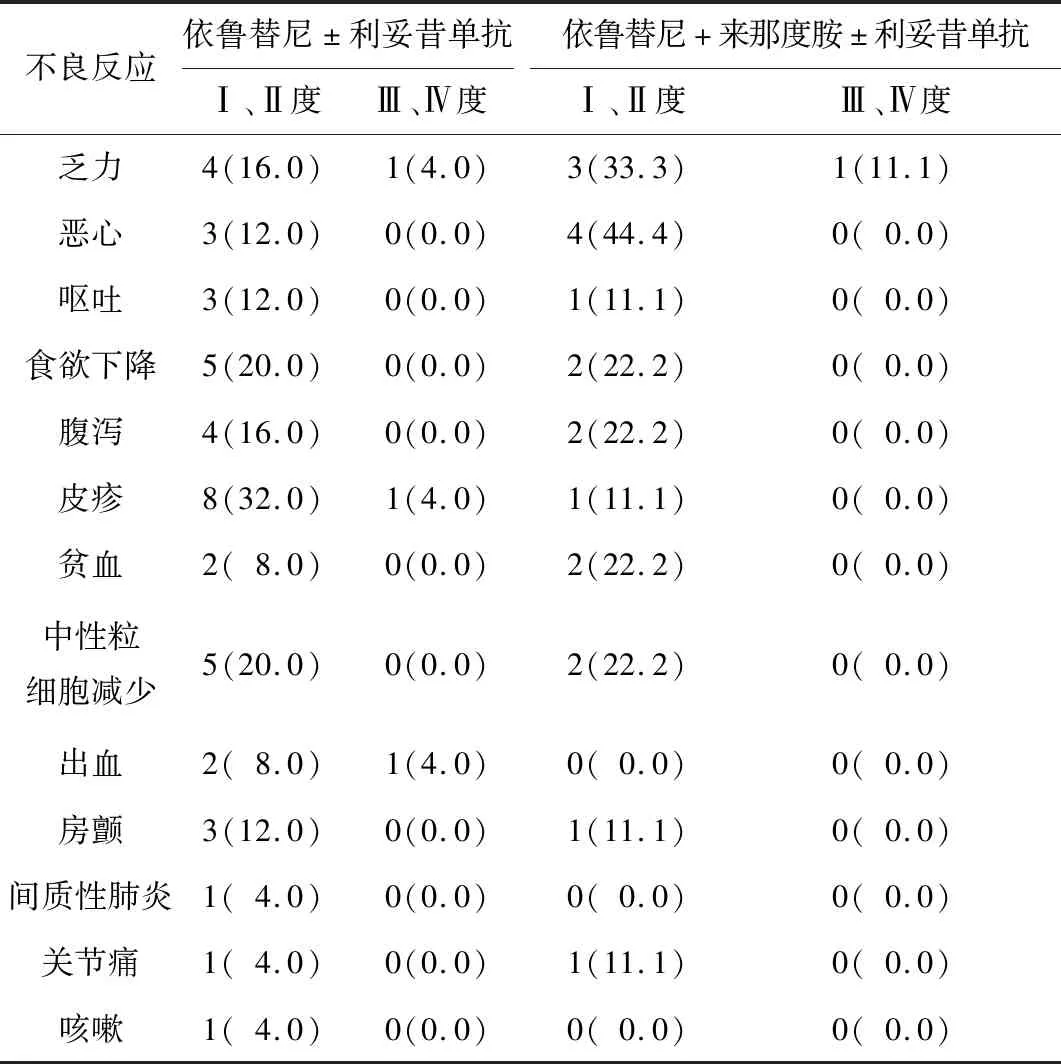
表1 34例复发性难治性DLBCL患者用药期间的不良反应 n(%)
2.4 预后因素分析Cox回归模型单因素分析发现,影响患者PFS的独立不良预后因素为ECOG评分≥2分,影响OS的因素暂未观测到。见表2。
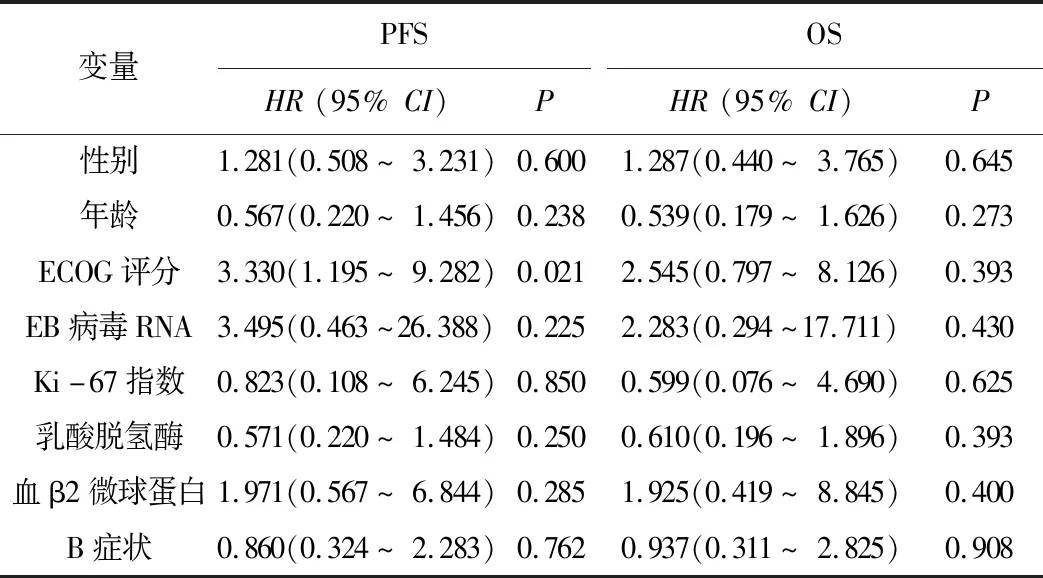
表2 34例复发性难治性DLBCL患者的生存预后因素分析
3 讨论
由于DLBCL高度的异质性及复杂的基因分型[16],使其很难达到良好的临床疗效[17]。标准的一线利妥昔单抗联合环磷酰胺+多柔比星+长春新碱+泼尼松方案治疗后5 a生存率为50%~75%[18],仍有部分患者无法从中获益。有研究[19]证实,复发性难治性DLBCL患者中位生存时间仅为4~6个月。故改善复发性难治性DLBCL预后成了现在许多研究的热点。近些年来,研究[20]发现共价BTK抑制剂依鲁替尼对多种B细胞恶性肿瘤高度有效。
Hou等[21]团队于2020年对依鲁替尼治疗DLBCL相关情况进行了Meta分析,结果发现,依鲁替尼治疗复发性难治性DLBCL患者的ORR和CR率分别为49.7%和27.7%。在临床上,确实观察到依鲁替尼内在的和获得性的耐药问题。Dobrovolsky等[22]发现,大约有1/3的套细胞淋巴瘤患者对依鲁替尼无反应。对于有反应的患者,获得性抗性会迅速出现,阻止依鲁替尼与BTK形成共价键,并显著降低其效价,导致中位疾病无进展生存时间较短[23]。因此,联合疗法是否会影响甚至改变依鲁替尼的耐药性或直接增加其疗效,这些是我们今后的研究重点。
Goy等[24]在2019年发起的一项有关“依鲁替尼+来那度胺+利妥昔单抗在复发性难治性DLBCL中应用”相关临床试验,其结果为:非GCB DLBCL患者的ORR为65.0%(CR率41.0%),复发性(16例)和继发难治性(27例)患者的ORR分别为69.0%和56.0%。这一结果表明:依鲁替尼对非GCB DLBCL患者更加敏感。值得惊喜的是,在本回顾性研究中,依鲁替尼+来那度胺+利妥昔单抗方案有6例患者,4例患者为非GCB DLBCL,但本研究病例数目较少,应继续收集相关报道,并适当扩大病例数,以寻求更多的证据来证明依鲁替尼+来那度胺+利妥昔单抗方案在治疗复发性难治性DLBCL患者中的疗效。
本研究34例患者中,CR为14.7%,PR为5.9%,SD为26.4%,7例患者达到ORR(20.6%),16例患者达到DCR(47.1%)。与实体瘤比较,淋巴瘤更在意的是有无CR,这对于患者预后评估尤为重要。但对于复发性难治性DLBCL患者来说:有30%左右DLBCL患者会出现复发,而且一线治疗后复发的患者预后极差[25],复发性难治性DLBCL患者亟需新的治疗方案;可供复发性难治性DLBCL选择的方案本就有限,正如前文所述,CAR-T疗法、自体造血干细胞移植这些也难以使得部分患者获益;本研究中,接受依鲁替尼治疗后,虽然CR和PR率较低,但就目前复发性难治性DLBCL治疗效果来看,长期得到控制也不失为另一种治疗方向,且近期疗效尚可。
本研究34例复发性难治性DLBCL患者在治疗过程中出现的不良反应主要为Ⅰ、Ⅱ度,Ⅲ、Ⅳ度较为少见。依鲁替尼±利妥昔单抗患者皮疹、食欲下降较为常见,依鲁替尼+来那度胺±利妥昔单抗患者恶心、乏力较为常见。
综上所述,不管依鲁替尼单药方案还是依鲁替尼联合其他药物方案都为治疗复发性难治性DLBCL提供了新思路,但仍存在一定局限性。结合前人的相关临床试验经验,仍需要大样本数据进行前瞻性、随机对照研究验证结果,针对性进行含依鲁替尼方案的研究,选出疗效更佳的方案,依鲁替尼合并其他药物能否在复发性难治性DLBCL治疗中发挥更大潜力,值得未来更有深度的研究。

