R-ESHAP方案和ESHAP方案治疗复发难治性弥漫大B细胞淋巴瘤的疗效比较
张贺真,范冰杰,张 蕾
(郑州大学第一附属医院肿瘤科,河南 郑州 450052)
弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL)是最常见的非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL),发病率约为非霍奇金淋巴瘤的30%~40%[1]。初治的患者通过利妥昔单抗、环磷酰胺、阿霉素、长春新碱、强的松(R-CHOP)方案治疗后可获得约80%的缓解率,但依然有30%的复发率,患者经过二线治疗后再次复发预后极差[2]。依托泊苷、地塞米松、阿糖胞苷、顺铂(ESHAP)方案是美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南推荐的二线治疗方案,安全性与有效性已经过相关文献验证。本研究通过探讨利妥昔单抗、依托泊苷、地塞米松、阿糖胞苷、顺铂(R-ESHAP)方案对复发难治性(recurrent or refractory,R/R)-DLBCL患者疗效的影响,旨在明确R-ESHAP方案用于改善R/R-DLBCL化疗患者临床疗效和安全性,并以ESHAP方案为对照。
1 资料与方法
1.1 研究对象收集2012年5月至2020年4月郑州大学第一附属医院肿瘤科收治的、病理确诊的R/R-DLBCL患者共64例。其中R-ESHAP方案治疗患者37例(R-ESHAP组)、ESHAP方案治疗患者27例(ESHAP组),收集患者临床病理资料包括性别、确诊年龄、是否为生发中心、有无B症状、是否骨髓浸润、Ann Arbor分期、美国东部肿瘤协作组(eastern cooperative oncology group score,ECOG)评分、国际预后指数(international prognostic index,IPI)评分、乳酸脱氢酶(lactate dehydrogenase,LDH)、β2微球蛋白等。
1.2 治疗方案2组均治疗4~6个周期。ESHAP组采用ESHAP方案化疗(依托泊苷60 mg/m2,静脉滴注,第1~5天;阿糖胞苷100 mg/m2,静脉滴注,第1~5天;顺铂75 mg/m2,静脉滴注,分3~4 d;地塞米松20 mg静脉滴注,第 1~5天)。观察组患者采用利R-ESHAP方案,化疗前1天给予利妥昔单抗375 mg/m2,其他药物剂量同ESHAP组,为预防利妥昔单抗过敏反应,用药前30 min给予静脉静推地塞米松5 mg和肌肉注射苯海拉明20 mg。每21 d为1个化疗周期。
1.3 疗效评价患者每2个周期进行1次疗效评价,相关检查包括:血常规、血生化、凝血功能、心电图、全身浅表淋巴结超声、电子计算机断层扫描、磁共振成像或正电子发射体层显像-X线计算机断层现象。根据国际肿瘤疗效评价标准[3],分为完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)和疾病进展(disease progression,PD)。
1.4 不良反应按照WHO抗肿瘤药物的急性和亚急性不良反应评价标准,分为Ⅰ~Ⅳ度,比较2组方案治疗期间出现的不良反应。
1.5 统计学处理采用SPSS 22.0分析处理数据;计数资料用百分数表示,比较用χ2检验;生存情况分析用Kaplan-Meier法,生存率之间的比较用log rank检验;检验水准α=0.05。
2 结果
2.1 2组患者临床病理特征比较2组患者的临床病理特征比较差异均无统计学意义(P均> 0.05),具有可比性。见表1。
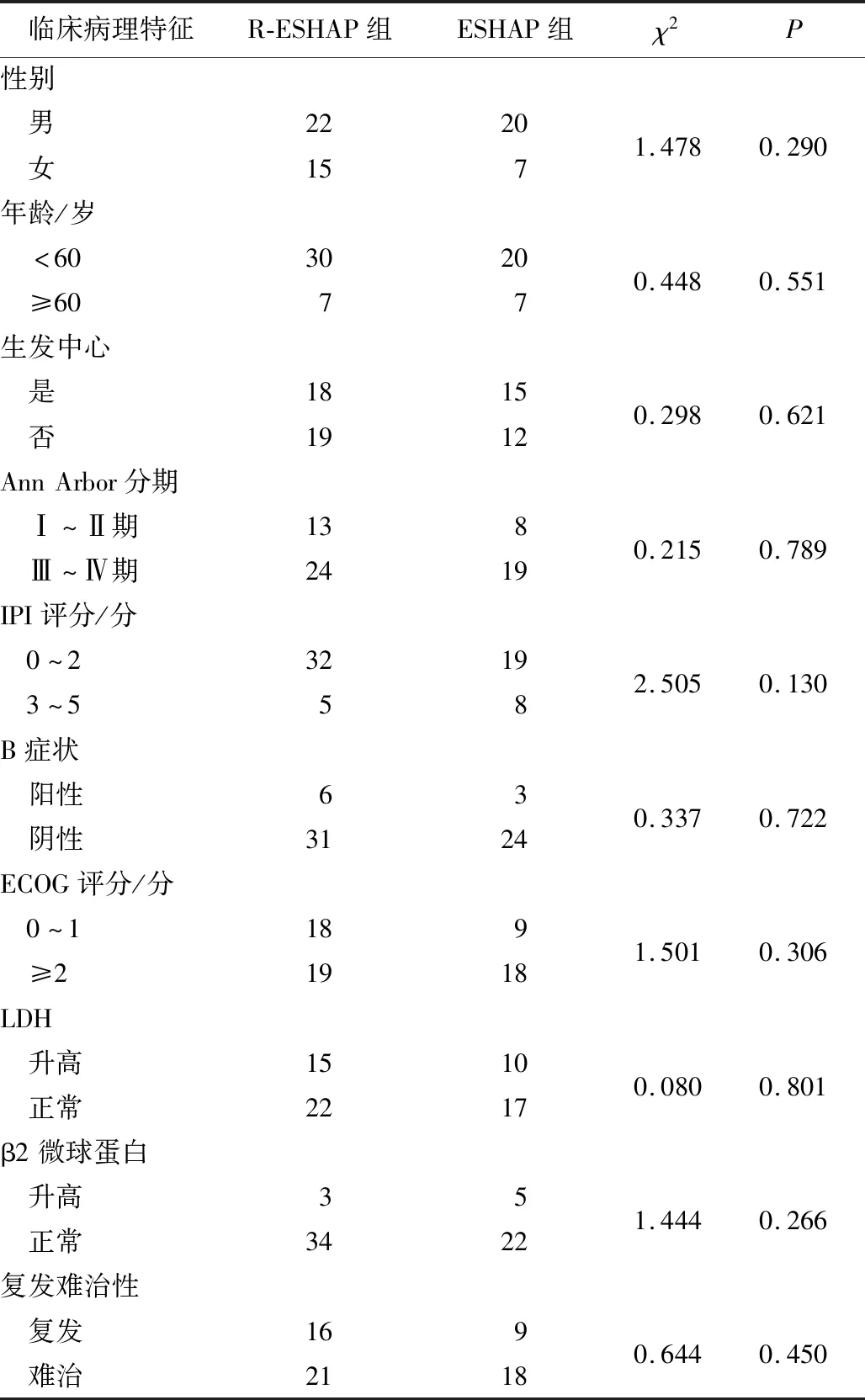
表1 2组患者临床病理特征比较 n
2.2 2组近期疗效比较R-ESHAP组客观缓解率为67.6%,高于ESHAP组的48.1%(χ2=2.440,P=0.096)。见表2。
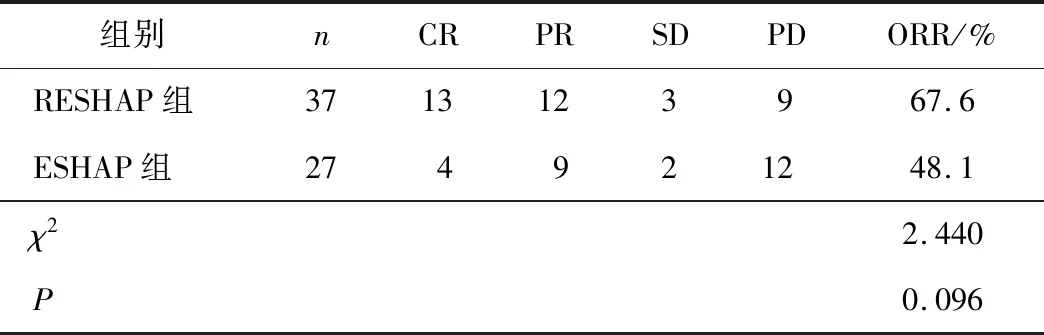
表2 2组近期疗效比较
2.3 2组远期疗效比较R-ESHAP组和ESHAP组患者中位疾病无进展生存期(progression free survival,PFS)分别为13.7个月、5.1个月,R-ESHAP组患者中1、2 a PFS率分别为52.2%和41.3%,ESHAP组分别为27.7%和23.0%(χ2=2.540,P=0.111)。R-ESHAP组和ESHAP组中位生存期分别为40.0个月、21.2个月,R-ESHAP 组1、2 a OS率分别为72.6%、58.5%,ESHAP组分别为68.0%、46.9%(χ2=0.647,P=0.421)。见图1、2。
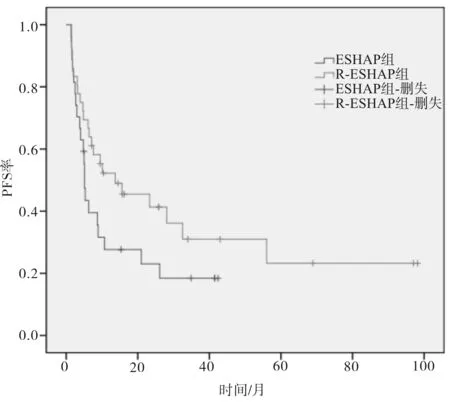
图1 2组患者PFS生存曲线比较
2.4 2组不良反应比较R-ESHAP组与ESHAP组最常见不良反应均为骨髓抑制;R-ESHAP组过敏反应发生率为32.4%,高于ESHAP组的3.7%(χ2=7.959,P=0.005)。所有不良反应经过对症处理后均较治疗前好转,过敏反应通过药物对症处理后可缓解。见表4。
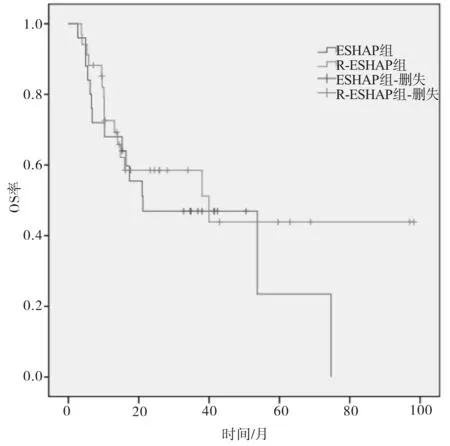
图2 2组患者OS生存曲线比较

表4 2组患者不良反应比较 n(%)
3 讨论
DLBCL是成人淋巴瘤中最常见的一种类型,并且是一组在临床表现和预后等多方面具有很大异质性的恶性肿瘤[4-5],患者接受蒽环类药物联合化疗,约1/3患者生存期可达到5 a年以上[6],接受利妥昔单抗联合CHOP方案的患者疗效率进一步提高[7-8]。经过一线治疗后仍有30%~40%的患者出现再次复发[9]。ESHAP方案是美国NCCN指南推荐的二线治疗方案,因此本文将对比ESHAP方案和R-ESHAP方案治疗R/R-DLBCL的疗效及不良反应。
利妥昔单抗是一种人鼠嵌合抗体,与跨膜抗原CD20结合,介导细胞毒性作用,促进B细胞溶解,加速其凋亡,并提高肿瘤细胞对化疗药物的敏感性,且有效调节机体内环境,阻止肿瘤血管新生[10-11],可有效提高CD20阳性DLBCL患者的预后。依托泊苷作用于拓扑异构酶,破坏DNA复制[12]。阿糖胞苷在胞内转化为三磷酸阿糖胞苷,干扰DNA合成,诱导癌细胞死亡,诱导肿瘤细胞死亡[13],顺铂与DNA相互作用,导致DNA链内或链间交联,破坏细胞调亡,最终导致肿瘤细胞死亡,同时顺铂为广谱抗肿瘤药物,与多种抗肿瘤药物具有协同作用[14-16]。
罗盛等[17]研究发现,对于复发难治性NHL患者行ESHAP方案化疗,B细胞来源的NHL患者的ORR为55.6%,血小板减少发生率为54.8%。Agustin等[18]评估ESHAP方案和R-ESHAP方案治疗R/R-DLBCL的疗效及安全性后发现,R-ESHAP组的ORR为61.0%,不良事件中白细胞减少发生率为88.2%、血小板减少发生率66.7%。本研究中R-ESHAP组ORR为67.6%,ESHAP组ORR为48.1%,R-ESHAP组明显高于ESHAP组,但差异无统计学意义,分析原因可能为样本量较少,扩充病例数有望得到阳性结论。在骨髓抑制、消化道不良反应事件中2组未见明显统计学差异,但在过敏反应的不良事件中,R-ESHAP组明显高于ESHAP组。
本研究中,R-ESHAP组患者中1、2 a PFS率高于ESHAP组,但2种治疗方案PFS相近。R-ESHAP组患者中1、2 a OS率高于ESHAP组,但2种治疗方案PFS相近,但R-ESHAP对比ESHAP仍具有远期优势。
相关研究[19]表明复发的NHL患者,既往未应用利妥昔单抗的患者二线治疗应用利妥昔单抗可提高ORR,本研究虽未明确分析一线治疗应用利妥昔单抗对二线治疗的影响,但是R-ESHAP组ORR明显高于ESHAP组,利妥昔单抗联合ESHAP化疗在改善R/R-DLBCL患者近期疗效及远期疗效中具有重要的意义。
综上所述,R-ESHAP方案治疗R/R-DLBCL患者安全性可控,且具有较好的临床治疗潜力,其近期疗效优于ESHAP方案,未来需要大样本和前瞻性研究进一步验证。

