恶性肿瘤植入放射性125I粒子出现迁移的研究现状与展望
朱俊军,葛乃建,杨业发
海军军医大学第三附属医院东方肝胆微创介入中心,上海 201805
癌症是严重危害全球人类健康的主要疾病之一,其发病数和死亡数仍呈持续增加态势,预计到2030年,全球每年将出现2 200万新发癌症病例和1 300万癌症相关死亡病例[1]。中国也不例外,每年恶性肿瘤的发病数和死亡数分别占全球的23.7%和30.0%,给中国的公共卫生系统带来了沉重的负担[2]。从古代的原始医学到当今的现代医学,人类一直在试图制服肿瘤。在与肿瘤长期的相处过程中,人类不放弃每一次科技进步带来的希望,形成了外科手术、微创、放疗、化疗、靶向治疗、免疫治疗等各种各样的治疗肿瘤的方法[3]。1895年,德国的伦琴发现X射线,之后不久,人们就开始探索将放射线用于肿瘤的治疗。1901年,法国的皮埃尔·居里提出用装有放射性元素镭的小管插进肿瘤内部来治疗肿瘤的设想,从此开启了近距离放射治疗肿瘤的历史。之后,人们将放射性元素封装成细珠状、粒子状、片状等各种不同的形状及尺寸,并在临床应用中逐一尝试[4]。经过100多年的发展[5],近距离放射治疗日臻完善,尤其是1980年代以来,得益于影像引导技术、计算机三维治疗计划及模板定位技术的快速发展,作为近距离放射治疗方法之一的放射性粒子治疗焕发青春,广泛应用于全身各部位实体肿瘤的治疗,成为肿瘤治疗谱家族中的重要一员[6]。在放射性粒子植入治疗的临床实践中,人们观察到了包括粒子迁移在内的各种各样的并发症[7]。现结合国内外文献对粒子迁移这种并发症形成的原因、产生的影响及如何预防等进行综述。
1 125I粒子近距离放疗
Pierre Curie和Marie Curie于1902年发现了放射性元素镭,其后,镭首先被应用于皮肤癌的治疗[8]。这种将放射源直接放置于肿瘤表面或肿瘤组织内并利用放射线杀伤肿瘤细胞的方法即近距离放射治疗[9],是最早开展的放射治疗技术,发展至今,已形成腔内近距离放疗、管内近距离放疗、组织间放疗、术中放射治疗及模治疗等在内的完整体系。根据放射源在体内驻留时间的长短,近距离治疗又可分为暂时性近距离治疗和永久性近距离治疗。对于永久性近距离放疗,常用的插植入组织内的放射性核素有125I、103Pd、198Au,其中,125I以其适宜的半衰期(59.7 d)、射线类型(低能γ射线)、射线能量(27.4~31.5 keV)等物理学特性及临床易防护(最大辐射半径为17 mm)等特点而成为最常用的粒子源[10],在头颈部、胸腹部、盆腔、皮肤等部位的恶性肿瘤及软组织肉瘤等治疗方面得以广泛应用,并取得了确切的效果[11]。目前常用的125I粒子大小为 4.5 mm×0.8 mm,呈圆柱状,钛合金外壳,粒子细小、表面光滑,在组织间易于滑动(图1)[12]。
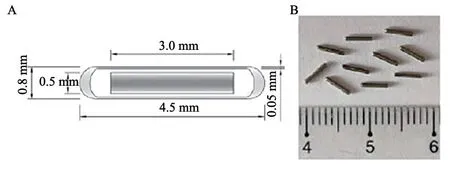
图1 125I粒子示意图(A)及实物照片(B)Fig.1 Shematic diagram (A) and photograph (B) of the encapsulated 125I seed
各医务工作者在粒子植入术后进行质量验证、疗效评估的过程中,经常会发现这种细小的放射性粒子在某些因素的作用下,可以离开瘤体内初始种植的位置,移行到瘤体内或瘤体外的其他部位,形成所谓的粒子迁移[7]。研究[13-14]显示,瘤体内的迁移引起的影响极小,故绝大部分文献讨论的粒子迁移是指离开瘤体到达其他部位的粒子迁移。有中国学者[15]将这种情况归类于粒子种植的围手术期并发症(粒子植入后1~30 d)。实际上,粒子迁移既可以发生于粒子种植的当时,也可以发生于粒子种植后的数年之后。粒子既可迁移至距初始种植位置仅数毫米的邻近区域,也可迁移至距初始种植位置很远的组织或器官。
2 125I粒子迁移的发生
粒子植入已被成功用于头颈部[16]、胸 部[17-18]、腹部[7,19]、盆腔[20]等各部位实体肿瘤的治疗。近年来,相关研究报道屡见不鲜。但各研究者随访时间长短不一,结果也不尽相同,最长随访时间为7年,最短随访时间为3个月,发现粒子迁移率最高可达100%,最低为0%(表1)。

表1 不同部位肿瘤植入放射性粒子后的迁移率Tab.1 Incidence of seed migration after implantation in different tumors
Nakano等[21]对2 160例前列腺癌患者的前列腺原发病灶植入125I粒子,术后为期3个月的跟踪调查显示,21.57%(466/2 160)的患者出现粒子迁移,其中迁移粒子最主要的到达器官是肺,占63.95%(298/466)。洪居陆等[22]对63例肺癌患者共计植入3 179个125I粒子后的调查显示,36.51%(23/63)的患者出现粒子迁移,迁移粒子占总粒子数的2.74%(87/3 179),这些迁移粒子最主要迁移至胸膜腔和异于初始种植部位的肺其他部位,占比86.21%(75/87)。Lin等[23]在399例肝癌患者的肝脏病灶内共计植入了13 977个125I粒子,术后跟踪调查3个月,结果显示,20.30%(81/399)的患者出现粒子迁移,迁移粒子占总植入粒子数1.07%(150/13977),这些粒子最主要迁移至肺,占74.67%(112/150)。
3 125I粒子迁移的机制
肿瘤组织内植入放射性粒子后发生粒子迁移是常见的并发症,且随着植入粒子数、穿刺针及靶体积的增加,此并发症有增加的趋势[30-31]。粒子外壳钛合金具有优良的生物组织相容 性[32],且粒子本身细小,表面光滑,使其不易被机体组织包裹局限化。另外,尚有许多学者从解剖学等其他不同的角度对粒子迁移提出了见解[13,22],主要有三个方面。
3.1 粒子种植部位周围的血管(丛)、潜在的腔隙
前列腺周围静脉丛、肝脏的门静脉及肝静脉、肺血管等因血管丰富均易使粒子顺其迁移至其他部位。脑室系统、支气管、胆管、胰管、输尿管等均可成为粒子迁移的天然通道。Brahimaj等[24]在研究颅内肿瘤粒子植入治疗时,经过长达7年的跟踪研究发现,肿瘤坏死后形成了潜在的腔隙,从而使部分粒子在脑白质内缓慢地移动,平均每年移动8.9 mm,最远的移动了 35.5 mm。
3.2 粒子种植部位的相对活动度
洪居陆等[22]分析肺部肿瘤病灶植入粒子的迁移情况时认为,胸部持续的呼吸活动、剧烈的咳嗽、心脏舒缩活动等均使肺部相对运动幅度大,粒子易于迁移。而腹腔内的肝、胰等器官相对运动幅度稍小,盆腔内的前列腺等器官运动幅度最小。所以,相对来说,种植于肺部病灶的粒子迁移率最高,腹部其次,盆腔最低。
3.3 术者的操作经验
在进行有创医学操作时,术者的操作经验对医疗质量及医疗安全起着重要的作用。加拿大、美国等均对外科医师培训期间的手术数量提出了具体要求,以保证相应的资质及能 力[33]。Taussky等[34]将495例前列腺癌患者按粒子植入的时间顺序平均分为5组,结果显示,第1组的100例患者发生粒子迁移的比率高达40%,平均每个粒子发生迁移的概率为0.012 5;之后每组的粒子迁移率及每个粒子迁移的概率均呈下降趋势;最后一组的100例患者发生粒子迁移的比率仅为9%,平均每个粒子发生迁移的概率为0.002 1。该研究者分析后认为,随着粒子植入实践的积累,操作者可显著提高临床技能,使粒子迁移率明显下降。El-Bared等[35]在分析由2名医师进行粒子植入治疗的1 087例患者之后也认为,操作者经验的差别会导致粒子迁移率不同。
4 125I粒子迁移的影响
粒子迁移可能会对靶区射线剂量产生负面影响,在体内还可引起相应的物理、化学损伤,甚至对所在器官的功能产生影响,但绝大多数情况下不会对机体产生明显影响。
4.1 对粒子迁出部位的影响
Beaulieu等[14]在计算机上用蒙特卡罗方法模拟出粒子种植的11种模型,然后又根据粒子活度、种植粒子数、迁移粒子数、粒子间距等参数模拟出不同的具体状态,并对各具体模型下粒子剂量分布特点、成本效益比等进行了分析比较。结果显示,对于125I这种低活度的粒子,少量粒子迁移(迁移率<5%)更可能影响初始种植部位靶组织的剂量分布,而对该部位肿瘤控制及其他部位正常组织几乎没有影响,认为这很有可能是植入粒子总数与植入粒子间距等因素相互作用的结果。Maletzki等[13]回顾性研究了63例前列腺癌植入粒子后的患者,结果显示,在术后3年及更长的时间内,少量粒子的迁移尚不足以对初始种植部位肿瘤的有效治疗剂量造成影响,认为这可能与125I粒子的半衰期相对较短、放射活度相对较低有关。Brahimaj等[24]研究颅内粒子迁移时发现,99.999 7%的射线剂量于植入粒子后3年内释放完毕,仅有极其微量的射线被迁移粒子带走。
4.2 对粒子迁入部位的影响
粒子迁移之后,可通过机械性梗阻、放射性损伤等作用影响迁入部位的组织或器官。Zhu 等[36]报道1例前列腺癌患者植入粒子后22个月,1个粒子迁移并堵在冠状动脉右支严重狭窄处从而诱发急性心梗。Calvert等[37]报道了1个案例,该前列腺癌患者于前列腺内的瘤体植入粒子后6年,粒子迁移至右肺上叶肺动脉分支从而导致呼吸困难。Miura等[38]在给1例前列腺癌患者的前列腺瘤体内植入粒子后的当天即发现粒子迁移至左肺下叶,随后为期12个月的胸部X线随访清楚地显示了粒子周围肺组织炎症从产生至消失的过程,全程未使用抗生素等特殊治疗,考虑为放射性肺炎。Chen等[39]报道,1例前列腺癌患者于前列腺瘤体内植入粒子10年后,发现右肺下叶约4 mm肿块,经病理学检查证实为小细胞肺癌,肿瘤切开后发现1个粒子藏匿其中。
5 125I粒子迁移的预防
粒子迁移的原因是多方面的,因此,为有效减少粒子迁移而应针对性地改进措施,比如提高操作技能、使用粒子链条、包膜粒子等。
Merrell等[30]将1 000例前列腺癌患者分为3组:单纯使用松散粒子组(391例)、单纯使用粒子链条组(566例)、混合使用松散粒子及粒子链条组(43例)。结果显示,第1组粒子迁移率为45.52%(178/391),第2组粒子迁移率为0.88%(5/566),第3组粒子迁移率为11.63%(5/43),粒子链条技术显著降低了粒子迁移率。但在实际使用中,粒子链条存在操作耗时、柔性不足、剂量调整难等缺点,甚至不同的链接材料、链条长度也会对粒子的迁移产生负面的影响[40]。为此,Warrell等[41]在粒子表面包被0.082 5 mm厚的可吸收聚合物膜,并进行了一项试验,将47例前列腺癌患者分为植入包膜粒子组(26例,共计植入2 227个粒子)和非包膜粒子组(21例,共计植入1 858个粒子)。结果显示,包膜粒子组粒子迁移率为3.14%(70/2 227),非包膜粒子组粒子迁移率为6.89%(128/1 858),使用包膜技术后即可达到降低粒子迁移率的目的,又可有效规避粒子链条的不足之处。
综上所述,作为一项成熟的技术,125I粒子植入肿瘤组织间近距离放射治疗已成为宫颈癌、子宫内膜癌、前列腺癌治疗方法中不可或缺的一员,在其他恶性实体肿瘤的治疗中也扮演着重要的角色。粒子迁移是该治疗方法常见的并发症,虽然大部分情况下并不会产生明显的影响,但仍需通过提高临床技能、改进粒子工艺等途径减少此并发症,并做好长期随访工作,加强临床监控,避免潜在的医疗风险。

