放疗影像自动分割效果评估中几何参数与剂量学参数之间的关联性
余行,刘欢,傅玉川
四川大学华西医院放疗科,四川成都610041
前言
靶区及危及器官的勾画是放射治疗流程中重要的一步,相较于手动勾画,自动分割具有提高勾画效率、降低勾画差异等优势[1]。目前,有基于图谱的自动分割商用软件可应用于临床,在对感兴趣区域(Region of Interest,ROI)(主要是危及器官)进行自动分割后,由医生对自动分割结果进行修改并确认[2]。近年来,基于深度学习的医学影像自动分割方法迅速发展并开始运用于放射治疗靶区及危及器官的自动分割[3-4],并以其鲁棒性和灵活性显示出巨大的潜力[5]。
无论是基于图谱的自动分割,还是基于深度学习的自动分割,对分割结果的评估和验证都是将其应用于临床必不可少的环节之一。在评估过程中使用最广泛的轮廓指标是几何指数,包括体积差异、质心距离、一致性指数和边缘分析等[6]。尽管几何指数计算方便,并且可以选择多种几何参量来进行较为全面的评估,但它们缺乏临床相关意义,不能直接反映勾画差异对靶区和危及器官剂量分布的影响[7]。
本文利用深度学习模型自动分割生成的靶区及危及器官轮廓与医生手动勾画轮廓进行多参量的对比评估,探讨对自动分割结果进行评估时将几何参数与剂量学参数联合使用的必要性与可行性,同时还分析了几种常用几何评估参数之间的相关性。
1 资料与方法
1.1 影像资料
图像数据来自于2015年2月至2019年7月在四川大学华西医院放疗科接受治疗的180例宫颈癌患者,分期为IB~IIA期,均于术后接受放射治疗,其中162套CT数据用于训练,18套CT数据用于测试。所有患者均在CT扫描前憋尿以保证膀胱充盈,扫描时采用仰卧位,双手举过头顶,使用头颈肩热塑性面罩固定,并注射对比剂。图像使用西门子模拟定位CT Siemens Somato(Siemens Healthcare,Forchheim,Germany)进行采集,图像重建分辨率为512×512,层厚为3 mm。危及器官包括膀胱、左右股骨头、小肠以及直肠。临床靶区(Clinical Target Volume,CTV)分为原发灶的CTV和盆腔淋巴结的CTV,原发灶CTV包括宫颈肿块、整个宫颈及宫体、宫旁组织及阴道,盆腔淋巴结CTV包括髂总、髂内、髂外、骶前及闭孔淋巴引流区[8]。
1.2 自动分割模型及结果
使用全卷积神经网络FCN-8s[9]构建我们的自动分割模型,采用有公开代码和参考模型的开源深度学习仿真工具Caffe[10],基于ImageNet数据库进行迁移学习完成预训练。使用Python作为编程语言对医学影像DICOM RT文件进行相关的转换、处理及计算。将162例患者的CT图像用于模型的训练,采用预训练与数据扩增避免过拟合,在NVIDIA GTX 1080TI GPU上进行模型训练。利用训练好的模型对18例测试患者的CT图像数据进行靶区和危及器官的自动分割,再将自动分割结果与医生手动勾画轮廓进行比较,表1列出了以几何指数表示的分割结果,每一个几何参数的定义将在第1.4节中详细说明。

表1 以几何参数表示的分割结果Tab.1 Segmentation results evaluated by geometric parameters
1.3 计划设计
所有计划均在Raystation 4.7计划系统上进行设计,计划靶区体积(Planning Target Volume,PTV)处方剂量为50.4 Gy/28次,危及器官的剂量限值分别为膀胱、直肠:V40<60%、V50<50%;左右股骨头:V50<5%;小肠:V30<40%。计划均采用容积旋转调强(Volumetric Modulated Arc Therapy,VMAT)计划,采用双全弧照射(180°~181°,181°~180°),对于靶区而言,至少95%的靶区体积接受100%的处方剂量,靶区热点剂量不超过处方剂量的107%。
1.4 几何评估参数
参考各类评估方法,我们选取了5种广泛应用的几何评估参数指标[6,11-12],基于面积/体积的评估方法包括Dice相似性系数(Dice Similarity Coefficient,DSC)和相对体积差(Relative Volume Difference,RVD);基于距离的评估方法包括最大Hausdorff距离(Max Hausforff Distance,Max HD)、95%Hausdorff距离(95% Hausforff Distance,95% HD)和质心差(Centroid Difference,CD)。以医生手动勾画为标准来评价自动分割效果,本文中几何参数的计算都基于开源软件3D Slicer[13]。
1.4.1 DSCDSC是医学图像分割中常用的指标,其计算公式如下所示:

其中,|A|代表医生手动勾画的分割区域,|B|代表自动分割区域,|A∩B|代表A和B的交集。DSC的数值范围介于0到1之间,其中1表示图像之间完全重叠,0表示没有重叠,数值越高代表分割效果越好。
1.4.2 RVDRVD表示分割图像二者的体积差异,其计算公式如下所示:

其中,|A|表示自动分割结果,|B|表示医生手动勾画结果。
1.4.3 Max HD对于两个给定的集合A和B,Max HD定义如下所示:

其中,||a-b||是欧几里得距离,a和b分别是A和B边缘上的点,同时h(A,B)通常被称为直接HD。
1.4.4 95%HD95%HD与Max HD相似,但95%HD基于A和B中边界点之间距离的第95个百分位的计算,其目的在于消除极端点对于分割结果的影响。
1.4.5 CDCD为两组勾画轮廓质心之间的距离,用于评价两组轮廓之间的总体位置偏差,其定义如式(5)所示:

其中,(Xauto,Yauto,Zauto)为自动分割结构的质心坐标,(Xmanual,Ymanual,Zmanual)为医生手动勾画结构的质心坐标。
1.5 剂量评估参数
本研究为回顾性研究,利用已实施的放疗计划,分别获得医生手动勾画轮廓和自动分割轮廓的剂量-体积直方图,如图1所示,并提取了多个剂量学参数。对于CTV,剂量学参数为ΔD95(95%靶区体积接受的最小照射剂量差)与ΔD98,对于危及器官,剂量学参数为ΔDmean,其公式如下所示:

其中,Dn,manual为医生手动勾画CTV剂量,Dn,auto为自动分割CTV剂量,Dmean,manual为医生手动勾画危及器官剂量,Dmean,manual为自动分割危及器官剂量。

图1 针对同一位患者医生手动勾画轮廓(实线)和自动分割轮廓(虚线)的剂量-体积直方图Fig.1 Dose-volume histogram of manual segmentation contours(solid lines)and automatic segmentation contours(dashed lines)for a patient
1.6 统计学方法
所有数据均使用SPSS 20.0版(SPSS,Chicago,IL,USA)进行分析,计量资料采用均数±标准差表示,线性回归分析探索靶区与危及器官剂量学参数与几何参数的关系,采用Spearman相关性分析探究几何参数间的相关性及医生勾画与自动分割剂量学间的相关性。P<0.05为差异有统计学意义。
2 结果
图2显示了对于不同ROI,医生手动勾画轮廓和自动分割轮廓之间的平均剂量对比。几何参数与剂量学参数间关系如图3所示。首先,几何参数与剂量学参数之间的关系较弱,如图3a所示几何参数与剂量学参数的关系研究中,66.7%(20/30)的关联系数R2<0.6,63.3%(19/30)的关联系数R2<0.4。靶区及危及器官的轮廓一旦确定,其几何参数就不会改变,而对于剂量学参数而言,它的参数选择较广,我们以靶区为例,分别选择了ΔD95、ΔD98两个参数作为剂量学参数(图3a、图3b),结果表明剂量学参数的选择影响了关联系数的数值大小,但其关联关系仍然较弱。
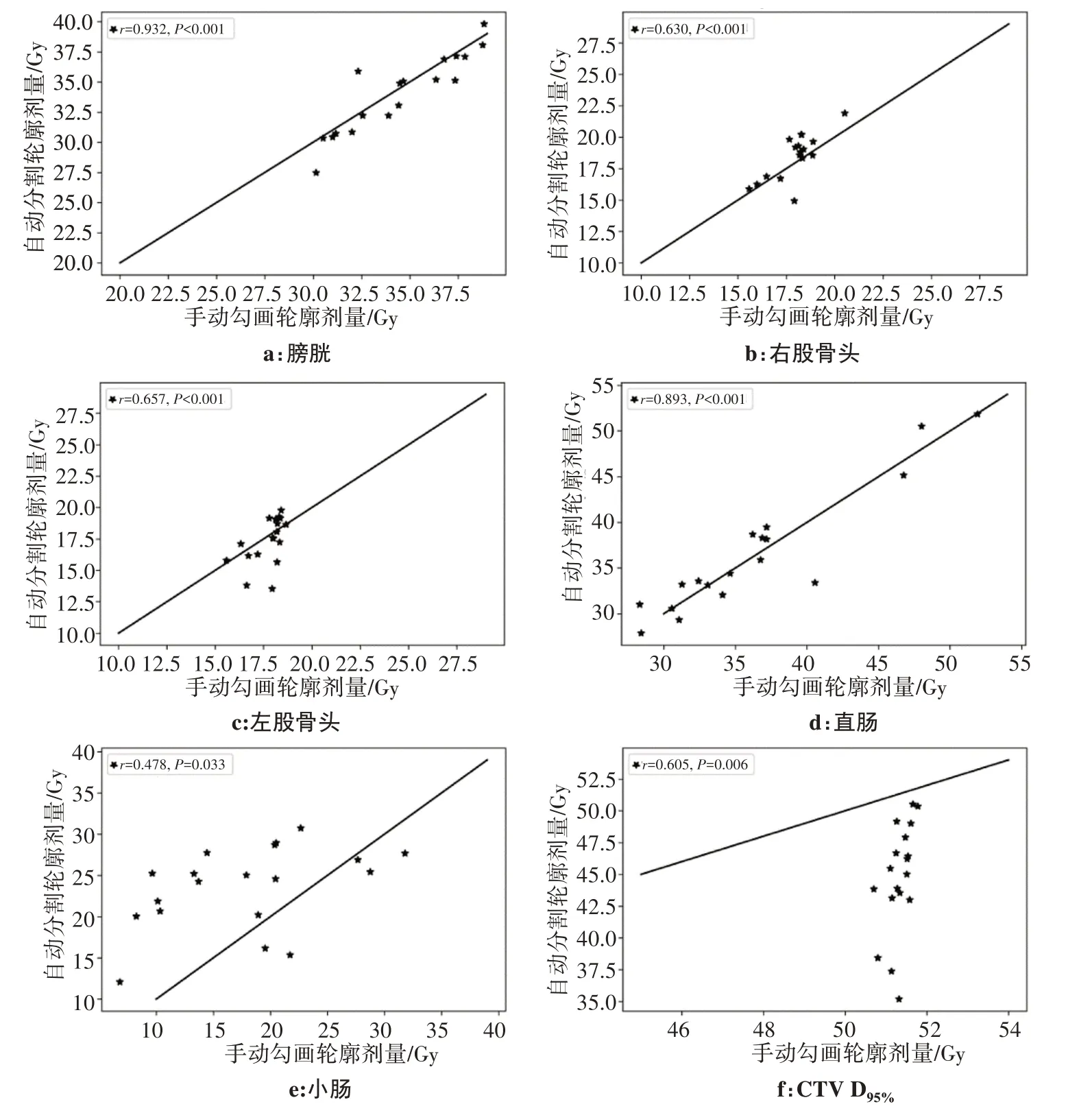
图2 医生手动勾画与自动分割的剂量对比Fig.2 Comparison of dose parameters between manual segmentation and automatic segmentation
其次,几何参数与剂量学参数之间的关系不稳定,没有单一的几何参数与剂量学参数始终显示出较高或者较低的相关性(图3a、图3b),小肠的平均剂量ΔDmean与DSC的关联系数R2为最高值0.922,而同样对于DSC而言,CTV的ΔD95与其关联系数R2仅为0.239,低于CTV与Max HD的关联系数0.556。
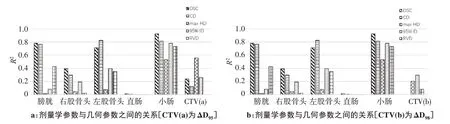
图3 剂量学参数与几何参数之间的关系Fig.3 Correlation between geometric parameters and dosimetric parameters
表2所示为几何参数间的关系,相关系数|r的数值不超过0.625,CD与95%HD的关系系数|r最大,其余几何参数间的|r|均小于0.5。
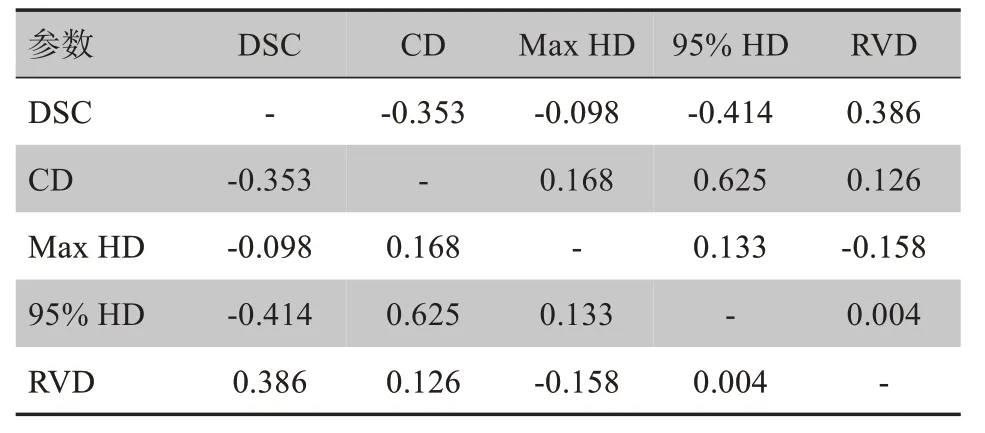
表2 几何参数间的相关系数rTab.2 Correlation coefficient r between geometric parameters
3 讨论
本研究利用基于caffe搭建的全卷积神经网络FCN-8s对宫颈癌外照射放疗中的危及器官和靶区进行自动分割,就常用的几何评估常数而言,其分割结果优于临床上常用的ABAS分割结果[14],因此用该模型的分割结果进行评估参数的关联性研究是可行的。
在这项研究中,我们发现大多数几何指数与关键剂量学终点之间关联较弱且不一致,这表明使用几何参数估算剂量学参数是不可接受的。剂量与几何评估方法呈弱相关;几何评估方法容易出现假阳性结果,这一般发生在危及器官上,即对于几何学参数而言,分割结果不可以接受,然而就剂量学而言,其满足临床要求。一般来说,当DSC大于0.7时,可认为分割结果是可以接受的[15]。Kaderka等[16]研究表明,有时候即使DSC值很低,其剂量学参数也符合临床要求,特别是对于小体积的危及器官。而对于靶区,评估容易出现假阴性结果,即靶区具有可以接受的几何结果但其剂量结果不符合临床要求,这是由于在靶区周围具有较高的剂量梯度,相同程度的轮廓改变,其剂量影响大于对危及器官的影响。
通常在对图像分割进行评估时,会选用不同的几何参数对图像分割进行评估。在我们的研究中,选取了评价标准中常见的5个参数[17-20],它们可以分为两大类,一种是基于体积/面积的评估方式例如DSC、RVD;另一种是基于距离的评估方式如Max HD、95%HD及CD。DSC容易受结构体积/面积的影响,而对边缘信息不敏感。例如两组结构有相同的重叠体积/面积,而总体积/面积的和不同,将会导致其DSC值不同。基于距离的评估方式如Max HD对错误的点非常敏感[17]。我们的研究分析了几种不同几何评估参数间的关系,结果表明几种参数间为弱相关(95%HD与CD)或者不相关。因此在对分割结果进行评估时,可以分别使用不同的参数。
本研究的不足之处在于,对于危及器官,我们仅提取了平均剂量作为剂量学参数,尽管对于靶区而言,我们选择了ΔD95、ΔD98作为剂量学参数,但是没有临床上常见的CI指数。我们的结果表明,不同参数的选择会对几何参数与剂量学参数的相关系数造成影响,但是其趋势及相关性强弱大致不变。因此,在后续研究中,将考虑纳入更多的剂量学参数。
4 结论
在对放疗领域的图像分割结果进行评估时,应该同时考虑到几何参数与剂量学参数。选择几何参数时,应联合使用基于面积/体积的评估方式与基于距离的评估方式。

