天然多糖在生物医用材料领域的应用研究进展
黄超伯,游朝群△,熊燃华,2,王飞
(1. 中比先进生物医学材料国际联合实验室,南京林业大学化学工程学院,南京 210037;2. 根特大学药学院,根特B-9000,比利时)
石油资源的稀缺和由此导致的石油基材料的逐渐短缺促使当前社会去寻求更多的环境可持续性材料资源。其中,可再生材料是一种理想的绿色替代品,可以最大限度地减少废物的产生[1]。天然多糖是自然界中广泛存在的一类大分子聚合物,一般由单糖或低聚糖聚合而成,其种类繁多,包括甲壳素及海藻酸、纤维素及其衍生物、淀粉、琼脂糖、壳聚糖等。天然多糖类聚合物具有结构稳定性高、对生物体无毒、生物相容性好、可生物降解等优点[2-4],在生物体内可实现多种功能化应用,包括机体组成部分[5-7]、能量储存[8-9]、药物递送[10-13]、机体保护[14-15]、蛋白质结构和功能的调控[16-17]、细胞信息传递[18]等。随着学科的交叉融合,天然多糖在生物医学领域的应用研究逐渐呈现多元化形式。例如,采用新颖及创造性的方法,利用天然多糖中的木质纤维素材料可有助于生物技术、生物工程和生物经济的可持续性发展[19-21]。该项新技术的应用推广对于进一步实现天然高分子材料的高值化利用有着重要意义。
1 天然多糖基材料在生物医学领域中的传统应用
在过去的几十年里,天然多糖由于具有多种保健作用而受到人们越来越多的关注。天然多糖可分为高等植物多糖(如菊糖和果胶)、海洋多糖(如琼脂、海藻酸、卡拉胶和壳聚糖)和微生物胞外糖(如右旋糖酐、结冷胶、葡聚糖、透明质酸、果聚糖和支链淀粉)[22-27]。近年来,以天然多糖材料作为基材在生物医学领域进行各种功能化设计已成为科研领域的热门课题。根据功能应用的分类,主要应用于包括药物载体[28-31]、组织工程[32-34]、支架材料[35-36]以及伤口敷料[37-40]等需求缺口较大的领域中。笔者分别介绍各个研究方向的近期代表性研究工作,呈现当前天然多糖基材料在传统生物医学领域中的应用现状。
1.1 药物载体
设计控释系统的目标是提供安全、理想的药物释放效果,提高靶向治疗的有效性。选用天然多糖作为基材去设计各种药物缓控释系统是近年来的研究热点。尽管纤维素水凝胶被认为是一种很有前途的药物释放载体,但其药物释放的被动方式和无远程刺激响应极大地限制了其进一步的应用效果。Lin等[41]报道了一种简单的单锅法制备磁性β-环糊精/纤维素水凝胶珠的方法,该方法在外磁场(EMF)作用下具有快速溶解能力,可远程控制药物由被动释放到逐步释放。接枝的β-环糊精使水凝胶具有较高的载药能力,同时,Fe3O4纳米粒子的加入通过电磁场诱导三维网络的快速可逆变形,为药物的逐步释放提供了能量。该水凝胶在药物逐步释放剂量和速率方面的效率可以通过开关电磁场和调整Fe3O4纳米颗粒的含量来进行控制。通过小鼠胚胎成纤维细胞系NIH 3T3细胞增殖验证了β-环糊精/纤维素水凝胶的无毒及生物相容性等优点,进一步证实了天然多糖基材料应用于可植入智能药物递送载体的可行性。
此外,天然多糖基材料除了具有无毒及生物相容性好等优点,基于天然多糖制备的水凝胶同样具有优异的溶胀性能从而在药物缓释方面显示巨大的应用潜力。Lin等[42]以阳离子纤维素纳米晶(CNC)和阴离子海藻酸盐为原料制备了具有双膜结构的生物相容性水凝胶。该双膜水凝胶的结构包括外膜由整齐的海藻酸盐组成,内膜由阳离子CNC和阴离子海藻酸盐静电相互作用巩固。将两种药物引入不同的水凝胶膜中,保证了络合的药物协同递送和不同药物在两层膜中的不同释放行为(外膜药物快速释放,内膜药物延长释放)。双膜水凝胶内膜上修饰的改性纤维素纳米晶(CCNC)不仅使该新型双膜结构水凝胶材料具有生物相容性,还可以提供持续的药物释放效果,该设计实现的协同释放效应或可能解决生物医学应用上的耐药性问题,突出了天然多糖及材料应用于药物载体的巨大潜力。
1.2 组织工程
2007年,Bodin等[43]报道了关于纳米纤维素在组织工程中的应用,重点研究了细胞黏附介导GRGDS寡肽功能化修饰细菌纤维素纳米纤维支架的构建。这些支架在体外增强了人血管内皮细胞的黏附,有望用于血管组织工程。在神经组织工程中,首次发现神经母细胞瘤细胞SH-SY5Y在三维细菌纳米纤维素(BNC)支架上培养时,有黏附、增殖和向成熟神经元分化的现象,电生理记录检测到的功能动作电位显示了这一现象[44]。Valarmathi等[45]采用静电纺丝(E-Spin)方法制备了羟基磷灰石/丝纤维/甲基纤维素(HAP/SF/MC)复合材料(图1)。结果显示,该电纺复合材料的拉伸强度范围达到25.39~102.93 MPa,且拉伸强度随孔隙率(66.24%~90.11%)的增加而增加。体外溶血研究表明,所有的样品都是非溶血的(<1%)。人成骨细胞增殖结果表明,与未加HAP的SF/MC复合材料相比,表面HAP的存在促进了细胞的黏附、增殖和碱性磷酸酶(ALP)活性。该研究进一步指出,以质量分数25%的HAP电纺复合材料制备的SF/MC(质量比为2∶1)在未来的骨科应用中有可能成为一种良好的骨替代品。天然多糖基材料可以互相之间进行复合从而获得比单一材料更好的力学性能,这些复合材料在组织工程中得到广泛的应用。
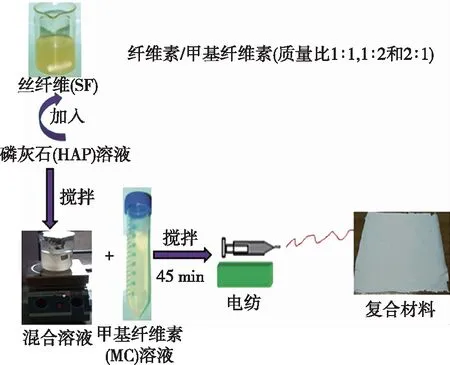
图1 电纺丝复合材料的制备[45]Fig. 1 Preparation of the electrospun composite
利用生长因子作为生化分子来诱导细胞分化是组织工程中常见的策略。然而,受到与生长因子有关的限制因素,如半衰期短、高有效生理剂量和高成本,促使人们寻找生长因子替代品。Ramos等[46]探索了利用胰岛素蛋白作为生化因子,在仿生电纺丝微纳米结构支架上帮助肌腱愈合和细胞分化。在该研究中,采用不同体积比例的聚己内酯(PCL)和醋酸纤维素(CA)合成天然共混物制备微纳米纤维,以平衡支架在机械强度、亲水性和胰岛素传递等方面的理化性能。结果表明,当PCL和CA的体积比为3∶1时,在促进细胞附着和胰岛素固定化方面是最佳的。此外,胰岛素固定化纤维基质也显示骨髓间充质干细胞MSCs的肌腱表型标记表达增加,与胰岛素补充培养基的结果类似,表明胰岛素生物活性得到了保存。该研究成果突出了天然多糖基功能化支架在肌腱愈合和再生方面有潜在的应用前景。
1.3 支架材料
随着经济不断发展以及生活质量的提高,人们对生物医用材料的需求越来越大,尤其是对关节、人工牙齿以及心血管等生物医用材料的需求量不断攀升。Nizan等[47]利用冷冻干燥技术成功制备了羟乙基纤维素/聚乙烯醇(HEC/PVA)和羟乙基纤维素/聚乙烯醇/纤维素纳米晶(HEC/PVA/CNC)多孔三维支架。结果显示,将HEC/PVA与CNC结合后,显示出优越的功能,使得平均孔径从~54.1 μm减小到~33.4 μm;热研究表明,HEC/PVA/CNC支架的熔点温度略有升高。此外,实验结果显示人SV转染成骨细胞hFOB能够在两种支架上附着和扩散,支持细胞的黏附和增殖。由于天然多糖基材料的生物相容性和生物可降解性,这些新开发的高孔支架可能为骨组织工程再生提供一种有前途的支架基质。
骨移植是目前临床的辅助手段。除了传统的骨移植,还有一种替代方法,即工程骨组织。Aki等[48]利用3D打印技术制备了新型聚乙烯醇/六方氮化硼/细菌纤维素(PVA/hBN/BC)复合材料骨组织支架(图2)。结果表明,BC的加入降低了支架的抗拉强度,其中PVA/hBN/BC质量分数比为12∶0.25∶0.5时的断裂伸长率最高,为93%,且可显著提高3D支架上的成骨细胞存活率。复合支架上的细胞形态显示,细菌纤维素掺杂支架具有黏附性。该研究工作充分表明,多孔结构清晰的细菌纤维素掺杂3D打印支架作为一种适合骨组织工程(BTE)的组织支架具有很大的潜力。
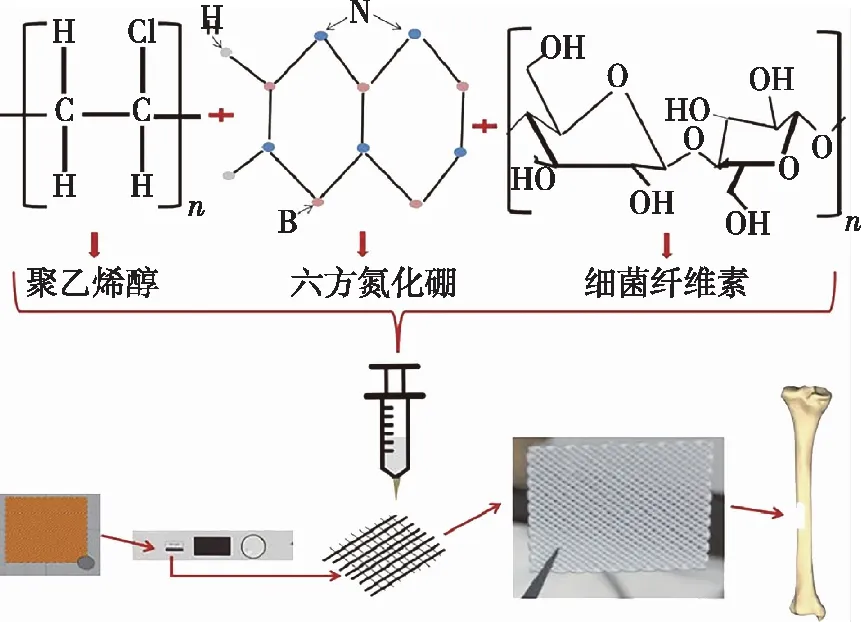
图2 新型聚乙烯醇(PVA)/六方氮化硼(hBN)/细菌纤维素(BC)复合支架的3D打印示意图[48]Fig. 2 Schematic diagram of 3D printing of PVA/hexagonal boron nitride/bacterial cellulose composite scaffolds
1.4 伤口敷料
近年来,研究人员对原位快速交联水凝胶的制备越来越感兴趣,天然多糖分子表面含有大量活性基团可进行功能化修饰,在材料的韧性、强度及疏水性方面都能获得良好效果,表现出独特的优势。Xu等[49]采用乙烯醚(VE)侧链在温和的条件下改性海藻酸钠(SA),结合双交联机理制备了一种凝胶性能优良的快速交联氢键水凝胶SA-VE/H2O;基于此机理,在紫外照射下引入巯基烯与二硫苏糖醇(DTT)发生点击化学反应又制备了一种双交联藻酸盐SA-VE/DTT。实验结果显示该水凝胶体系不仅快速凝胶,而且表现出储能模量高达13 373 Pa和稳定性超过1个月等优点。两种水凝胶对小鼠胚胎成纤维细胞系NIH 3T3均无细胞毒性。此外,在大鼠尾止血实验中表现出26 s内快速止血行为。天然多糖基水凝胶生物相容性优异、溶胀性好、稳定性高,在创面敷料中显示出巨大潜在应用价值。
此外,天然多糖类大分子在伤口护理敷料中的应用也受到越来越多的关注,因为它们具有生物相容性和生物降解性等优点。Trevisol等[50]在研究中利用海藻酸盐和羧甲基纤维素(CMC)制作薄膜作为伤口敷料的应用材料。这些膜分别铸型为带有和不带有双氯芬酸的单层(ML)和双层(BL) 结构。结果显示,双分子层对负载的药物分子双氯芬酸的吸附效率(77.3%)高于单分子层的吸附效率(57.5%),且两种膜的形态结构均质且具有黏性。BLD膜的释放时间(600 min)比MLD膜的释放时间(420 min)要慢,这说明无药层对传质起到了阻碍作用,降低了爆震效应。该项研究表明,海藻酸盐和CMC基质有潜力作为药物传递系统应用于伤口敷料。
2 天然多糖基材料在生物医学领域中的新型应用
目前,生物基材料的高值化利用是现代林业发展的重点内容,凭借自身独有的无毒、生物相容性好及可生物降解等优势,天然多糖不仅可以在传统生物医学领域大放异彩,还能通过学科交叉跨领域解决技术瓶颈,进一步拓展其应用方向,实现生物质材料的深层次增值增效。笔者以下主要综述本课题组在细胞共培养、药品防伪编码、病毒检测及仿生自驱动等方面的代表性研究工作,呈现当前天然多糖基材料在生物医学领域中的创新性应用研究。
2.1 细胞共培养
目前,有害的有机试剂被用作连续相的微流体技术导致的细胞毒性仍是一个急需解决的难题。因此,对于微颗粒中三维细胞培养,在无油、无表面活性剂条件下简单、高通量制备微球是一个理想的策略。Tang等[51]通过微加工技术手段制备芯壳微针头组件,成功制备一系列木质纤维素基多面异向(MCM) 微球(2~8面各异向微球);在对 MCM 的形貌、粒径尺度分布等关键性质进行深入研究之后,对木质纤维素聚合物溶液在接收浴中的离子交联和不良溶剂固化成球过程进行了系统分析,建立了适用于水相及有机相溶解的木质纤维素基聚合物的新方法。 该研究首次实现了木质纤维素基多尺寸均匀分布(约50~1 400 μm) 的8面各异向微球的可控制备,可应用于细胞封装。凭借木质纤维素基材料的优良特性,所制备的木质纤维素基 MCM 展现出了良好的生物相容性,已被证明可用于8种细胞的3D共培养(图3),实现多种细胞的有序组装和任意编队,对研究细胞之间的相互作用提供了新思路。
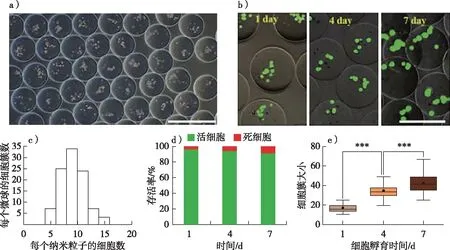
a)负载HepG2细胞的Ca-Alg微球; b)1,4,7 d后Ca-Alg微球的荧光显微镜图像; c)每个微球的细胞簇数; d)1,4,7 d后细胞存活率; e) 1,4,7 d后细胞团簇大小; ***p < 0.001。图3 一步法制备负载细胞的单面微球[51] Fig. 3 One-step fabrication of the one-faced microspheres carrying cells
2.2 药品防伪编码
近年来条形码引起了广泛的关注,特别是在医学和生物医学应用中的多路生物检测和防伪方面。然而,大多数条形码或防伪方法将不可避免地使用化学光引发剂、交联剂、表面活性剂,或美国食品药品监督管理局(FDA)未经批准的聚合物,这不利于敏感生物分子或细胞的存在。Tang等[52]提出了一种可实现的气体剪切方法,通过使用含有不同荧光纳米颗粒组合的预凝胶溶液在10面微球中程序化调整每个隔间的颜色,成功制备生成了10面微球条形码,并对每个隔间的性能进行精确控制(图4)。在该设计中,采用三原色(红、绿、蓝)获得多达7种合并荧光色,构成大量编码信息,能够有效地实现高通量信息存储。更重要的是,利用具有生物相容性的海藻酸钠构建多色微球条形码,有望推动食品和医药防伪领域的发展。该研究开辟了利用生物基材料制备药物编码防伪体系的新思路,首次将生物基编码微球应用于药品防伪这一前沿领域,增加了生物基材料在防伪领域广阔应用的可能性, 为生物基材料的高值化利用基础研究奠定了基础。
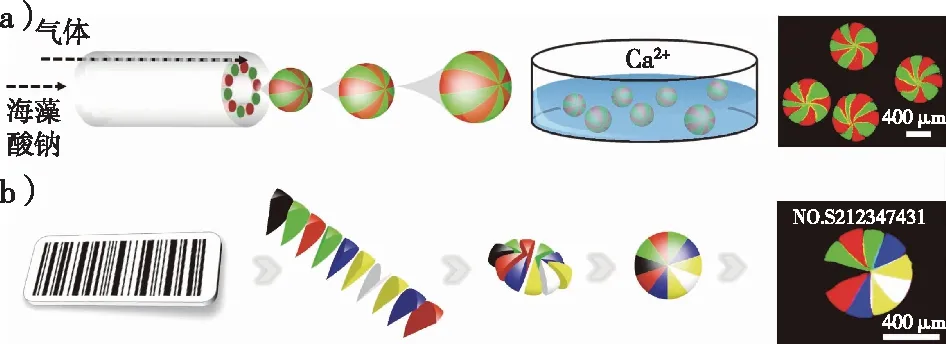
图4 10个面的多分区微球(a)/记忆微球示意图(b)[52]Fig. 4 Schematics showing the preparation of 10-faced (a) multicompartmental microspheres and (b) memomicrospheres to store information
2.3 病毒检测
针对人类免疫缺陷病毒HIV防治过程中的多种局限性,Hua等[53]提出了利用兼具良好生物相容性与 pH 响应型的邻苯二甲酸乙酸纤维素(CAP)制备快速响应的纤维素基纳米纤维膜的新思路与新方法。基于CAP在结构上超细直径(纳米级)的巨大优势,以及其他诸如高比表面积、高灵敏度和快速响应等优点,Hua等[53]利用静电纺丝工艺制备出了高效负载抗 HIV 药物(替诺福韦)的超细 pH 响应木质纤维素基纳米纤维 (图5),测试表明,其对人类精液快速响应,8 s内即完全溶解,快速释放药物。该研究建立了利用木质纤维素制备抗 HIV 高灵敏智能响应型木质纤维素基纳米纤维的工艺流程,实现了木质纤维素基纳米纤维在阴道低 pH 环境下的结构稳定,而少量精液刺激即快速药物释放的良好效果。所构建的快速响应型预防 HIV 病毒感染的方法高效简便,有望在 HIV 防治领域作为新一代的预防产品而得以应用,可产生巨大的社会效益与经济效益。

a)纯CAP纤维的扫描电镜(SEM)图像;b) 纯PU纤维的SEM图像;c)PU/CAP同轴纤维的SEM图像;d)PU/CAP同轴光纤的共具焦图像(绿色为CAP;红色为PU);e)PU/CAP同轴纤维的TEM图像;f)电纺PU/CAP同轴纤维(质量分数28% PU)、纯CAP和纯PU纤维的热重分析;g)分别分散在SVF和PBS中负载罗丹明b的PU/CAP同轴纤维荧光显微图像(质量分数28% PU)。标尺: 50 μm。 图5 纤维的结构表征[53]Fig. 5 Characterization of the structure of the fibers
2.4 仿生自驱动
受天然微生物游动行为的启发,设计开发人造微/纳米马达模拟这些特征自然生物的行为去实现各种功能化应用越来越受到关注。目前在开发功能性微型马达方面尽管投入了大量精力,但是受限于有机溶剂、紫外线照射及细胞毒性试剂的不可避免的使用,将它们应用于生物相关介质受到了很大的阻碍。Tang等[54]采用简单、灵活、生物相容性和高通量的气体剪切策略,以具有生物相容性的海藻酸钠(Na-Alg)构建了仿生自驱动微球(图6)。通过巧妙设计磁性纳米颗粒和过氧化氢酶在多室微球特定腔室中的空间分布,成功实现了自驱动微球的双重驱动,设计获得多种复杂运动。该研究首次建立了一系列以生物基材料组成的多功能双驱动微球,为了确保设计的生物相容性,采用美国FDA批准的生物基材料和生物催化过氧化氢酶或生物相容性Fe3O4纳米颗粒为微电机提供推进运动,最大化地实现了驱动微球的生物可相容性。鉴于这种气体辅助策略制备的自驱动微球可用于装载两种或多种不同类型的功能性纳米颗粒或酶,这为将来设计其他软质和生物相容性微马达提供了相当大的潜力,为自驱动微马达在生物医药领域的应用提供了更多的可能性。
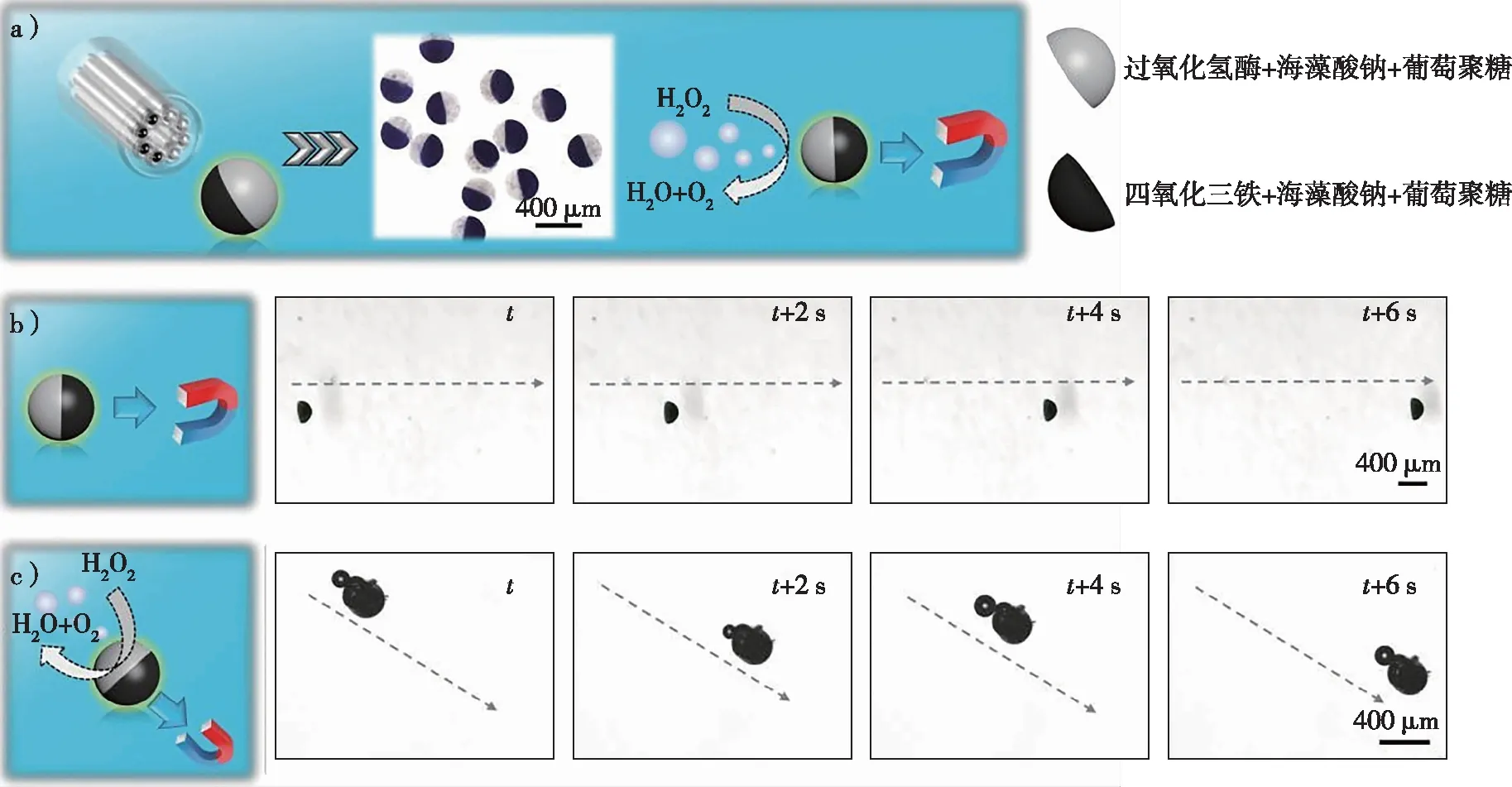
a)基于四氧化三铁纳米粒子和过氧化氢酶获得的微球制造Janus微型马达的示意图;b)磁石引导的微型马达图解和延时拍摄照片; c)微型电机浸在4%H2O2中并由磁铁引导的原理图和延时拍摄照片。图6 仿生自驱动微球[54] Fig. 6 Biomimetic self-driving microspheres
3 展 望
笔者主要综述了纤维素及其衍生物等常见天然多糖分子在药物递送、组织工程、支架材料及伤口敷料等传统生物医学领域方面的研究进展及其通过学科交叉进一步拓展的应用领域,包括在细胞共培养、药品防伪编码、病毒检测及仿生自驱动等新型应用领域的研究进展。开发具有优异结构与性能的新型生物医用材料是当今科学界研究的热点。相对于无机高分子,天然高分子材料的化学组成、分子结构和物理化学性质与生命体更为接近,因此更多地用来制备生物医用材料,也一直是当今高分子科学研究的前沿。然而,天然多糖基功能材料在生物医学领域的应用目前大部分设计还处于科学研究阶段,在临床转化前其生物安全性需要得到有效评估。为了增强天然多糖基材料的功能,使其更好地应用于生物医学跨领域,未来对天然多糖基材料的研究可以从以下方面进行思考:
1)传统的材料加工方法不可避免使用化学光引发剂、交联剂、表面活性剂,或FDA未经批准的聚合物等对生物体有毒害的物质,开发新型绿色无溶剂的材料制备方法是天然多糖基材料应用于生物医学领域的关键一步。
2)生物基材料的高值化利用是现代林业发展的重点内容,可通过学科交叉将天然多糖基材料的应用拓展到病毒检测、异向材料及人工细胞等新兴领域。

