失匹配负波在意识障碍评估中的临床价值探讨
周良,刘子源,刘劲芳
颅脑创伤、脑卒中、缺血缺氧性脑病等急性脑损伤造成的昏迷,通常有四种转归:苏醒(包括闭锁综合征)、慢性昏迷、脑死亡及慢性意识障碍(disorders of consciousness,DoC)。随着医疗技术水平的提高,昏迷患者存活率有所升高;然而,DoC的患病率仍不低,据国外文献报道,植物状态(vegetative state,VS)或无反应性觉醒综合征(unresponsive wakefulness syndrome,UWS)为(0.2~3.4)/10万,微意识状态(minimally conscious state,MCS)约为1.5/10万[1]。对这部分患者进行准确的诊断及预后评估至关重要,却又比较困难,其直接影响临床医生及患者家属的医疗决策及患者结局。目前,对急性脑损伤患者昏迷程度的评估常使用格拉斯哥昏迷量表(Glasgow coma scale,GCS)及全面无反应性量表(full outline of unresponsiveness,FOUR)评分[2]。而对于DoC的诊断,目前认为昏迷恢复量表修订版(coma recovery scale-revised,CRS-R)评分是行为学评估的金标准,其误诊率却依然高达约40%[3]。因此,DoC的诊断还需借助神经影像学、神经电生理及神经生物学标志物等相对客观的手段。
大脑活动所产生电场和磁场的变化可以从头皮上记录下来,这是神经电生理检查得以应用的基础。现有的证据表明,表面上无意识的患者中若存在前注意加工,将预示延迟的显性行为恢复。事件相关电位(event-related potentials,ERPs)中的失匹配负波(mismatch negativity,MMN)代表的就是对两种物理刺激的自动辨别及诱导注意定向,即所谓的前注意加工[4-5]。近年来,许多研究表明,MMN的存在及波幅的动态变化与DoC患者的苏醒及意识状态改变密切相关,是预测这类患者预后的重要指标。目前,对于MMN在意识障碍中的临床价值研究取得了较大的进展,但同时也存在一些困难和疑惑。为此,本文对MMN的产生机制、在意识障碍中的临床意义、判读方法及其影响因素综述如下。
1 意识及意识障碍
意识的起源自古以来被称作“整个科学领域最深奥,最令人着迷的问题之一”。意识是个多层面的概念,主要包含两个成分:觉醒和觉知。觉醒主要表现为能够自动睁眼,有正常的睡眠-觉醒周期等;觉知是指对自身及外界环境的感知。昏迷是一种无法被唤醒的完全无反应性状态,这种状态在急性脑损伤后通常持续数天或数周[2]。DoC是指意识障碍持续≥28 d,包括VS或UWS、MCS-及MCS+[6]。VS/UWS是一种无临床觉知迹象的觉醒状态,此类患者可自动睁眼,但仅表现出反射性(即非意向性的)行为,因此被认为对自己及周围环境无意识[3]。MCS患者表现出明确的皮层介导的行为迹象[7],对环境刺激的反应不稳定但可重复;尽管某些MCS患者可能会在一定程度上遵循指令,但却无法进行功能性交流[8]。觉醒的维持依赖脑干上行网状系统及其投射到的丘脑及大脑皮层神经元的功能完整,而觉知的产生依赖于皮层及皮层下环路结构的功能完整性。除此之外,中央环路(前额叶-苍白球-中央丘脑-皮质环路)中任一结构的损伤均可能导致意识障碍的发生[9]。当然,这些机制也是神经电生理检查得以应用的结构基础。
2 MMN的概念及发生机制
MMN是1978年由芬兰认知心理学家Näätänen首次提出的,是将反复出现的大概率刺激(标准刺激)及随机的小概率刺激(偏差刺激)分别叠加平均,然后再将偏差ERP成分与标准ERP成分相减得到的差异波[4]。临床上,听觉刺激是最常用的引出MMN的方式,且偏差刺激相较标准刺激可以是声音频率、强度、音长、间隔时间等的差异。MMN是在oddball范式作用下产生的位于100~250 ms之间的最大负向偏转(负波)[10]。当然,对于意识障碍患者,其潜伏期可延长至300 ms[11]。Alho等[12]利用头皮脑电图及脑磁图检查,发现MMN主要起源于听觉皮层联合区,其次是额叶,通常在额-中央区波幅最高[11]。MMN主要参与大脑对不同声音的自动辨别及诱导注意的定向,即所谓前注意加工[12]。MMN不受主动注意的影响[4],在某些意识障碍[4,11]、镇静[13]、麻醉[14]、睡眠状态中[15]也可引出;这也是MMN在意识障碍患者中得以应用的前提。目前,关于MMN的产生机制存在三种假说。
2.1 变化察觉假说 这一假说基于三种神经元及三个皮层区域(图1)。假定稳定性神经元位于初级听觉皮层,对重复的声音产生基本一致的反应,得到标准N1;而可塑性神经元位于次级听皮层,由于突触抑制作用对重复的声音产生惯化,反应逐渐降低,而对突变的声音反应强烈,这就产生了偏差N1。第三种神经元则是位于听觉皮层联合区的非线性神经元,只对刺激的变化产生反应,可同时接受来自初级和次级听觉皮层神经元的信息输入。如果刺激是新的,兴奋超过抑制,神经元就会被激活;如果刺激是重复的,抑制超过兴奋,神经元保持沉默。这样,当偏差刺激传入后,变化察觉被激活,从而产生MMN[16]。这一假说在Kropotov等[17]用立体定向脑电图分析听觉皮层对声音的辨别研究中得到了验证。
2.2 记忆痕迹假说 这一假说认为MMN是由于异常的听觉输入和代表标准刺激的感觉记忆痕迹之间的神经元失匹配造成的。声像记忆是一种注意前的听觉存储,在这种记忆中,声音细节会被完整地保留几秒钟,当一个稳定的声音被改变了音高或音质时,大脑会产生自动比较加工(失配响应);通过脑电后处理技术即可将这一响应表现出来,即MMN[5,12]。
2.3 适应性假说 该假说认为并不存在产生MMN的独立神经元,MMN的产生主要依赖于听觉标准刺激诱发的N1a及偏差刺激诱发的N1p。偏差刺激作用下的听觉皮层神经元的反应大于对标准刺激产生了适应性的神经元,因此,用处理技术将两者的波形相减,MMN便可视化了[18]。
假说一与假说二相似相通,而此两者与假说三的矛盾之处在于是否存在独立的神经元产生MMN。至今为止,大多数学者还是支持前两种假说[5,12,14]。
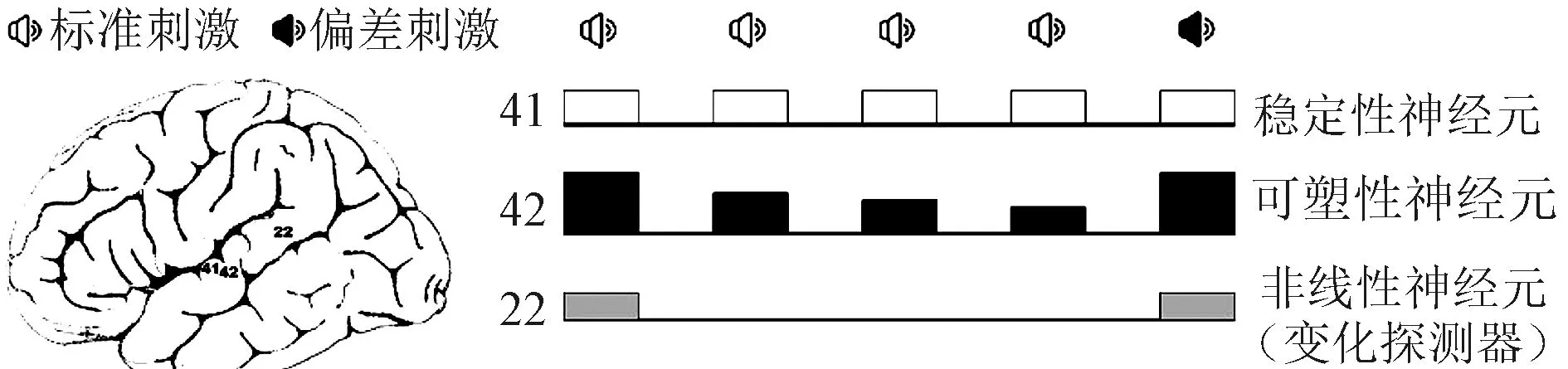
41:初级听觉皮层区,42:次级听觉皮层区,22:听觉皮层联合区
3 MMN在意识障碍评估中的临床意义
3.1 MMN与急性脑损伤昏迷 昏迷是一种严重的意识障碍,是导致死亡和残疾的主要原因。然而,由于部分昏迷患者无法对外界刺激作出反应,影响临床医生对患者残存神经功能及环境感知能力的评估,如认知-运动分离[20]。这样,床旁ERPs就显得尤为重要了,而MMN就是其中重要组成成分之一。
两种纯音oddball范式刺激下引出的MMN预测各种原因导致昏迷患者(GCS评分≤8分)意识恢复的特异度达90%~100%,而灵敏度为31.6%~90%[21-23],这两种纯音间的差异为频率或刺激持续时间上的不同。MMN的存在提示患者听觉传导通路的相对完整及额-颞叶部分神经元功能连接的保留。而造成各研究灵敏度差异大的原因可能主要是刺激范式的差异,以及目前没有严格定义MMN存在与否,使研究者在结果判读方面有较大个体差异。昏迷患者的MMN波幅(0.36~2.77 μV)明显低于健康对照(0.87~5.16 μV)[21],这提示MMN的波幅与意识水平相关,只是个体差异较大,这也是目前MMN波幅的量化分析没有得到推广的原因之一。Tzovara等[22]对缺血缺氧后昏迷患者采用交叉设计方法检测MMN引出情况,发现预测意识恢复的准确性为78%,这种交叉设计方式避免了因刺激物之间的物理差异而产生的早期差异。另外也有学者将自编的相对复杂音作为偏差刺激,纯音作为标准刺激引出MMN,其阳性检出率较纯音更高,且得到的MMN波幅普遍高于纯音,与昏迷患者预后呈现明显相关性[24],提高了检测的灵敏度。目前,多数基于听觉系统的神经生理学研究使用的都是正弦波音调,而实际上其在自然界中从未出现过。在听觉系统的高级中枢,如皮层,只有当声音刺激具有自然和生物属性时,才更有可能以功能上有意义的方式激活大量神经元群。
当然,也有少数学者认为MMN不太可能成为检测患者意识的临床工具,其认为MMN对不同病因昏迷的预测价值可能不同[25]。需要注意的是,由于在脑损伤急性期,患者病情变化快,因此,重复多次的动态MMN监测是必要的。另外,考虑到ICU嘈杂的环境,相比频繁出现的声音刺激,罕见的刺激也许会与伪差更为相关,这种差异不仅代表了皮层信号的差异,同时也可能代表与背景噪声的差异,因此MMN的获得需要合适的刺激时间及优化的后期自动处理程序。
3.2 MMN与慢性意识障碍 自上而下的额-颞叶皮层投射的损伤是VS患者的显著特征。虽说这类患者可存在自下而上的前反馈,但长潜伏期诱发电位及事件相关电位是自上而下的后反馈来调节的,这为利用MMN研究DoC,区分VS和MCS及清醒状态提供了可能[26]。与急性脑损伤昏迷不同的是,DoC患者一般病情较为稳定,且一般未使用镇静、镇痛药物,因此在检测MMN那段时间内,影响因素相对较少,从而越来越多学者以这部分人群作为研究对象,认为MMN是评估患者意识状态及预后的可靠指标。
哈佛医学院的Wijnen等[27]对10例VS患者进行为期3.5个月的随访,每两周进行一次MMN测试。结果显示,随着患者意识状态的改善,MMN波幅会有较为明显的上升,且一般早于患者与外界环境产生交流。除此之外,患者第一次检查时MMN的潜伏期和波幅可用于预测VS患者意识恢复的可能性。这种纵向观察的方法可以消除个体差异带来的MMN异质性,值得积极借鉴。随着神经调控技术的发展,有学者研究发现高分辨率经颅直流电刺激治疗Doc患者后第1、7、14 d,其CRS-R评分及MMN波幅较治疗前基线值依次增高,因此MMN有望成为评估DoC患者治疗效果的可靠指标[28]。将呼唤患者姓名、罕见纯音分别当偏差刺激,出现频繁的纯音作为标准刺激,对DoC患者进行测试,同时以健康者作为对照,发现意识障碍人群中也可观察到类似正常人的MMN模式,且相比纯音作为偏差刺激,唤名这一偏差刺激可引出潜伏期更短、波幅更高的MMN[29]。无论是在正常对照者还是DoC患者中,当被叫到自己名字时,人类大脑皮层自动获取并注意这一听觉信息的灵敏度会提高,且在200~400 ms时引起相应的脑功能连接相对最强[30]。研究发现,在DoC患者中,MMN波幅绝对值与CRS-R评分呈显著正相关,且偏差刺激与标准刺激的频率差越大,MMN波幅越高,与CRS-R评分的相关性也越显著,而这种差异性主要分布于额-中央区[11]。这体现了MMN分布的空间特性,同时也强调了规范MMN刺激范式的重要性。2018年版慢性意识障碍的神经调控外科治疗中国专家共识[31]将MMN列入意识障碍临床评估手段,并对应不同的意识状态,给出了MMN波幅参考值:≤0.5 μV为昏迷,0.5~1.0 μV为VS,1.0~1.7 μV为MCS-,1.7~2.0 μV为MCS+。这是目前唯一的以MMN波幅参考范围定义不同意识状态的文献,且无疑是未来研究的一个方向和目标,因为这有利于临床实践中的个体评估。
4 MMN与镇痛镇静
虽然镇痛、镇静药物和病情本身对MMN均有影响,且难以区分,但由于病情需要,ABI昏迷患者常需用到镇静、镇痛药物。因此目前关于急性脑损伤昏迷与MMN相关性的研究大多数都有镇静、镇痛药物介入,包括近期在新英格兰医学杂志上报道的利用机器学习方法探测ABI患者中认知-运动分离情况的研究[20]。当然,也有研究只纳入未使用镇痛、镇静药物或停用满24 h的患者,但似乎不太符合真实世界临床试验的理念,因为这无形中就排除了许多需要使用镇痛镇静药物的重症患者,而这部分患者往往病情更重。
Azabou等[13]对ICU持续机械通气或恶性颅高压需要使用强镇静患者,使用丙泊酚或/和咪达唑仑联合/不联合舒芬太尼,使其RASS评分<-3分,发现这部分患者MMN仍存在,只是整体潜伏期延长且波幅下降;提示在深度(但不完全)镇静/麻醉期间,一些前注意加工和自下而上的自动注意定向功能被保留下来[14],而在意识丧失时消失。与丙泊酚、咪达唑仑(γ-氨基丁酸受体激动剂)作用机制不同,右美托咪定属于选择性α2肾上腺素受体激动剂,作用于蓝斑核而负反馈抑制去甲肾上腺素释放,从而抑制前额叶皮层。右美托咪定诱发的脑电纺锤或慢波震荡均小于丙泊酚,这可能反映了右美托咪定对神经元活动的干扰程度低于丙泊酚[32-33],同时也说明了为何右美托咪定诱导的镇静可被唤醒,而丙泊酚不行[34];由此推测其对MMN的引出及形态可能有影响,但影响不如丙泊酚类药物那么大。
另外,一研究发现在镇痛药物瑞芬太尼1.0 ng/mL效应部位浓度静脉泵入作用下,健康受试者听觉MMN波幅增加,特别是在女性受试者中;考虑这与疼痛处理相关的μ型阿片类受体区域(包含颞叶及额叶等)的血氧水平依赖反应和局部脑血流量增加有关[35]。当然,无论是镇痛还是镇静药物,对MMN相关指标的影响大多是剂量依赖性的。
5 MMN的判读与分析
人类大脑对声音改变的察觉或探测所引出的MMN成分发生源主要位于颞叶听皮层,而随后出现的额叶MMN亚成分则与诱导注意定向或自动注意转移相关[36]。由于颞区听皮层会不同程度地受到来自外界环境声音的影响;与之相比较,额区MMN成分显得更为稳定,且波幅总体更高。因此,目前临床上主要参考Fz处(脑电图国际10-20系统,额中线)MMN的引出情况来评估意识障碍严重程度及预测苏醒预后。当然,也有学者提出对这部分患者MMN的分析还应在颞叶,而健康者才应在额-中央区[29]。因此,进行意识障碍相关研究时,最好在双侧额-中央、颞区同时记录,以减少额颞区连接受损及MMN空间分布特性差异所造成的漏诊[11]。
回顾众多的国内外研究,大多数的分析重点在于MMN是否引出,而未明确何为MMN引出,且未将MMN的波形特征(如潜伏期、波幅等)进行量化。所以目前对于MMN的判读还是以目测波形的分化情况为主,掺杂了研究者的主观因素,导致各判读者间的个体差异较大,从而影响数据质量和试验结果。因此,这个问题需要被解决。有学者将MMN严格规定为潜伏期150~250 ms[23],甚至是250~269 ms间的最大负波[13]。另外,考虑到N1为听觉门控系统的代表指标之一[37],因此MMN引出的前提是标准及偏离N1[23]甚至是P2引出[28],且消除噪音后,N1波幅须大于0.1~0.5 mV[37]。还有研究记录包括Fz、Cz(脑电图国际10-20系统,中央中线)在内的9个电极,使用方差分析各区域在150~250 ms的平均波幅,且各区域的条件效应存在统计学差异即认为MMN引出[24]。更有研究将记录到的波形由5位经验丰富的神经生理学家进行互盲的个体视觉分析,而后利用Fleiss’kappa分数行组间分析得出有意义的MMN[13]。后两种事后分析的方法较为精准、严格地定义了MMN是否存在,提高了意识障碍患者苏醒预测的特异性。但是,作为临床神经功能检查工具,这些分析方法显得过于繁琐、复杂了。因此,近期有研究以健康被试者作为基线对照,利用机器学习自动识别MMN,欲达到快速准确评估的目的[38]。虽然此系统暂时还缺乏大量昏迷患者进行测试,但确实提供了一个新的可行性思路。
6 结 语
ERPs是对严重意识障碍患者残存认知功能有效的评估方法,在自动听觉辨别及诱导注意定向方面,MMN范式的有效性较高,因为多数存在MMN反应的患者预后较好。但由于MMN的产生机制未明确、刺激范式及后期处理方法未统一、波形判读和分析方法需要进一步研究等原因,以往的研究在质量和结果方面存在较大差异。因此,在今后的临床试验或实践中,应该从以下几个方面严格规范和创新:首先,要尽可能减少仪器设备的电磁干扰以及周围环境噪音干扰,以获得可靠的数据,这是前提。其次,必须要平衡刺激时间过短导致的信噪比低与刺激时间过长导致的产生干扰可能性增高之间的利弊,寻找合适的刺激时间。此外,尽管有ERPs相关的专家共识、建议可供参考[23],但仍需要探索更优化、更适用于临床的听觉刺激范式、后期自动处理程序及MMN的计算分析方法,才能更快速准确地得出更符合实际的结果。当然,这需要大样本多中心研究,且需要进行分类,如病因分类、急、慢性意识障碍分类及使用镇静、镇痛药物情况分类等,最终将MMN相关值量化分层,为临床实践提供便利。实际上,结合临床表现、神经影像及包括MMN在内的神经电生理检查,利用机器学习的方法,综合评估意识障碍患者脑功能,个体化预测预后,才真正符合精准化医疗的理念。

