特发性矮小症和生长激素缺乏症应用重组人生长激素的临床效果观察
蒋苇苇 高莉莉 陈风展


【摘要】 目的:觀察与分析特发性矮小症和生长激素缺乏症应用重组人生长激素的临床效果。方法:选取2016年3月-2018年3月本院收治的80例特发性矮小症和生长激素缺乏症患者为研究对象。将其随机分为对照组(常规治疗干预组)和观察组(常规治疗加重组人生长激素组),每组40例。比较两组治疗前后身高、身高SDS、生长速率、血清生长因子及骨代谢相关指标,观察两组不良反应发生情况。结果:治疗前,两组的身高、身高SDS、生长速率、血清生长因子、血清骨代谢相关指标比较,差异均无统计学意义(P>0.05)。治疗3、6、12个月后,观察组身高、身高SDS、生长速率、血清生长因子、血清骨代谢相关指标均显著优于对照组,差异均有统计学意义(P<0.05)。两组不良反应发生率比较,差异无统计学意义(P>0.05)。结论:特发性矮小症和生长激素缺乏症应用重组人生长激素的临床效果较好,安全性值得肯定,因此在特发性矮小症和生长激素缺乏症患者中的应用价值较高。
【关键词】 特发性矮小症 生长激素缺乏症 重组人生长激素
Clinical Effect of Recombinant Human Growth Hormone in Patients with Idiopathic Short Stature and Growth Hormone Deficiency/JIANG Weiwei, GAO Lili, CHEN Fengzhan. //Medical Innovation of China, 2021, 18(01): -117
[Abstract] Objective: To observe and analyze the clinical effect of Recombinant Human Growth Hormone in the patients with idiopathic short stature and growth hormone deficiency. Method: A total of 80 patients with idiopathic short stature and growth hormone deficiency admitted to our hospital from March 2016 to March 2018 were selected as the research objects. They were randomly divided into control group (routine treatment intervention group) and observation group (routine treatment plus Recombinant Human Growth Hormone group), 40 cases in each group. Height, height SDS, growth rate, serum growth factor and bone metabolism were compared between two groups before and after treatment, the occurrence of adverse reactions in the two groups was observed. Result: Before treatment, there were no statistically significant differences in height, height SDS, growth rate, serum growth factor and serum bone metabolism between two groups (P>0.05). At 3, 6 and 12 months after treatment, the height, height SDS, growth rate, serum growth factor and serum bone metabolism related indexes of the observation group were all significantly better than those of the control group, with statistically significant differences (P<0.05). There was no statistically significant difference in the incidence of adverse reactions between two groups (P>0.05). Conclusion: The clinical effect of Recombinant Human Growth Hormone on idiopathic short stature and growth hormone deficiency is good, and its safety is worthy of affirmation. Therefore, it has high application value in patients with idiopathic short stature and growth hormone deficiency.
[Key words] Idiopathic short stature Growth hormone deficiency Recombinant Human Growth Hormone
First-authors address: Taizhou Second Peoples Hospital, Taizhou 225500, China
doi:10.3969/j.issn.1674-4985.2021.01.029
矮小症在临床并不乏见,其包括多种类型,其中特发性矮小症和生长激素缺乏症是较为常见的类型,严重影响到患儿的生存质量,也是家长及患儿亟待治疗与改善的方面[1]。上述两类情况均与生长激素的缺乏及敏感性降低等因素有关,因此对其采用相关方面的补充与治疗是临床研究的重点与热点[2]。本研究就特发性矮小症和生长激素缺乏症应用重组人生长激素的临床效果进行全面细致的观察与探究,以了解重组人生长激素在上述患儿中的综合应用价值,现报道如下。
1 资料与方法
1.1 一般资料 选取2016年3月-2018年3月本院收治的80例特发性矮小症和生长激素缺乏症患者为研究对象。纳入标准:3~16岁;男女不限。排除标准:合并其他代谢性疾病;合并骨科疾病;骨折史;已经进行过相关治疗;合并慢性基础疾病;存在药物禁忌证。将其随机分为对照组(常规治疗干预组)和观察组(常规治疗加重组人生长激素组),每组40例。患儿和/或家属知情同意,本研究经医院伦理学委员会批准。
1.2 方法
1.2.1 治疗方法 對照组的患儿进行常规治疗干预,主要为进行饮食营养、钙剂补充等方面的治疗。观察组则在常规治疗基础上加重组人生长激素[生产厂家:安徽安科生物工程(集团)股份有限公司,批准文号:国药准字S19990022,规格:2 IU/0.67 mg/支],采用0.1 IU/(kg·d)的剂量进行应用,1次/d,睡前皮下注射。两组均连续干预12个月。
1.2.2 检测指标及方法 于治疗前及治疗3、6、12个月后分别检测两组身高、身高SDS、生长速率、血清生长因子及骨代谢相关指标。分别于上述时间采集两组空腹静脉血,将血标本进行离心,离心后取血清进行生长因子及骨代谢相关指标的检测,生长因子包括IGF-1及IGFBP-3,骨代谢相关指标为ICTP、CTX及AKP,上述方面均采用酶联免疫法试剂盒进行定量检测,并均由两名经验丰富者进行操作检测。
1.3 观察指标 记录并比较两组治疗前后身高、身高SDS、生长速率、血清生长因子及骨代谢相关指标、不良反应发生情况。
1.4 统计学处理 采用SPSS 23.0软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 对照组中男27例,女13例;年龄3~15岁,平均(9.9±2.6)岁;BMI值15~20 kg/m2,平均(17.1±1.3)kg/m2;其中特发性矮小症31例,生长激素缺乏症9例。观察组中男25例,女15例;年龄3~15岁,平均(9.8±2.5)岁;BMI值15~19 kg/m2,平均(17.0±1.2)kg/m2;其中特发性矮小症30例,生长激素缺乏症10例。两组患儿的上述一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
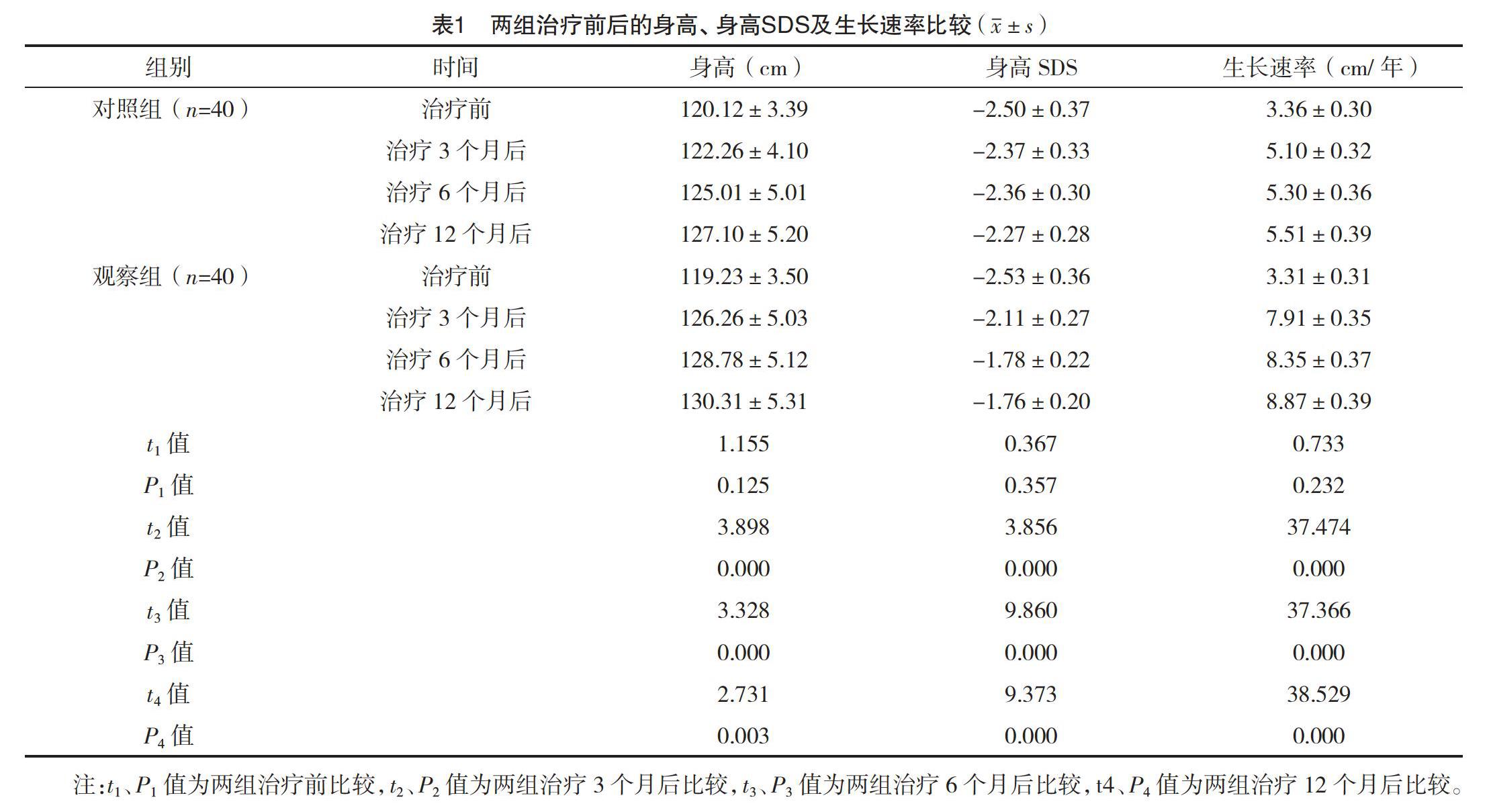
2.2 两组治疗前后身高、身高SDS及生长速率比
较 治疗前,两组身高、身高SDS及生长速率比较,差异均无统计学意义(P>0.05);治疗3、6、12个月后,观察组身高、身高SDS及生长速率均显著优于对照组,差异均有统计学意义(P<0.05)。见表1。
2.3 两组治疗前后血清骨代谢相关指标比较 治疗前,两组血清骨代谢相关指标比较,差异均无统计学意义(P>0.05);治疗3、6、12个月后,观察组血清骨代谢相关指标均显著优于对照组,差异均有统计学意义(P<0.05)。见表2。
2.4 两组治疗前后血清生长因子比较 治疗前,两组血清生长因子比较,差异均无统计学意义(P>0.05);治疗3、6、12个月后,观察组血清生长因子均显著优于对照组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组不良反应发生情况比较 两组不良反应发生率比较,差异无统计学意义(字2=0.346,P=0.556),见表4。
3 讨论
特发性矮小症和生长激素缺乏症患儿的不良影响及对患儿、家长造成的心理负担突出,且其日益受到各界认知。因此特发性矮小症和生长激素缺乏症的临床就诊率持续升高,与之相关的诊治研究也持续增多[3-5]。研究显示,本类患儿普遍表现出IGF-1及IGFBP-3等生长因子的异常表达,而较低的IGF-1表达水平可导致骨代谢较慢,同时是与生长密切相关的方面[6-7],而IGFBP-3则对IGF-1作用的发挥起到促进作用,因此对其表达水平的调控与监测意义较高。另外,ICTP、CTX及AKP等骨代谢指标在特发性矮小症和生长激素缺乏症患儿中呈现较低的表达状态[8-10],也在一定程度上对患儿的生长状态起到较高的反应意义,是临床亟待改善的方面。临床中用于上述患儿治疗的研究众多,其中重组人生长激素的应用效果受肯定程度较高[11-13],但是与此同时,本方面研究结果的差异也普遍存在,且全面性研究不足。
本研究就特发性矮小症和生长激素缺乏症应用重组人生长激素的临床效果进行观察与分析,结果显示,重组人生长激素治疗的效果相对于未应用者更为突出,表现为重组人生长激素治疗3、6、12个月后身高、身高SDS、生长速率、血清生长因子及骨代谢相关指标均相对更好,且未见不良反应发生率明显升高的情况,因此较为全面地肯定了重组人生长激素的应用价值。分析原因,笔者认为可能与重组人生长激素对骨骺端软骨细胞分化、增殖等具有较好的促进作用[14-16]。因此在促进软骨基质细胞增长护成骨细胞分化、增殖方面效果较好[17-18],同时对于骨代谢的调节作用也较好,而这也是上述患儿生长发育的重要基础[19-21]。
综上所述,特发性矮小症和生长激素缺乏症应用重组人生長激素的临床效果较好,安全性值得肯定,因此在特发性矮小症和生长激素缺乏症患者中的应用价值较高。
参考文献
[1]夏雅,潘秋飞,吴安乐,等.重组人生长激素治疗特发性矮身材儿童对骨代谢指标的影响[J].中国妇幼健康研究,2020,31(1):30-34.
[2]翟磊.重组人生长激素联合强化营养指导、体育锻炼治疗特发性矮小症患儿的疗效分析[J].首都食品与医药,2020,27(15):68.
[3]刘小庆,赵瑛,于鸿悦,等.重组人生长激素治疗特发性矮小症儿童的疗效观察及对胰岛素样生长因子的影响[J].中国保健营养,2020,30(18):235.
[4]宋婷婷,马慧娟.生长激素缺乏症及替代治疗与骨代谢研究进展[J/OL].世界最新医学信息文摘(连续型电子期刊),2020,20(68):111-112.
[5]赵起仙,关玉云,关则想,等.重组人生长激素结合心理干预对生长激素缺乏症患儿效果的影响[J].海峡药学,2020,32(8):173-174.
[6]杨志敏,鞠海超.重组人生长激素对特发性矮小症患儿身高及血清胰岛素样生长因子1的影响[J].中国基层医药,2020,27(19):2334-2338.
[7] Díez Juan J,Susana S A,Fernando C.Treatment with Growth Hormone for Adults with Growth Hormone Deficiency Syndrome: Benefits and Risks[J].Int J Mol Sci,2018,19(3):893.
[8]田志刚.rhGH治疗儿童生长激素缺乏症和特发性矮身材的疗效观察[J].中国实用医刊,2020,47(13):87-90.
[9] Alzahrani A K,Algethami A K,Barnawi G M,et al.Differences in Response to Recombinant Growth Hormone Therapy on Height Gain in Patients with Idiopathic Short Stature Vs. Patients with Growth Hormone Deficiency[J].Cureus,2020,12(3):7319.
[10]殷威,曹兰芳,朱铭强.rhGH对生长激素缺乏症儿童IGF-1、IGFBP3水平及骨代谢状况的影响[J].中国妇幼保健,2020,35(2):281-283.
[11]高静,刘晓景,陈永兴,等.重组人生长激素治疗生长激素缺乏症的疗效观察及对患儿肾上腺皮质功能的影响分析[J].首都食品与医药,2020,27(16):52-53.
[12]郭艳艳,蒋成霞,姚兰,等.不同剂量重组人生长激素治疗对特发性矮小症患儿身高、体重以及血清IGF-1和IGFBP-3表达的影响[J].解放军医药杂志,2020,32(3):44-47.
[13]王秋兰.重组人生长激素对儿童生长激素缺乏症和特发性矮小症的效果评价[J].中国实用医药,2020,15(7):167-169.
[14]王伟,肖雅,罗向阳,等.高迁移率蛋白A2基因多态性与青春期前特发性矮小患儿及重组人生长激素疗效的相关性研究[J].中华实用儿科临床杂志,2020,35(17):1351-1353.
[15]谭迪.重组人生长激素治疗特发性矮小症对患儿IGF-1水平及体质指数的影响[J].黑龙江中医药,2020,49(1):77.
[16] Chung W Y,Yoo H W,Hwang J S,et al.Effect of Growth Hormone Therapy on Height Velocity in Korean Children with Idiopathic Short Stature: A Phase Ⅲ Randomised Controlled Trial[J].Horm Res Paediatr,2018,90(1):44-53.
[17]林秀雯,彭树勋,刘玲.维生素D辅助重组人生长激素治疗儿童生长激素缺乏症对儿童生长及骨代谢的影响[J].新医学,2020,51(6):473-477.
[18] Hwang J S,Lee H S,Lee K H,et al.Once-Weekly Administration of Sustained-Release Growth Hormone in Korean Prepubertal Children with Idiopathic Short Stature: A Randomized, Controlled Phase Ⅱ Study[J].Horm Res Paediatr,2018,90(1):54-63.
[19]舒静娜,祁建凤.重组人生长激素对特发性矮小症患儿胰岛素样生长因子-1、胰岛素样生长因子结合蛋白-3的影响[J].中国妇幼保健,2020,35(3):486-488.
[20]王慧,庄昭明.重组人生长激素联合芳香化酶抑制剂治疗特发性矮小症的效果及安全性[J].中外医学研究,2020,18(8):32-34.
(收稿日期:2020-11-18) (本文编辑:姬思雨)

