抗amphiphysin抗体相关自身免疫性癫痫1例报告
胡小林,王安素,梁涛,罗忠
癫痫发作是神经科常见的临床症状,是由中枢神经系统过度、同步化异常放电引起的症状,见于多种疾病的发病过程中,如脑炎、脑血管病和颅脑肿瘤等。在美国,每年约有1.5万成年人出现无明显诱发因素的首次癫痫发作[1]。对于成年人癫痫发作,最重要的是尽可能寻找引起癫痫发作的病因,而引起癫痫发作的病因很多,越来越多的证据表明自身免疫机制也参与了癫痫的发生,因此,有学者将一系列自身抗体介导的癫痫命名为自身免疫性癫痫(autoimmune epilepsy,AE),认为AE是自身免疫性脑炎的一种类型[2],但后来的学者认为自身免疫性脑炎的癫痫样发作不等同于AE[3],AE与自身免疫性脑炎是两组独立的疾病实体[3-4],2017年国际抗癫痫联盟发布的最新癫痫分类将癫痫病因划分为6大类,正式将“免疫性”作为癫痫的病因之一[4]。广义上说,AE包括所有自身抗体及免疫反应所致的癫痫,如桥本脑病、狼疮脑病、抗心磷脂抗体等内科疾病所致的癫痫,也包括部分与免疫相关的特殊癫痫,如婴儿痉挛症、抗谷氨酸受体抗体脑炎等。狭义上说,AE仅指在发病机制上全部或主要有针对神经胞膜、突触或者胞质成分的抗原抗体反应所致的癫痫[5]。因此,AE是癫痫在病因学层次的诊断。本文报道1例抗突触囊泡蛋白(amphiphysin)抗体相关AE,并进行文献复习,以期加强大家对该病的认识。
1 病例报告
患者郑某某,男性,26岁。因“发作性意识丧失,伴头痛5 d”就诊。病前有上呼吸道感染史,5 d前于上班时突发意识丧失,呼之不应,当时伴随症状不详,约持续数分钟后神志转清,后感头痛,双侧颞部持续性搏动样疼痛。就诊于当地医院后头痛缓解不明显,遂就诊于我科。既往无类似发作史,无头部外伤、脑炎病史,无家族史。入院查体:生命体征平稳,内科系统查体颈强四横指,余神经系统无阳性体征。入院查血常规示白细胞总数12.85×109/L,中性粒细胞绝对值 10.79×109/L,肝肾功能、电解质等无明显异常。行腰椎穿刺示压力210 mmH2O,脑脊液白细胞 68×106/L,蛋白含量630 mg/L(表1)。脑脊液真菌、抗酸杆菌阴性。脑脊液TB-GeneXpert阴性。血抗核抗体谱、ANCA抗体等风湿免疫指标均阴性。长程视频动态脑电图提示右侧半球背景减低,局限性慢波活动(图1)。头颅MRI未见明显异常。根据患者病史、体征及辅助检查,临床诊断为病毒性脑膜脑炎,予以阿昔洛韦0.25 g iv q 8 h抗病毒、甘露醇25 g iv q 12 h脱水降颅压、丙戊酸钠缓释片500 mg 口服2次/d控制癫痫发作,经治疗14 d后头痛缓解,未再次出现癫痫发作,医嘱出院。出院后规律服用丙戊酸500 mg 2次/d,门诊规律随诊,未出现癫痫发作。6个月后患者无明显诱因出现右手不自主抽动,每次持续数分钟不等,不伴有意识丧失、肢体抽搐、二便失禁,每天发作约5~10次,未重视,逐渐加重出现发作性右手及面部、颈部不自主抽动,无意识丧失,无牙关紧闭、尿便障碍,每次发作约数分钟后自行缓解,每天发作10次左右,故再次就诊于我科。入院查体:神志清楚,神经系统无阳性体征。完善血常规、肝肾功无异常、抗核抗体谱、类风湿因子等指标均阴性,长程视频动态脑电图未见异常。再次行腰椎穿刺压力125 mmH2O,白细胞15×106/L,脑脊液蛋白含量405 mg/L。头颅MRI增强示左顶叶异常信号灶(图2)。鉴于其反复出现癫痫发作,且既往有颅内感染病史,需警惕自身免疫性脑炎可能,故外送血清、脑脊液查自免脑相关抗体谱,结果提示血清抗amphiphysin阳性,脑脊液阴性(图3)。完善胸部CT、腹部彩超、肿瘤相关抗原标记物等检查筛查肿瘤,未发现肿瘤征象。给予泼尼松50 mg口服1次/d,奥卡西平0.3 g口服2次/d等治疗后患者癫痫发作控制良好出院,出院后逐渐停用激素。出院后随访半年无癫痫发作。

图1 本文患者第1次入院时脑电图。提示右侧半球可见持续性2.5~4 Hz中波幅的δ波活动,右侧背景活动波幅较左侧明显减低。
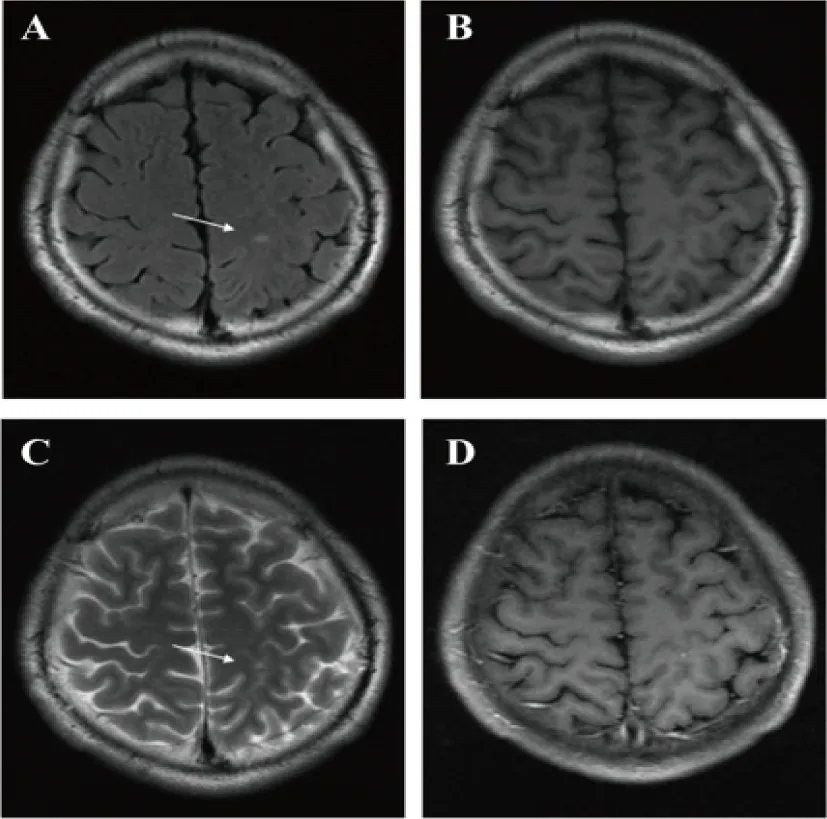
图2 本文患者第2次入院时头颅MRI。提示左顶叶斑片、斑点状T2WI信号,FLAIR呈高信号,增强扫描未见明确强化(A:T2 FLAIR像;B:T1像;C:T2像;D:增强扫描)。

图3 免疫斑点法检测血清抗amphiphysin抗体阳性(免疫斑点法,箭头所示)

表1 本文患者两次住院脑脊液检查结果比较
2 讨论
近年来,得益于细胞转染、免疫斑点等试验技术的进步和发展,一系列抗神经元细胞表面或者细胞内的自身抗体陆续被发现,AE与自身免疫性脑炎均是近年来随着神经免疫学发展而提出的临床新概念。对于伴有癫痫样发作、抗神经元抗体阳性的患者,诊断为自身免疫性脑炎还是AE,往往困扰着神经内科医师,由于其存在共同的抗神经元抗体,且自身免疫性脑炎常有癫痫发作,临床极易误诊[6]。AE的临床特征有:①癫痫反复发作;②血清和(或)脑脊液检出神经元抗体;③脑脊液和(或)头颅MRI出现炎性改变[7]。也就是说,癫痫的发生直接源于自身免疫功能障碍所致的脑部炎性病理改变,且癫痫发作为其唯一或核心的临床表现[3],虽然癫痫发作可以是自身免疫性脑炎常见的临床症状,但其往往伴有认知功能损害以及其他中枢神经损害的临床表现,与AE有一定重叠之处,但又不完全等同,而以癫痫为突出临床表现或仅有癫痫发作、病程相对较长、抗癫痫药物控制不佳,特别是“脑炎”后出现的患者,可考虑为AE。该患者符合以上特征,虽然未进行脑脊液病毒相关检查,脑电图均未发现棘波、尖波等异常波形,考虑可能是患者磁共振病灶较小,且检查期间未出现临床发作,但患者以癫痫发作为主要临床症状,未合并其他认知功能减退及精神行为异常,头颅未见典型病毒感染病灶,且血清抗amphiphysin抗体阳性,故临床诊断AE可能性大。根据现有文献报道,癫痫患者中有10%可归类为AE,但AE的患病率尚不清楚[8]。有学者认为,神经元特异性细胞内或细胞膜抗体可通过不同途径介导癫痫发作。胞内抗体主要通过细胞毒性T细胞导致神经元死亡,进而引起神经功能损害。而胞膜抗体主要与B细胞免疫反应有关,部分可伴发肿瘤,其主要通过影响兴奋性或抑制性神经递质合成及其作用而致病[9]。李乐超等[10]认为分子模拟与交叉反应性自身抗体可能参与了发病过程,其提出外源性病原体入侵或某些恶性肿瘤产生异己抗原产生内源性物质与自身中枢神经系统 (CNS) 某些组分相似,机体免疫系统发生错误的识别,通过一系列炎症反应或神经递质的产生,导致癫痫发作,具体到本报道中,该患者第一次入院有呼吸道感染史,以头痛、癫痫发作为主要临床症状,查体颈强四指,入院后查脑脊液白细胞、蛋白稍高,头颅未见明显异常,脑电图提示异常,予以抗病毒、抗癫痫治疗好转,故临床诊断病毒性脑膜脑炎。但患者6个月后再次出现癫痫发作,入院后再次查脑脊液提示白细胞高,不同于上次,患者头颅MRI提示左顶叶异常信号灶,进一步查抗神经元相关抗体提示血清amphiphysin阳性,故临床诊断AE。amphiphysin,即两性蛋白,是位于神经元胞质内突触抗原,其主要生理功能是协同神经突触中dynamin蛋白完成神经末梢突触小泡的内吞作用。1993年,Folli等人首次报道了3例乳腺癌患者合并僵人综合征的临床表现,其中2例患者的脑脊液中检测出IgG寡克隆带[11],最后被证实为amphiphysin。随着时间的延长及检测技术的发展,越来越多的抗amphiphysin抗体脑病被发现,其临床表现多表现为僵人综合征、舞蹈病、认知功能下降、脑干脑炎和精神症状等,在这些抗体阳性患者中,多数患者单纯为血或脑脊液抗amphiphysin抗体阳性,同时为阳性者少见[12-13]。目前发现多种神经抗体与AE相关,如NMDAR、AMPAR、GLBAbR、LGI1和CASPR2等[11]。AE患者脑电图表现各异,部分患者可表现为正常脑电图,部分患者可出现痫样放电,如弥漫性或局灶性尖波、棘波,也可表现为节律性慢波[14]。目前对AE被广泛接受的治疗方式包括免疫治疗和抗癫痫治疗,免疫治疗包括激素、IVIG、血浆置换及免疫抑制剂等,合并肿瘤患者还必须抗肿瘤治疗,总体预后良好,但合并恶性肿瘤者效果较差[15]。目前,越来越多的学者开始关注AE,但其发病机制尚未完全阐明,因此,需要更多的基础及临床研究来了解自身免疫与癫痫发病的关系并指导治疗。

