2020 中国动态血压监测指南
中国高血压联盟《动态血压监测指南》委员会
高血压是心脑血管疾病的重要危险因素,与心脑血管疾病的发病及死亡密切相关[1-3]。随着我国人口老龄化及城镇化进程的加速,我国的高血压患病率也呈逐年上升趋势。2012 年至2015 年的全国高血压抽样调查显示,我国18 岁以上成人的高血压(≥140/90 mm Hg)患病粗率约为27.9%,即全国约有2.45 亿例高血压患者[4],与2002 年第四次全国营养与健康调查相比,高血压患病率显著升高[5],提示我国高血压及其相关心脑血管疾病负担日益加重,已成为重大的公共卫生问题。与欧美人群相比,我国人群中高血压导致的脑卒中患者更为多见[6],故对个体进行全面、准确的血压评估,从而制定适合我国人群的高血压诊疗策略非常重要。
近期发表的多部国内外高血压指南[7-9],包括《中国高血压防治指南2018 年修订版》[10],均强调了诊室外血压的监测(包括动态血压监测及家庭血压监测)在高血压诊治中的重要性。动态血压监测可以评估个体在日常生活状态下的血压,排除白大衣效应;同时,可测量其全天的血压水平,包括清晨、睡眠过程中的血压,以便发现隐蔽性高血压。相较于诊室血压测量,动态血压监测能够更准确地预测个体的心脑血管事件发生风险及死亡风险[3]。事实上,我国人群在诊室外血压升高很常见,存在如清晨高血压、夜间高血压、夜间血压下降不足等多种病理状态。不仅如此,动态血压监测还可以评估个体在不同环境、体位及情绪状态下的血压变化趋势及短时血压变异情况[11]。因此,动态血压监测已成为诊断高血压、评估心脑血管疾病风险、评估降压治疗疗效、指导个体化降压治疗不可或缺的手段[8-10]。
迄今为止,已经有许多国家及区域的学术组织专门制定了动态血压监测指南或共识[11-12]。2015 年,中国高血压联盟组织全国专家撰写并发布了《动态血压监测临床应用中国专家共识》[13]。2018 年,HOPE Asia Network 发表了规范动态血压监测的亚洲地区文件[12,14]。在既往的中国血压监测学术会议上,学者们也对动态血压监测的相关研究证据进行了深入讨论,希望在已有共识的基础上,制定一项“中国动态血压监测指南”,以期协助指导临床实践,提升我国的血压监测质量,优化高血压管理,降低人群的心脑血管事件发生风险,减轻我国的心脑血管疾病负担。
动态血压计的选择和使用
为获得准确、可信的动态血压监测结果,需要选择正确的动态血压计,遵从规范的动态血压监测方案(见表1),根据标准化的血压指标和判别标准,对动态血压监测结果进行专业判断。
一、动态血压计的选择
推荐按照国际标准验证方案,选择经独立临床验证、准确性达到要求的动态血压计。标准的验证方案包括美国医疗仪器发展协会、英国高血压学会、欧洲高血压学会血压监测工作组及国际标准化组织等制定的验证方案,以上各验证方案的标准大致相似,仅在评估的方法学上略有差异。2018 年,美国医疗仪器发展协会、英国高血压学会、国际标准化组织的专家合作发表了血压计验证的通用标准,以替代既往的其他标准或协议[15]。经验证的血压计具体型号信息可查询欧洲高血压学会血压测量工作组建立的网站(www.stridebp.org),查询选择时需注意血压计的适用人群(见表2)。除此之外,在临床应用过程中,还要定期对血压计进行校准,以确保血压计在使用后各个时间段的准确性。

表1 动态血压监测方案
截至目前,临床前瞻性的动态血压研究多使用“示波法上臂式”动态血压计。但随着技术的发展,动态血压计也越来越呈现多功能化,除了监测外周肱动脉血压,有些血压计还增加了其他功能,如检测中心动脉血压、反射波增强指数或脉搏波传导速度、血氧饱和度,或可记录24 h 动态心电图,或通过体动记录仪评估睡眠质量等。这些附加功能在选择血压计时有参考意义,但这种多功能设备仍需要通过准确性验证才能进行临床使用。
二、动态血压的监测方法
首先应测量臂围,根据臂围选择大小合适的血压计袖带。与诊室血压测量相同,大部分成年人通常选择标准袖带,如果肥胖、上臂臂围较大(≥32 cm),则应选择大袖带;如果臂围较小(<24 cm),则选择小袖带。儿童动态血压计袖带选择也应遵循“袖带气囊长度覆盖至少80%的上臂周径,宽度为长度的40%”的原则,根据臂围大小选择对应的袖带[15]。开始动态血压监测前,最好先测量受检者双侧上臂的诊室血压,或了解其既往的双侧上臂血压测量结果,如果个体的双侧上臂间血压相差≥10 mm Hg,应选择血压较高一侧的上臂进行动态血压监测;如果两侧血压差别<10 mm Hg,则建议选择非优势臂进行监测,以减少手臂活动对血压监测的影响。同时,受检者在动态血压计进行自动测量时,应保持被测手臂静止不动。受检者在佩戴好血压计后,先用动态血压计手动测量2 次,以测试血压计是否正常工作。监测结束后,在卸下血压计之前,最好再次用动态血压计手动测量2 次,确认血压计为正常工作。另外,在诊室测量的这几次血压也有助于判断有无白大衣效应。推荐使用日记卡(见图1)记录受检者血压监测当天的生活作息,包括起床、睡眠、午休、三餐时间以及活动、服药信息、精神状态和症状,有助于后期书写动态血压评估报告。建议在工作日进行动态血压监测,以提供与受检者日常工作、生活状态更为接近的血压数据。

表2 动态血压监测的血压计型号及适用人群

图1 动态血压日记卡模板
动态血压监测的时间应尽可能不少于24 h,最好每小时都有1 个以上的血压读数。自动测量的时间间隔推荐设定为,白天每15~30 min 测量1 次,夜间每30 min 测量1 次。动态血压监测的有效读数在设定应获得读数的70%以上,当白天血压的读数至少20 个,同时夜间血压的读数至少7 个,可作为有效监测[11-12],如不满足上述条件,则应重复进行监测。
动态血压监测的标准化报告
动态血压监测报告的内容应标准化,不同设备出具的动态血压报告内容应同质化。一份合格的动态血压监测报告应该包括以下内容。①24 h 血压随时间波动的曲线图,白天和夜间时段应根据受检者监测当日的作息时间予以标记;②原始血压、心率数据;③计算各时段的平均收缩压、舒张压、心率、测量次数和有效率;④计算夜间收缩压/舒张压下降率;⑤计算各时段的收缩压、舒张压以及心率的标准差、变异系数、最大及最小值等(见图2、3)。
动态血压监测的结果判定及临床应用
动态血压监测的临床应用主要有以下4 个方面。①诊断高血压,提高高血压诊断的准确率;②评估心脑血管疾病的发生风险,提高风险评估的水平;③评估降压治疗的效果;④指导高血压的个体化治疗,提高降压治疗的质量,实现24 h 血压控制,充分发挥降压治疗、预防心脑血管并发症的作用。
用于高血压诊断的动态血压指标主要包括24 h 及白天时段、夜间时段的平均收缩压/平均舒张压。建议以动态血压监测日记卡所记录的早晨觉醒及晚上入睡时间来定义白天和夜间。白天时段定义最好扣除午睡时段[16]。如果没有记录作息时间,也可根据当地居民的生活方式,采用狭窄的固定时间段,去除血压变化较大的清晨起床和晚上上床睡觉的时间段,来定义白天和夜间,例如上午8 时至晚上8 时,共12 h 定义为白天;晚上11 时至凌晨5 时,共6 h 定义为夜间。我国新疆、西藏等西部各省、自治区可按照北京时间顺延1~2 h。近年来,清晨血压管理的重要性已逐渐得到临床医师的重视,清晨时段可定义为日记卡记录的清晨觉醒后2 h以内;如果没有记录清晨觉醒时间,清晨时段也可以采用固定时间段定义,如上午6 点至上午10 点[17-18]。
一、动态血压的诊断阈值
目前,根据动态血压诊断高血压的阈值主要基于流行病学研究证据[19-22],而非随机对照临床试验。既往报道的动态血压诊断阈值多来源于横断面研究,是基于动态血压在正常人群中的分布情况[19],或基于动态血压与诊室血压间的线性相关关系[21]。近期,有研究依据包含中国人群在内的国际多中心动态血压数据库[22],报道了基于心脑血管事件的动态血压诊断高血压的阈值,根据诊室血压水平对应的心血管风险,计算出相应的动态血压水平。该研究显示,在取整之后,与诊室血压140/90 mm Hg 相对应的24 h、白天时段、夜间时段动态血压的阈值分别为130/80 mm Hg、135/85 mm Hg、120/70 mm Hg;各级别的诊室血压与动态血压间的对应数值参见表3。
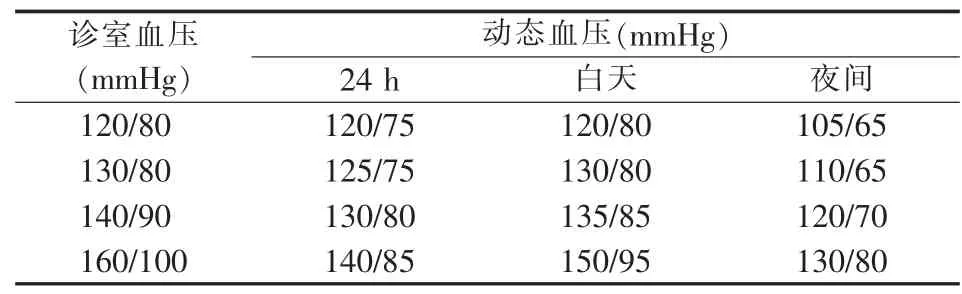
表3 不同诊室血压水平的动态血压阈值(基于人群的事件发生风险[22])
基于上述研究[19-22],本指南建议动态血压诊断高血压的标准定为,24 h 的平均收缩压/平均舒张压≥130/80 mm Hg,或白天平均收缩压/平均舒张压≥135/85 mm Hg,或夜间平均收缩压/平均舒张压≥120/70 mm Hg。不论患者是否接受降压药物治疗,不论患者其他时段血压是否升高,如果其清晨血压≥135/85 mm Hg,均可以诊断为“清晨高血压”。
二、白大衣性高血压与隐蔽性高血压
通过与诊室血压对比,利用24 h 动态血压监测结果可以确立以下诊断(见图4),包括尚未接受降压药物治疗的白大衣性高血压(诊室血压≥140/90 mm Hg,而24 h 动态血压及白天、夜间血压均正常) 和隐蔽性高血压(诊室血压<140/90 mm Hg,而24 h 动态血压或白天或夜间血压升高)以及正在接受降压药物治疗的白大衣性未控制高血压、隐蔽性未控制高血压(血压判别标准同未治疗者)。与家庭血压测量相比,动态血压监测对于隐蔽性高血压、白大衣性高血压的诊断灵敏度更高[23-24]。我国的多中心动态血压和家庭血压登记研究[23]显示,相较于24 h 动态血压监测,家庭血压测量会高估约5%的白大衣性高血压患病率,低估约10%的隐蔽性高血压和持续性高血压患病率。
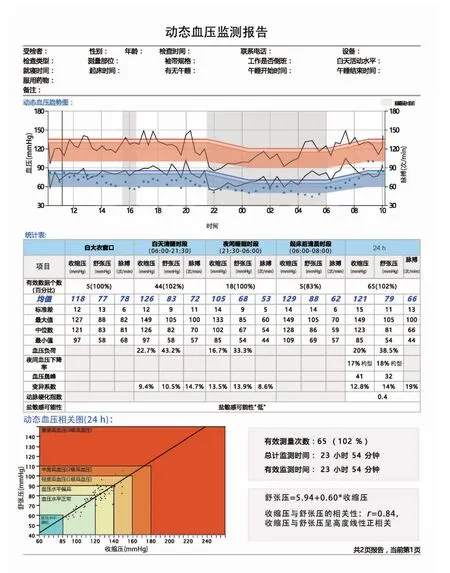
图2 动态血压监测报告模板(第一页)
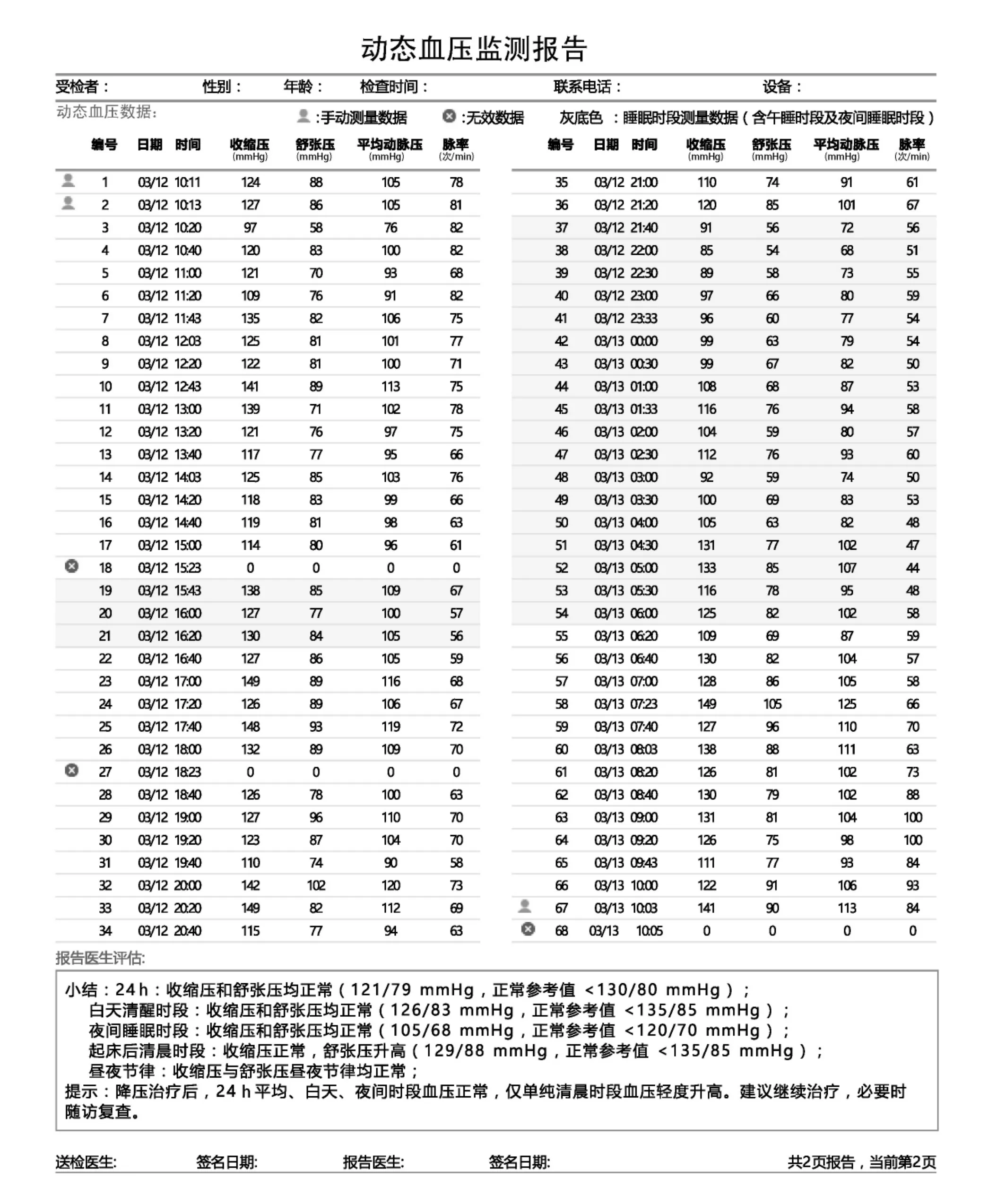
图3 动态血压监测报告模板(第二页)
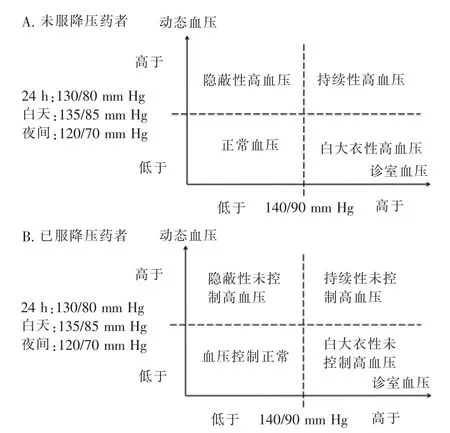
图4 根据诊室血压及动态血压的高血压分类
白大衣性高血压在我国自然人群中的患病率约为10%[25],在临床因高血压就诊的患者人群中其患病率为13%~23%[23,26],且随着年龄增长,白大衣性高血压的患病率逐渐升高。研究表明,与血压正常者相比,真正的白大衣性高血压患者(即24 h、白天和夜间动态血压均正常)的心脑血管疾病患病风险没有明显增加,而单纯依靠动态血压白天时段平均值正常来诊断的白大衣性高血压者的心脑血管疾病风险高于血压正常者[27]。利用动态血压对白大衣性高血压进行精确识别,可避免过度治疗给患者带来的不良反应和经济负担。值得注意的是,白大衣性高血压患者发展为持续性高血压的风险比正常血压者高2~3 倍[28-29],如果发展为持续性高血压后仍不治疗,患者发生心脑血管疾病的风险将会增加[29]。因此,对于白大衣性高血压患者,应加强随访,推荐每年进行1 次动态血压监测。对于明确的白大衣性高血压或白大衣性未控制的高血压患者,通常无需启动降压药物治疗或强化已有的降压治疗。
与白大衣性高血压临床表现相反的是隐蔽性高血压。国内外研究结果均一致表明,隐蔽性高血压患者的靶器官损害及心脑血管疾病的发生风险与持续性高血压患者相仿,显著高于血压正常者[27,30-32];且无论是单纯白天高血压或单纯夜间高血压[27,33],无论是诊室血压属于理想血压还是正常高值[34],只要是动态血压异常升高,患者的心脑血管事件风险都显著升高。对于已经接受降压治疗的患者,隐蔽性未控制高血压者的心脑血管风险约为血压控制正常者的1.8 倍[35]。我国的隐蔽性高血压患病率为10%~18%[23,25-26],其患病率随着诊室血压水平升高而升高。但临床目前尚无法对所有诊室血压正常的患者进行隐蔽性高血压筛查,因此对于隐蔽性高血压的高危人群,如男性、超重或肥胖患者、吸烟者及合并代谢综合征、慢性肾脏病 (chronic kidney disease,CKD)的患者等[34,36-38]推荐进行筛查。对于诊室血压处于正常偏高水平但已出现明显的靶器官损害者,又无其他明显心脑血管疾病危险因素,则需要考虑进行24 h 动态血压监测来筛查隐蔽性高血压,以免漏诊。
尽管缺乏直接的临床试验证据,但大量研究证实隐蔽性高血压及隐蔽性未控制高血压患者存在较高的心脑血管疾病风险,推荐对这类患者进行积极的生活方式干预,并及时启动或强化降压药物治疗。
三、特殊时段的血压评估
1.清晨高血压:清晨是心脑血管事件的高发时段,心肌梗死、心源性猝死及脑卒中等的发病高峰时间均在觉醒前后4~6 h。清晨血压过度升高可能是导致清晨时段心脑血管事件发生率显著升高的主要原因。早期的研究多集中于血压晨峰,即夜间睡眠时段到晨起血压的上升幅度。多数研究结果表明,血压晨峰与心脑血管事件尤其是出血性脑卒中密切相关[39-40]。异常血压晨峰引起的高风险主要是由于清晨血压升高[41],清晨血压每升高10 mmHg,脑卒中发生风险增加约44%[42],无症状颅内动脉狭窄患病风险增加约30%[43]。与血压正常者相比,单纯清晨高血压患者(仅清晨血压升高,其他时段血压正常)发生动脉硬化[44]、左心室肥厚等靶器官损害的程度均显著增加[45]。因血压晨峰测量重复性差,定义和计算方法不统一,目前主要用于临床研究,还难以应用于临床实践,而清晨血压测量评估方法简单,易在临床实践中广泛使用。《清晨血压临床管理的中国专家指导建议》[17]将清晨时段的动态血压平均水平≥135/85 mmHg 定义为清晨高血压,不论其他时段的血压是否升高。
控制清晨高血压,可以采用的降压治疗策略包括长效药物、足剂量药物、联合治疗等[17-18,46]。
2.夜间高血压:与白天血压升高相比,夜间血压升高与全因死亡及心脑血管死亡风险更密切相关,且能独立于白天高血压来预测患者的死亡风险[47]。荟萃分析显示,夜间收缩压每增加20 mmHg,全因死亡及心脑血管事件风险分别增加约23%和36%[3]。单纯夜间高血压患者表现为夜间血压升高,而白天血压正常。与血压正常者相比,单纯夜间高血压患者的靶器官损害[左心室肥厚(22.1%比7.6%)、颈动脉斑块(55.8%比32.9%)]等百分比增加[48],其心血管死亡及心血管事件风险亦均增加约30%[33]。我国人群中单纯夜间高血压的患病率约为10%,显著高于欧美人群(6.0%~7.9%)[31],这可能与我国人群中盐敏感性高血压多见[49-50]及高钠饮食[51-53]、近端肾小管钠重吸收增多有关[54]。同时,在继发性高血压、合并阻塞型睡眠呼吸暂停低通气综合征、CKD、糖尿病等人群中,夜间高血压也更为常见[12,55-57]。控制夜间高血压患者的血压,首先需要筛查并排除继发性原因,如存在失眠、阻塞型睡眠呼吸暂停低通气综合征、昼夜倒班等,并针对病因进行处理。
排除继发性因素后,对于白天、夜间血压均升高的患者,优选作用时效能够覆盖夜间的长效药物,或者使用能有效降低夜间血压的新型降压药物,如血管紧张素受体脑啡肽酶抑制剂沙库巴曲缬沙坦钠等[58];如夜间血压仍控制不佳可睡前加服中短效药物。对于单纯夜间高血压患者,目前尚没有指导降压治疗的直接临床试验证据,考虑其属于隐蔽性高血压的一种类型,推荐参照有关隐蔽性高血压的降压治疗方案。
四、血压昼夜节律和短时血压变异评估
人体血压在生理状态下呈现较为明显的昼夜节律,即睡眠时段的血压较白天清醒时段明显下降,而在清晨时段,从睡眠到觉醒,血压呈明显上升趋势。在生理情况下,夜间的收缩压和舒张压会比白天血压下降10%~20%。临床上常根据夜间血压下降的比值 [(白天血压-夜间血压)/白天血压×100%]来定义 “杓型”(10%~20%)、“非杓型”(0~10%)、“反杓型”(<0)及“超杓型”(>20%)血压节律(见图5)。非杓型及反杓型血压节律与靶器官损害及心脑血管死亡风险增加有关[3,47]。根据患者的血压昼夜节律,可优化高血压降压治疗。对于非杓型及反杓型血压节律的患者,宜加强夜间的血压控制,而对于超杓型血压节律的高血压患者,要注意避免夜间血压过度下降导致的缺血性心脑血管事件发生风险增加。
24 h 动态血压监测过程中,除了存在昼夜血压节律的明显变化外,由于不同时间点的血压测量可能受到外界刺激、运动、睡眠等因素的影响,血压水平会存在不同程度的波动。24 h 动态血压提供的短期血压变异的参数包括标准差、变异系数、血压最大与最小值差值、平均实际变异、独立于均值的变异等。总体而言,这些参数的临床价值仍处于研究阶段[59-61],且目前尚缺乏公认的24 h 血压变异参数参考值范围,也没有干预的手段及试验证据。国际动态血压合作研究[62]表明,24 h 血压平均实际变异虽与心脑血管事件发生风险显著相关,但并不能在血压平均水平的基础上进一步提升风险预测能力。减少短时血压变异,是否能改善患者的预后,也需要进一步研究。
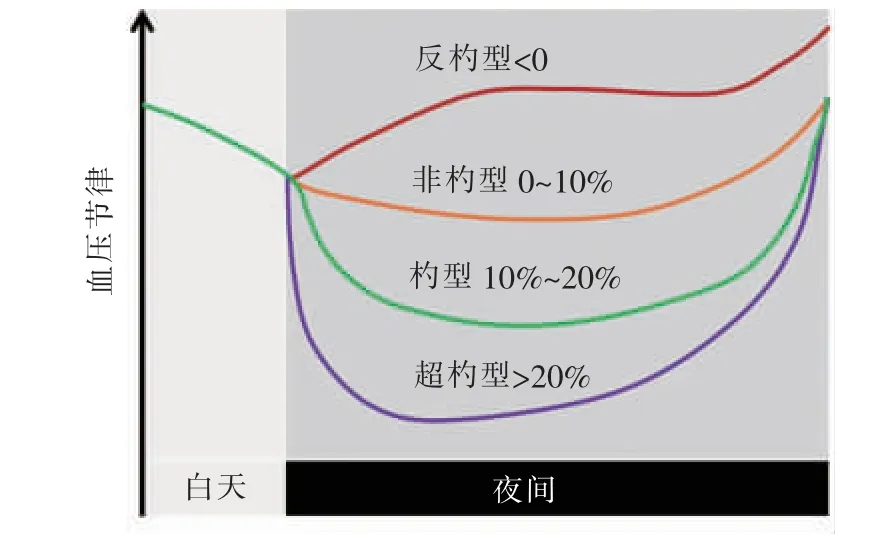
图5 动态血压昼夜节律
五、动态血压其他衍生参数
1.血压负荷:血压负荷一般是指某一时段内(白天、夜间或24 h)血压超过正常值的次数占总血压测量次数的比例。为更准确地反映血管承受的压力负荷程度,临床研究中也常将血压测量的时间和血压描绘成曲线,将血压超过正常值的曲线下面积作为血压负荷。研究表明,在成年人中应用血压负荷虽然也能诊断高血压,但在已经考虑收缩压与舒张压的平均值后,血压负荷对预测靶器官损害或并发症发生风险并无附加价值[63-64];在儿童中,血压负荷的临床意义仍有争议,美国青少年成人及儿童高血压筛查指南[65]使用了血压水平≥95%百分位和血压负荷≥25%组合来定义动态高血压,而欧洲指南[66]仅采用血压平均值来定义。关于在儿童中血压负荷是否存在独立于血压水平的预测价值,还需要更多的研究证据支持。
2.动脉硬化参数:当人体动脉血管较有弹性时,收缩压升高,舒张压也会相应升高;而当血管弹性降低时,收缩压升高时舒张压升高不明显,甚至可降低。因此,收缩压与舒张压之间的动态关系在一定程度上可以反映动脉的弹性功能。利用24 h动态收缩压与舒张压之间的回归关系,计算动态动脉硬化指数 (ambulatory arterial stiffness index,AASI) 可以评估动脉硬化的程度,其计算公式为AASI=1-(24 h 舒张压与收缩压之间的回归斜率)[67]。AASI 与其他动脉硬化参数,如颈-股脉搏波传导速度、反射波指数等有关,与动态血压变异间也有关联,可受夜间血压下降率影响。AASI≥0.55时,患者发生致死性脑卒中的风险将增加1.4 倍[68],靶器官损害风险也明显增加[69]。与AASI 类似,收缩压与舒张压之间的差值,即脉压差也反映了动脉硬化的程度。近期有学者提出,将脉压分解为反映非压力依赖性动脉硬度 (elastic pulse pressure,elPP)的脉压以及反映压力依赖性动脉硬度(stiffening pulse pressure,stPP)的脉压,在特定人群中这2 种脉压均分别被证实能够预测心脑血管事件及死亡风险[70-71],其临床意义值得在中国人群中继续进行验证研究。
动态血压监测过程中也检测脉率,并衍生出多个血压与脉率关联的指标,如血压与脉率的乘积可评估心脑血管事件的发生风险[72],收缩压变化与脉率变化的比值可用来评估自主神经功能[73],血压的昼夜节律及脉率的快慢情况可评估受检者的盐敏感性等[74]。但这些指标的临床意义尚需进一步研究。脉率本身在血压管理中可能也具有重要的临床意义,除了可以预测心脑血管事件外[75],也有助于确定患者是否需要使用肾上腺素β 受体阻滞剂或非二氢吡啶类钙拮抗剂等减慢心率的降压药物。
动态血压监测的适应证
一、新发1~2 级诊室高血压
目前,多项国内外指南[7-10]均推荐采用24 h 动态血压监测诊断高血压。建议对新发现的1~2 级诊室高血压患者进行动态血压监测,以排除白大衣性高血压,明确高血压诊断。动态血压监测能够评估24 h 血压的动态变化,发现阵发性血压升高等血压波动过大的情况;能够有效识别诊室外时段出现的血压异常,尤其是夜间血压不下降、夜间高血压等病理状态,这些血压特征对临床排查继发性高血压有一定的提示作用。对于诊室血压处于正常高值或已出现明显的靶器官损害的患者,需警惕其是否合并隐蔽性高血压的危险因素,应予行24 h 动态血压监测,以筛查隐蔽性高血压,避免漏诊。
二、接受降压治疗的高血压患者
在已经接受降压治疗的高血压患者中,单纯采用诊室血压进行血压控制情况的评估,既可能低估血压控制情况,也可能高估血压控制情况。对于服用降压药物后,诊室血压仍然控制不佳的患者,动态血压监测可以识别出其中的白大衣性未控制高血压,从而避免给予这些患者过度治疗;对于持续性未控制高血压,也可根据动态血压监测结果来调整降压方案。对于服药后诊室血压<140/90 mmHg 的患者,如果出现新发的心脑血管并发症或靶器官损害,或其靶器官损害进行性加重,亦应评估24 h 及白天、夜间血压是否达标,有无清晨高血压,以排查隐蔽性未控制高血压。需要注意的是,利用动态血压监测评估降压治疗效果时,应维持原有的降压药物治疗方案,不需要停用降压药物,这样才能获取可靠的降压疗效评价。
作为血压评估的标准方法,动态血压监测亦可用于临床准确评估试验药物或器械的降压疗效。此外,动态血压监测还有助于筛查一些特殊的血压变化情况,如发作性低血压、体位性低血压、餐后低血压、卧位高血压等,并根据这些血压特征识别出一些疾病,如阻塞型睡眠呼吸暂停低通气综合征、帕金森病等。
作为一项无创的血压测量方法,动态血压监测没有绝对的禁忌证,但在部分人群中需要谨慎评估其检测结果。心房颤动(房颤)患者由于心律绝对不齐,单次血压测量容易产生误差,多次测量可提高血压评估的准确性[7]。但在已发表的几项小样本研究中,动态血压的监测成功率在房颤患者与窦性心率人群间并无差异;而在心室率不快的持续性房颤患者中,动态血压计测得的诊室收缩压与听诊法类似,但舒张压可能略高于听诊法[76]。此外,对于失眠及夜间多尿等患者,需要考虑这些因素对夜间血压的影响。对于双臂血压不对称者,应选择血压较高的一侧进行监测。
特殊人群的动态血压监测
一、难治性高血压患者
疑似难治性高血压患者中白大衣效应常见,因此可根据动态血压监测结果,区分真性与假性难治性高血压。国外研究显示,8 295 例疑似难治性高血压患者的动态血压监测结果表明,其中有37.5%存在白大衣效应,为假性难治性高血压[77]。
二、其他特殊人群
肥胖、代谢综合征、糖尿病、肾脏疾病、阻塞型睡眠呼吸暂停低通气综合征等患者常有隐蔽性高血压患病风险增加、血压昼夜节律异常、血压波动较大等特征,因此需要进行动态血压监测,以准确评估血压及血压变异情况(见表4)。
1.阻塞型睡眠呼吸暂停低通气综合征:在睡眠过程中,阻塞型睡眠呼吸暂停低通气综合征患者可能发生间歇性低氧事件,因此易出现非杓型血压、夜间高血压、血压晨峰升高及血压变异性增加等[78-81]。
2.糖尿病、肥胖和代谢综合征患者:此类患者易合并高血压。我国一项多中心登记研究显示,在心内科就诊的高血压患者中有32.9%同时患有糖尿病;而在内分泌科就诊的糖尿病患者中有58.9%同时患有高血压[82]。糖尿病和代谢综合征患者都常表现为血压变异性增加、昼夜节律消失,患隐蔽性高血压、难治性高血压的比例增加,从而面临更高的心脑血管疾病风险[83-84]。
3.CKD:夜间高血压及隐蔽性高血压在CKD 患者中十分常见。有研究显示,我国1 282 例没有服用降压药物的CKD 患者中,夜间高血压的患病率为71%,而单纯性夜间高血压的患病率为20%[85]。与血压正常的CKD 患者相比,合并隐蔽性高血压的CKD 患者靶器官损害较为严重,全因死亡、心脏事件以及肾功能恶化风险较高[37,86]。一项纳入980 例CKD 患者(其中约90%服用降压药物)的荟萃分析显示,诊室血压正常的CKD 患者中有超过40%存在隐蔽性高血压或隐蔽性未控制高血压[87]。另有研究发现,约56%服用降压药物的CKD 患者存在隐蔽性未控制高血压,半数为夜间血压未控制[88]。CKD 患者的血压波形不仅会表现为昼夜节律消失,也常表现为短期血压变异性增加,肾功能恶化程度越严重,血压变异性增加也越明显[89]。
4.帕金森病:心血管自主神经功能紊乱是帕金森病患者常见的非运动症状之一,多表现为异常的血压变异,甚至可在运动症状出现之前就已存在[90-91]。我国一项多中心帕金森患者登记研究报道,在无血压异常病史的帕金森病患者中,约25%存在体位性低血压,超过50%存在反杓型血压;若患者24 h 血压昼夜节律呈现反杓型,则其合并体位性低血压的概率明显增大[92]。合并体位性低血压的帕金森病患者,其非运动症状、自主神经功能障碍和认知障碍更为严重同时也存在更为严重的心脑血管损害[92-93]。
5.继发性高血压:多种原因导致的继发性高血压患者,如嗜铬细胞瘤患者可出现血压阵发性升高及短时血压变异增大;肾血管性高血压、原发性醛固酮增多症、库欣综合征患者更容易表现为夜间高血压及非杓型血压[12,55]。
6.老年人:老年人常见白大衣性高血压、血压昼夜节律消失,且随着年龄的增加,其收缩压升高明显,而舒张压不升高,甚至可有轻度降低,单纯收缩期高血压多见。因自主神经功能减退,老年人常出现血压变异增加,表现为体位性低血压及餐后低血压、血压晨峰增大。
7.儿童:与诊室血压相比,儿童时期的动态血压可以更准确地预测高血压的发生[94-95],有助于发现隐蔽性高血压和继发性高血压[96],因此推荐利用动态血压监测明确儿童高血压诊断[65-66]。隐蔽性高血压在肥胖、患有CKD 或主动脉缩窄修复术后的患儿中更为常见,患儿常伴有较明显的靶器官损害[95,97]。与诊室血压相比,根据24 h 动态血压进行血压管理,能够将CKD 患儿发生肾功能衰竭的风险降低35%[98]。考虑到动态血压监测需要患儿的配合,美国青少年及儿童高血压筛查指南推荐,对大于5 岁的患儿进行动态血压监测可能更合适[65]。目前,不同指南中关于儿童动态血压诊断高血压的标准仍有差异[65-66],需要进一步行研究验证,尤其需收集我国儿童的数据。

表4 特殊人群的动态血压特征
8.孕妇:24 h 动态血压监测可发现孕妇孕中期发生的夜间血压下降不足,有助于识别妊娠高血压及预测子痫前期风险[99]。孕妇发生白大衣性高血压的比例较高,约为16%[100]。对在妊娠早期合并左心室肥厚等高血压靶器官损害但诊室血压无明显升高者,应警惕隐蔽性高血压的可能。对于怀疑有白大衣性高血压、隐蔽性高血压或孕期血压波动较大的孕妇,推荐进行24 h 动态血压监测[101]。
社区动态血压监测的应用
社区是高血压防治的主战场,但基层医疗卫生机构存在缺乏动态血压监测设备,缺少分析解读动态血压报告的有经验的医师,且患者依从性差等实际问题[14,102]。为提升社区高血压管理质量,推荐从多个维度提高社区动态血压监测的普及性,促进监测质量的同质化。
首先,积极开展有关动态血压临床应用的专业培训,使基层医师了解到,通过动态血压监测可以提升高血压诊断的准确性和降压治疗的质量,更有效地保护靶器官、预防心脑血管并发症、减少死亡和残疾,最大程度地减少高血压的危害。同时,建议社区卫生服务中心及其站点配备经验证合格的动态血压监测设备,满足社区进行高血压优质管理的需求。
其次,推广应用网络化的动态血压远程分析报告平台和医联体模式,可解决基层专业技术人力不足的瓶颈[103]。社区医师可以登录建立在互联网、无线通讯以及云计算基础上的远程分析报告平台,根据系统提示规范地设置动态监测方案。在动态血压监测完成后,社区医疗技术人员可将测量数据上传至平台,填写血压监测日记卡记录的相关信息,由平台专业软件进行标准化分析,获取动态血压监测报告。动态血压数据也可同时传输给高血压专科医师,由后者对其进行评估、分析和判断,再将信息反馈至社区(见图6)。纵向整合医疗资源,形成资源共享、分工协作,有助于患者获得同质化的动态血压监测结果,优化社区医院的诊疗流程,提高患者的依从性。
动态血压监测临床应用的展望
相较于诊室血压测量,动态血压监测成本较高,但从长远的角度来看,动态血压监测是一项成本效益较高的检测项目。我国学者运用成本-效益分析法,最保守估算,动态血压监测每投入1 元,在未来5~7 年内可以节省12 元不必要的高血压及并发症医药费用支出[104]。英国[105]及美国[106]的学者也发现,动态血压监测可以降低高血压的误诊率,延长患者的期望寿命,其较高的检测成本可被更加有效的针对性治疗、更显著减少心脑血管事件而节省的费用所抵消,故成本效益较高。
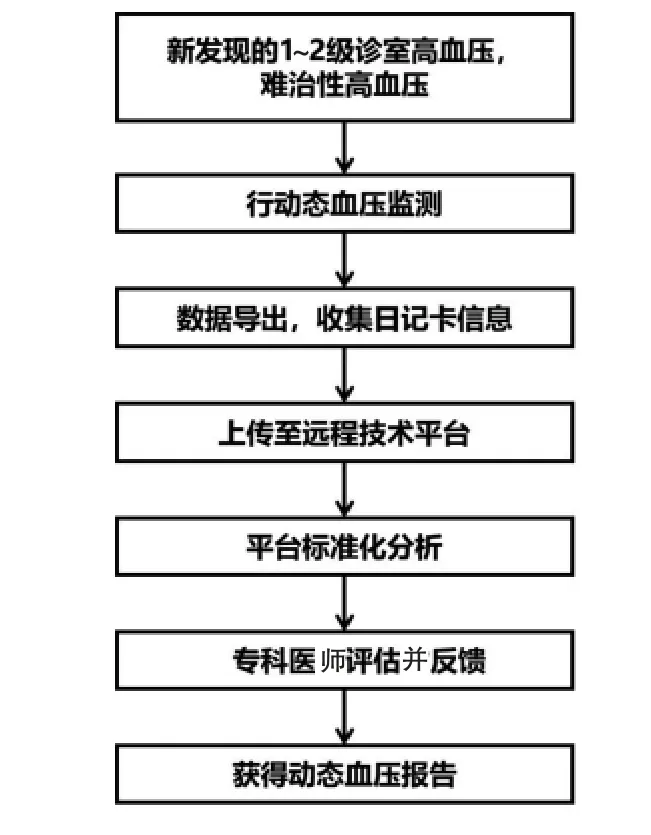
图6 社区动态血压监测流程图
动态血压监测过程中测量血压的次数较多,且在受检者睡眠期间也进行测量,因此会有不适感,可能影响受检者的睡眠,从而影响了其接受度及依从性。为减少上臂袖带充气带来的不适感,腕式动态血压计已在研发应用中。相较于上臂式血压计,腕式血压计佩戴较为舒适,袖带充气造成的夜间噪音较小,可减轻血压监测对患者夜间睡眠的干扰程度,提高舒适度及患者的依从性,但其测量的准确性尚待进一步验证。因为不需要充放气,非袖带式的血压测量可以最终实现每个心动周期的血压实时监测。以袖带测量的肱动脉血压作为参照,通过心电活动和血管容积描记曲线获得脉搏波传导时间,根据转化公式推算出血压水平[107]。目前,非袖带式血压测量还存在技术瓶颈,且缺乏标准的验证方案,尚不能用于人体血压监测。
除此以外,合并动脉血氧饱和度测定、心电监测功能以及中心动脉压的24 h 动态血压监测,也可为高血压优化管理提供重要数据。基于信息和通信技术,采用可穿戴设备连续监测动态血压、心率、血氧饱和度等数据,将数据存储或传输至远程医疗中心,可用于优化高血压及心脑血管疾病干预管理策略。新技术的发展正在逐步减少动态血压监测的弊端与不足,新技术与家庭血压监测的逐渐融合,临床可不再局限于24 h 监测,可实现长时监测。增加监测的便利性和多功能性可能是未来动态血压监测的发展趋势。
推荐要点总结
进行动态血压监测时,建议选择经过验证的动态血压计,根据受检者臂围选用大小合适的袖带;动态血压监测的时间应尽可能不少于24 h,白天每15~30 min 测量1 次,夜间每30 min 测量1 次;有效读数需在应获得读数的70%以上,白天至少有20 个有效读数,夜间至少有7 个有效读数;推荐使用标准化的动态血压监测报告。
动态血压监测诊断高血压的标准为,24 h 平均血压≥130/80 mmHg,或白天平均血压≥135/85 mmHg,或夜间平均血压≥120/70 mmHg。
动态血压监测的适应证为,①新发现的诊室1~2 级高血压;②诊室血压正常高值,或合并靶器官损害或高心血管风险;③血压波动较大,或怀疑体位性低血压、餐后低血压、继发性高血压等;④诊室血压已达标(≤140/90 mmHg),但仍发生了心脑血管并发症,或新出现了靶器官损害,或靶器官损害进行性加重;⑤难治性高血压,或诊室血压未达到治疗标准,为了解夜间、清晨血压及血压昼夜节律情况;⑥在临床试验中,评价药物或器械治疗的降压效果。
建议在基层社区推广应用动态血压监测,可通过网络化动态血压远程平台及医联体模式,优化社区高血压诊疗流程,提升高血压管理质量。
中国高血压联盟《动态血压监测指南》委员会(按姓名拼音字母排序)
宾建平(南方医科大学南方医院),卜培莉(山东大学齐鲁医院),陈伟伟(卫生部心血管病防治研究中心),陈晓平(四川大学华西医院),陈歆(上海交通大学医学院附属瑞金医院),程艾邦(秘书,上海交通大学医学院附属瑞金医院),程文立(首都医科大学附属北京安贞医院),崔兆强(复旦大学附属中山医院),戴秋艳(上海交通大学附属第一人民医院),冯颖青(广东省人民医院),郭子宏(云南省阜外心血管病医院),黄晶(重庆医科大学附属第二医院),贾楠[青岛市市立医院(集团)],姜一农(大连医科大学附属第一医院),雷成宝(大同煤矿集团有限责任公司总医院),李觉(同济大学医学院),李南方(新疆维吾尔自治区人民医院),李卫华(厦门大学附属第一医院),李燕(上海市高血压研究所),李勇(复旦大学附属华山医院),林金秀(福建医科大学附属第一医院),刘敏(河南省人民医院),牟建军(西安交通大学第一附属医院),商黔惠(遵义医科大学附属医院),苏焱伦(连云港市中医院),孙宁玲(北京大学人民医院),汤松涛(东莞市寮步镇社区服务中心),王成(中山大学附属第五医院),王刚(上海交通大学医学院附属瑞金医院),王红宇(山西医科大学第二医院),王继光(上海交通大学医学院附属瑞金医院 上海市高血压研究所),汪文娟(中南大学湘雅三医院),向全永(江苏省疾病预防控制中心),谢建洪(浙江省人民医院),谢良地(福建医科大学附属第一医院),徐新娟(新疆医科大学第一附属医院),薛浩(中国人民解放军总医院),尹新华(哈尔滨医科大学附属第一医院),余静(兰州大学第二医院),俞蔚(浙江医院),张海锋(南京医科大学第一附属医院),张宇清(中国医学科学院阜外医院),郑启东(玉环市第二人民医院),周碧蓉(安徽医科大学第一附属医院),祝之明(重庆大坪医院)

