土田七中化学成分的分离与鉴定
马丽芳,李 燕,陈 凯,汪 伦
(1.四川大学化学工程学院,四川成都610065;2.四川大学 生物治疗国家重点实验室,四川成都610041)
土田七[Stahlianthus involucratus(King ex Bak.)Craib],别名也叫姜七、三七姜、姜叶三七、竹叶三七,为姜科土田七属植物土田七的块根和根茎。姜科植物是多年生草本植物大家族,种类繁多,是热带和亚热带地区分布最广的植物之一,大约有47属1400种。姜科植物是次生代谢产物的来源,具有丰富的化学结构和重要的生物活性。目前,姜科植物因其植物化学和药理特性被广泛研究,许多姜科植物中分离出多种具有药理作用的活性化合物。
植物土田七,分布于中国的云南、广西、广东、福建等省,在印度也有分布[1]。其味辛、微苦,性温,具有散瘀消肿,活血止血之功效。作为一种民间药,它的根茎长期以来一直用于传统医学中治疗炎症,疼痛和发烧[2]。
根据已有文献报道,目前从土田七中分离得到的化合物包含麦角烷二聚物、倍半萜类、卡丹烷二聚体[3-6]。由于对该植物成分与活性的报道较少,给该药用植物的使用、推广以及鉴定等方面带来较大的困难。为了进一步寻找土田七中化学成分,给土田七的应用奠定物质基础,作者利用半制备型高效液相色谱、柱色谱等多种色谱分离技术对土田七进行分离纯化,并采用质谱和核磁共振波谱鉴定了所得化合物的结构,为土田七的活性研究奠定物质基础。
1 实验部分
1.1 主要仪器与材料
Bruker avance 400型核磁共振仪,德国布鲁克公司;QTOF质谱仪和ESI离子源,英国沃特世公司;旋转蒸发仪,瑞典BUCHIR200;半制备型高效液相色谱,美国沃特斯;Water 2695液相色谱仪,美国Waters公司;中压柱层析系统,瑞士Buchi Flawil公司;MCI-gel CHP 20树脂,日本三菱公司;Sephadex LH-20,美国Amersham P-harmacia Biotech公司;柱层析硅胶,德国默克公司。
药材由四川大学生物治疗国家重点实验室胡以国教授提供,采自云南,并鉴定为土田七[Stahlianthus involucratus(King ex Bak.)Craib]。
1.2 提取与分离
土田七提取流程图如图1所示。土田七根茎2 kg,经粉碎后,采用60目的筛网过筛,用75%乙醇(3 L)加热回流提取,每次提取3 h,提取3次合并提取液,用旋转蒸发仪减压浓缩得到浸膏412 g。将浸膏用温水(5 L)分散,分别用正己烷(5 L/次)、乙酸乙酯(5 L/次)、正丁醇(5 L/次)3种溶剂进行萃取,每种溶剂萃取3次,将各部分用旋转蒸发仪减压浓缩,得到正己烷部分26 g,乙酸乙酯部分61 g,正丁醇部分146 g。

图1 土田七提取分离流程图Fig.1 Flowchar t for extraction and isolation of Stahlianthus involucratus
将正己烷部分(20 g)用硅胶(60~100目)干法拌样,旋干后进行中压柱层析(100~200目)分离,用石油醚-乙酸乙酯作流动相进行梯度洗脱(1∶0~0∶1,v/v),每250 mL收集1次,通过TLC(薄层色谱法)进行检测,用旋转蒸发仪将洗脱液分别减压回收溶剂,得到6个组分(Fr.P.1~Fr.P.6)。Fr.P.3(2.69 g)采用中压柱层析(200~300目),用石油醚和乙酸乙酯进行梯度洗脱(50∶1~0∶1,v/v),每50 mL收集1次,通过TLC进行检测,用旋转蒸发仪将洗脱液分别减压回收溶剂,得到5个组分(Fr.P.3.1~Fr.P.3.5)。进一步对Fr.P.3.1用中压柱层析(200~300目)分离,用石油醚和乙酸乙酯作流动相进行梯度洗脱(50∶1~0∶1,v/v),经TLC检测后得到了4个组分(Fr.P.3.1.1~Fr.P.3.1.4)。Fr.P.3.1.3采用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),用甲醇和水(95∶5,v/v)进行等度洗脱,得到化合物1。
将乙酸乙酯部分(50 g)用硅胶(60~100目)干法拌样,旋干后进行中压柱层析(100~200目)分离,用石油醚-乙酸乙酯作流动相进行梯度洗脱(1∶0~0∶1,v/v)。通过TLC进行检测,每500 mL收集1次。用旋转蒸发仪将收集的洗脱液分别减压回收溶剂,得到7个组分(Fr.E.1~Fr.E.7)。Fr.E.3(2.3 g)用硅胶(200~300目)干法拌样,旋干后进行中压柱层析(200~300目)分离,用石油醚和乙酸乙酯作流动相进行梯度洗脱(40∶1~0∶1,v/v),每100 mL收集1次,通过TLC进行检测,用旋转蒸发仪将收集的洗脱液分别减压回收溶剂,得到6个组分(Fr.E.3.1~Fr.E.3.6)。Fr.E.3.6用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),在甲醇和水(80∶20,v/v)的条件下等度洗脱,得到化合物8。Fr.E.4(5.9 g)用Sephadex LH-20柱(填料为Sephadex LH-20,50μm),采用二氯甲烷和甲醇(1∶1,v/v)进行等度洗脱,共得到5个组分(Fr.E.4.1~Fr.E.4.5)。Fr.E.4.3采用SephadexLH-20柱(填料为Sephadex LH-20,50μm),用二氯甲烷和甲醇(1∶1,v/v)进行等度洗脱,得到9个组分(Fr.E.4.3.1~Fr.E.4.3.9)。进一步采用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm)对Fr.E.4.3.1分离,用甲醇和水(60∶40,v/v)进行等度洗脱得到化合物2。Fr.E.4.3.4采用中压柱层析(200~300目),用石油醚和乙酸乙酯作流动相进行梯度洗脱(20∶1~1∶1,v/v),共得到5个组分(Fr.E.4.3.4.1~Fr.E.4.3.4.5)。Fr.E.4.3.4.1用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),用甲醇和水(60∶40,v/v)作流动相进行等度洗脱,得到化合物4和5。Fr.E.4.3.4.2用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),用甲醇和水(55∶45,v/v)作流动相进行等度洗脱,得到化合物3。Fr.E.4.3.4.4利用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),用甲醇和水(50∶50,v/v)作流动相进行等度洗脱,得到化合物7。Fr.E.4.3.6利用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm),用甲醇和水(45∶55,v/v)进行等度洗脱得到化合物6,利用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm)对Fr.E.4.3.7分离,用甲醇和水(45∶55,v/v)进行等度洗脱得到化合物9和10。采用MCI柱(填充材料为MCI-gel CHP 20P,70~150μm)对Fr.E.7(25.6 g)进行分离,用乙醇和水(1∶3,1∶1,3∶1和1∶0,v/v)进行梯度洗脱得到4个组分(Fr.E.7.1~Fr.E.7.4)。将Fr.E.7.3进一步采用乙醇和水(3∶1~1∶0,v/v)做流动相用MCI柱(填充材料为MCI-gel CHP 20P,70~150μm)分离,得到5个组分(Fr.E.7.3.1~Fr.E.7.3.5)。最后采用半制备液相色谱柱(填料为Sunfire C18,5μm,4.6×150 mm)纯化Fr.E.7.3.3,用甲醇和水(35∶65,v/v)进行等度洗脱得到化合物11。
分离纯化所得化合物进一步采用核磁共振波谱鉴定化合物的结构,根据核磁谱图和薄层色谱(TLC)可判定化合物纯度无杂质,纯度较高。
1.3 结构鉴定
化合物1:无定型粉末。ESI-MS(m/z):413.3705([M+H]+)。1H NMR(400 MHz,CDCl3):δ:5.35(1H,m,H-6),5.15(1H,dd,J=8.4,H-22),5.02(1H,dd,J=8.4,H-23),3.53(1H,m,H-3),2.30~0.64(43H,m)。13C NMR(101 MHz,CDCl3):δ:140.77(C-5),138.32(C-22),129.30(C-23),121.72(C-6),71.81(C-3),56.88(C-14),55.98(C-17),51.25(C-24),50.18(C-9),42.32(C-4),42.23(C-13),40.49(C-20),39.70(C-12),37.27(C-1),36.53(C-10),36.16(C-25),31.89(C-8),31.68(C-2),28.92(C-7),25.41(C-15),24.37(C-16),24.31(C-28),21.22(C-21),21.10(C-11),19.41(C-19),18.99(C-26),12.25(C-18),12.06(C-29)11.87(C-27)。以上数据与文献报道[7]一致,故鉴定化合物1为豆甾醇。
化合物2:无定型粉末。ESI-MS(m/z):253.0641([M+H]+)。1H NMR(400 MHz,CD3OD):δ:7.40(1H,d,J=3.6,H-2),6.60(1H,d,J=3.6,H-3),6.38(1H,d,J=3.1,H-2′),6.30(1H,d,J=3.1,H-3′),5.40(1H,s,H-7),4.63(2H,s,H-5),4.51(2H,s,H-5′)。13C NMR(101 MHz,CD3OD):δ:178.06(C-6),161.82(C-4),154.70(C-4′),152.50(C-1),150.65(C-1′),123.43(C-2),109.51(C-3),108.83(C-2′),107.47(C-3′),97.89(C-7),56.25(C-5),55.98(C-5′)。以上数据与文献报道[8]一致,故鉴定的化合物2为5,5′-二羟甲基糠醛。
化合物3:无定型粉末。ESI-MS(m/z):257.1025([M+H]+)。1H NMR(400 Hz,CD3OD):δ:5.98(1H,q,J=6.8,H-2),5.20(1H,s,H-10),4.86(1H,s,H-10),3.02(2H,s,H-4),1.97(1H,s,CH3-12),1.91(3H,d,J=6.8,CH3-1),1.62(3H,s,CH3-7)。13C NMR(101 MHz,CD3OD):δ:172.39(C-7),170.04(C-11),169.53(C-8),146.38(C-5),138.64(C-2),130.56(C-3),111.61(C-10),82.98(C-6),35.54(C-4),20.94(C-9),19.84(C-12),14.55(C-1)。命名为顺式-6-甲基-5-亚甲基-3-亚乙基-6-乙酰氧基己二酸。
化合物4:无定型粉末。ESI-MS(m/z):259.1103([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.06(1H,d,J=7.1,H-2),2.61(1H,m,H-4),2.18(1H,m,H-5),2.10(1H,m,H-4),2.09(3H,s,CH3-11),2.02(3H,d,J=7.1,CH3-1),1.72(3H,s,CH3-9),0.82(3H,d,J=7.2,CH3-12)。13C NMR(101 MHz,CD3OD):δ:173.02(C-10),170.12(C-7),169.77(C-8),138.28(C-2),130.83(C-3),83.49(C-6),35.61(C-4),32.23(C-5),21.02(C-9),19.93(C-11),14.52(C-1),12.11(C-12)。以上数据与文献报道[9]一致,故鉴定化合物4为反式-(2R,3S)-2,3-二甲基-5-亚乙基-2-乙酰氧基己二酸。
化合物5:无定型粉末。ESI-MS(m/z):217.0154([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.16(1H,d,J=7.6,H-2),2.57(1H,m,H-4),2.28(1H,m,H-5),2.20(1H,m,H-4),2.01(3H,d,J=7.6,CH3-1),1.39(3H,s,CH3-9),0.92(3H,d,J=6.8,CH3-10)。13C NMR(101 MHz,CD3OD):δ:174.70(C-7),165.42(C-8),145.06(C-2),122.48(C-3),84.69(C-6),34.47(C-4),32.53(C-5),20.67(C-9),15.12(C-1),12.23(C-10)。以上数据与文献报道[10-11]一致,故鉴定化合物5为反式-(2R,3S)-2,3-二甲基-5-亚乙基-2-羟基己二酸。
化合物6:无定型粉末。ESI-MS(m/z):125.0541([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.93(1H,s,H-2),6.82(1H,d,J=7.5,H-5),6.68(1H,d,J=7.5,H-4),1.96(3H,s,H-1)。13C NMR(101 MHz,CD3OD):δ:147.90(C-6),145.38(C-3),126.58(C-1),121.33(C-5),115.09(C-4),113.66(C-2),21.33(C-7)。以上数据与文献报道[12]一致,故鉴定化合物6为2,5-二羟基甲苯。
化合物7:无定型粉末。ESI-MS(m/z):115.0681([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.99(1H,m,H-2),2.43(1H,m,H-4),2.23(1H,m,H-4),1.67(3H,d,J=6.3,H-5),0.88(3H,d,J=7.1,H-1)。13C NMR(101 MHz,CD3OD):δ:167.98(C-6),141.03(C-3),124.81(C-2),28.51(C-4),12.66(C-5),12.64(C-1)。以上数据与文献报道[13]一致,故鉴定化合物7为2-乙基-2-丁烯酸。
化合物8:无定型粉末。ESI-MS(m/z):165.0475([M+H]+)。1H NMR(400 MHz,CD3OD):δ:7.52(1H,d,J=16,H-7),7.34(2H,d,J=8.5,H-2/6),6.73(1H,d,J=8.5,H-3/5),6.18(1H,d,J=16,H-8)。13C NMR(101 MHz,CD3OD):δ:169.67(C-9),159.76(C-4),145.25(C-7),129.68(C-2/6),125.85(C-1),115.42(C-3/5),114.40(C-8)。以上数据与文献报道[14]一致,故鉴定化合物8为糠酸。
化合物9:无定型粉末。ESI-MS(m/ z ):165.0521([M+H]+)。1H NMR(400 MHz,CD3OD):δ:7.49(2H,d,J=8.5,H-2/6),6.72(1H,d,J=12,H-7),6.65(1H,d,J=8.5,H-3/5),5.66(1H,d,J=12,H-8)。13C NMR(101 MHz,CD3OD):δ:169.62(C-9),157.98(C-4),142.61(C-7),132.23(C-2/6),126.36(C-1),115.98(C-8),114.37(C-3/5)。以上数据与文献报道[14]一致,故鉴定化合物9为反式-4-羟基肉桂酸。
化合物10:无定型粉末。ESI-MS(m/z):336.1721([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.16(1H,s,H-2),5.76(1H,q,J=7.2,H-20),5.35(1H,d,J=11.6,H-9),5.26(1H,s,H-7),4.94(1H,s,H-8),4.32(1H,m,H-3),4.14(1H,d,J=11.6,H-9),3.80(1H,m,H-3),3.05(1H,m,H-5),2.48(1H,m,H-6),2.39(1H,m,H-6),2.15(1H,m,H-14),1.75(3H,d,J=7.2,CH3-21),1.72(1H,m,H-14),1.59(1H,m,H-13),1.29(3H,s,CH3-18),0.79(3H,d,J=7.4,CH3-19)。13C NMR(101 MHz,CD3OD):δ:176.78(C-11),166.78(C-16),135.46(C-20),132.55(C-2),132.39(C-1),130.66(C-15),77.97(C-8),76.80(C-12),73.43(C-7),60.90(C-3),57.94(C-9),52.82(C-5),38.60(C-13),37.95(C-14),33.71(C-6),23.81(C-18),13.89(C-21),9.74(C-19)。以上数据与文献报道[15]一致,故鉴定化合物10为千里光宁碱。
化合物11:无定型粉末。ESI-MS(m/z):376.1682([M+H]+)。1H NMR(400 MHz,CD3OD):δ:6.07(1H,s,H-2),5.98(1H,q,J=7.2,H-20),5.30(1H,s,H-7),5.21(1H,s,H-19),4.97(1H,s,H-19),4.65(1H,d,J=11.6,H-9),4.99(1H,s,H-8),4.44(1H,d,J=11.6,C-9),4.35(1H,m,H-3),3.86(1H,m,H-3),3.81(1H,m,H-5),3.25(1H,m,H-14),3.07(1H,m,H-5),2.87(1H,m,H-14),2.33(1H,m,H-6),1.98(3H,d,J=7.2,CH3-21),1.82(3H,s,H-23),1.65(3H,s,CH3-18)。13C NMR(101 MHz,CD3OD):δ:170.24(C-11),169.86(C-22),166.20(C-16),145.45(C-13),137.67(C-20),131.46(C-2),130.76(C-1),130.72(C-15),114.97(C-19),82.65(C-12),77.67(C-8),72.86(C-7),60.35(C-3),58.75(C-9),53.35(C-5),36.73(C-14),33.41(C-6),20.65(C-18),19.81(C-21),14.29(C-23)。以上的数据与文献报道[16]一致,因此鉴定化合物11为乙酰化千里光菲林碱。
2 结果与讨论
化合物3为新化合物,无定型粉末。质谱数据给出[M+Na]+=279.0841,可确定该化合物的分子式为C12H16O6,不饱和度为5。1H NMR谱数据给出3个烯烃氢信号,分别为[δ(H)5.98(1H,d,J=6.8,H-2),5.21(1H,s,H-10),4.86(1H,s,H-10)],2个亚甲基氢信号[δ(H)3.02(2H,s,H-4)],9个甲基氢信号[δ(H)1.91(3H,d,H-1),1.62(3H,s,H-9),1.97(3H,s,H-12)]。
13C NMR谱图显示化合物共12个碳,与高分辨数据对应。13C NMR数据给出1个烯烃上的次甲基和亚甲基信号δ(C)138.64(C-2)和111.61(C-10),1个亚甲基信号δ(C)35.54(C-4),3个甲基信号δ(C)20.94(C-12),19.84(C-9),14.55(C-1),3个羰基信号δ(C)172.39(C-7),170.04(C-11),169.53(C-8),2个烯烃季碳信号δ(C)146.38(C-5)和130.56(C-3),1个季碳信号δ(C)82.98(C-6)。
如表1所示,通过结合13C NMR和HSQC数据可以更进一步的确定C-H关系:δH 5.20(1H,s,H-10),4.86(1H,s,H-10)为末端烯烃双氢,1个孤立的亚甲基信号δH 3.02(2H,s,H-4),1个与次甲基耦合的甲基信号δH 1.91(3H,d,J=6.8,CH3-1),2个甲基信号δH 1.97(1H,s,CH3-12)和1.62(3H,s,CH3-9)。
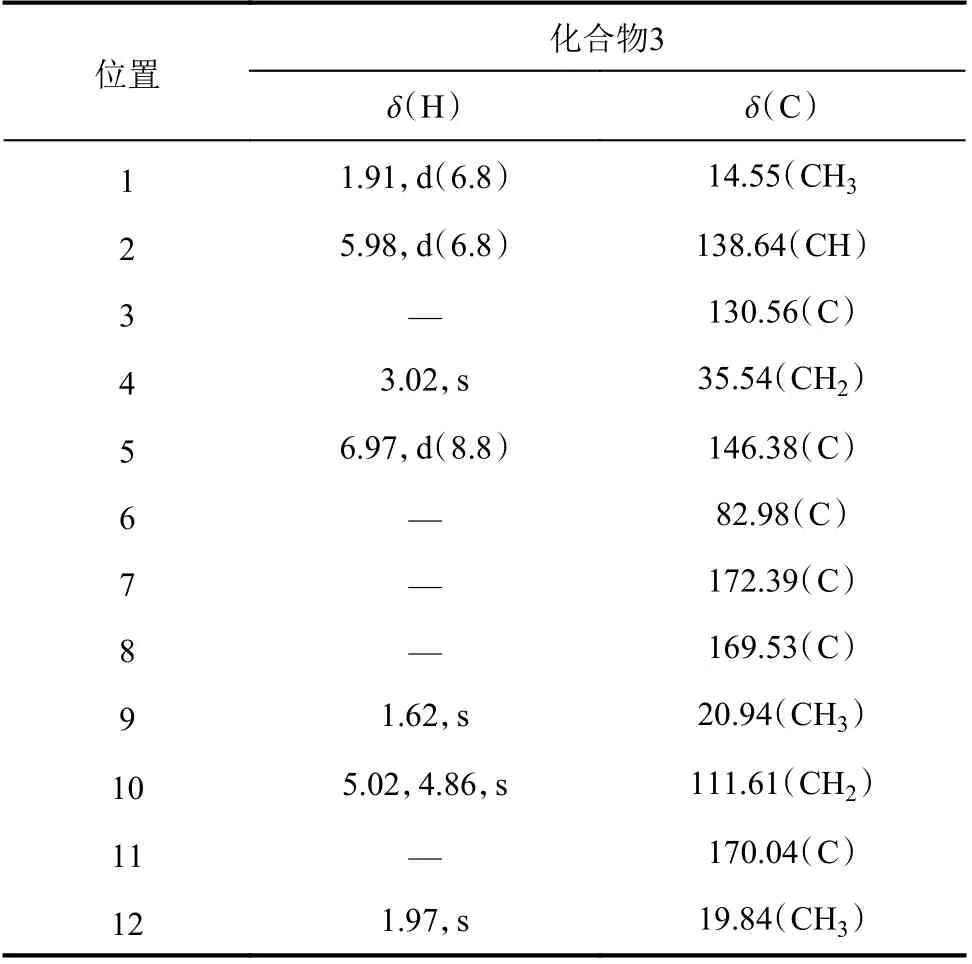
表1 化合物3的核磁数据Tab.1 NMR spectral data of compound 3
如图2所示,根据COSY谱可以推断C-2位烯烃与C-1位甲基具有相关性,在HMBC谱中,4-H和5-C、6-C、3-C、8-C以及10-C、2-C,1-C均相关,2-H和1-C、3-C,4-C、5-C、8-C相关,10-H与5-C、6-C、7-C相关,9-H与7-C、6-C、5-C相关,12-H与11-C相关,根据以上分析可以知道该化合物结构与已知化合物4的骨架相似,可以推测出该化合物的基本碳骨架为―CO―C-(=CH―CH3)―CH2―C(=CH2)―C(CH3,CH3COO)―CO―,再结合该化合物的分子式可以推断该化合物结构。
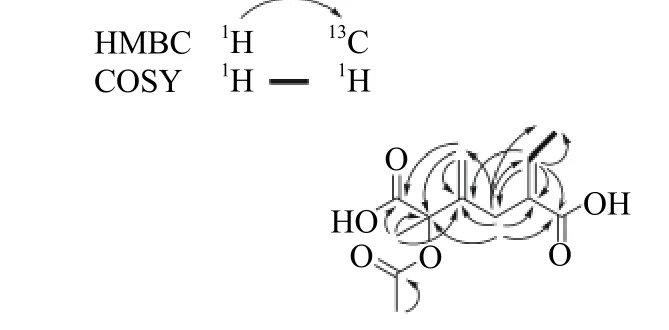
图2 化合物3的2D-NMR耦合信息Fig.2 2D-NMR correlationsof compound 3
根据表1,C-2烯烃质子(1H,d,J=6.8 Hz)可推测C-2和C-3之间的烯烃为Z型。根据以上的分析,可以知道该化合物的结构如图3所示,命名为顺式-6-甲基-5-亚甲基-3-亚乙基-6-乙酰氧基己二酸。
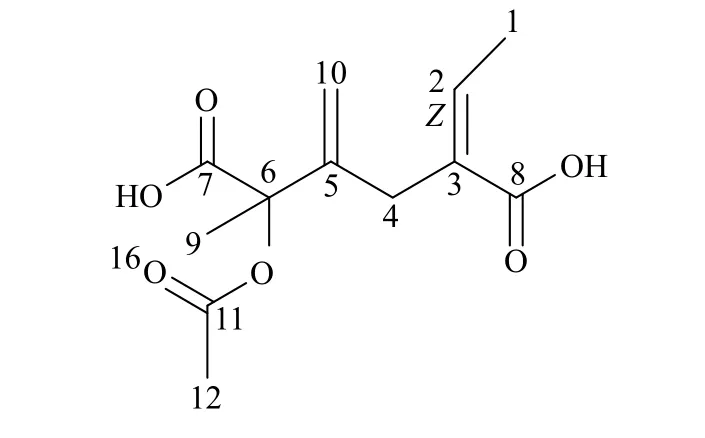
图3 化合物3结构Fig.3 Structureof compound 3
3 结 论
综合运用多种现代色谱分离纯化技术和波谱鉴定技术,从土田七中分离、鉴定出11个化合物,其中化合物3为新化合物顺式-6-甲基-5-亚甲基-3-亚乙基-6-乙酰氧基己二酸,丰富了土田七植物的化学成分研究,为土田七植物的使用和开发提供参考。

