基于TCGA和GEO数据挖掘分析PRC1在肺腺癌中的表达及预后意义
刘细帮 胡旭钢 唐夏莉 陈清勇
肺癌是全球发病率和死亡率最高的恶性肿瘤。肺腺癌(lung adenocarcinoma,LUAD)是肺癌最常见的病理亚型,患者5年平均生存率仅为15%[1-2]。尽管近年来诊断和治疗方法不断改进,但LUAD患者的总体生存率并未提高。因此,有必要寻找新的预后生物标志物,这不仅有助于改善个体化治疗,还能为开发新的治疗靶点提供参考。胞质分裂蛋白调节因子1(protein regulator of cytokinesis 1,PRC1)基因位于人体15号染色体上(15q26.1),编码含有620个氨基酸的蛋白;属于微管相关蛋白家族,参与细胞有丝分裂和细胞周期调控[3]。研究发现,PRC1 是乳腺癌[4]、膀胱癌[5]、肝细胞癌[6]和胃癌[7]等肿瘤的致癌因子,并且PRC1的表达与LUAD细胞的增殖、侵袭和凋亡相关,可能是LUAD潜在的治疗靶点[8-9]。但目前PRC1对LUAD患者总体预后影响的相关研究较少。本研究旨在通过对公共数据库的挖掘,分析PRC1 mRNA表达水平与LUAD患者总体预后的相关性,探讨其作为LUAD预后标志物的可行性,为今后有关PRC1的机制研究提供一定的理论基础。
1 材料和方法
1.1 PRC1数据的获取 33种肿瘤数据来自肿瘤免疫评估资源(tumor immune estimation resource,TIMER)数据库(https://cistrome.shinyapps.io/timer/),通过 Diff Exp模块检索PRC1在肿瘤组织与正常对照组织中的表达情况。通过肿瘤基因图谱(the cancer genome atlas,TCGA)数据库(https://portal.gdc.cancer.gov/)获取 PRC1表达的RNASeq数据,获得的数据中包含517例原发性LUAD患者和59例正常肺组织,其中504例LUAD患者记录了生存数据,并以PRC1 mRNA表达的中位数分为高表达组和低表达组。利用基因表达综合(gene expression omnibus,GEO)数据库(https://www.ncbi.nlm.nih.gov/geo)分别下载包含LUAD组织及正常对照组织或癌旁正常组织的基因表达谱芯片数据集GSE31210、GSE75037和 GSE68465,其中 GSE31210、GSE68465 数据集各包含226、362例LUAD患者完整的临床资料以及生存信息,并以PRC1 mRNA表达的中位数分为高表达组和低表达组。同时,从人类蛋白质图谱(human protein atlas,HPA)数据库(https://www.proteinatlas.org/)获取肿瘤以及正常对照组织中PRC1蛋白免疫组化染色数据。
1.2 基因集富集分析(gene set enrichment analysis,GSEA)采用GSEA 4.0进行分析。根据TCGA数据库中PRC1 mRNA表达的中位数分为高表达组和低表达组,以Hallmark基因集作为参考基因集,通过GSEA分析PRC1参与LUAD发展的可能机制,设置置换次数为1 000次,以P<0.05、错误发现率(false discovery rate,FDR)<0.25为显著富集基因集。
1.3 统计学处理 采用R 3.6和GraphPad 8.0统计软件。计量资料以表示,两组比较采用两独立样本t检验或配对t检验;多组比较采用单因素方差分析。生存曲线分析采用Kaplan-Meier法,组间比较采用log-rank检验。采用R软件ROC的时间序列分析(timeROC)包绘制ROC曲线并计算AUC值。Cox回归模型分析PRC1与LUAD患者总生存期(overall survival,OS)、无进展生存期(progression-free survival,PFS)的关系,并计算HR值及其95% CI。P≤0.05为差异有统计学意义。
2 结果
2.1 肿瘤组织中PRC1 mRNA表达 在TIMER数据库提供的33种肿瘤数据中,膀胱尿路上皮癌(bladder urothelial carcinoma,BLCA)、乳腺浸润癌(breast invasive carcinoma,BRCA)、胆管癌(cholangiocarcinoma,CHOL)、结肠癌(colon adenocarcinoma,COAD)、食管癌(esophageal carcinoma,ESCA)、头颈鳞状细胞癌(head and neck squamous cell carcinoma,HNSC)、肾嫌色细胞癌(kidney chromophobe,KICH)、肾透明细胞癌(kidney renal clear cell carcinoma,KIRC)、乳头状肾细胞癌(kidney renal papillary cell carcinoma,KIRP)、肝细胞肝癌(liver hepatocellular carcinoma,LIHC)、LUAD、肺鳞癌(lung squamous carcinoma,LUSC)、胰腺癌(pancreatic adenocarcinoma,PRAD)、直肠腺癌(rectum adenocarcinoma,READ)、胃癌(stomach adenocarcinoma,STAD)、甲状腺癌(thyroid car-cinoma,THCA)、子宫内膜癌(uterine corpus endometrial carcinoma,UCEC)17种肿瘤组织中PRC1 mRNA表达水平均高于正常对照组织,见图1。

图1 肿瘤组织中胞质分裂蛋白调节因子1(PRC1)表达
2.2 LUAD组织和正常对照组织中PRC1的表达 在TCGA数据库和GSE31210数据集中,LUAD组织中PRC1 mRNA表达水平均明显高于正常对照组织,差异均有统计学意义(均P<0.01),见图2a-b。在GSE75037数据集中,LUAD组织中PRC1 mRNA表达水平明显高于癌旁正常组织,差异有统计学意义(P<0.01),见图2c。在HPA数据库中,PRC1免疫组化染色结果显示,PRC1蛋白在正常对照组织中弱表达,而在LUAD组织中强表达,见图2d-e。

图2 肺腺癌(LUAD)组织和正常对照组织中胞质分裂蛋白调节因子1(PRC1)的表达[a-b:肿瘤基因图谱(TCGA)数据库、GSE31210数据集中LUAD组织和正常对照组织中PRC1 mRNA表达水平比较,与正常对照组织比较,**P<0.01;c:GSE75037数据集中LUAD组织和癌旁正常组织中PRC1 mRNA表达水平比较,与癌旁正常组织比较,**P<0.01;d-e:正常对照组织和LUAD组织中PRC1蛋白表达的比较,免疫组化染色,×40]
2.3 PRC1 mRNA表达水平与LUAD患者临床特征的关系 通过TCGA数据库分析发现PRC1 mRNA表达水平与LUAD患者的年龄、M分期均无关(均P>0.05),但与LUAD患者的性别、吸烟、T分期、N分期和TNM分期均有关(均P<0.01),见表1。

表1 TCGA数据库中不同临床特征LUAD患者PRC1表达水平比较
2.4 PRC1 mRNA表达与LUAD预后的关系
2.4.1 PRC1 mRNA表达与OS和PFS的关系 在TCGA数据库、GSE31210和GSE68465数据集中,通过Kaplan-Meier生存曲线分析发现,除GSE68465数据集中的PFS外,其余PRC1高表达组患者PFS和OS均差于低表达组(均 P<0.05),见图 3(插页)。
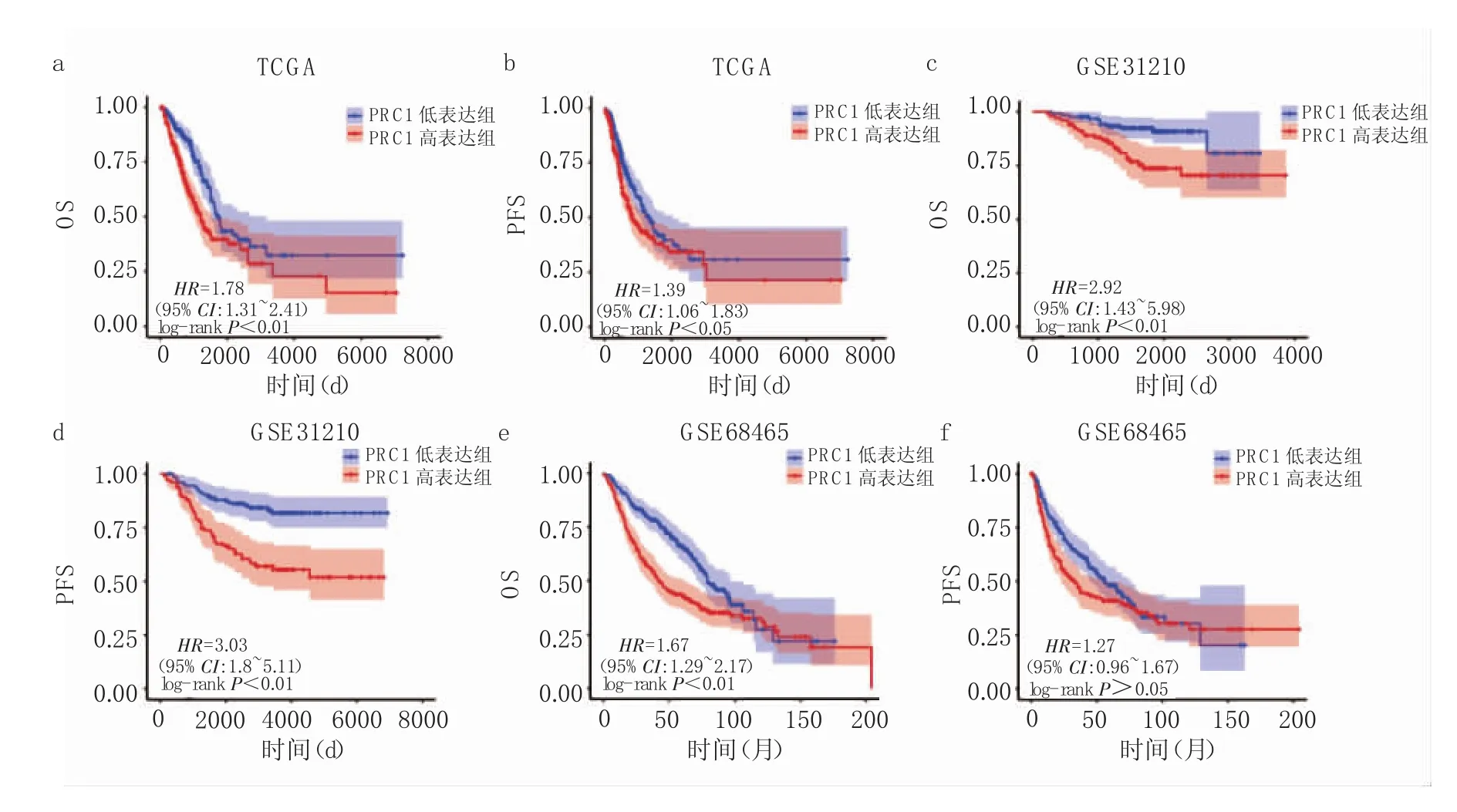
图3 胞质分裂蛋白调节因子1(PRC1)表达与总生存期(OS)和无进展生存期(PFS)的关系[a-b:肿瘤基因图谱(TCGA)中PRC1高表达组与低表达组OS和PFS生存曲线比较;c-d:GSE31210数据集中PRC1高表达组与低表达组OS和PFS生存曲线比较;e-f:GSE68465数据集中PRC1高表达组与低表达组OS和PFS生存曲线比较]
2.4.2 影响LUAD患者预后的临床特征分析 在TCGA数据库中,ROC曲线模型的OS显示,1、3、5年生存率AUC值分别为0.674、0.632、0.590;ROC曲线模型的PFS显示,1、3、5年生存率 AUC 值分别为 0.611、0.583、0.506,见图4a-b。单因素Cox回归分析结果显示LUAD患者的性别、年龄和吸烟与OS均无关(均P>0.05),但T分期、N分期、TNM分期和PRC1 mRNA表达水平与OS均有关(均P<0.05);单因素Cox回归分析结果显示LUAD患者的性别、年龄、TNM分期和吸烟与PFS均无关(均P>0.05),但T分期、N分期和PRC1 mRNA表达水平均与PFS均有关(均P<0.05)。将以上所有单因素纳入多因素Cox回归分析显示,T分期、N分期和PRC1 mRNA表达水平均是影响LUAD患者OS和PFS的独立危险因素(均P≤0.05),见图4c-f。

图4 影响肺腺癌(LUAD)患者预后的临床特征分析[a-b:肿瘤基因图谱(TCGA)数据库中总生存期(OS)和无进展生存期(PFS)的ROC曲线;c-d:TCGA数据库中OS单因素和多因素Cox分析;e-f:TCGA数据库中PFS单因素和多因素Cox分析]
2.5 GSEA识别与PRC1相关的信号通路 为了确定PRC1作用的潜在信号通路,在TCGA数据库中,GSEA分析结果显示,PRC1高表达样本富集在有丝分裂纺锤体、G2M检查点、E2F信号通路、DNA修复等基因集中,见图5。

图5 基因集富集分析(GSEA)识别与胞质分裂蛋白调节因子1(PRC1)相关的信号通路
3 讨论
细胞周期是哺乳动物细胞生长和发育所必需的进化保守过程,因为细胞周期畸变是癌症的标志[10]。PRC1被认为是细胞周期蛋白依赖性激酶(CDK)底物,在早期细胞分裂中,是维持纺锤体中段所需的微管相关蛋白[11-12]。细胞分裂是一个复杂的过程,涉及复杂的生化和细胞动力学因素[10],而PRC1作为细胞分裂的关键蛋白,其表达异常可引起细胞分裂的紊乱。研究表明,PRC1的过表达通过调节Wnt信号通路促进肝癌细胞增殖和转移,并与早期复发和患者预后不良相关[6]。敲除PRC1可显著抑制胃癌细胞增殖,减少胃癌细胞克隆形成并抑制其侵袭和迁移[7]。但是,目前PRC1在肺癌的发生、发展机制方面的研究较少,尤其是与患者临床预后生存及标志物筛查的研究鲜有报道。
本研究中,笔者通过对多个大样本数据库进行分析发现,PRC1的表达水平在包括LUAD在内的多种肿瘤组织中上调,LUAD组织中PRC1表达也明显高于正常对照组织和癌旁正常组织;且免疫组化结果提示,LUAD组织中PRC1蛋白表达水平明显高于正常对照组织。在TCGA数据库和GSE68465数据集中,PRC1表达与肿瘤的T分期、N分期和TNM分期均有关,提示PRC1可能参与LUAD的进展。基于多个数据库的生存分析结果,表明PRC1 mRNA表达水平与LUAD患者的PFS、OS呈负相关,其表达水平越高,LUAD患者预后越差。并且该结果与Bu等[13]研究结果类似,该研究发现在卵巢癌组织PRC1呈高表达,并且PRC1的表达与生存时间呈负相关。
单因素及多因素Cox回归分析显示,T分期、N分期和PRC1 mRNA表达水平均是影响LUAD患者的独立危险因素。为了进一步探讨PRC1在LUAD中的潜在功能,GSEA分析结果表明,在有丝分裂纺锤体、G2M检查点、E2F信号通路、DNA修复等通路高度富集。G2M检查点能在DNA损伤的情况下阻止细胞周期,使细胞在进入下一个细胞周期阶段前修复DNA损伤,从而维持基因组完整性[14]。因此,PRC1过表达时可能通过影响细胞周期和DNA修复,从而促进LUAD细胞的增殖分化。CDK-RB-E2F轴是细胞周期进程的核心转录机制,该轴的一个或多个关键组成部分的变化几乎发生在所有肿瘤中,并导致致癌E2F活性增强,使肿瘤细胞增殖不受控制,进而导致肿瘤进展[15]。而PRC1作为CDK底物,过表达时可能促进该轴的转录,进一步增加E2F活性,导致肿瘤进展。由此可见,PRC1可能参与LUAD发生、发展过程,可能是LUAD治疗的潜在靶点。
综上所述,PRC1基因在LUAD中可能是一个潜在的致癌基因。PRC1在LUAD中的表达与肿瘤的发生、发展以及患者的预后有着非常密切的关系,可作为一个重要的候选生物标志物。因此,有必要对该基因在LUAD中的机制以及功能进一步研究,为全面掌握PRC1在肿瘤中的作用以及LUAD的预防诊治提供更多依据。

