尼可地尔对缺血性心力衰竭大鼠心功能的保护作用及机制
邢晓娜, 刘利君, 何元军
(四川省广元市中心医院 心脏血管中心, 四川 广元, 628017)
尼可地尔是具有硝酸盐性质的ATP敏感性钾离子通道开放剂,适用于各类型心绞痛[1], 能显著降低心血管事件的发生风险,可对心脏病患者的心脏起保护作用[2]。研究[3]认为,尼可地尔可减少冠心病患者心脏重构的发生发展,降低缺血性心力衰竭患者的死亡率[4]。心室重构是指各种损伤使心脏原来存在的物质和心脏形态学发生变化,是机体的一种适应性反应,也是病变修复和心室整体代偿继发的病理生理反应过程[5]。但是,关于尼可地尔是否能抑制缺血性心力衰竭的左室重构及其机制尚未明确。本研究探讨尼可地尔对缺血性心力衰竭大鼠心功能和左室重构的影响和机制,现报告如下。
1 资料与方法
1.1 实验动物
40只雄性SD大鼠,体质量160~200 g, 购于中国食品药品检定研究院[(生产许可证号: SCXK(京)2019-0017)]。尼可地尔购于长春大政药业科技有限公司(国药准字H22024008)。将40只大鼠随机分为4组,每组10只。① 空白对照组(Con组): 不进行任何手术干预,仅给予等体积、等时间生理盐水灌胃。② 尼可地尔组(NIC组): 麻醉满意后,采用Johns法建立大鼠缺血性心力衰竭模型。麻醉大鼠后,打开胸腔,在无菌手术条件下分离心包,然后抬起左耳廓,心脏被挤出。在大约1/3的下端结扎左冠状动脉前降支。从尾部记录每只大鼠的收缩压、舒张压和心率,对每个参数进行3次测量。术后3 d至8周末,给予尼可地尔3 mg/kg·d灌胃。③ 生理盐水组(NS组): 手术方式同NIC组,但给予等体积、等时间生理盐水灌胃。④ 假手术组(Sham组): 在不结扎冠状动脉的情况下行开胸手术,灌胃生理盐水。术后8周对各项指标进行评估,记录体重、呼吸模式、活动量和毛色。
1.2 超声心动图
术后8周所有大鼠均行超声心动图检查。麻醉满意后,仰卧位固定,胸部备皮,测量室间隔收缩末期厚度(IVSS)、室间隔舒张末期厚度(IVSd)、左室收缩末期内径(LVIDs)、左室舒张末期内径(LVIDd)、左室收缩末期后壁厚度(LVPWs)和左室舒张末期后壁厚度(LVPWd)。用Teichholtz方程计算左心室射血分数(LVEF)和左心室短轴收缩分数(LVFS),并计算左心室舒张末期容积(LVEDV)和左心室收缩末期容积(LVESV)。大鼠手术后LVEF均低于50%, 提示心力衰竭。
1.3 左心室重量和肺重的测定
实验结束后,测量心脏和左心室重量,计算左心室/体重比值(LVW/BW), 评价左心室肥厚程度。取肺称重,计算肺脏重量指数(LUNGW/BW)作为充血指标。
1.4 组织病理学检查
处死大鼠后,提取左心室前壁组织。部分组织在液氮中快速冷冻,然后保存在-80 ℃以备分析。甲醛固定和石蜡包埋,切成4 μm的切片,烤片,冷却后低温冻存。经二甲苯脱蜡,乙醇梯度水化。苏木精染色30~60 s, 冲洗5 min, 伊红染色30 s, 冲洗5 min; 乙醇梯度脱水,干燥,二甲苯透明,中性树胶封固,晾干,光学显微镜下观察。其余组织采用戊二醛-锇酸双重固定,脱水,使用前置于-80 ℃中保存。在电镜下进行心肌超微结构观察。
1.5 Western blot检测
在组织裂解缓冲液中提取蛋白并测定蛋白浓度。从每个样品中分离等量的蛋白质(40 μg), 并将其电转移到PVDF膜上。5%的BSA封闭,与一抗在4 ℃孵育过夜。洗膜3次后,将膜与HRP偶联二抗孵育。使用标准ECL检测条带,并使用Image J软件通过密度分析进行定量。
1.6 统计学分析
2 结 果
2.1 尼可地尔改善缺血性心力衰竭大鼠的一般情况
NS组大鼠除了呼吸急促甚至喘息外,还表现出活动减少和神经松解,体重减轻,毛发颜色暗淡。NIC组大鼠的活动量、体重和整体健康状况明显好于NS组。术后8周, Con组、Sham组、NS组、NIC组体重分别为(486.70±29.30)g、(478.40±28.30)g、(369.85±47.26)g、(426.85±51.22)g, NS组体重最低, NIC组次之。
2.2 尼可地尔对缺血性心力衰竭大鼠的降压作用
术后8周末, NIC组收缩压和和舒张压分别为(126.3±6.9)mmHg、(94.0±6.2)mmHg, 均明显低于NS组的(141.7±10.1)mmHg、(103.1±5.9)mmHg的和Sham组的(159.6±11.3)mmHg、(113.1±8.5)mmHg, 差异有统计学意义(P<0.05)。NS组收缩压(141.7±10.1)mmHg明显低于Sham组(159.6±11.3)mmHg和Con组(150.8±10.2)mmHg, 差异有统计学意义(P<0.05)。Sham组舒张压(113.1±8.5)mmHg与NS组(103.1±5.9)mmHg相比,差异无统计学意义(P>0.05)。
2.3 尼可地尔改善缺血性心力衰竭大鼠的心功能
与Con组及Sham组相比, NS组及NIC组LVEF、E/A均降低,且NS组LVEF低于NIC组,差异有统计学意义(P<0.05)。LVEDV则呈相反趋势,3组间存在差异, NS组LVEDV最高,差异有统计学意义(P<0.05)。NS组LVESV、LVIDd和LVIDs高于NIC组和Sham组,差异有统计学意义(P<0.05)。NIC组和Sham组之间相关指标水平比较,差异无统计学意义(P>0.05)。各组大鼠的IVSd水平比较,差异无统计学意义(P>0.05)。见表1、图1。

表1 各组大鼠超声心动图指标水平比较
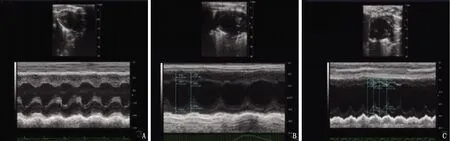
A: Sham组; B: NS组; C: NIC组
2.4 尼可地尔对缺血性心力衰竭大鼠左心室肥厚、纤维化和肺充血的影响
HE染色及电镜下观察结果均显示, Sham组大鼠心肌细胞排列规则,横纹清晰; NS组心肌细胞排列紊乱,形状不规则,还表现出明显的纤维组织增生。与NS组相比, NIC组的这些异常明显减弱,心肌纤维结构趋于正常。Sham组和NIC组LVW/BW和LUNGW/BW均明显低于NS组,差异有统计学意义(P<0.05)。见表2、图2。

表2 各组大鼠LVW/BW和LUNGW/BW比较
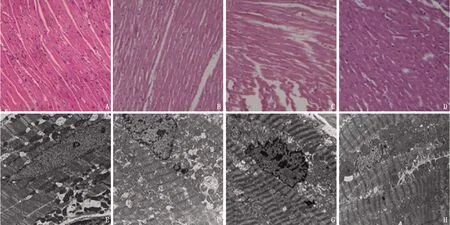
A、E: Con组; B、F: Sham组; C、G: NS组; D、H: NIC组。
2.5 尼可地尔对大鼠心肌Akt/Bcl-2/Bax信号通路的影响
Western blot检测显示,与Con组及Sham组相比, NS组p-Akt、Bcl-2及Bax蛋白相对表达量增加,差异有统计学意义(P<0.05)。与NS组相比, NIC组p-Akt、Bcl-2蛋白相对表达量更高,但Bax蛋白表达量下降,差异均有统计学意义(P<0.05)。见图3。
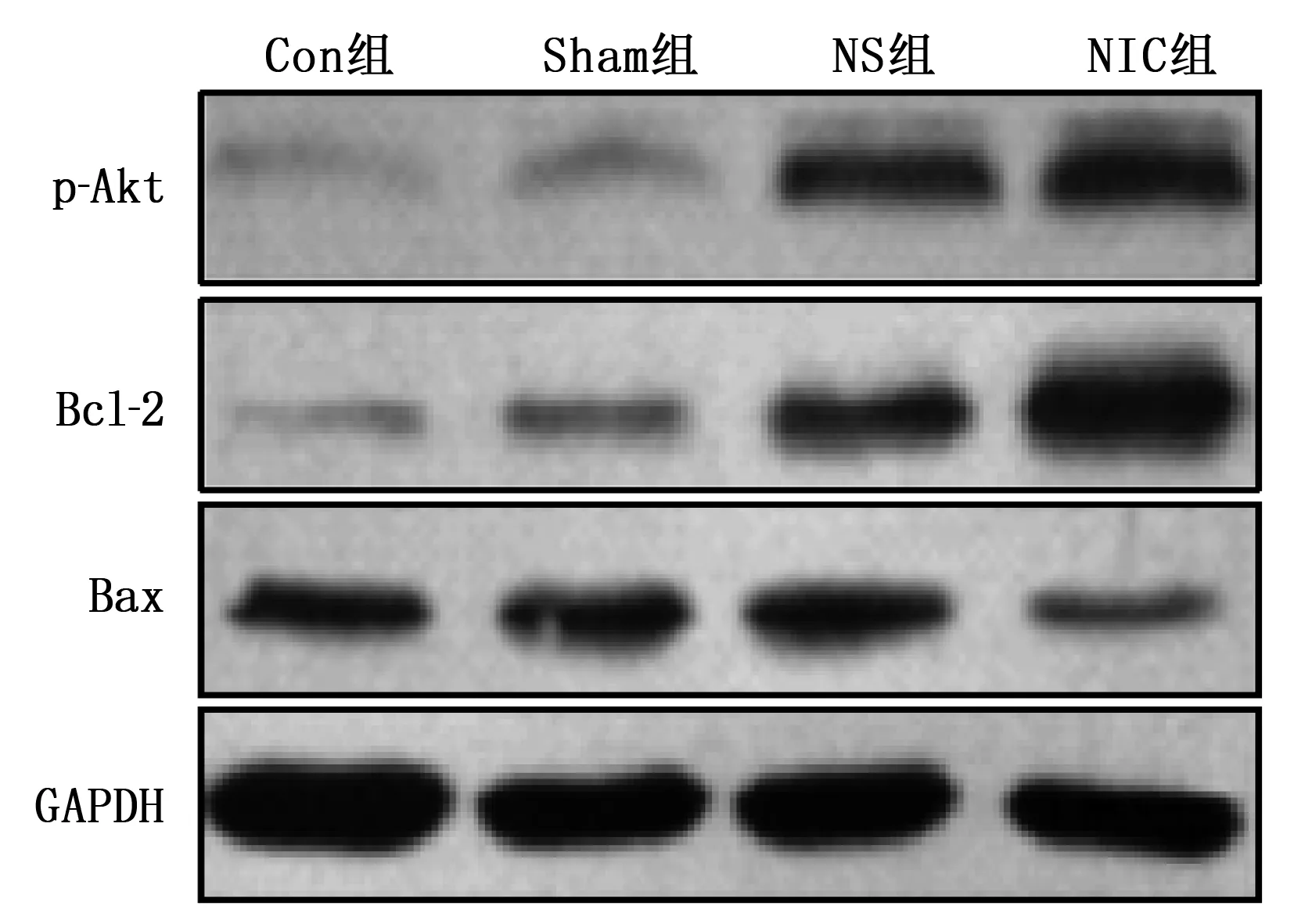
图3 4组p-Akt/Bcl-2/Bax蛋白水平表达图
3 讨 论
尼可地尔是第一种ATP依赖性钾通道开放剂,作为一种新型血管扩张剂在临床实践中表现出独特的优势。尼可地尔具有双重的血管扩张机制[6],通过刺激血管平滑肌细胞中的鸟苷酸环化酶起到硝酸酯类的作用,导致冠状动脉血流量增加和静脉扩张[7]。此外,尼可地尔是一种ATP敏感性钾通道开放剂,可引起血管平滑肌和线粒体钾离子外流,使细胞电位超极化,诱导电压门控钙通道失活,减少细胞内游离钙离子[8],松弛冠状动脉和阻力血管,增加流向心肌的血流量。尼可地尔还可扩张全身阻力和容量血管,降低心脏前负荷和后负荷以及心肌耗氧量,缓解冠状动脉痉挛,增加侧支循环和心内膜下血供[9]。本研究发现尼可地尔可改善缺血性心力衰竭大鼠的心功能,并在正常范围内降低血压。
研究[10]表明,尼可地尔不仅能缓解缺血性心脏病的症状,还能抑制冠心病患者的心肌肥大和重塑。心力衰竭是最常见的心源性死亡原因,心脏重构在其发生发展中起重要作用[11]。本研究结果发现,尼可地尔改善了缺血性心力衰竭大鼠的一般情况,且提高了LVEF、LVFS和E/A,降低了LVEDV、LVESV、LVIDd和LVIDs水平,改善了缺血性心力衰竭大鼠的左室收缩功能。尼可地尔干预后大鼠LVW/BW和LUNGW/BW比值也显著低于NS组大鼠。本研究组织学观察结果显示, Sham组心肌细胞排列规则,横纹清晰; Con组排列紊乱,形状不规则,左心室心肌组织呈明显的纤维组织增生; NIC组心肌细胞的这些病理改变不那么明显,而且较少出现增生。这提示尼可地尔可改善缺血性心力衰竭时的心功能和左室重构。
尼可地尔的保护机制尚未阐明。RAAS系统激活、氧化应激和心肌内钙超载在心力衰竭的发生发展中起重要作用,其中钙超载对心功能影响最大[12]。尼可地尔可以开放线粒体中的钾通道,抑制氧化应激诱导的心肌细胞凋亡。研究[13]表明,尼可地尔作为NO供体,可能通过激活有丝分裂钾通道和NO/可溶性鸟苷酸环化酶依赖机制来抑制氧化应激或高氧诱导的心肌细胞凋亡。此外,尼可地尔已被证明与凋亡相关蛋白的调节有关。Bcl-2与Bax共属于一个家族,通过控制线粒体膜的通透性来调节凋亡激活物。bax二聚体在膜上打开通道,增加细胞膜通透性; bcl-2与bax可形成异聚体,降低细胞通透性[14]。bcl-2水平的升高和bax的降低表明细胞对凋亡的抵抗性增强,为保护药物发挥作用的标志。本研究中,尼可地尔抑制缺血性心力衰竭引起的大鼠心肌Bax水平的上调,提示尼可地尔对缺血性心力衰竭大鼠的心脏保护作用可能是通过抑制Bax的表达来实现的。鉴于Bax的促凋亡作用,推测尼可地尔的保护作用可能参与控制缺血性心力衰竭大鼠的凋亡过程。
综上所述,本研究发现,尼可地尔通过改善心功能和左室重塑对缺血性心力衰竭大鼠起到保护作用,其机制可能与尼可地尔抑制Bax蛋白表达有关。

