病毒预防环境下的《氯气》“生活化”教学设计
李先栓
(宿迁高等师范学校,江苏 宿迁 223800)
教育家陶行知先生在他的“生活教育”中提出“生活即教育, 用生活来教育,为生活而教育”;“化学——我们的生活,我们的未来”,“国际化学年”的主题思想揭示化学教学应更多联系化学与生活、关注化学与未来,培养学生情感态度与价值观,提高学生科学素养,培养学生利用化学知识解决生活问题、探讨社会决策的意识等。《氯气》“生活化”教学设计,突出新冠肺炎病毒预防新环境下的实践应用,充分体现化学教学的生活教育作用。
1 设计策略
中职学校化学教学注重学生的参与互动,教学设计体现动手、动脑、动口的相互交流合作;注重教学理论联系生活实际,使学生在兴趣和实用中了解化学,在过程中体验、学会学习方式,训练思维能力;重视化学在生活中的应用,警惕化学物质在生活中的不法使用,提高小学教师的化学素养,通过他们,教育幼年儿童从小认识生命的重要意义,关注社会健康,实现衣食住行方面的自我保健,从而实现全民的科学素养。
新冠肺炎病毒预防环境下情境导入的策略:
①导入新课“生活化教学设计”:新冠肺炎病毒预防环境下你使用过84消毒液进行环境消毒吗?生活中还有哪些方面使用到84消毒液?
②氯气物性“生活化教学设计”:打开84消毒液瓶会闻到刺激性难闻的气体,这是氯气的气味,微溶于水(2 VCl2/VH2O);氯气毒性:第一次世界大战第一次使用的化学武器——氯气。
③课题理解“生活化教学设计”:“富集在海水中的元素——氯”:海水如何富集盐——趣味地理资料“死海”。
④氯气和金属Na反应“生活化教学设计”:生活中的NaCl——食盐,加碘盐。
⑤氯气和非金属H2反应“生活化教学设计”:生活中的盐酸——洁厕灵、胃酸。
⑥氯气与水和碱反应“生活化教学设计”:生活中氯气与水或碱的反应——自来水消毒和84消毒液;生活实践与就业指导——自制“84消毒液”;如何正确使用84消毒液?使用84消毒液预防新冠病毒,高浓度下可引起肺水肿。84消毒液不能用于空气消毒。
2 教学设计
2.1 教学目标
2.2.1 知识与技能
①通过科学推测、实验探究、归纳出氯气单质的物理性质和化学性质,认识氯气的性质在生活中的应用;
②培养学生联网搜寻技能,学会探究,培养创新能力。
2.2.2 策略与方法
①通过引导发现、联网搜寻、实验探究、合作学习的过程,体验科学探究的方法,同时强化合作能力;
②在学习过程中培养学生的学习方式,训练学生的思维、推理及归纳总结能力。
2.2.3 情感态度与价值观
①通过“氯气的发现及确认过程”,体会科学探究艰辛和喜悦的过程,树立不畏艰难的科学探究精神,并同时加强环保意识,强化团队精神;
②使学生进一步明确化学是一门以实验为基础的科学,增强亲身实践的意识,保持不断探索的兴趣,形成勇于探究的习惯。
2.2 教学重、难点
(1)重点:氯气的化学性质:氯气与水和碱的反应。
(2)难点:认识次氯酸的强氧化性、氯气与水和碱反应的化学方程式难点化解。
2.3 教学手段、方法
多媒体教学,运用探究法、对比法等化解难点。
2.4 教学过程
2.4.1 情境导入,生活中的氯:84消毒液、自来水消毒、食盐、胃酸等
[引导发现]你在新冠肺炎病毒预防环境下使用过84消毒液进行环境消毒?生活中还有哪些方面使用到84消毒液?
[生答]来客聚餐后的碗筷消毒、生吃水果洗涤消毒、白色衣物漂白洗涤等。
[引导发现]84消毒液使用中有什么感觉?
[生答]有刺激气味、引起咳嗽,有“烧手”的感觉。
[衔接]下面我们来学习84消毒液的生产、消毒原理和使用方法。
2.4.2 初试新知,氯气的物性
[引导发现]打开84消毒液瓶会闻到刺激性难闻的气体,这是氯气的气味,微溶于水(2 VCl2/VH2O)。
[课堂展示]氯气储气瓶。氯气的颜色:黄绿色气体(顾名思义:氯气绿色气体),刺激呼吸道粘膜产生粘液、引起咳嗽——毒气。
[生活化教学设计]学生搜寻:历史资料:第一次世界大战第一次使用的化学武器——氯气
[幻灯2]1915年4月22日上午,伊普尔(Ypres)前线德军阵地前沿宽6公里的战线上,英法联军看到德军阵地上突然出现的黄绿色烟雾,一种难以忍受的强烈刺激性怪味弄得英法官兵死去活来,先是打喷嚏、咳嗽,流泪不止,后来就觉得空气没有了,像是掉进了大闷罐中一样。不一会儿,一个个英法官兵窒息倒地。在这次毒气袭击中,英法联军有1.5万人中毒,至少有5000人死亡。
第二次Ypres战役:两天后,德军以同样方式用氯气攻击加拿大第一师的阵地。加拿大军得到医官的指示,在纱布、毛巾上撒尿,蒙在脸上隔着呼吸。尿液里的尿素和氯气发生化学作用(合成双氯尿素) 降低了氯气的效果。加拿大第一师就是这样撑住,直至英军其他的部队抵达增援。他们因为使用“尿布”这样简单的方法,所以,氯气直接导致的伤亡只有228名[2]。
[生]阅读课文“科学史话”,了解氯气的发现,感知、感悟科学探究艰辛和喜悦的过程。
[师]简介舍勒生平事迹,激励学生学习科学家热爱科学、追求科学、献身科学的精神
学生搜寻:化学史资料:舍勒(Karl Wihelm Scheele1742.12.19-1786.5.21)
[幻灯3]舍勒经常处于穷困之中,大量的实验工作是用简陋的仪器在寒冷的实验室中进行的。他还经常在夜里工作,这大大损害了他的健康,得了哮喘病,使他在1786年5月21日过早地病故了,终年仅44岁。舍勒一生发现的新物质有30多种,最为突出的贡献是发现氧气和氯气[3]。
[衔接]吸入氯气刺激呼吸道粘膜产生粘液、引起咳嗽——长期侵害得哮喘病?了解氯气的毒性原理。
2.4.3 探索应用,氯气的化性
2.4.3.1 与金属的反应
氯气可以和绝大多数的活泼或不活泼金属直接反应,生成相应的氯化物。如:
[生活化教学设计1]生活中的NaCl——食盐
学生搜寻:食盐
[幻灯4]国家法定盐业公司生产经营,包括海水制盐、开发岩盐、湖盐和天然卤水制盐等。
未经加碘的食用盐,不得进入碘缺乏病地区食用盐市场。
在农村,部分居民使用大粒粗盐腌制咸菜。从市场上购买低价的粗盐腌制咸菜很容易买到劣质的工业用盐,长期食用工业用盐腌制出的咸菜,容易因为亚硝酸盐而引起中毒[4]。
[生活化教学设计]2.课题理解:富集在海水中的元素——氯。
海水中最多的元素,海水中的盐的巨大储藏。地球表面70%的面积覆盖着海洋,海水中盐的含量占3.5%。如果把这些盐全部取出,平铺于地面,可使地面高度升高150米。海盐主要是NaCl及少量的MgCl2、MgSO4等。
[启发推测]海水如何富集盐?海水富集盐的含量是否在增加?
学生搜寻:海水如何富集盐趣味地理资料:死海
[幻灯片1]
死海位于约旦和以色列之间一个南北走向的大裂谷的中段,南北长80.4 km,东西最宽处17 km。深水中达到饱和的氯化钠沉淀为化石化。
湖水呈深蓝色,非常平静、富含盐类的水使人不会下沉或无法游泳。死海水的比重是1.17~1.227,而人体的比重只有1.02~1.097。游客可以手拿画报阅读,随波漂浮(图1)。死海——不能生长动植物的盐湖;死海——不能让人沉入淹死的海。

图1 湖水富含盐类游客随波漂浮
死海的海水富含矿物质,常在海水中浸泡,可以治疗关节炎等慢性疾病。富含矿物质的死海黑泥,由于健身美容的特殊功效,使它成为以色列和约旦两国宝贵的出口产品[1]。
多媒体展示海洋、海水晒盐图片或视频(略)。
[衔接]洁厕灵的主要成分是什么?
2.4.3.2 与非金属H2的反应
[视频1]实验1:制备氢气,在空气中点燃,然后将导管伸入氯气瓶中。
现象:纯净的氢气在氯气中安静地燃烧,发出苍白色火焰,集气瓶口形成白雾。
[用途]工业上利用食盐水电解产生的H2和Cl2生产盐酸HCl。
[自主建构]对比氢气在氧气、氯气中燃烧的现象,对燃烧的条件及其本质有何新的认识?
[幻灯5]燃烧的条件及其本质
①促燃物不一定是氧气,可燃物与氧化剂达到燃点即可燃烧。
②燃烧是反应剧烈的现象,具有发光(火焰)、发热或发烟的特征。
燃烧定义:任何发光发热的剧烈的氧化还原反应都叫燃烧。
[生活化教学设计2]洁厕灵的主要成分是盐酸,还有微量表面活性剂、香精等,能快捷有效地消灭卫生间臭味、异味,清洁空气。洁厕灵的使用原理是
MgCO3+2HCl═MgCl2+H2O+CO2↑
[生活化教学设计3]生活中的盐酸——胃酸
学生搜寻:胃酸
[幻灯4] 胃液中的胃酸(0.2%~0.4%的盐酸,pH约为0.9~1.5),杀死食物里的细菌,确保胃和肠道的安全,同时增加胃蛋白酶的活性,帮助消化。胃液对消化食物起着重要作用,正常胃液呈酸性,空腹时为20~100 mL,胃液分泌有一定的量,如分泌过多,就会出现吞酸、反胃、吐酸水等现象。
胃舒平,是由能中和胃酸的氢氧化铝和三硅酸镁两药合用,并组合解痉止痛药颠茄浸膏而成[5]。
[衔接] 为什么可以使用84消毒液环境消毒预防新冠病毒?
2.4.3.3 与氧化物H2O和碱的反应
[学生实验] 1. 氯气与水和碱溶液反应的对比实验
操作方法如下:
取两个装有氯气的集气瓶(带导管),先观察黄绿色。然后向一个瓶的导管里注入5 mL自来水(实验后多余氯气用氢氧化钠溶液吸收),向另一个瓶的导管里注入等体积的浓氢氧化钠溶液,振荡,片刻后,对比瓶里的氯气的颜色。
现象:注入碱液的瓶里黄绿色褪去,而注入水的瓶里的黄绿色变化不明显。
原理:氯气微溶于水,少量与水反应:


[用途]工业上生产“84消毒液”(NaClO)和漂白粉[Ca(ClO)2] :

[学法指导]难点化解:化学方程式理解、记忆方法:“理解不用记”:“反应机理法”

②Cl2+NaOH=NaCl+NaClO+ H2O:反应机理:Cl2先与H2O反应,生成物HCl、HClO 再与NaOH反应生成NaCl、NaClO、H2O:



[学生实验2] 氯气的杀菌、漂白探究
操作方法如下:
分别收集干燥的氯气和氯化氢气体,放入干燥的有色布条各一条,观察发生的现象,然后加蒸馏水润湿有色布条观察发生的现象。
现象:干燥的有色布条在干燥的氯气和氯化氢气体中变化均不明显;加水润湿后氯气中有色布条褪色,氯化氢中的有色布条变化不明显。
结论:氯气的杀菌、漂白原理是因为氯气与水反应生成具有强氧化性的次氯酸(HClO)。次氯酸是弱酸不稳定,分解释放的氧原子具有很高的活性,结合病毒 (杀菌)、结合有色物质形成无色物质(漂白)、没有物质结合时自身结合形成氧气(图2)。
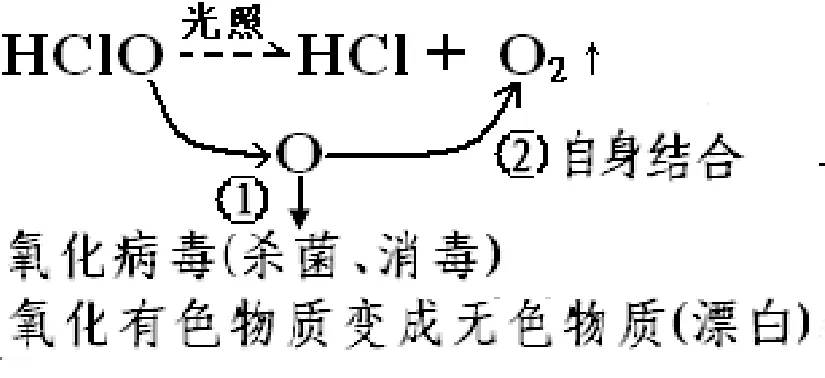
图2 次氯酸杀菌、漂白原理
[环保意识]在通风厨等通风设备下实验,多余氯气用氢氧化钠溶液吸收。
[生活指导] 氯气刺激呼吸道粘膜产生粘液、产生咳嗽:氯气与水反应生成具有强腐蚀性的盐酸、强氧化性的次氯酸——毒气。
[学习指导] 次氯酸的不稳定,使其在生活中使用很不方便,只能现配现用;NaClO则比较稳定,半年时间才能分解一半。“84消毒液”(NaClO)、漂白粉[Ca(ClO)2]等均是以盐的形式存在,可以有效保存8个月,其消毒原理是利用水中、空气中的CO2(碳酸)形成HClO。


上二式反映出HClO的酸性弱于H2CO3。
[拓展] 洁厕灵和84消毒液不能混用,否则会产生有毒的氯气。高浓度氯气可致人晕厥,甚至死亡。因为84消毒液的主要成分是次氯酸钠(NaClO),二者反应的化学方程式为:

[错例指导] 解释次氯酸的杀菌、漂白原理:次氯酸是弱酸不稳定,易分解放出氧气。
评析:次氯酸的氧化性是因为易释放氧原子;释放的氧原子具有很高的活性,能与病毒、有色物质结合(杀菌、漂白),分解产物氧气是没有杀菌、漂白能力的。错误利用次氯酸不稳定的性质。
[自主建构] 新制氯水和久存氯水的成分。
新制氯水:较多Cl2,较少HCl、HClO;
久存氯水:主要是盐酸HCl。
[应用思考] 书后习题P87-2[7]: 新制氯水滴入AgNO3溶液、蓝色石蕊试纸、红墨水的现象。
[生活化教学设计] 生活中氯气与水或碱的反应——自来水消毒和84消毒液
学生搜寻:自来水消毒
[幻灯4] 氯系列消毒剂主要有:液氯、次氯酸钠、漂白粉等,它们的杀菌机制基本相同,主要靠水解产物次氯酸起作用。自20世纪70年代发现氯消毒产生三致(致癌、致畸、致突变)物质以后,在传统的生物消毒方法进行突破同时,也开始推广一些新的处理技术,如二氧化氯、臭氧、紫外线消毒等[8]。
二氧化氯ClO2消毒剂。性价比最优的一种。二氧化氯的氧化能力约为氯的2.6倍,灭菌效果是次氯酸的5~10倍;特别是它与水中的有机物反应不生成三氯甲烷等三致物质,被确认是医疗卫生、食品加工鱼保鲜、饮水和工业循环水等方面消毒杀菌理想药剂,被世界卫生组织(WHO)列为A1级安全杀菌剂[9]。
84消毒液。高效消毒剂,无色或淡黄色液体,有效氯含量5.5~6.5%。被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒[10]。
使用84消毒液预防新冠病毒,高浓度下可引起肺水肿。如何正确使用84消毒液?
①稀释84消毒液时要先倒水再倒消毒液;
②84消毒波属于含氧消毒剂.千万不能和含强酸的消毒产品混合使用;
③日常使用中应采取擦试方式,如使用喷酒方式,只能近距离喷洒在物体表面;
④84消毒液不能用于空气消毒;
⑤在清理下水管道、厨房水槽、沟渠、垃圾桶等,可直接倒入84消毒原液两瓶盖或者把原液喷洒在物品的表面。10分钟后再用清水冲洗干净。
[生活实践与就业指导] ①自制“84消毒液”。电解NaCl稀溶液并搅拌可直接制备“84消毒液”。通电时氯气(封闭)被溶液完全吸收,反应原理为:
生成的Cl2与NaOH反应:

②漂白粉。将电解NaCl产生的Cl2通入冷的消石灰Ca(OH)2反应:

[小结与板书设计](略)。
[课后作业]
[课后作业1]“生活化学”实践活动:①在生物老师的指导下,利用显微镜检测天然河水、井水与自来水中细菌菌落总数、大肠菌群数;利用84消毒液杀菌。
②将自己有汗渍的白色衣物,利用84消毒液漂白洗涤。
[课后作业2]实践理论提高:习题P87~88[7]:第4题:不能使有色布条褪色的物质;第5题:燃烧的错误说法;第6题:84消毒液的有效成分;第8题:漂白粉的有效成分;第9题:漂白粉购买和存放应注意哪些问题;第11题:储氯罐意外泄漏,疏散人群的方法和消防队员应急处理方法。
3 教学反思与设计论证
3.1 把握教学理念——突出生活、友好实用
教学设计要跳出教材,“从生活到化学,从化学到社会”的角度去设计教学。课前提炼教材中“生活化学”元素,“生活化学”设计教学情境;课堂上启发学生联想生活,进行“生活化学”教学;课后引导学生练习,进行“生活化学”实践活动。
氯气的毒性给化学蒙上了恐怖的色彩,教学中应注意正面引导,教友好的、实用的化学:通过对氯气的性质及用途的介绍,让学生明白氯气的毒性并非是绝对的。合理、有效的手段和方法,不仅可以避免氯气毒性的危害,更可以化害为利,让其为我们的生产、生活服务。在引入环节上,向学生展示一些生活中常见的含氯的食物、衣物、药物、试剂、肥料及84消毒剂等实物图片,可以使学生在心理上对氯元素产生一种亲切感,形成友好型化学的印象[12]。
3.2 把握教学时间——详略得当、重点突出
本节教学时间拟定1课时,教学时间操控如下。教学导入及死海地理资料、氯气的物理性质及氯气作为化学武器的资料、氯气的化学性质中与金属和非金属H2的反应及生活中的食盐和胃酸的资料作简单介绍,重点突出氯气与H2O和碱的反应,在实验操作、现象原理、学法指导、生活化教学设计、生活实践与就业指导等方面达到较详细的研究,突出教学的重点内容,突出生活实际应用。教学时间的把握由课堂实际教学操控,利用课件进行展示,以缩短讲述和板书的时间,特别是死海资料、化学武器的资料、食盐和胃酸的资料信息,通过展示一笔带过,尽量占用较少时间。
3.3 把握教学难度——取舍有度、化解迁移
本节教学的难点是氯气与水和碱反应的化学方程式掌握,水和碱虽是两类物质,但反应原理有必然的联系,实际应用亦属同类(都是通过形成次氯酸),教学设计中作为一个知识点来介绍。氯气与碱反应主要以NaOH为主,生活中主要使用84消毒液,很少用到漂白粉,教学处理是将漂白粉知识放到习题8、9两题中讨论。
在氯气与水和碱反应方程式的学法指导、认识次氯酸的强氧化性等方面介绍难点化解、知识迁移的方法,进行教师职业示范培训,培养学生良好的学习方式、方法。

