土壤pH 测定的影响因素探讨
李朝英,郑 路,2
(1 中国林业科学研究院热带林业实验中心,凭祥532600;2 广西友谊关森林生态系统国家定位观测研究站,凭祥532600)
土壤酸碱性受气候、地形、母质、植被、人类活动及盐基饱和度等多种因素影响,是土壤的重要化学性质之一[1-2]。土壤酸碱性与土壤诸多理化性质密切相关,对土壤养分存在的形态和有效性、微生物活性、营养元素的传递和有效吸收以及植物生长发育有很大影响;同时,土壤酸碱性还是重金属元素吸附和解析及污染物降解的关键因素之一[3-5]。随着工业和农业的发展,土壤酸化程度日益加剧,随之引发了土壤退化、农作物减产、重金属污染程度加重等诸多问题,制约了土地可持续性发展。土壤酸碱性通常以土壤pH 衡量,准确测定土壤pH 对改良土壤、发展农林及保护环境等有着重要的现实意义。土壤pH 测定方法主要为电位法,其操作方便,检测高效,适用于实验室日常检测分析。但是,不同资料所述电位法中,样品处理时间及静置时间、悬液测定状态等存在差异,至今无统一标准,也未见相关比较讨论[6-7]。此外,国内标准指出水、氯化钾浸提液用于酸性和中性土壤pH 测定,氯化钙浸提液用于碱性土壤pH 测定,而3 种浸提液测定土壤pH 的比较及其相关性分析少有报导,如何选择使用并不清楚[8-10]。目前,多以水浸提液测定pH,但该方法重复性不好,尤其是检测pH 变化较大的样品,读数稳定时间偏长,检测误差大。鉴于此,本试验在不同检测条件下测定土壤pH,探讨土壤pH 测定的影响因素,并对3 种浸提液所测土壤pH 进行比较分析,探讨三者的相关性,以期探寻pH 测定误差产生的原因,确定适宜的检测条件,为土壤pH 测定提出一种优选方法,为准确测定土壤pH 提供可行的参考与指导。
1 材料与方法
1.1 试剂与仪器
氯化钾、氯化钙、pH 4.01 标液、pH 6.86 标液均为分析纯;水为去离子水。
pH 计(复合电极)、磁力搅拌器、往复式振荡器。
1.2 样品采集与处理
2018年4月在中国林业科学研究院热带林业实验中心青山实验场人工林样地采集11个土壤样品,在广西友谊关森林生态系统国家定位观测研究站设置的伏波实验场人工林样地采集10个土壤样品。土壤样品风干后,去除残留的植物残体,压碎过孔径2 mm 筛,装袋标识。
1.3 试验地概况
试验地位于广西凭祥市(21°57′—22°19′N,106°39′—106°59′E)的青山实验场和伏波实验场,属于南亚热带季风气候,年均气温21.5 ℃,年均降水量1200—1400 mm,土壤为花岗岩发育成的赤红壤和红壤。
1.4 试验方法
(1)土壤样1—9 共称取9 份,每个样8 g,9 份土壤均分为3 组,按液土比2.5∶1加入20 mL 水。各组分别振荡5 min、30 min、60 min 后,分别静置0 min、30 min、60 min,将转子放入待测液,待转子转动稳定后,将电极放入搅拌中悬液测定土壤pH水(表示以水浸提所测pH)。以上试验重复3 次。
(2)土壤样1—9 共称取5 份,每个样8 g,按液土比2.5∶1加入20 mL 水,振荡30 min 后,分别静置30 min、60 min、120 min、180 min、240 min,将电极放入搅拌中悬液测定土壤pH。
(3)土壤样1—9 共称取6 份,每个样8 g,6 份土壤均分为2 组,按液土比2.5∶1加入20 mL 水,振荡30 min 后,静置30 min,一组将电极放入上清液中测定,一组将电极放入搅拌中悬液测定土壤pH。
(4)土壤样1—21 共称取9 份,每个样8 g,9 份土壤均分为3 组,3 组分别按液土比2.5∶1加1 mol∕L氯化钾浸提液20 mL、0.01 mol∕L 氯化钙浸提液20 mL、水20 mL,振荡30 min 后,静置30 min,将电极放入搅拌中悬液测定土壤pH。以氯化钾、氯化钙浸提液所测pH 分别表示为pH氯化钾、pH氯化钙。
1.5 数据处理
采用Excel 2013 软件进行数据统计及绘图,使用SPSS 19.0 软件进行方差分析。
2 结果与分析
2.1 样品处理及测定初始时间对土壤pH 测定的影响
由表1 可见,相同振荡时间下,静置0 min 所测pH 的标准偏差(SD)偏高,静置30 min、60 min 所测pH 的SD均呈下降趋势。振荡5 min、静置60 min 所测结果与振荡30 min、静置30 min 或60 min 及振荡60 min、静置30 min 或60 min 的SD趋于一致,且小于0.12,说明以上条件下检测稳定,精密度良好。长时间振荡后立即测定或者较短时间振荡后静置时间不足均会对测定结果有一定影响,说明振荡与静置对测定的作用并不等同,两者不能相互取代。不同振荡时间下,悬液静置0 min 所测pH 与静置30 min、60 min 均有显著差异,静置30 min、60 min 所测pH 无显著差异。
由表2 可见,振荡时间与静置时间交互作用Sig.=0.996(P>0.05),说明两者交互无显著性影响。可见,振荡5 min、静置60 min 后可开始检测,振荡30 min、静置30 min 后可开始检测,这两种做法的样品准备时间短,检测结果准确稳定。

表1 不同振荡时间与静置时间所测土壤pHTable 1 Soil pH measured by different oscillation time and standing time
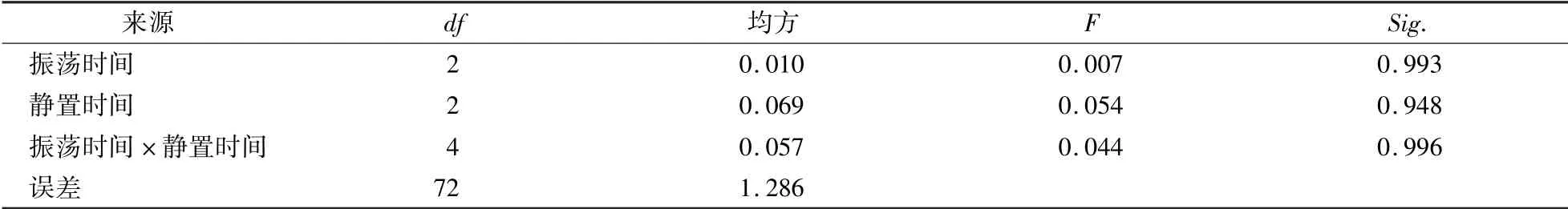
表2 振荡时间与静置时间对土壤pH 测定结果的影响Table 2 Effects of oscillation time and standing time on soil pH determination results
2.2 样品测定时限对土壤pH 测定的影响
由图1 可见,振荡30 min 后,悬液静置30 min、60 min、120 min、180 min 所测pH 趋于一致,悬液静置240 min 所测pH 有明显波动。静置30—60 min、静置30—120 min 所测pH 变幅分别为0—0.07、0—0.09,静置30—180 min 所测pH 变幅为0—0.13,静置30—240 min 所测pH 变幅为0.02—0.29,其中有4个样品的pH 变幅超过0.15, 说明悬液静置120 min、180 min、240 min 所测结果的稳定性依次下降。本试验在28 ℃室温下进行,pH 计开启了温度补偿功能,可排除温度对测定的影响,说明悬液随静置时间延长发生的变化影响了测定结果。以上结果表明,为了保证测定结果的准确稳定,悬液静置时间在30—120 min 为宜。
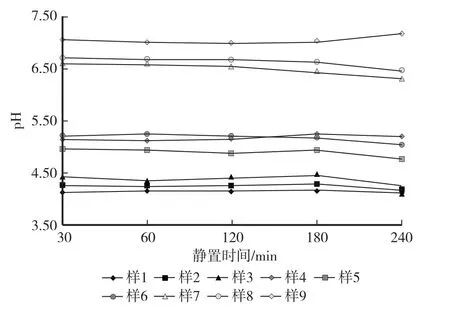
图1 悬液静置不同时间的测定结果Fig.1 Determination results of suspension standing for different time
2.3 测定状态对土壤pH 测定结果的影响
由表3 可见,pH 小于6 的样品,测定上清液、搅拌中悬液的pH 差值在0.13 以内,SD分别为0.01—0.16、0.02—0.11。pH 大于6 的样品,两种状态的pH 差值为0.10—0.48,SD分别为0.06—0.20、0.04—0.09。可见,pH 小于6 的样品两种状态的测定结果差异小于pH 大于6 的样品,搅拌中悬液所测pH 精密度高于上清液。方差分析表明,pH 小于6 的样品两种测定状态的pH 无显著差异,pH 大于6 的样品两种测定状态的pH 有显著差异,说明不同测定状态对pH 不同的样品测定结果有不同影响。
由图2 可见,样3、样7、样8、样9 在搅拌中悬液所测结果稳定用时在20—60 s,上清液所测结果稳定用时在80—100 s,说明电极在搅拌中悬液的响应速度快于上清液,更有利于pH 检测分析。
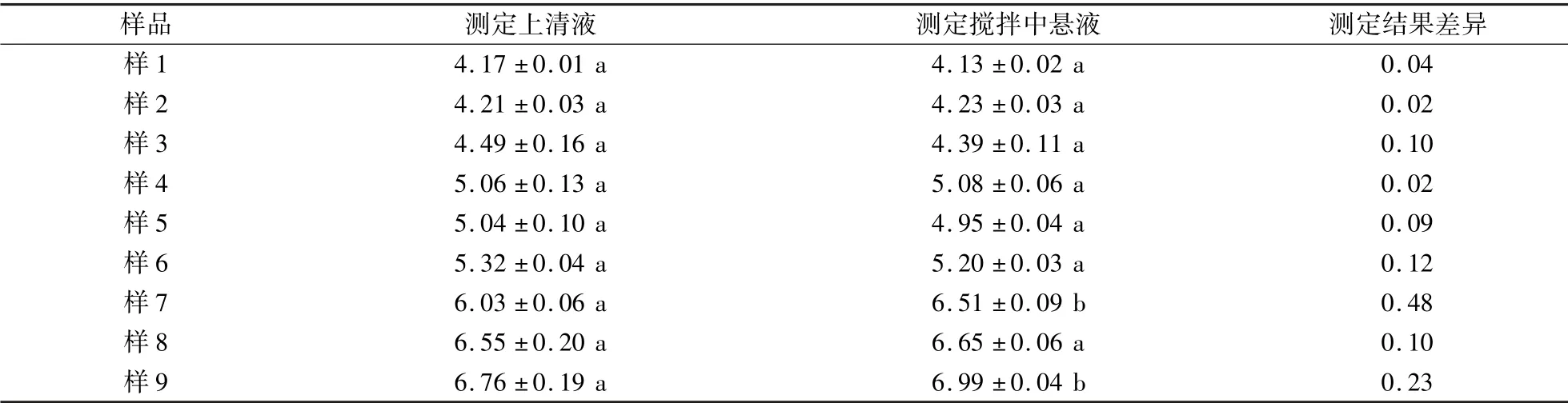
表3 两种不同测定状态所测土壤pH(n=3)Table 3 Soil pH measured by different determination status of samples(n=3)
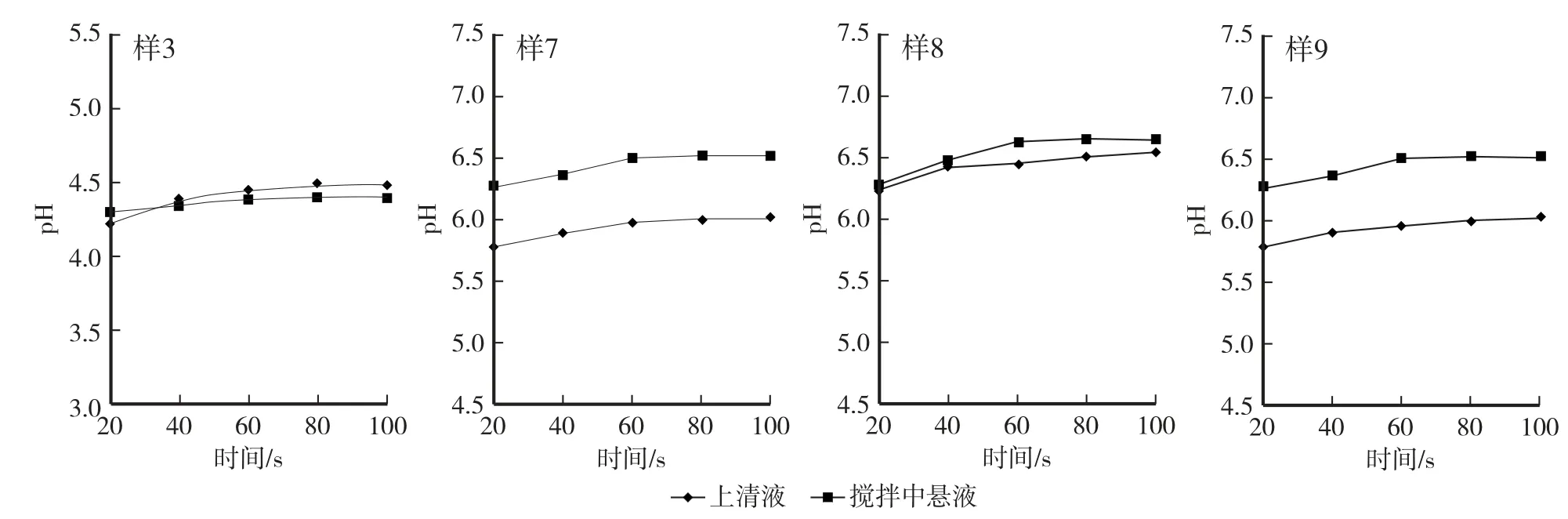
图2 四个样品在两种测定状态不同时间点的测定结果Fig.2 Determination results of 4 samples of two determination status at different time points
2.4 不同浸提液所测土壤pH 比较
由图3 可见,pH水高于pH氯化钾、pH氯化钙,pH水与pH氯化钾、pH氯化钙的差值分别在0.61—1.70、0.81—1.15,3 种浸提液所测pH 有显著差异。
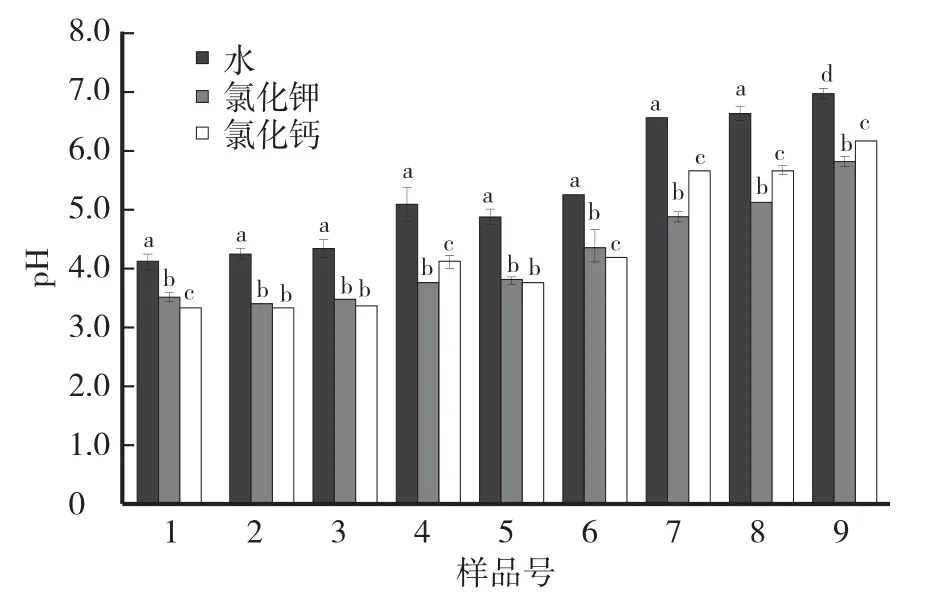
图3 三种浸提液所测土壤pH 结果的比较Fig.3 Comparison of soil pH measured by 3 kinds of extracts
对3 种浸提液所测土壤pH 进行相关性分析,pH水与pH氯化钾的拟合线性方程为y=1.230x+0.130(R2=0.922),pH水与pH氯化钙的拟合线性方程为y=0.986x+1.018(R2=0.990),pH氯化钾与pH氯化钙的拟合线性方程为y=0.744x+0.952(R2=0.936)。三种浸提液所测pH 趋势一致,具有显著相关性,所拟合的线性方程具有良好相关性,说明三者测定值之间可以进行转换计算。其中pH水与pH氯化钙的相关性较高,两者转换计算的误差较小。
由表4 可见,21个土壤样品根据pH水与pH氯化钙和pH氯化钾的拟合线性方程,测得的pH氯化钙和pH氯化钾转换计算为水浸提液的pH,分别为pH氯化钙转换值、pH氯化钾转换值。pH氯化钙转换值与pH水的差值在0.03—0.30,差值大于0.20 的样品占14%,差值在0.10—0.19 的样品占38%,差值小于0.10 的样品占48%。pH氯化钙的SD在0.04 以内。pH氯化钾转换值与pH水的差值在0.02—1.34,差值大于0.20 样品占67%,差值在0.10—0.19 的样品占9.5%,差值小于0.10 的样品占23.5%。pH氯化钾的SD在0.11 以内。pH水的SD在0.02—0.32,高于pH氯化钙、pH氯化钾。在同样检测条件下,pH氯化钙、pH氯化钾读数稳定时间均在30 s 以内,较pH水的稳定时间短,说明pH氯化钙、pH氯化钾干扰因素小,精密度较高,测定稳定,重复性良好;pH水测定结果变异较大,精密度欠佳。21个土壤样品的pH 在4—9,pH氯化钙转换值与pH水差值较小。pH 小于5 的土壤,pH氯化钾转换值与pH水接近,两者差值小于0.45;pH 在5—9 的土壤,pH氯化钾转换值与pH水差值有增大趋势,说明氯化钙浸提液可用于多种土壤pH 测定,氯化钾浸提液适用土壤范围有限。所测pH氯化钙稳定快捷,与pH水接近。因此,采用氯化钙浸提液测定土壤pH 具有明显优势。

表4 三种浸提液所测土壤pH 的转换计算及差异比较(n=3)Table 4 Conversion calculation and difference comparison of soil pH measured by 3 kinds of extracts(n=3)
3 结论与讨论
土壤pH 取决于土壤溶液中H+、Al3+与OH-的差值大小。土壤悬液中交换性离子与土壤颗粒表面交换性H+、Al3+与OH-的交换情况以及电极的液接电位变化等均可造成pH 的偏移。此外,有研究发现,未引入H+的条件下,土壤盐分量变化也会引起pH 的明显变化。可见,影响土壤pH 的机理较为复杂[11-12]。
为了使土壤悬液达到平衡,保证pH 测定准确,林业行标提出振荡1—2 min、静置30 min 后测定;农业行标提出搅拌5 min、静置60—180 min 测定;国际标准指出振荡60 min、静置60—180 min 测定;环境行标及土壤普查技术规范指出振荡或搅拌2 min、静置30 min,在60 min 内完成检测。本试验表明,振荡5 min、静置30 min,所测pH 不稳定;振荡5 min、静置60 min,以及振荡30 min 或60 min、静置30 min 或60 min,在120 min 以内完成检测,所测pH 稳定,是适宜的检测条件。本试验提出的样品处理时间及静置时间与现行农业行标、国际标准的要求一致,与环境行标及林业行标有所不同[13-14]。
现有资料对于土壤pH 待测液状态有不同说法,如测定搅拌中的悬液、上清液和滤液等,关于待测液状态对测定结果的影响存在分歧[14-15]。本试验表明,电极置于搅拌中悬液测定,能迅速甩掉电极玻璃球上的水膜,减小液接电位的影响,提升电极的响应速度及灵敏度,较测定上清液更易于保证测定结果的准确性[16-18]。这与林业行标所述不同,但与农业行标与国际标准所述一致。本试验还表明,pH 小于6 的土壤样品在两种测定状态下所测结果差异较小,pH 大于6 的土壤样品在两种测定状态下所测结果差异大于0.3。液接电位导致的pH 变化一般小于0.3,说明除了液接电位外,还受其他因素影响。现有资料对此未见相关报导,有待于进一步探讨[19-20]。
国内标准方法指出水与氯化钾浸提液用于酸性和中性土壤pH 测定,氯化钙浸提液限于碱性土壤的测定。本试验表明,pH氯化钾、pH氯化钙均小于pH水,三者存在显著性差异,但三者有良好的相关性,可进行转换计算。尤其是pH氯化钙与pH水拟合的线性方程斜率接近1,相关系数R2大于0.98,两者相关性较高。由于氯化钙、氯化钾浸提液的离子强度较高,电极响应速度迅速,液接电位影响减小,检测结果重复性好;水的离子强度较弱,电极响应速度慢,液接电位影响明显,易造成读数偏移,检测结果重复性差。pH水的精密度低于pH氯化钾、pH氯化钙。试验表明,所测pH氯化钙根据pH氯化钙与pH水的线性方程转换计算值与pH水的差异较小,两者有较强的可比性及参考性。pH 小于5 的土壤,pH氯化钾的转换计算值与pH水差异较小,pH 在5—9 的土壤,pH氯化钾转换值与pH水差异增大,两者可比性欠佳。可见,氯化钙浸提液所测pH氯化钙精度高,误差小,适用于酸性、弱酸性及中性土壤的pH 测定,是土壤pH 测定的优选方法,可代替水浸提法测定土壤pH[21-23]。本试验所述与国内标准所述有所不同,但与国际标准提出的土壤pH 通用测定方法一致。本试验样地所属区域为典型南亚热带气候,土壤多为酸性、中性,所用土壤样中碱性土壤少,其pH水与pH氯化钙有待进一步研究比较。
当前对土壤pH 测定方法的研究及选择通常忽视了土壤复杂多样的情况对测定结果的影响,很少提及测定干扰的排除。本试验对土壤pH 测定方法中的主要检测条件进行了分析,对检测条件进行了优化,提出了土壤pH 准确测定的方法。然而土壤pH 的检测条件只是准确测定的基本前提,并不能完全避免液接电位、土壤可溶盐等干扰而引发的检测误差,以及检测重复性差、精密度差的问题。氯化钙浸提液测定土壤pH,避免了水浸提测定存在的液接电位、电极响应慢以及土壤可溶盐等方面的干扰,提高了检测准确性。尤其是酸性及中性土壤的pH氯化钙转换值与pH水有良好的可比性,为准确测定土壤pH 及深入研究土壤提供了可行的参考。

