中药抗脑缺血再灌注损伤的作用及其机制的研究进展
于 潇,王贵阳,侯宇东,姜艳艳,张 薇*,刘 斌*
1.北京中医药大学中药学院,北京 102488
2.北京大学 医学部药学院,北京 100191
脑血管疾病是当今世界威胁人类健康与生存的重大疾病之一,其中又以脑缺血较为多见,它主要是由于血管栓塞所造成脑血流量减少、脑组织血氧供应不足以致损伤,这种情况持续时间越久,脑损伤越严重,故通过溶解血栓或机械再通等方式尽早恢复缺血区的血液再灌注至关重要。然而这些治疗措施在使闭塞的脑血管再通的同时却常使缺血组织以及神经系统的病理损害进一步加重甚至不可逆,临床症状恶化,这种现象被称为脑缺血再灌注损伤(cerebral ischemia reperfusion injury,CIRI)。
CIRI 的病理机制十分复杂,涉及钙超载、线粒体损伤、炎症反应、细胞凋亡、氧自由基累积和兴奋性氨基酸过度释放等多个环节[1]。在CIRI 发生发展过程中,缺血区的脑组织由于得不到充足的血氧供应,通过无氧酵解途径获得能量时Na+,K+-ATP酶活性降低,导致细胞内的钠离子(Na+)和钙离子(Ca2+)浓度升高。伴随着Ca2+浓度升高,兴奋性氨基酸递质谷氨酸大量释放。当谷氨酸与α-氨基-3-羟基-5-甲基-4-异唑丙酸(α-amino-3-hydroxy-5-methyl-4-isoxazole-propionic acid,AMPA)受体结合后会进一步促进Ca2+内流,导致线粒体功能障碍。当谷氨酸与N-甲基-D-天冬氨酸(N-methyl-Daspartic acid,NMDA)受体结合则会产生大量的活性氧与活性氮,从而诱发氧化应激和硝化应激损伤,进而影响血脑屏障通透性,促进细胞自噬因子表达,造成血脑屏障破坏和细胞自噬。此外,当发生CIRI 时,由于小胶质细胞、星形胶质细胞和巨噬细胞被激活,大量炎性因子如肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素(interleukin,IL)-6、IL-1β 的释放又进一步诱发了炎症反应。这些不同因素在CIRI 发生和发展的多个环节中彼此相织,互为因果,相互影响,共同诱导脑组织神经细胞损伤、坏死或凋亡,CIRI 的主要病理机制见图1。
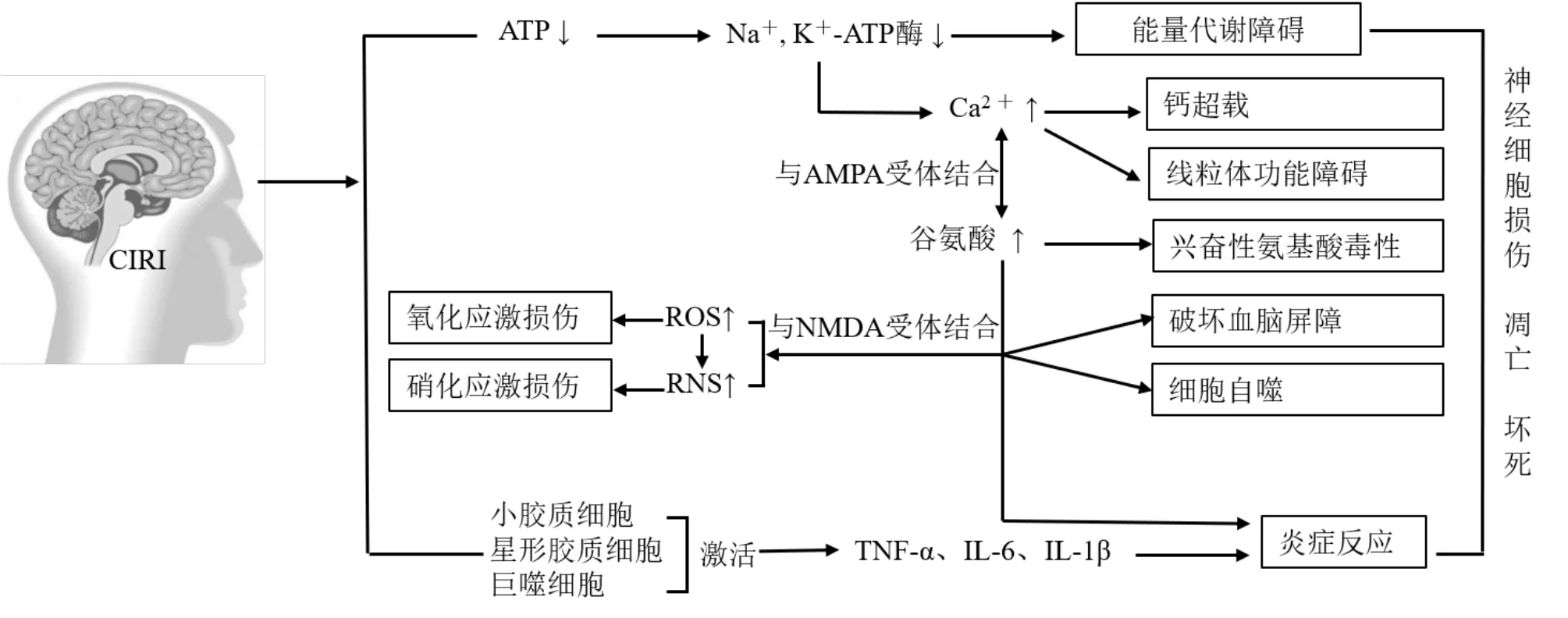
图1 CIRI 的主要病理机制Fig.1 Main pathological mechanism of CIRI
CIRI 在中医学理论中归属于“中风”范畴。中医对中风的认识由来已久,在医疗实践中逐步形成了较为完善的病因病机认识、辨证分型和治疗方法,建立了有效的治疗体系。《景岳全书》记载“中风麻木不仁等证,因其血气不至,所以不知痛痒,盖气虚则麻,血虚则木,麻木不已,偏枯痿废,渐至日增。”《症因脉治》记载“半身不遂之因,或气凝血滞,脉痹不行,或胃热生痰,流入经遂。”传统中医理论认为气滞血瘀、气虚不能统血、脉络不通或脑窍闭阻为该病的病机,血瘀及肾虚为该病的根本病因,活血化瘀、益气活血、清热解毒、化痰通络、开窍醒神、养阴生津、平肝息风、健脾补肾为该病的基本治法[2]。基于中医学理论对“中风”的认识,现代医学对具有不同功效的中药发挥抗CIRI 的作用及其机制作了进一步阐释。基于“气滞血瘀”病机的益气活血化瘀类中药可通过抗氧化、抑制细胞凋亡及拮抗炎症反应等方式发挥作用[3-4];基于“毒损脉络”病机的清热解毒类中药可通过抑制炎症反应、提高超氧化物歧化酶活性等方式发挥作用[5-6];基于“痰阻脉络”病机的化痰通络类中药可通过抑制炎症反应,调节内质网应激反应等方式发挥作用[7-8];基于“气虚不能统血”病机的健脾补肾中药可提高抗氧化酶的活性、抑制脂质过氧化损伤,通过抗氧化损伤和清除自由基等方式发挥作用[9];基于“窍闭神匿、神不导气”病机的开窍醒神类中药可通过抑制炎症反应和氧化应激水平发挥抗CIRI 作用[10-11]。
近年来CIRI 的发病率、死亡率和致残率仍居高不下,严重危害和影响着人类的生命健康和生活质量。目前临床上主要采用溶栓剂、钙通道拮抗剂、自由基清除剂、兴奋性氨基酸调控剂等药物,通过干预CIRI 发生的某一个病理环节进行治疗,但由于治疗时间窗窄、作用靶点单一等问题使上述药物用于CIRI 的临床治疗具有一定的局限性[12]。近年来研究发现中药及其复方因其所含化学成分结构种类多样,可通过多靶点、多途径整体干预CIRI 发生的病理过程,在治疗CIRI 方面具有独特的优势和潜力,中药防治CIRI 的研究受到愈来愈多的关注。本文以中药药效物质及其作用机制为切入点,综述了近10年来具有抗CIRI 作用的中药及其作用机制的相关研究进展,以期对CIRI 的药物研发提供理论依据,为中医药防治CIRI 的深入研究提供科学基础。
1 治疗CIRI 的单味中药
在治疗缺血性脑中风的用药历史中,活血类、清热类、补益类、祛湿类以及平肝类等中药可通过活血祛瘀通络、清热泻火解毒、补肾益气、祛风除湿、化痰通腑及调和营卫等方式发挥较好的治疗作用。现代研究发现这些单味药中的主要有效部位或有效成分对CIRI 同样具有较好的治疗效果,如人参中的人参皂苷、天麻中的天麻素、当归中的当归多糖等。
1.1 天麻
天麻Gastrodiae Rhizoma为兰科植物天麻Gastrodia elataBl.的干燥块茎,具有息风止痉、平抑肝阳、祛风通络的功效,可通过减轻氧化应激损伤、抑制细胞凋亡和减轻神经毒性等途径发挥抗CIRI 的作用。天麻中主要含有天麻素和酚性成分。研究发现天麻素可明显抑制中枢神经特异性蛋白在CIRI 后的过度表达而发挥抗CIRI 作用;天麻脂溶性酚性成分则可通过调节钙调蛋白依赖性蛋白激酶2 的表达水平而发挥神经保护作用;天麻中的对羟基苯甲醛又可通过抑制细胞凋亡而实现抗CIRI 作用[13-15]。此外,陈亭亭等[16]还围绕氧化应激和神经毒性这2 个方面的作用机制探讨不同粒径的天麻粉末抗CIRI 的作用差异,结果发现不同规格的天麻粉末均可改善CIRI 大鼠的神经功能,其中500 目的天麻超微粉较其他规格的天麻粉末相比,神经保护作用更为明显。
1.2 当归
当归Angelicae Sinensis Radix为伞形科植物当归Angelica sinensis(Oliv.) Diels 的干燥根,具有补血活血、调经止痛的功效,可通过促进血管生成、减轻氧化应激损伤、抑制炎症反应、细胞凋亡及细胞自噬水平等方式发挥神经保护作用。多糖和挥发油是其主要的化学成分。Cheng 等[17]研究发现0.5、1 mg 当归水提物干预后可明显提高缺血再灌注损伤大鼠模型海马CA1 区神经元的存活率,这提示当归水提物对CIRI 大鼠脑组织的保护作用主要与激活磷酸化丝氨酸-苏氨酸激酶/磷酸化Bad 蛋白(serine-threonine kinase,p90RSK/p-Bad)和磷酸化丝氨酸-苏氨酸激酶/环磷腺苷效应元件结合蛋白/脑源性神经营养因子(p90RSK/cAMP-response element binding protein,CREB/brain derived neurotrophic factor,BDNF)信号通路,从而保护线粒体的完整性和抑制细胞凋亡有关。此外,研究显示当归中的挥发油成分可通过激活磷酸化蛋白激酶B/雷帕霉素靶蛋白(phosphorylated protein kinase B,p-Akt/mammaliantargetofrapamycin,mTOR)信号转导通路,进而调节细胞自噬蛋白从而发挥抗CIRI 作用[18]。当归多糖同样表现出较显著的神经保护作用,这可能与抗炎、抗氧化、抑制神经细胞凋亡及促进血管生成等密切相关[19-20]。
1.3 大黄
大黄Rhei RadixetRhizoma为廖科植物掌叶大黄Rheum palmatumL.、唐古特大黄R.tanguticumMaxim.ex Balf.或药用大黄R.officinaleBaill.的干燥根和根茎,具有泻下攻积、清热泻火、凉血解毒、逐瘀通经、利湿退黄等功效,可通过抑制氧化应激、炎症反应及细胞凋亡等方式实现对缺血脑组织的保护作用。大黄中主要含有蒽醌类成分。研究发现蒽醌类成分为大黄抗CIRI 的主要物质基础,其抗CIRI 的作用机制与抗氧化和抗炎有关[21]。大黄酚、大黄素等成分还被发现可分别通过抑制环磷酸腺苷/蛋白激酶A(cyclic adenosine monophosphate,cAMP/PKA)信号转导通路和调节线粒体蛋白乙酰化水平,调控腺苷酸活化蛋白激酶/糖原合成酶激酶3β(adenosine monophosphate activated protein kinase,AMPK/glycogen synthase kinase 33β,GSK3β)及第10 号染色体缺失的磷酸酶和张力蛋白同源物基因/磷脂酰肌醇 3 激酶/丝氨酸苏氨酸蛋白激酶( phosphatase and tensin homology deleted on chromosome ten,PTEN/phosphatidylinositol 3 kinase,PI3K/Akt)信号通路等方式实现对CIRI 模型大鼠脑组织的神经保护作用[22-25]。
1.4 雷公藤
雷公藤Tripterygii Radix为卫矛科植物雷公藤Tripterygium wilfordiiHook.f.的干燥根,具有祛风除湿、活血通络、消肿止痛、杀虫解毒的功效,主要通过抑制炎症反应及细胞凋亡、调节免疫系统而发挥抗CIRI 作用。雷公藤主要含有萜类成分,雷公藤甲素是其主要活性成分。Bai 等[26]研究发现雷公藤甲素干预后能够明显改善CIRI 模型组大鼠的神经功能,推测雷公藤甲素可通过抑制核转录因子-κB(nuclear factor-kappaB,NF-κB)信号通路激活而发挥抗CIRI 保护作用。此外还有研究显示雷公藤甲素发挥抗CIRI 作用还与调节半胱氨酸蛋白酶-3(Caspase-3)、诱导型一氧化氮合酶和TNF-α 等的表达、NF-κB/p53 正向凋亡调节因子(p53 up-regulate modulator of apoptosis,PUMA)信号通路等密切相关[27-29]。
此外,早在19世纪已有研究表明人参中的人参皂苷[30-36]、三七中的三七皂苷[37-39]、川芎中的川芎嗪、藁本内酯[40-43]、丹参[44-49]及黄芩[50-55]等中药有效成分或单味中药对CIRI 具有较好的保护效果。近年来,研究发现藏红素[56-57]、白芍总苷[58]、芍药苷[59-60]、丹皮酚[61]、知母皂苷[62]、败酱总黄酮[63]、贝母素甲[64]、钩藤碱[65]、β-石竹烯[66-67]、山楂总黄酮[68]、牡荆苷[69]、Z-没药甾酮[70]、11-羰基-β-乙酰乳香酸[71]、黄芪甲苷[72]、葛根素[73-74]、茯苓酸[75]、紫草素[76-77]、没食子酸[78]、柚皮苷[79-80]、白藜芦醇[81-82]、蜂胶总黄酮[83-84]、木犀草素[85]、银杏内酯[86-88]、姜黄素[89-91]、枸杞多糖[92]等中药有效成分或有效部位同样被证实对CIRI 具有较好的治疗效果,见表1。
2 治疗CIRI 的中药药对
中药药对是中医临床常用的相对固定的2 种药味的配伍组合,是中药配伍应用中的基本形式,是连接中药和方剂的重要桥梁[93]。研究发现许多中药药对配伍具有较好的抗CIRI 作用,如丹参-红花药对、当归川-芎药对等。
2.1 丹参-红花药对
丹参与红花均属于活血化瘀类中药,这2 味药的配伍组合是中药复方中常见药对之一。该药对组合具有活血化瘀、通经止痛等功效,在妇科和心血管疾病的临床治疗方面应用广泛。近年来研究发现该药对主要通过抑制氧化应激和炎症反应、减轻内质网应激水平等方式发挥抗CIRI 作用。陈裕琳等[94]选取丹参素、丹酚酸A 和B、羟基红花黄色素A 这4 种丹参和红花药材中的主要有效成分为实验对象,考察丹参红花药对的抗CIRI 作用。研究结果显示该药对能够较好地减轻脑缺血再灌注造成的脑组织损伤,同时推测丹参红花药对可通过抗炎、调节内质网应激等方式实现神经保护作用。夏颖[95]则对丹参素与羟基红花黄色素A 这2 种成分的抗CIRI活性及治疗最佳配比展开研究,结果显示丹参素与羟基红花黄色素A(1∶1)配伍的治疗组可使模型组大鼠的神经功能评分得到明显改善。此外,另有研究表明丹参红花配伍治疗CIRI 的效果明显优于2 味药单用,这也进一步阐释了中药药对配伍的科学内涵[96]。
2.2 乳香-没药药对
乳香与没药同属于活血止痛类中药,2 味药配伍后气血兼顾,活血止痛、消肿生肌作用增强,对于跌打损伤、关节疼痛等疾病的临床治疗效果显著,并可通过促进血管新生等方式实现较好的神经保护作用。11-羰基-β-乙酰乳香酸和Z-没药甾酮为乳香和没药治疗CIRI 的主要活性成分,研究表明上述2 种成分单独作用于CIRI 模型大鼠便已显示出较好的治疗效果。汪继涛等[97]对11-羰基-β-乙酰乳香酸和Z-没药甾酮联合应用的治疗效果进行研究,结果表明上述2 种成分联合应用后可明显减轻CIRI 模型大鼠的神经机能损伤程度,并呈现出一定的剂量相关性,其作用机制可能与调节血管内皮生长因子(vascular endothelial growth factor,VEGF)、δ 样配体-4(delta-like ligand 4,DLL4)的蛋白表达有关。
2.3 黄芪-红花药对
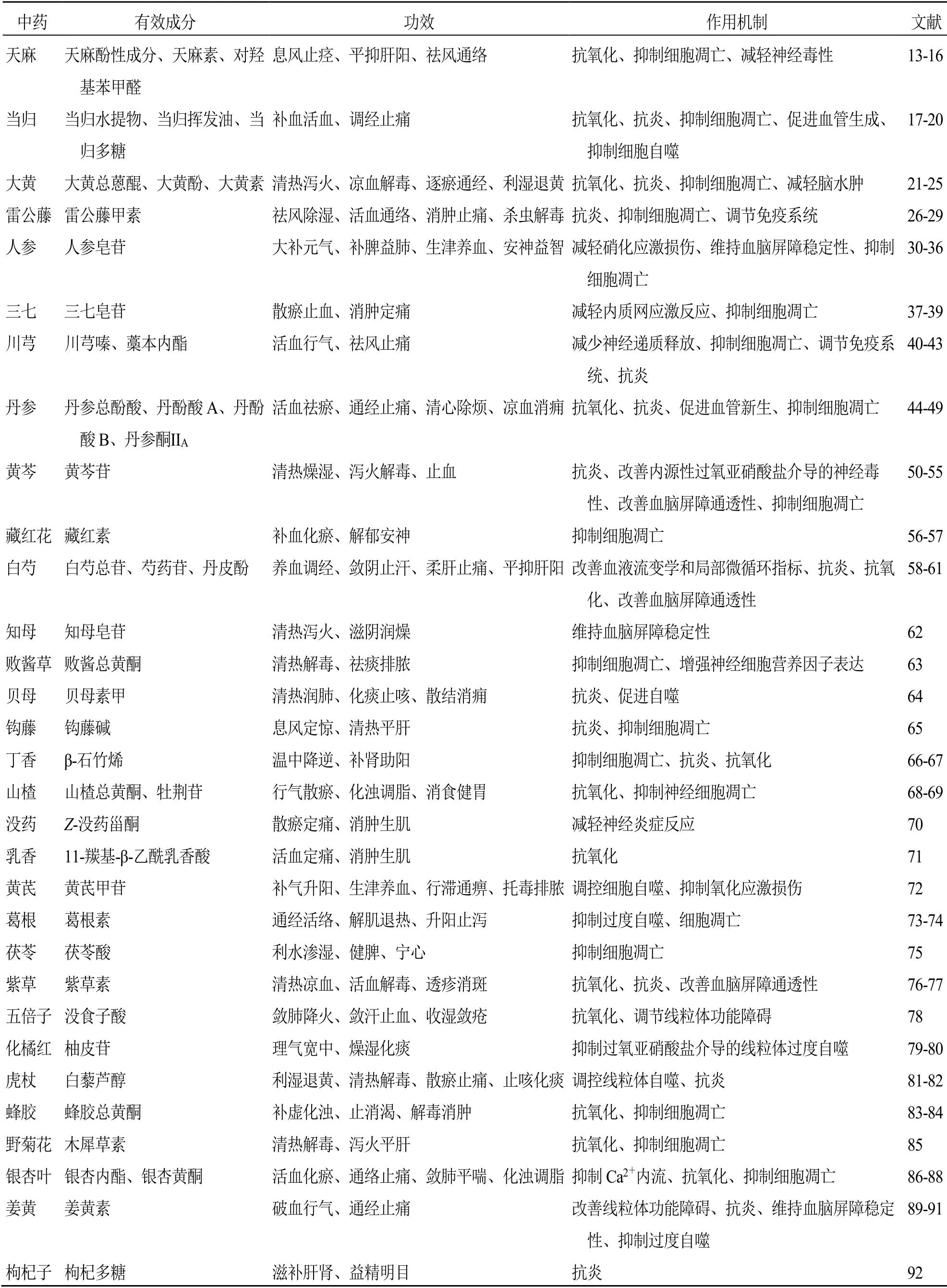
表1 抗CIRI 的中药及其作用机制Table 1 Traditional Chinese medicine against CIRI and their mechanisms
黄芪具有补中益气健脾的功效,为临床常用的补气类中药,而红花具有活血通经、散瘀止痛功效,为临床常用的活血类中药,2 味药合用后对于气虚血瘀证的治疗具有较好的临床疗效。黄芪红花配伍可通过抑制炎症及氧化应激反应、促进血管新生等方式发挥抗CIRI 作用。文献报道黄芪中的黄芪甲苷、黄芪多糖,红花中的羟基红花黄色素A 对CIRI均具有一定的保护作用。研究发现黄芪与红花2 味药配伍应用后对CIRI 的治疗效果明显优于2 味药单用,其抗CIRI 作用机制与调节转化生长因子和B淋巴细胞瘤-2 基因(B-cell lymphoma-2,Bcl-2)的表达密切相关[98-99]。
2.4 当归川芎药对
当归具有养血活血、调经止痛的功效,以养血为主,而川芎具有行气活血、祛风止痛的功效,以行气为要,二者合用气血兼顾,增强补血活血之功效。目前该药对在妇科和脑血管疾病等方面应用较为广泛。当归川芎配伍药对可通过改善神经可塑性、维持血脑屏障的稳定性发挥对脑血管疾病的治疗作用。蔺俊斌[100]以当归和川芎中的主要活性成分当归多糖和川芎嗪开展当归与川芎配伍组合抗CIRI 作用研究。研究结果表明当归、川芎单味药治疗组、当归与川芎配伍治疗组均可使局灶性再灌注损伤模型大鼠的神经功能得到改善,当归多糖和川芎嗪的配伍比例为5∶2 时治疗效果最佳。当归与川芎抗CIRI 作用的发挥与当归多糖和川芎嗪调节神经可塑性、降低血脑屏障通透性有关。此外研究发现CIRI 的大鼠脑组织随着缺血再灌注损伤治疗时间的延长,其损伤程度不断减轻。由此可推测缺血再灌注损伤脑组织神经功能的恢复除可被药物治疗外,还可能存在一个自我恢复的过程。
此外,除上述中药药对对CIRI 有较好的保护作用外,人参与三七配伍[101]、冰片与川芎配伍[102]、黄芪与三七配伍[103-104]、川芎与赤芍配伍[105]、山楂与三七配伍[106]、灯盏细辛与赤芍配伍[107]等其他中药药对配伍方式对CIRI 的治疗也具有较好的疗效,见表2。
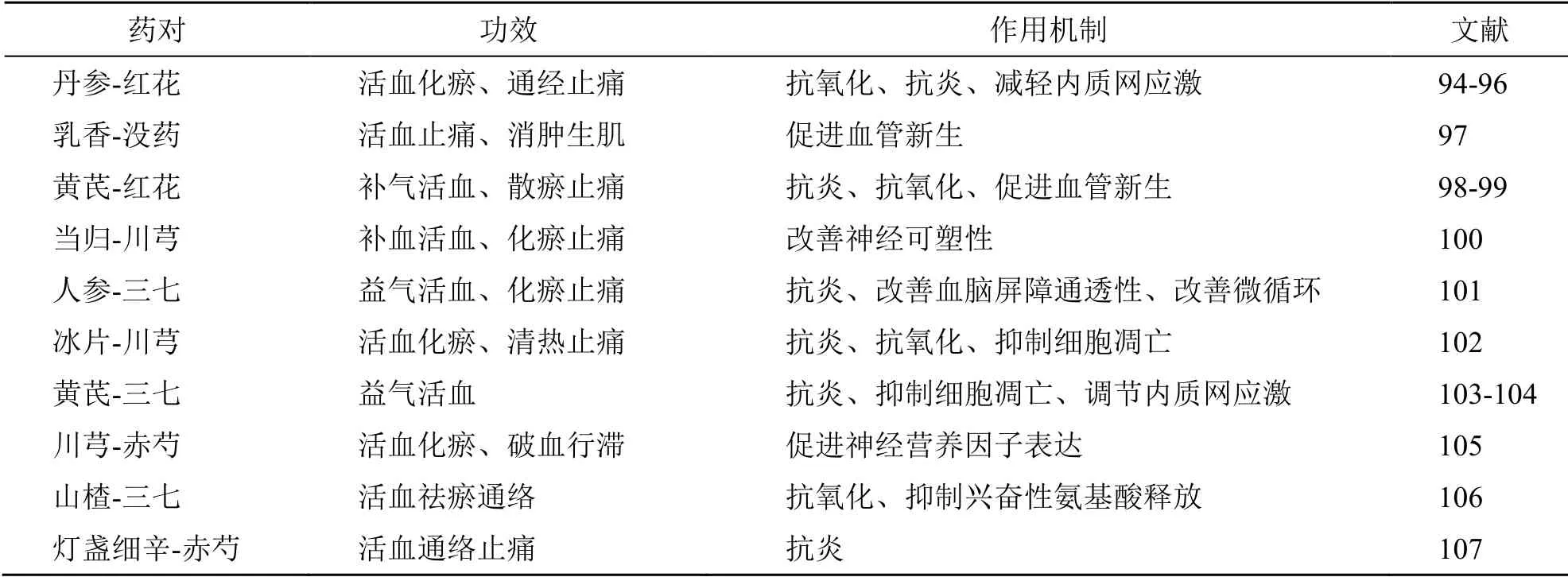
表2 抗CIRI 的中药药对及其作用机制Table 2 Traditional Chinese medicine pairs against CIRI and their mechanisms
3 治疗CIRI 的中药复方
中药复方是中医临床用药的主要形式。研究发现许多经典名方具有抗CIRI 的作用,如补阳还五汤、桃红四物汤等。此外,部分现代中药复方制剂如脉络宁注射液、脑保健颗粒等对CIRI 也具有保护作用。
3.1 补阳还五汤
补阳还五汤出自于清代名医王清任的《医林改错》,由黄芪、当归、赤芍、川芎、桃仁、红花和地龙7 味中药配伍而成,是治疗缺血性脑血管病的经典名方,临床疗效确切。补阳还五汤可通过抑制血小板活化以及谷氨酸过度释放,抑制兴奋性氨基酸毒性等方式发挥抗CIRI 的作用。Zhao 等[108]研究发现补阳还五汤可明显缓解缺血再灌注造成的脑组织损伤,确定了该复方的最佳治疗时间窗为缺血再灌注4 h 内,提示在发生CIRI 早期应用补阳还五汤进行治疗效果更好,此外还推测补阳还五汤发挥疗效与调节谷氨酸受体和抑制谷氨酸释放有关。另有研究表明补阳还五汤发挥抗CIRI 作用还可通过提高脑组织抗氧化水平,减轻脂质过氧化损伤程度,抑制血小板聚集和活化,调节PI3K/Akt 信号通路,促进缺血再灌注损伤后的脑组织修复而实现[109-110]。
3.2 黄连解毒汤
黄连解毒汤为临床常用的清热剂,由黄连、黄芩、黄柏和栀子4 味中药配伍组成,具有清热解毒之效,可泻三焦之热毒。黄连解毒汤可通过抑制氧化应激及炎症反应、调节能量代谢和线粒体功能、抑制细胞凋亡等方式发挥抗CIRI 的作用。已有研究报道称黄芩中的黄芩苷等成分具有较好的抗CIRI 作用。Wang 等[111]采用1H-NMR 代谢组学结合多变量统计分析全面评价了黄连解毒汤抗CIRI 的作用。大鼠血清和脑组织样品的1H-NMR 数据显示黄连解毒汤可明显缓解CIRI 所致的代谢混乱,改善乳酸、葡萄糖和肌酐等代谢产物水平,并可通过保护线粒体膜、调节神经递质和抗氧化、抗炎等方式使脑组织恢复正常状态从而发挥脑保护作用。此外,黄连解毒汤对由缺血再灌注造成的脑组织损伤的保护功能还可通过PI3K/Akt 信号通路激活低氧诱导因子-1α 的表达,进而抑制缺血再灌注诱导的神经凋亡等方式来实现[112-114]。
3.3 地黄饮子
地黄饮子是由熟地黄、巴戟天、山茱萸、石斛、肉苁蓉、附子、五味子、官桂、白茯苓、麦门冬、菖蒲和远志12 味中药根据中医理论配伍而成的传统方剂,具有滋肾阴、补肾阳、开窍化痰的功效,可通过促进神经干细胞增殖、减轻氧化应激损伤、抑制细胞凋亡和促进血管新生等方式发挥抗CIRI的作用。现代临床也逐渐将地黄饮子作为治疗CIRI的有效方剂之一。研究发现地黄饮子可通过激活Notch 信号通路从而改善CIRI 模型大鼠的神经功能,具有一定的剂量相关性[115]。另有研究显示地黄饮子还可使缺血再灌注损伤大鼠模型脑组织中的Bax、Bcl-2、Caspase-3 蛋白和VEGF 的表达水平明显增加,提示地黄饮子还可通过抗氧化、抑制神经细胞凋亡和促进血管新生的方式减轻缺血再灌注所致的神经功能损伤[116]。
3.4 通心络胶囊
通心络胶囊是由人参、水蛭、全蝎、土鳖虫、蜈蚣、蝉蜕、赤芍、檀香、冰片、降香、乳香、酸枣仁12 味中药制成的中药复方制剂,具有益气活血、通络止痛的功效,目前临床上多用该方剂治疗心脑血管疾病。通心络胶囊治疗缺血性脑卒中的作用机制包括抑制炎症反应、改善血脑屏障通透性和促进血管新生等。高志杰等[117]利用动物实验结合网络药理学的方法探讨通心络胶囊对CIRI 的保护作用及其作用机制。动物实验以神经行为学评分、脑损伤程度和脑梗死面积为指标进行评价,结果显示通心络胶囊对CIRI 大鼠的脑组织具有明显的保护作用,并具有一定的剂量相关性。此外为进一步探讨通心络胶囊中真正发挥疗效的化学成分及作用机制,采用网络药理学从通心络胶囊12 味中药中筛选出132 个有效成分和240 个与脑缺血靶基因相交集的基因。网络药理学结果认为重组cAMP 依赖型蛋白激酶A 催化亚基a(protein kinase cAMPactivated catalytic subunit alpha,PRKACA)、腺苷酸环化酶1、多巴胺D2 受体等为通心络胶囊治疗CIRI的核心基因,cAMP 和环磷酸鸟苷酸/环磷酸鸟苷酸依赖性蛋白激酶(cyclic guanosine monophosphate,cGMP/cyclic guanosate-dependent protein kinase,PKG)为通心络胶囊起效的主要信号通路,这为通心络胶囊作用机制的深入研究提供了一定的理论支持。此外,还有研究表明通心络胶囊可有效保护血脑屏障,从而对CIRI 疾病具有预防作用[118]。
除上述复方制剂外,研究发现活血开窍汤[10-11]、三黄泻心汤[119]、桃红四物汤[120-122]、血府逐瘀汤[123]、侯氏黑散[124]、清脑益元汤[125]、芪参益气方[126]、参芎化瘀胶囊[127-130]、复方血栓通胶囊[131]、丹灯通脑胶囊[132]、安脑片[133]、桑芪首乌片[134]、醒脑静注射液[135]、脉络宁注射液[136]、豨莶通栓制剂[137]、栝楼桂枝颗粒[138-140]、脑保健颗粒[141]和复方菖蒲益智汤[142]等中药传统复方及现代复方制剂也具有一定的神经保护作用,见表3。
4 结语与展望
以往对CIRI 的临床治疗多采用尼莫地平、依达拉奉和右美托咪定等能够直接作用于CIRI 病理机制某个靶点或某一环节的药物[143-146]。虽然这些药物起效迅速,但因CIRI 的发生常同时涉及多个环节,其复杂的病理生理机制严重制约着这些药物对该类疾病的临床治疗效果。
具有CIRI 治疗作用的中药及其复方所含有效成分结构类型复杂多样,可协同作用于CIRI 发生与发展的多个病理环节与靶点。即使作用机制或作用靶点相同的中药,其有效成分依然可能具有不同的化学结构类型。如人参皂苷、黄芩苷、丹皮酚虽然分别属于三萜皂苷、黄酮、酚类,化学结构上存在较大差异,分属于不同的结构类型,但3 者均可以通过改善血脑屏障通透性来发挥抗CIRI 的作用[32,53,61]。这为后续从中药中开发新的抗CIRI 候选药物分子提供更多可能。此外,中药配伍(药对配伍和复方配伍)中常含有多种类型的有效成分,这些成分可通过多种途径、多个靶点对CIRI 发挥治疗作用。如丹参与红花配伍后可以通过抗炎和减轻内质网应激发挥抗CIRI 作用[94-96]。补阳还五汤可分别通过抑制血小板活化和谷氨酸过度释放来发挥治疗作用[108-110]。这对于具有复杂病理机制的CIRI 显示出了独特的治疗优势和潜力。

表3 抗CIRI 的中药复方及其功效、作用机制Table 3 Compound traditional Chinese medicine against CIRI and their effects and mechanisms
近年来,中药在防治CIRI 方面取得了不少令人瞩目的研究进展,许多中药有效成分、中药复方在药理实验及临床应用中表现出较显著的治疗效果。但是中药抗CIRI 的研究仍有许多方面需要深入和延续。首先,尽管目前研究发现不同中药中含有结构类型多样的有效成分可对CIRI 的同一靶点发挥作用,但作用机制研究不够深入,研究范围相对局限,研究指标相对单一,这些有效成分对该靶点的作用方式有何异同尚不清楚。这些问题的阐明将为从中药中开发出新型抗CIRI药物,解释中药抗CIRI科学内涵奠定基础。其次,由于单味药及中药复方中有效成分复杂多样,相互间作用关系尚不明晰,阻碍了中药抗CIRI 的深入研究和临床应用。今后应进一步明确中药(复方)抗CIRI 的活性成分(组分群),加强中药有效成分以及单味、配伍之间关系的研究。再者,要注意药理实验与临床验证相结合。药理学研究应体内和体外实验联合,发挥现代药理学的优势,从多方面探讨中药抗CIRI 的作用及机制。临床试验前,应选择与临床病例相近的动物实验和动物模型,对药物的作用机制、治疗窗、药动学和药效学进行详细研究和验证。
中药治疗疾病的短板之一是起效较慢,对于治疗窗窄的疾病往往达不到满意的治疗效果。化学药作用靶点单一、不良反应较多,但起效迅速是其相对于中药治疗的优势之一。因此,可考虑将中药与化学药合理联用,为抗CIRI 研究提供新方向。随着CIRI 发病机制研究的不断深入,中药及其复方抗CIRI 的作用机制、治疗时间窗和药代动力学等研究也日渐明朗。相信随着科学研究和临床研究的循序推进,CIRI 治疗困难的现况定会取得突破性进展。
利益冲突所有作者均声明不存在利益冲突

