血压与2型糖尿病患者视网膜神经纤维层厚度的相关性
王晓光,刘杰,杜金秋,张慧娟
(哈尔滨医科大学附属第一医院内分泌科,哈尔滨 150001)
糖尿病视网膜病变(diabetic retinopathy,DR)是2型糖尿病( type 2 diabetes mellitus,T2DM) 常见慢性微血管并发症之一,严重者可导致失明。最新研究表明T2DM在出现临床可见的视网膜微血管改变前已出现视网膜神经退行性改变[1-3]。有报道证实,视网膜神经退行性改变涉及神经元凋亡、节细胞体丢失和胶质细胞反应性缺陷。在神经元改变中,视网膜神经纤维层(retinal nerve fiber layer,RNFL)变薄是视网膜神经退行性病变的早期表现[4],可通过光学相干断层成像(optical coherence tomography,OCT)对RNFL厚度进行精确测量,观察其变化[5]。随着生活方式的改变,高血压成为糖尿病患者的常见合并症, 同时也是心、脑、肾等器官病变的已知高危因素, 其对视网膜血管病变有一定的促进作用[6]。本研究通过分析T2DM患者血压与RNFL的相关性,为探讨血压对DR的影响提供依据。
1 对象与方法
1.1 研究对象
回顾性分析2017年1月至2018年12月就诊于哈尔滨医科大学附属第一医院内分泌科的123例T2DM患者,中位年龄53(46,59)岁,中位糖尿病病程8(3,13)年。根据荧光素眼底血管造影(fundus fluorescein angiography,FFA)结果, 按糖尿病性视网膜病变新的国际临床分级标准(2002年)[7],将患者分为无糖尿病视网膜病变(non-diabetic retinopathy,NDR)组65例和非增殖期糖尿病视网膜病变(non-proliferative diabetic retinopathy,NPDR)组58例。纳入标准:(1)符合WHO 1999年制订的《糖尿病诊断标准》[8];(2)根据最新的ESC/ESH动脉高血压管理指南,入组患者最多1级高血压,血压<160/100mmHg(1 mmHg=0.133 kPa)[9];(3)无高眼压病史,眼压范围11~21 mmHg;(4)无特殊眼部病史。排除标准:(1)增殖期糖尿病视网膜病变;(2)1型及特殊类型糖尿病;(3)阿尔茨海默症等神经系统疾病,全身系统性疾病及高血压导致的视网膜病变。本回顾性研究遵循《赫尔辛基宣言》,获得哈尔滨医科大学附属第一医院伦理委员会批准,免除患者签署知情同意书。
1.2 方法
1.2.1 收集患者基线资料 收集入组患者的一般资料,包括年龄、性别、病程、体质量指数(body mass index,BMI)等。所有患者均进行眼压、FFA检查。
1.2.2 血生化检查 收集研究对象空腹血糖(fasting plasma glucose,FPG)、糖化血红蛋白A1c(glycosylated hemoglobin A1c,HbA1c)、总胆固醇(total cholesterol,TC)、甘油三酯(triglycerides,TG)、血肌酐(serum creatinine,SCr)、尿素氮(blood urea nitrogen,BUN)等检验结果。
1.2.3 血压检查 选取温度适宜、环境安静的房间。嘱患者静坐休息5~10 min后使用台式水银血压计测量两次血压,两次测量间隔5 min。记录收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP),取两次测量平均值作为血压结果用于分析。计算平均动脉压(mean arterial pressure,MAP),MAP=(SBP+2×DBP)/3。
1.2.4 OCT测定RNFL厚度 应用德国海德堡OCT仪(870 nm波长,40000 Hz/s)进行检查,以视盘中点为中心,进行直径为3.45 mm的圆盘区域扫描,行3次重复性较好的优化扫描。利用计算机图像分析系统进行RNFL厚度的测量,测量参数包括: 鼻上(superonasal, NS)、鼻下(inferonasal, NI)、鼻侧(nasal, N)、颞上(supratemporal, TS)、颞下(infratemporal, TI)、颞侧(temporal,T)RNFL厚度。同一操作者选用同一设备,同一患者双眼病变程度相同者随机选一只眼的OCT数据,病变程度不同者选取病变严重的眼OCT数据入组。每眼至少扫描3次,取信号最好、重复率最高的数值进行保存分析。
1.3 统计学处理

2 结 果
2.1 2组患者基线资料比较
与NDR组相比,NPDR组年龄、病程、BMI、SBP、MAP和尿素氮明显增高,RNFL厚度在NI、TI象限明显变薄,差异均有统计学意义(P<0.05;表1)。
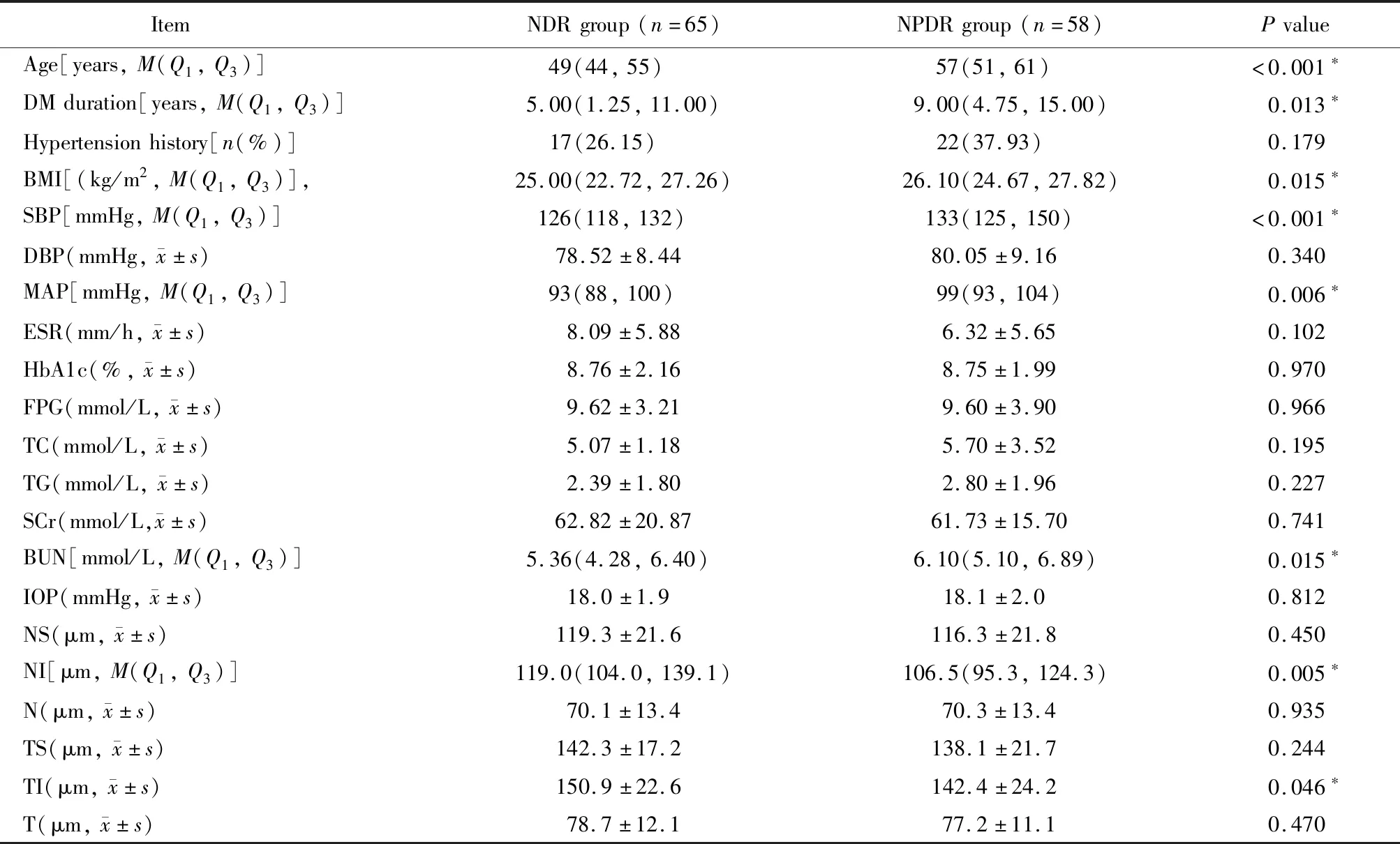
表1 2组患者基本资料比较
2.2 各象限RNFL厚度与相关指标的相关性分析
年龄与视网膜TS(r=-0.184,P=0.041)、TI(r=-0.224,P=0.013)象限 RNFL 厚度均显著负相关;BMI与视网膜NI(r=-0.256,P=0.004)象限RNFL厚度显著负相关;SBP与视网膜NS(r=-0.203,P=0.024)、TI(r=-0.272,P=0.002)、T(r=-0.286,P=0.001)象限 RNFL 厚度均显著负相关;MAP 与视网膜NS(r=-0.185,P=0.041)、TI(r=-0.264,P=0.003)、T(r=-0.253,P=0.005)象限 RNFL 厚度均显著负相关;HbA1c与视网膜TS(r=-0.234,P=0.009)、TI(r=-0.201,P=0.025)象限 RNFL 厚度均显著负相关。详见表2。

表2 各象限 RNFL厚度与相关指标的相关性分析
2.3 单因素线性回归分析结果
以T2DM 患者各象限RNFL为因变量,进行单因素线性回归分析,结果显示,年龄、BMI、SBP、MAP、HbA1c与T2DM 患者RNFL厚度相关(P<0.05;表3)。
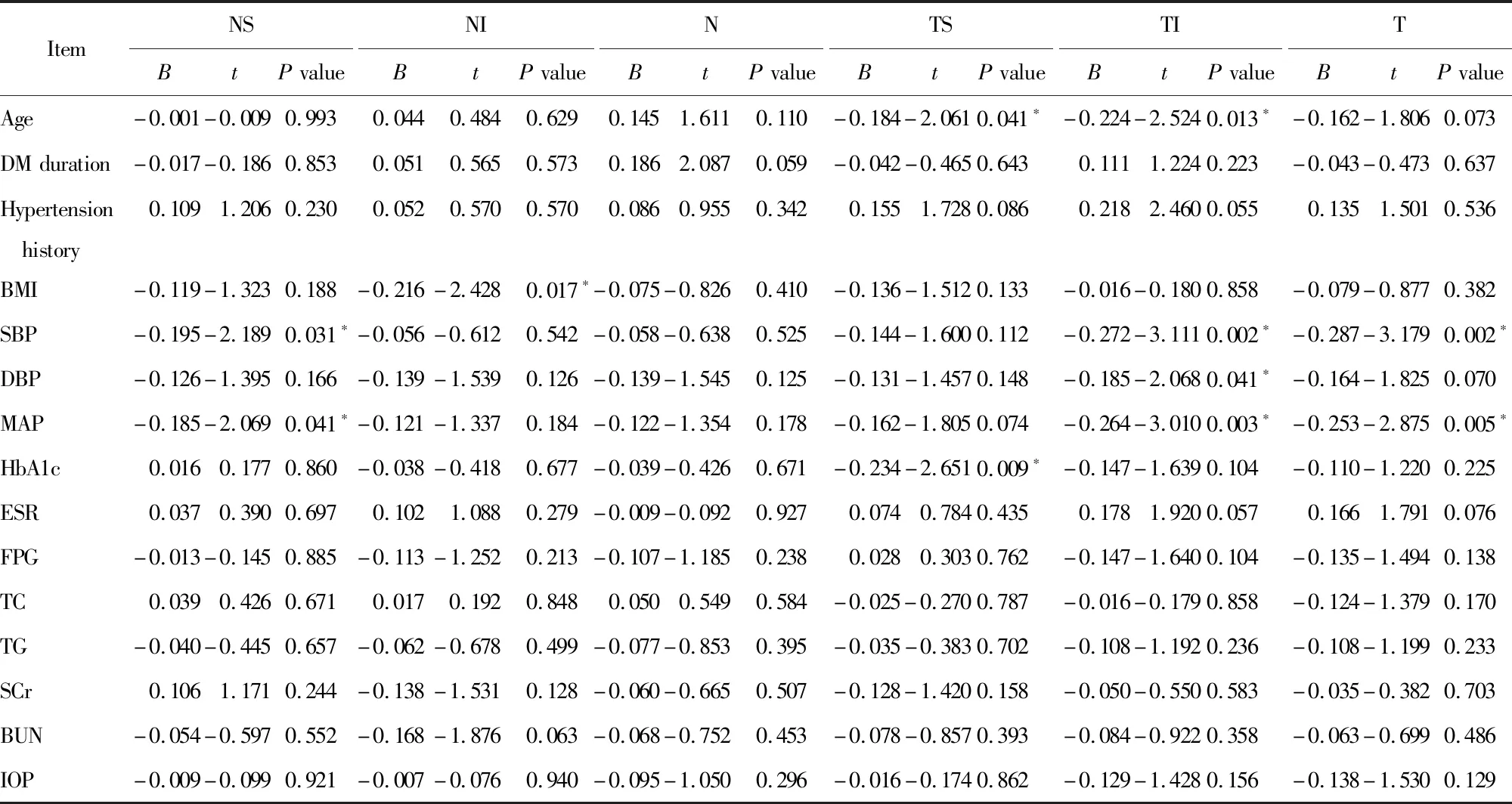
表3 T2DM 各象限 RNFL 厚度单因素线性回归分析
2.4 多因素线性回归分析结果
在上述单因素线性回归分析基础上,以T2DM患者各象限RNFL为因变量,以年龄、BMI、HbA1c、SBP为自变量,行多因素线性回归分析,结果显示SBP是视网膜NS、TI、T象限RNFL厚度的独立影响因素(P<0.05;表4)。
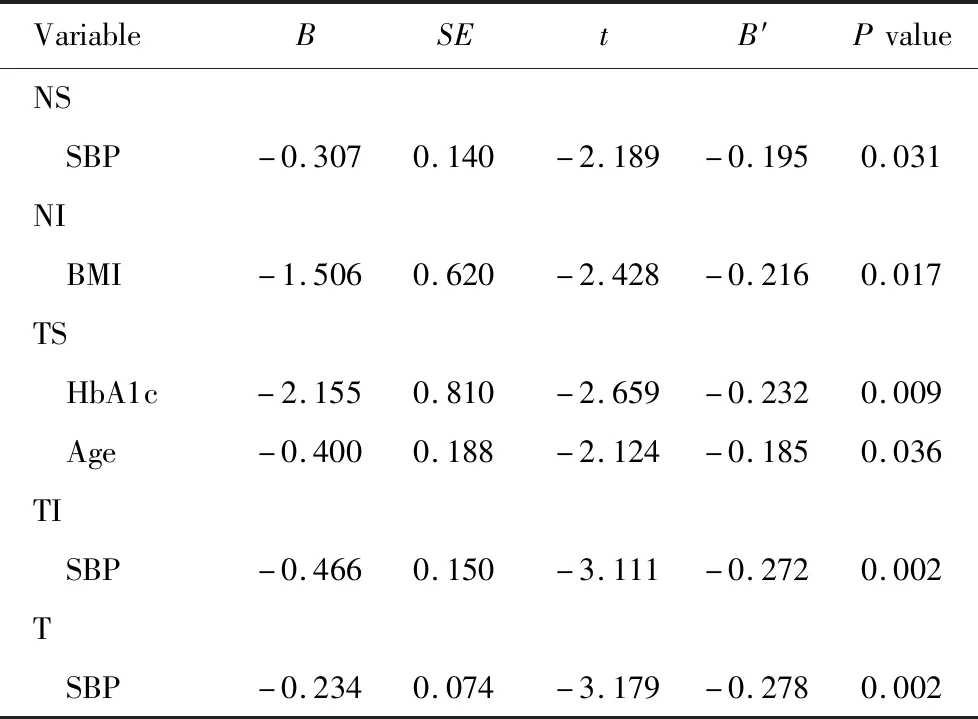
表4 T2DM患者各象限RNFL厚度多因素线性回归分析
3 讨 论
既往临床研究证实了高血压是大血管和微血管功能障碍的重要决定因素[10,11]。轻度升高的血压也会导致脑血管损伤,引起神经退行性改变[12]。RNFL作为视网膜神经退化的早期指标,临床上常用OCT技术对其进行精确测量,OCT具有轴向高分辨率、可量化测量、可重复性强及安全性好的特点。目前关于中国糖尿病人群血压和RNFL相关性的研究较少,本研究探讨了血压与T2DM患者RNFL厚度之间的相关关系。
有研究证实血压升高会导致RNFL厚度显著降低[13],一项关于恒河猴的动物实验表明,慢性高血压会导致RNFL的萎缩[14]。既往以高血压人群为研究对象的横断面研究发现,SBP、DBP及MAP的增高会导致RNFL厚度变薄[15]。本研究以T2DM患者为研究对象,相关性结果显示,SBP、DBP和MAP与RNFL厚度呈显著负相关。对结果进一步进行单因素及多因素线性回归分析,在调整年龄、BMI、HbA1c混杂因素后,显示SBP仍然是RNFL厚度变薄的独立危险因素。可能原因是在视网膜内存在重要的血流调节机制[16,17],有助于在灌注压力变化期间使血流保持相对恒定。灌注压=MAP-眼压(intraocular pressure,IOP)[16]。灌注压主要受血压影响,血压升高时,灌注压会明显升高,当灌注压高于血流调节机制的正常调节范围上限时,会使视网膜血流调节机制异常,导致视网膜神经组织局部缺血。另一项临床调查结果显示,高血压患者的视网膜小动脉口径与SBP和DBP水平呈负相关[18],随着血压升高,视网膜小动脉口径变小,血管内血流阻力增加,从而影响视网膜血流灌注,扰乱视网膜血流调节功能[19],最终导致RNFL变薄[20,21]。这两项临床研究从不同角度得到了相同的结论,均证实了血压通过不同的方式影响了RNFL厚度。但目前血压升高导致RNFL变薄的具体机制尚未明确,有待进一步研究。
综上所述,对于T2DM患者,1级高血压也会加速视网膜神经退行性改变,临床上对T2DM患者的血压管理应更为严格。本研究存在一定的局限性:(1)样本量小且缺少健康对照组,实验结果可能存在抽样误差,有待进一步大样本多中心研究加以证实;(2)因是回顾性研究,缺少24小时动态血压监测结果数据。

