心痛定联合拉贝洛尔治疗妊娠期高血压疾病效果及患者血清IGF-1、HSP70水平变化
王妍,王立媛,王静
本溪市中心医院,辽宁本溪117000
妊娠期高血压疾病(HDP)是常见的妊娠合并症,表现为血压升高、蛋白尿、血液流变学改变,严重者可导致抽搐、昏迷、多系统功能紊乱、胎盘早剥、血管内溶血等后果,威胁母婴安全[1-2]。研究表明,血清胰岛素样生长因子1(IGF-1)、热休克蛋白70(HSP70)指标水平与HDP发病及胎盘着床密切相关[3-4]。目前,临床治疗HDP以镇静、解痉、降压、吸氧等综合方案为主。拉贝洛尔为HDP一线治疗药物,主要通过降低周围血管交感神经兴奋性发挥降压效果[5]。心痛定是一种钙离子拮抗剂,多项研究证实其在HDP防治中发挥积极作用[6-7],但与拉贝洛尔联合应用能否进一步提高疗效尚未见报道。2017年3月—2019年1月,我们观察了心痛定联合拉贝洛尔治疗HDP的效果,并分析其对血清IGF-1、HSP70水平的影响。
1 资料与方法
1.1 临床资料 经本溪市中心医院医学伦理委员会批准,收集同期我院收治的HDP患者。纳入标准:①均符合《妊娠期高血压疾病疾病诊治指南(2015)》[8]中相关诊断标准;②单胎妊娠;③患者及家属知情并签署同意书。排除标准:①妊娠期糖尿病;②凝血系统障碍;③精神疾病;④对本研究药物过敏;⑤肝肾功能不全;⑥治疗前存在胚胎畸形。共选取HDP患者141例,随机分为三组各47例。观察组年龄(28.07±2.87)岁,BMI(21.75±1.58)kg/m2,初产妇31例、经产妇16例,孕(29.82±2.94)周,病情为轻度15例、中度19例、重度13例;对照A组年龄(28.32 ± 3.05)岁,BMI(21.89 ± 1.65)kg/m2,初产妇33例、经产妇14例,孕(30.08±3.15)周,病情为轻度16例、中度17例、重度14例;对照B组年龄(28.51 ± 2.96)岁,BMI(21.96 ± 1.74)kg/m2,初产妇34例、经产妇13例,孕(29.94±2.86)周,病情为轻度14例、中度20例、重度13例;三组年龄、BMI、产妇类型、孕周、病情具有可比性。
1.2 治疗方法 三组均给予吸氧、镇静、解痉等基础治疗。在此基础上,观察组予以心痛定(天津太平洋制药有限公司,国药准字H12020305)10 mg/次,舌下含服,每6 h服药1次;拉贝洛尔(郑州凯利药业有限公司,国药准字H41024906)100 mg/次,口服,每天3次。对照A组予以心痛定治疗,对照B组予以拉贝洛尔治疗,用法用量同观察组。三组均持续治疗7 d。
1.3 临床疗效判定方法 显效:蛋白尿与水肿显著改善,平均动脉压降低>20 mmHg;有效:蛋白尿与水肿改善,平均动脉压降低10~20 mmHg;无效:未达到上述标准。有效率=(显效+有效)例数/总例数×100%。
1.4 观察指标及方法 ①血压:治疗前后采用电子血压仪测量血压;②尿蛋白:治疗前后收集尿液,用BECKMAN IMMAGE 800全自动尿蛋白仪测定24 h尿蛋白;③血液流变学:治疗前后采静脉血,用M850血液流变分析仪(美国Grace公司)检测血液流变学指标(全血高切黏度、全血低切黏度、血浆黏度、纤维蛋白原);④血清IGF-1、HSP70:治疗前后空腹抽取静脉血3 mL,以3 500 r/min离心9 min后取血清,以酶联免疫吸附法检测IGF-1、HSP70,试剂盒由北京普尔伟业生物科技有限公司提供;⑤母婴结局:随访至产后,记录新生儿窒息、宫内窘迫、早产、产后出血等母婴不良结局发生情况。
1.5 统计学方法 采用SPSS22.0统计软件。计数资料以例或百分比表示,组间比较行χ2检验;计量资料以表示,多组间比较行单因素方差分析,组内两两比较行LSD-t检验。P<0.05为差异有统计学意义。
2 结果
2.1 三组临床疗效比较 观察组显效17例、有效27例、无效3例、总有效率93.62%,对照A组显效10例、有效25例、无效12例、总有效率74.47%,对照B组显效12例、有效24例、无效11例、总有效率76.60%;观察组临床疗效总有效率高于对照A、B组(P均<0.05),对照A、B组间差异无统计学意义。
2.2 三组治疗前后血压比较 治疗前,三组舒张压、收缩压差异无统计学意义;治疗后,观察组舒张压、收缩压低于对照A、B组(P均<0.05),对照A、B组间差异无统计学意义。见表1。
表1 三组治疗前后血压比较(mmHg,)
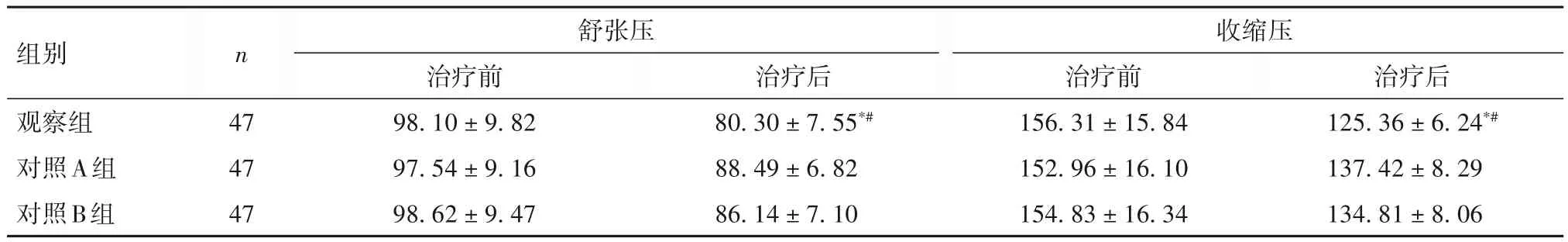
表1 三组治疗前后血压比较(mmHg,)
注:与对照A组同时点比较,*P<0.05;与对照B组同时点比较,#P<0.05。
images/BZ_77_235_2381_2243_2499.png观察组对照A组对照B组 125.36±6.24*#137.42±8.29 134.81±8.06 98.10±9.82 97.54±9.16 98.62±9.47 47 47 47 80.30±7.55*#88.49±6.82 86.14±7.10 156.31±15.84 152.96±16.10 154.83±16.34
2.3 三组治疗前后24 h尿蛋白比较 治疗前,三组24 h尿蛋白差异无统计学意义;治疗后,观察组24 h尿蛋白低于对照A、B组(P均<0.05),对照A、B组间差异无统计学意义。见表2。
2.4 三组治疗前后血液流变学指标比较 治疗前,三组各项血液流变学指标差异无统计学意义;治疗后,观察组血液流变学指标均低于对照A、B组(P均<0.05),对照A、B组间差异无统计学意义。见表3。
表2 三组治疗前后24 h尿蛋白比较(mg/24 h,)
注:与对照A组同时点比较,*P<0.05;与对照B组同时点比较,#P<0.05。
组别治疗后478.82±35.41*#832.56±40.15 816.47±39.83 n观察组对照A组对照B组47 47 47 24 h尿蛋白治疗前1 257.74±154.63 1 248.69±165.24 1 253.67±159.61
表3 三组治疗前后血液流变学指标比较()
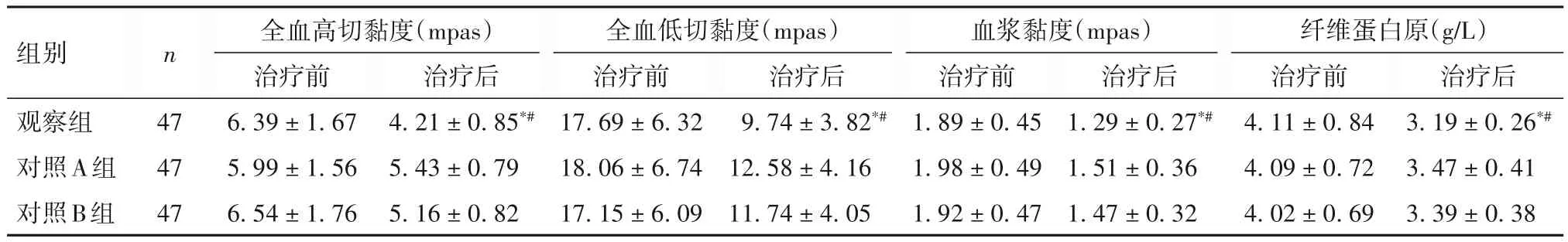
表3 三组治疗前后血液流变学指标比较()
注:与对照A组同时点比较,*P<0.05;与对照B组同时点比较,#P<0.05。
组别观察组对照A组对照B组n治疗后3.19±0.26*#3.47±0.41 3.39±0.38治疗后4.21±0.85*#5.43±0.79 5.16±0.82 47 47 47全血高切黏度(mpas)治疗前6.39±1.67 5.99±1.56 6.54±1.76全血低切黏度(mpas)治疗前17.69±6.32 18.06±6.74 17.15±6.09治疗后9.74±3.82*#12.58±4.16 11.74±4.05血浆黏度(mpas)治疗前1.89±0.45 1.98±0.49 1.92±0.47治疗后1.29±0.27*#1.51±0.36 1.47±0.32纤维蛋白原(g/L)治疗前4.11±0.84 4.09±0.72 4.02±0.69
2.5 三组治疗前后血清IGF-1、HSP70水平比较 治疗前,三组血清IGF-1、HSP70水平差异无统计学意义;治疗后,观察组血清IGF-1水平高于对照A、B组而HSP70水平低于对照A、B组(P均<0.05),对照A、B组间差异无统计学意义。见表4。
表4 三组治疗前后血清IGF-1、HSP70水平比较()

表4 三组治疗前后血清IGF-1、HSP70水平比较()
注:与对照A组同时点比较,*P<0.05;与对照B组同时点比较,#P<0.05。
images/BZ_78_235_1044_2243_1162.png 302.54±80.41 294.25±78.41 289.36±75.37观察组对照A组对照B组1.47±0.56*#1.89±0.54 1.82±0.60 376.34±79.67*#333.49±72.58 340.74±70.69 47 47 47 2.34±0.92 2.63±0.98 2.14±0.85
2.6 三组母婴不良结局情况比较 观察组宫内窘迫、早产、产后出血发生率低于对照A、B组(P均<0.05),对照A、B组差异无统计学意义。见表5。

表5 三组母婴不良结局情况比较[例(%)]
3 讨论
HDP是导致孕妇及围产儿死亡的主要原因,约占妊娠相关致死因素的15%[9]。研究发现,小动脉痉挛导致管腔狭窄、内皮细胞损伤、血管通透性与阻力增加为HDP基本病理改变[10]。同时,患者各组织器官由于缺血缺氧损伤,严重时可诱发肾、心、脑等重要脏器病变,导致抽搐、昏迷、脑水肿、脑出血、肝细胞坏死、肺水肿、胎盘绒毛退行性变、弥散性血管内凝血、胎盘早剥等严重并发症。因此,积极寻找一种有效、安全、可行的治疗方案对HDP患者尤为关键。
拉贝洛尔为水杨酰胺的衍生物,可舒张血管,抑制交感神经兴奋,发挥降压作用;并可改善冠状动脉、脑血管痉挛,预防脑缺血与心肌缺血[11]。心痛定通过抑制钙离子通道,抑制平滑肌收缩,松弛血管平滑肌,扩张全身血管,具有强效持久的降压作用;同时,其对循环系统功能压力小,不良反应少,可有效预防先兆流产,防治抽搐发生;此外,含服更易吸收,可更好地发挥其药理作用,生物利用度高。多项研究认为,心痛定可有效缓解HDP动脉痉挛,降低血压[12-13]。本研究首次联合心痛定、拉贝洛尔治疗HDP患者,结果显示,观察组临床疗效高于对照A、B组,治疗后观察组舒张压、收缩压低于对照A、B组,观察组宫内窘迫、早产、产后出血发生率低于对照A、B组。究其原因为拉贝洛尔、心痛定均降压明确,或具有协同增效作用。蛋白尿为HDP重要临床表现,其含量可反映患者病情程度与治疗效果。本研究结果显示,治疗后观察组24 h尿蛋白较对照A、B组显著降低。这表明拉贝洛尔、心痛定联合治疗HDP可有效降低尿蛋白滤过,保护肾脏功能。研究表明,HDP患者均伴不同程度血液流变学改变,可增加血栓形成风险,也是并发脑血管意外的重要因素[14]。本研究结果显示,治疗后观察组全血高切黏度、全血低切黏度、血浆黏度、纤维蛋白原均低于对照A、B组。分析其原因在于,心痛定通过松弛平滑肌、扩张血管、抑制血小板活化等作用,改善微循环;与拉贝洛尔协同降低血浆黏度,从而改善血液流变学指标。
目前,HDP发病机制仍未完全明确,对其病因及发病机制的研究一直为产科重要课题之一。IGF-1、HSP70在HDP发生发展中起到重要作用。IGF-1具有多功能细胞调控作用,对细胞增殖、分化、生长、迁移均有促进作用。研究表明,胎盘组织具有极强的内分泌功能,可合成IGF-1并参与滋养细胞功能调控;IGF-1表达不足可影响绒毛合体滋养细胞对母体蜕膜及螺旋动脉的侵入,导致胎盘血流灌注不足[15]。米娜瓦尔·艾则孜[16]研究发现,HDP患者血清IGF-1水平降低。HSP70是重要的应激反应蛋白,当机体处于应激状态时,细胞可短时间内大量合成HSP70,以降低应激损伤。研究报道,HDP患者血清HSP70水平增高,且随妊娠周期增加而逐渐增高,并认为其参与胚胎发育与细胞增殖[17]。本研究结果显示,治疗后,观察组血清IGF-1水平高于对照A、B组,HSP70水平低于对照A、B组。这表明心痛定联合拉贝洛尔可调节HDP患者血清IGF-1、HSP70水平,考虑与血压得到有效控制、血液流变学改善等有关。但本研究未探究IGF-1、HSP70表达是否存在相关性及通过哪种通路形成反馈调节关系,有待进一步论证。
综上所述,心痛定联合拉贝洛尔治疗HDP患者可通过调节血清IGF-1、HSP70水平,改善血液流变情况,提高血压控制效果,减轻蛋白尿,进而改善母婴结局。

