维格列汀通过调控炎症细胞因子和Nrf2途径促进糖尿病足溃疡创面愈合
王晓娟,曹海泉,袁 宁,何明海
(1川北医学院第二临床医学院,南充市中心医院内分泌科,南充 637000;2南充市中心医院重症医学科;3南充市中心医院内分泌科;*通讯作者,E-mail:yixueyan2020@163.com)
糖尿病足溃疡(diabetic foot ulcer,DFU)是糖尿病患者的严重并发症之一,与神经病变、肾病、心肌病变、血管病变、酮症酸中毒并列[1]。DFU创面愈合过程是一个复杂的、多阶段的过程,由于各种复杂性,患者血管生成和再上皮化不足,严重炎症是中性粒细胞浸润引起的另一个有害因素。此外,DFU是剧烈炎症的结果[2]。由于糖尿病患者发生DFU的风险增加,导致生活质量下降,生产力损失,也给医疗系统带来了巨大的经济负担,患有DFU的2型糖尿病患者每年的直接和间接医疗费用为13 561美元[3]。有证据表明导致伤口愈合延迟的各种因素包括血糖水平升高、胰岛素抵抗增加、血管生成和胶原沉积减少、浸润反应延迟、伤口部位血液供应受阻、颗粒组织形成减少和血液黏度增加[4]。尽管在过去的几十年里对DFU的研究取得了巨大的突破,但有效地治疗DFU仍然是一个挑战。有报道指出,维格列汀在治疗糖尿病方面具有较好的效果[5],但关于其对DFU创面修复的研究还尚未清晰,由此,本研究拟观察维格列汀对DFU大鼠创面修复的影响,为其治疗DFU提供理论依据。
1 材料和方法
1.1 实验动物及分组
成年雌性SD大鼠45只,体质量(210±10)g,购于成都达硕实验动物有限公司,许可证号:SCXK(川)2019-031。饲养于恒温(20-25 ℃)、恒湿(50%±5%)环境中,自然采光,自由饮水。大鼠适应性饲养1周后随机分为3组:空白组、模型组(糖尿病鼠足溃疡)、维格列汀组,每组15只。
1.2 主要试剂及设备
维格列汀购自诺华公司(批号:H20160037);IL-1β ELISA试剂盒(货号:ZC-36391)、IL-6 ELISA试剂盒(货号:ZC-36404)和TNF-α ELISA试剂盒(货号:ZC-37624)购自上海茁彩生物科技有限公司;苏木素染液(批号:C200301)、伊红染液(批号:C200403)购自珠海贝索生物技术有限公司。Collagen-Ⅰ(货号:ab260043)、Keap1(货号:ab139729)、Nrf2(货号:ab137550)、TGF-β(货号:ab215715)、α-SMA(货号:AF1032)一抗抗体购自英国Abcam公司;过氧化物酶标记羊抗兔IgG(上海晶天生物)、BMJ-A型包埋机购自常州郊区中威电子仪器厂;SpectraMAX Plus384酶标仪购自美谷分子仪器有限公司;生化自动分析仪(Beckman Coulter Inc.,爱尔兰)。
1.3 糖尿病足溃疡大鼠模型的建立及给药
大鼠自适应喂养1周后,进行模型制备,除空白组外,其余大鼠造模,造模前大鼠禁食12 h,但可饮水,造模大鼠采用高糖高脂饲料喂养4-6周,大鼠腹腔注射链脲佐菌素(STZ)50 mg/kg诱发罹患糖尿病,用药72 h后,自尾静脉微量采血检测随机血糖,当血糖值超过16.7 mmol/L,即为糖尿病大鼠造模成功。随后造模大鼠用10%戊巴比妥钠麻醉,于大鼠的足背皮肤,以印章作3 mm×7 mm的矩形标记,切除全层皮肤,75%酒精棉球消毒创面,形成足部皮肤溃疡大鼠模型[6]。空白组大鼠始终予以标准饲料喂养,不进行STZ注射,但进行印章创口手术。大鼠创面造模成功后24 h,空白组和模型组予以等体积生理盐水灌胃(2 ml/100 g),维格列汀组灌胃维格列汀(57 mg/kg),1次/d。分别连续给药3,6,9 d,每组各取5只进行取材,大鼠禁食12 h,用10%戊巴比妥钠腹腔注射进行麻醉,剪取创面及周围3 mm组织,将70%的组织迅速置于-20 ℃低温冰箱保存,30%的组织用4%多聚甲醛溶液固定,待测。
1.4 大鼠创面组织病理学观察
将4%多聚甲醛溶液固定的创面组织经全自动脱水机脱水,包埋,切片,放入苏木精中染色约10 min,自来水冲洗使切片颜色变蓝,1%盐酸酒精分化数秒钟,使细胞核呈紫蓝色,1%氨水中数秒,至返蓝,1%伊红染色3 min左右,脱水,透明,中性树胶封存,镜检观察组织病理变化。
1.5 生化参数测定
空腹动物经颈静脉采集血样,所有大鼠的血糖水平通过数字血糖仪获得,采用生化自动分析仪测定血清总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白(HDL)和低密度脂蛋白(LDL)浓度。
1.6 ELISA法检测创面组织IL-1β、TNF-α和IL-6含量
取0.1 g创面组织,加入500 μl PBS研磨,12 000g4 ℃离心15 min收集上清液。分别设置空白孔、标准品孔和待测样品孔,空白孔不加样品;标准品孔加入配好的标准品50 μl,然后加入辣根过氧化物酶100 μl;待测样品孔加入样本50 μl,然后辣根过氧化物酶100 μl,37 ℃温育60 min。随后小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置1 min后弃去,如此重复5次。按照ELISA试剂盒说明操作,最后每孔加终止液50 μl,终止反应,在15 min内,450 nm波长依序测量各孔的吸光度(OD值)。绘制标准曲线,根据样品的OD值由标准曲线计算相应的浓度。
1.7 Western blot检测创面组织Nrf2、Keap1、collagen-Ⅰ、TGF-β和α-SMA蛋白表达
取-20 ℃低温冰箱保存的大鼠创面组织样本,RIPA裂解液裂解,BCA蛋白定量试剂盒测定蛋白浓度,样品煮沸变性后于-20 ℃保存备用。使用等量蛋白质上样,选择10%的SDS-PAGE进行分离,分离后的蛋白质转移至PVDF膜上,用5%的脱脂奶粉封闭1 h,封闭结束后按照实验目的结合一抗β-actin(1∶10 000)、Nrf2(1∶2 000)、Keap1(1∶1 000)、collagen-Ⅰ(1∶1 000)、TGF-β(1∶1 000)、α-SMA(1∶1 000),4 ℃孵育过夜后TBST清洗,然后选择合适的二抗在室温孵育1 h,TBST清洗,ECL暗室显色。使用Bio-Rad全功能成像系统采集图像,Image-ProPlus分析光密度,以β-actin为内参计算各组蛋白质的相对表达量。
1.8 统计学分析
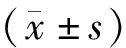
2 结果
2.1 维格列汀对溃疡创面组织病理学变化的影响
空白组大鼠分别在给药3,6,9 d真皮内胶原纤维交错排列,成纤维细胞团状排列,胞质红染,皮下脂肪层及肌层结构较清晰可见,细胞核形态正常。模型组大鼠在给药后3 d创面组织内表皮、真皮、皮下脂肪层大面积坏死脱落,细胞形态基本消失;给药6 d创面组织内表皮中复层扁平上皮层明显增厚,表面覆有由变性坏死细胞及出血混合而成的痂皮,真皮层大量胶原纤维坏死和皮下脂肪层和肌层坏死;给药9 d创面组织复层扁平上皮层明显增厚,毛囊和皮脂腺等皮肤附属器基本坏死消失,表皮表面覆有由变性坏死细胞及出血混合而成的痂皮,真皮层较多大量胶原纤维坏死,坏死区域可见较多炎症细胞浸润。维格列汀给药3 d创面组织内表皮中复层扁平上皮层明显增厚,表皮层细胞坏死,胞核崩解,见表皮表面覆有由变性坏死细胞及出血混合而成的痂皮;给药6 d表皮层细胞坏死,表皮表面覆有由变性坏死细胞及出血混合而成的痂皮,真皮层较多胶原纤维坏死,出血;给药9 d真皮层胶原纤维坏死区域可见淋巴细胞浸润及纤维细胞增生,亦可见新生毛细血管形成,皮下肌层清晰可见,胞核形态正常,其他未见明显病理变化;与模型组9 d相比,病理损伤明显改变(见图1)。

A.HE染色(×100) B.HE染色(×400)
2.2 维格列汀对溃疡创面空腹血糖和血脂水平的影响
与空白组比较,给药3 d,模型组TC、TG、HDL、LDL和GLU水平均无明显变化(P>0.05);给药6,9 d,TC、HDL和LDL明显升高(P<0.05);与模型组比较,维格列汀给药6,9 d,HDL和LDL水平明显降低(P<0.05),而TC、TG和GLU水平差异无统计学意义(P>0.05,见表1)。

表1 各组大鼠空腹血糖和血脂水平变化
2.3 维格列汀对溃疡创面炎症细胞因子的影响
与空白组比较,给药3,6,9 d模型组IL-1β、IL-6、TNF-α含量均明显升高(P<0.05),与模型组比较,给药9 d维格列汀组IL-1β、IL-6、TNF-α含量明显降低(P<0.05,见图2)。

与空白组比较,*P<0.05,**P<0.01;与模型组比较,#P<0.05,##P<0.01
2.4 维格列汀对溃疡创面Nrf2途径的影响
与空白组比较,给药3,6,9 d模型组Nrf2、collagen-Ⅰ、TGF-β、α-SMA蛋白表达均明显降低,Keap1蛋白表达明显升高(P<0.05)。与模型组比较,给药9 d维格列汀组Nrf2、collagen-Ⅰ和α-SMA蛋白表达明显升高(P<0.05);给药6 d,Keap1蛋白表达明显降低(见图3)。

与空白组比较,*P<0.05,**P<0.01;与模型组比较,#P<0.05,##P<0.01
3 讨论
糖尿病可影响皮肤损伤修复的止血、炎症、增殖、成熟步骤,导致延迟修复或发展为慢性伤口,DFU是糖尿病最致命的并发症之一,目前临床上治疗DFU的主要措施为降糖、降脂、抑制炎症反应等,但DFU的现有治疗如改善感觉神经传导速度的肌醇,高压氧治疗等促进创面愈合的疗效有限[7]。研究证明维格列汀在治疗糖尿病方面具有较好的效果,可能是治疗DFU的一种有前途的治疗选择[8]。因此,本研究评估维格列汀对糖尿病引起的伤口延迟愈合的潜在作用。在各种动物模型中,STZ诱导的模型重复性较高,可模拟大多数延迟伤口愈合的临床病理条件,包括再上皮化、伤口闭合和生长因子形成[9]。研究报道伤口愈合是对创伤组织的一种反应,导致组织完整性的重建,因此,伤口收缩和闭合是开放创面愈合过程中的重要标志,而创面模型的愈合阶段在此过程中受到不同程度的影响[10]。与模型组大鼠相比,维格列汀组治疗9 d创面胶原纤维排列整齐,成纤维细胞增多,新生血管形成,创面修复良好。研究指出改善创面愈合可以洞察疾病状况[11]。在本研究中,维格列汀可明显改善STZ引起的伤口延迟愈合。提示维格列汀能够促进DFU大鼠创面愈合,可成为治疗DFU的潜在药物。
血液循环中的葡萄糖动态平衡是由输入葡萄糖速率和输出葡萄糖速率之间的平衡来调节的。在正常情况下,胰岛素抑制外周组织中葡萄糖的排出,但在糖尿病情况下,葡萄糖生成量增加,因此葡萄糖在循环中的出现超过了葡萄糖的消失,导致高血糖[12]。同样,在本研究中,空白组大鼠有基础水平的血糖,相反,DFU大鼠血糖水平升高,而维格列汀对DFU大鼠的血糖具有改善作用。维格列汀的有益作用可以归因于改善胰岛素敏感性,刺激葡萄糖代谢,并有助于将葡萄糖作为糖原储存在脂肪细胞中,这种改善与维格列汀治疗的DFU大鼠TC、TG和LDL水平的降低相一致,说明维格列汀具有良好的降血脂作用,这一观察结果与大多数降血糖药物具有改善糖尿病脂质代谢异常的潜力是一致的[13]。研究显示创面愈合作用机制可能有多种,包括促进上皮细胞迁移、加快胶原的成熟和减轻炎症[14]。在生理条件下,活性氧有利于抵抗微生物的入侵,控制少量的细胞内信号转导途径。然而,在糖尿病患者中,高血糖诱导氧化应激,从而使伤口愈合过程停止在不受调控的炎症阶段[15]。核相关因子2(Nrf2)是细胞防御机制的一部分,用于应对严重的氧化应激。在氧化损伤后,Nrf2从其细胞质抑制因子Keap1中解离出来,与细胞核中编码抗氧化酶的细胞保护基因结合,以刺激相关靶基因的转录,包括collagen-Ⅰ、TGF-β、α-SMA[16]。Sun等[17]也证实Nrf2在糖尿病创伤愈合中起关键积极作用。本研究结果显示,模型组大鼠创面愈合速度较慢,这是因为剥夺Nrf2导致抗氧化防御反应不足,提高了脂质过氧化水平。而在维格列汀治疗后,Nrf2被激活,进而通过相关基因collagen-Ⅰ、TGF-β、α-SMA使创面更快地缩小。研究报道[18]炎症在伤口愈合过程中起着中心作用,血糖水平升高会导致过氧化物产生过多,从而刺激促炎介质的释放,临床上糖尿病患者与局部伤口中TNF-α、IL-1β和IL-6水平升高有关。且文献支持TNF-α和延迟愈合过程之间存在直接联系[19]。此外,TNF-α可以抑制TGF-β的激活,从而抑制collagen-Ⅰ的增殖和合成,而IL-6的增加对血管生成有负面影响[20]。在本研究中,我们检测了局部促炎因子TNF-α、IL-1β和IL-6的表达,结果表明伤口愈合延迟与伤口区域炎症反应加重有关,这与前人研究的发现一致[21]。而维格列汀的应用明显减少了伤口处的炎性渗入,表明其具有抗炎的潜力。
综上所述,本研究结果证实了维格列汀对糖尿病创面延迟愈合的潜在作用,维格列汀通过抑制炎症标志物(TNF-α、IL-6)、激活Nrf2、collagen-Ⅰ、TGF-β、α-SMA发挥其潜能,促进创面愈合。

