非那西丁的合成与复方阿司匹林的主成分分析
——推荐一个有机化学实验
胡水,赖瑢,李厚金,朱可佳,周磊,邵光,2,*
1中山大学化学学院,广州 510275
2中山大学化学工程与技术学院,广东 珠海 519082
复方阿司匹林(APC药片)是常见的镇痛消炎药,其有效成分包括A-乙酰水杨酸,P-非那西丁和C-咖啡因,结构如图1所示,其中“乙酰水杨酸的合成”和“从茶叶中提取咖啡碱”[1]作为经典本科实验教学,常用于培养学生的基本操作,也有基于这些实验的教学改革[2,3],但对于非那西丁,却较少有人提及。薄层色谱在实际工作中应用频率很高,也是本科教学重点之一,高效液相色谱是飞速发展的前沿技术,功能强大。选择这两种色谱作为分析方法,既可以锻炼学生的基础实验技能,又可以让学生接触前沿分析技术。而进行横向对比的设置,有利于学生更好地理解它们的区别和各自的优缺点,从而更好地在日后科研工作中灵活运用这两种色谱技术。60兆赫兹的台式微型核磁共振波谱不需要超导的配件,仪器价格较为便宜,可以使学生获得直接动手操作核磁共振波谱仪的机会。本文介绍了非那西丁的制备,并且通过薄层色谱和高效液相色谱对市售的APC药片进行分析,与学生自制的产品进行对比,可以使实验更贴近实际,让学生体验药物组分提取、合成和分析这一完整的实际研究流程,增强其综合实验能力。

图1 乙酰水杨酸、非那西丁、咖啡因结构式
1 实验目的
(1) 了解缓冲体系在可逆反应合成中的应用。
(2) 掌握重结晶和离心的实验操作方法。
(3) 掌握台式核磁共振波谱仪的基本操作并运用1H-NMR对有机化合物进行结构解析的方法。
(4) 了解薄层色谱和高效液相色谱的原理以及两种技术的区别与联系,掌握有机化合物的定性与定量分析方法。
2 实验原理
本实验通过对氨基苯乙醚和乙酸酐之间的酰化反应制备非那西丁。在第一步反应中,通过加入过量乙酸,将对氨基苯乙醚转化为乙酸盐,提高反应物溶解度,同时成盐后酰化反应效率提升。由于酰化反应是可逆反应,为了使反应正向进行,在反应第二步中,加入乙酸钠与体系中的乙酸构成缓冲体系,使溶液维持在pH = 4-5的弱酸性环境中,有利于提高转化率。
3 仪器和试剂
仪器:电磁加热搅拌器(HS7 control,IKA公司)、核磁共振波谱仪(Spinsolve 60 Carbon,Magritek公司)、离心机(L3-5K,湖南可成公司)、紫外分析仪(ZF-7,上海嘉鹏公司)、水纯化系统(Milli-Q Direct 8,Millipore SAS公司)、高效液相色谱(UltiMate 3000,Thermo Fisher Scientific公司)。
试剂:对乙酰氨基苯酚(化学纯),无水碳酸钾(化学纯)、碘乙烷(化学纯)、丙酮(化学纯)、氩气(99.9%)、石油醚(化学纯)、乙酸乙酯(化学纯)、对氨基苯乙醚(化学纯)、冰乙酸(化学纯)、乙酸酐(化学纯)、乙酸钠(化学纯)、乙腈(色谱纯)、氘代DMSO(美国CIL公司)、APC药片(远大医药(中国)有限公司)。
4 实验内容
4.1 试验筛选
我们参考了两种反应路线,为了验证实验是否可行,我们设计了一系列实验方案并进行优化,并确定最优实验方案。
方案一[4]:以对乙酰氨基苯酚为原料,反应路线如图2所示,以对乙酰氨基苯酚:无水碳酸钾:碘乙烷=1 : 1.1 : 1.1 (摩尔比)条件下进行实验,以丙酮为溶剂,在氩气氛围下保持回流,以石油醚:乙酸乙酯=1 : 1 (体积比)作为展开剂,薄层色谱监测反应进程(表1)。由于反应时间过长,我们调整了试剂比例,对乙酰氨基苯酚:无水碳酸钾:碘乙烷=1 : 6 : 4 (摩尔比),以期待缩短反应时间,但是发现效果并不理想(表1),由于此时无水碳酸钾和碘乙烷已经较大程度地过量于对乙酰氨基苯酚,再进一步增大碘乙烷和无水碳酸钾比例,对反应速率的影响也不明显,而且也造成试剂浪费,所以我们舍弃了这种教学方案。

图2 方案一的反应路线

表1 薄层色谱监测的反应结果(1)
方案二[5]:以对氨基苯乙醚为原料,反应路线如图3所示,以对氨基苯乙醚:乙酸:乙酸酐=1 : 3 :1.1 (摩尔比)作为初始反应条件,石油醚:乙酸乙酯=1 : 1 (体积比)作为展开剂,薄层色谱监测反应进程,不断优化试剂比例,最终确定以对氨基苯乙醚:乙酸:乙酸酐= 1 : 1.5 : 1.3 (摩尔比)作为实验比例(表2)。

图3 方案二的反应路线

表2 薄层色谱监测方案的反应结果(2)
4.2 实验部分
4.2.1 非那西丁的合成与测试
在100 mL三颈烧瓶上装上回流冷凝管,加入对氨基苯乙醚(1.37 g,0.01 mol)、乙酸(0.90 g,0.015 mol)、水(20 mL)和搅拌子,插入温度计,且温度计保持在液面以下,40 °C反应1 h。升高温度,向上述溶液中加入乙酸酐(1.33 g,0.013 mol),以乙酸钠水溶液(1 mol·L-1)调节pH为4-5 (约5 mL),加热回流30 min。冷却至室温后,析出白色晶体,3000 r·min-1离心5 min促进结晶,抽滤,将粗产品烘干后称量。粗产品用水重结晶(每克粗产品用约5 mL水),并加入0.2 g活性炭脱色,用事先预热的抽滤瓶和布氏漏斗趁热过滤,静置、冷却至室温,析出晶体抽滤,烘干并计算收率,取5 mg非那西丁溶于0.5 mL氘代DMSO进行1H-NMR测试,并进行结构解析。另取非那西丁1 mg溶于3 mL乙腈中,经过0.45 μm尼龙66微孔滤膜后进行液相色谱测试,测试条件如下:液相色谱柱为Syncronis C18柱,250 × 4.6 mm,柱温25 °C,流速为1.0 mL·min-1,进样量为1 μL,检测波长为280 nm,流动相为乙腈:1%乙酸水溶液=1 : 1 (体积比)。
4.2.2 APC药片的薄层色谱分析
将APC药片粉末100 mg溶于1.5 mL乙酸乙酯,下层沉淀为淀粉等添加剂,取上清液作为待测液标记为Pill,阿司匹林样品、非那西丁样品和咖啡因样品各20 mg,分别溶于1.5 mL乙酸乙酯。采用乙酸乙酯:石油醚:二氯甲烷:冰乙酸=20 : 5 : 3 : 2 (体积比)为展开剂,在254 nm紫外灯下观察分离效果并计算Rf值。
4.2.3 APC药片的高效液相色谱分析
取APC药片粉末1 mg溶于2 mL乙腈中,阿司匹林样品、非那西丁样品和咖啡碱样品各1 mg溶于3 mL乙腈中,经过0.45 μm尼龙66微孔滤膜后作为待测样品,测试条件与非那西丁相同。取50 mg非那西丁样品,以乙腈溶于50 mL容量瓶中,定容至刻度线,分别取溶液0、2、5、10和15 mL稀释至50 mL,以溶液浓度X为横坐标,峰面积Y为纵坐标进行线性拟合[6]。
5 结果与讨论
5.1 非那西丁表征
非那西丁的数据如下:白色晶体,收率约为60%-70%。1H-NMR (62 MHz, DMSO):δ9.73 (s, 1H),7.46 (d,J= 9.1 Hz, 2H),6.83 (d,J= 9.0 Hz, 2H),3.97 (q,J= 7.0 Hz, 2H),1.99 (s, 3H),1.29 (t,J=7.0 Hz, 3H),如图4所示,结果与文献[7]相符。液相色谱中仅在t= 4.663 min处出现一个单峰,如图5所示,结合1H-NMR可确定产品为非那西丁,且纯度非常高,接近于100%。

图4 非那西丁的1H-NMR
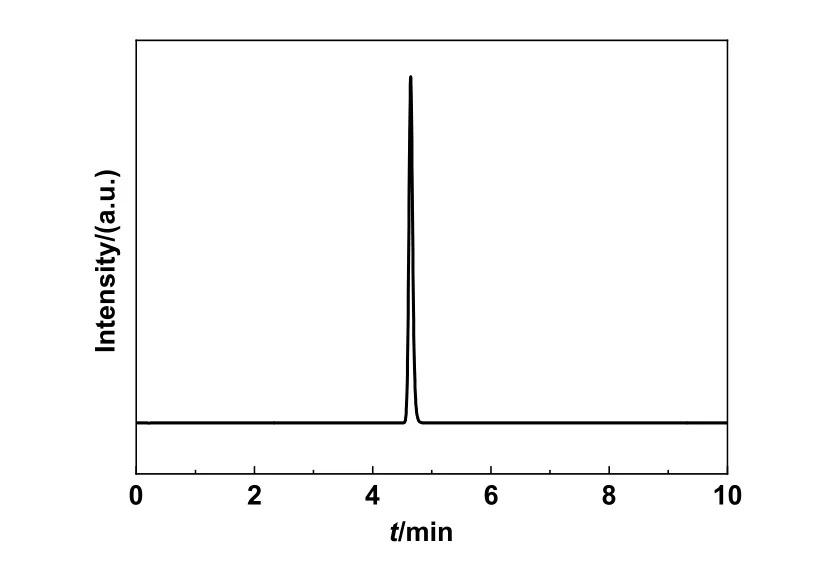
图5 非那西丁的高效液相色谱图
5.2 APC药片分析
薄层色谱中三组分完全分离,各组分Rf值如图6所示。高效液相色谱中的峰形对称且相邻两峰完全分开,各组分保留时间分别为tC= 2.650 min,tA= 4.163 min,tP= 4.663 min,如图7所示。溶液浓度与峰面积的关系见表3,拟合得到的方程为Y= 8.0415X+ 0.0135,R2= 1。APC药片中非那西丁峰面积为1.1019 mAU·min,计算得到浓度为0.1353 mg·mL-1,药片质量平均0.53 g,进而得出药片中非那西丁含量为143.4 mg,与说明书中每片含量150 mg相近,证明高效液相色谱可以较好地应用于药物分析等方面[8]。TLC与HPLC都是有效的物质分离与鉴定手段,二者均属于吸附色谱,根据物质的极性不同实现分离,也都可以调节流动相的极性改变分离效果。然而二者仍有较多不同,TLC方便、快捷、成本低,预处理简单,可同时展开多组样品但鉴别能力较差且无法做定量分析;HPLC准确性高且可实现定量分析,但维护成本较高,实验时间较长。

图6 APC药片的薄层色谱分析
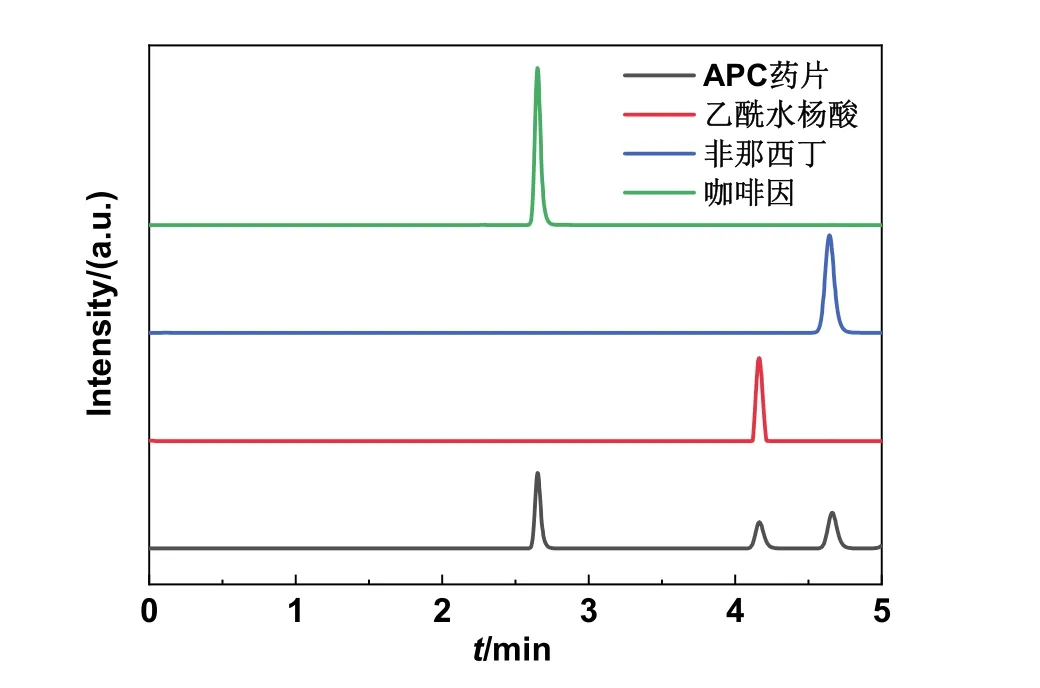
图7 APC药片的高效液相色谱分析

表3 非那西丁溶液浓度与高效液相色谱峰面积关系
6 结语
APC药片及其三组分分析作为经典实验教学案例,学生不需花过多时间去了解新化合物和新反应原理,因此适合基础操作教学,同时也十分适合结合前沿技术,整合新的综合性实验。本文介绍了非那西丁的两种合成方法并对比了优劣性,在对产物进行表征的过程中,涉及到核磁共振波谱、高效液相色谱等现代分析技术,将前沿技术与基础知识相结合,有利于培养学生的科学兴趣。台式核磁目前并没有十分普及,若相关高校不具备条件仍可将超导核磁纳入实验教学。本实验用时6-7 h,由于教学时长限制,乙酰水杨酸与咖啡因的定量分析实验不再重复,本实验综合性较强适合针对化学或药学专业的综合有机化学实验开设,学生单人进行实验,课前需要了解TLC与HPLC的区别与联系,引导学生课前查阅有关资料,加强学生理论与实际相结合的能力。

