透明血管型Castleman病的多排螺旋CT影像学特征*
罗义琳,顾芳,范海晴,杜金辉,高勤,余晖,廖欣*
(1.贵州医科大学 影像诊断学教研室,贵州 贵阳 550004;2.贵州医科大学附属医院 病理科,贵州 贵阳 550004)
Castleman病(castleman disease,CD)又名巨淋巴结增生症,病因不明,由Castleman首次报道[1]。CD最常发生在胸部,也可发生在全身其它各个部位。在形态学上根据淋巴结受累的范围和程度,分为单中心型CD(unicentric CD,UCD)和多中心型CD(multicentric CD,MCD);经典的病理学分型为透明血管型(hyaline vascular variant,HVV)和浆细胞型(plasma cell variant,PCV)[2]。CD临床比较少见,且无特异性的体征和症状,术前诊断困难,大多数病例是根据术后病理检查确诊[3]。CD在影像上主要表现为孤立的、密度均质的软组织密度肿块,边界清楚,增强后显著强化,但关于其多期增强影像表现的研究较少,本文通过分析18例发生在全身多个部位的CD,结合文献资料,探讨其多排螺旋CT(multi-deterctor row helical computed tomography,MDCT)平扫及多期增强后的影像学特征,现报道如下。
1 资料与方法
1.1 一般资料
选择2010年3月—2018年6月经手术病理证实的CD患者18例,其中12名女性和6名男性,年龄18~66岁、平均43.3岁;6例患者无明显不适、为健康体检时意外发现,3例体表扪及包块就诊。患者临床症状表现为咳嗽和胸闷各2例,表现为发热、胸痛、腹痛、血压升高以及气促各1例。18例中有12例同时行MDCT平扫和多期增强检查,2例行MDCT平扫检查,4例行MDCT多期增强检查。
1.2 检查方法
采用Siemens sensation definition 128层多排螺旋CT机,颈部CT扫描范围从颅底到胸骨颈静脉切迹,胸部CT扫描范围从胸廓入口到两膈角下缘,腹部CT扫描范围从乳头水平线到坐骨结节水平,盆腔CT扫描范围从髂嵴到坐骨结节下2 cm;扫描条件为管电压120 kV,管电流180~250 mA·s,层厚5 mm,层间距5 mm。增强扫描的对比剂为碘帕醇,生产厂家为上海博莱科信谊药业有限公司;采用Ulrich高压注射器,经肘静脉团注射非离子型对比剂碘帕醇(370 g/L)100 mL,注射速度2.5~3.0 mL/s;于注射造影剂后30、60和120 s时分别行动脉期、静脉期及延迟期扫描,扫描后将所有图像传入picture archiving and communication system(PACS)工作站进行薄层轴位、冠状位及矢状位多平面重组(multiplanar reconstruction,MPR)分析。照相条件为胸部纵隔窗400 Hu/40 Hu,颈部、腹盆部软组织窗350 Hu/40 Hu。
1.3 图像分析
由两位影像科主治医师双盲阅片诊断,意见一致的结果作为最终统计数据;结果不一致时,则与副主任医师商讨达成一致后得出最终的结果。影像学资料分析包括病灶部位、形态、内部结构特点(有无钙化、均质或不均质)及瘤周有无滋养血管,病变在CT上显示单个明显肿块伴或不伴卫星结节时,被定义为UCD;病变在CT上表现为多个解剖区域的多发结节或肿块而无明显优势病灶时,被定义为MCD。强化程度的判断为轻度强化(增强后病灶高于邻近肌肉密度值<20 Hu)、中度强化(增强后病灶高于邻近肌肉密度值20~40 Hu)以及显著强化(增强后病灶高于邻近肌肉密度值40 Hu以上)。
2 结果
2.1 CD的MDCT影像学特征
18例CD发生部位:胸部9例、腹部4例、颈部2例、盆腔2例以及同时累及双侧腹股沟区及盆腔右侧1例,病灶最长径0.5~8.2 cm;17例为UCD,1例为MCD。14例CD患者MDCT平扫表现:6例密度不均质,6例病灶内可见点状、结节状或树枝状钙化,2例病灶与周围脂肪分界不清,1例表现为累及多个解剖区域的多发软组织密度肿块,其余表现为质地均匀、边缘清楚的单发软组织密度结节或肿块。16例多期增强扫描病灶动脉期呈中度或显著强化,静脉期及延迟期呈显著强化,其中11例可见瘤周滋养血管。见表1、图1~图3。
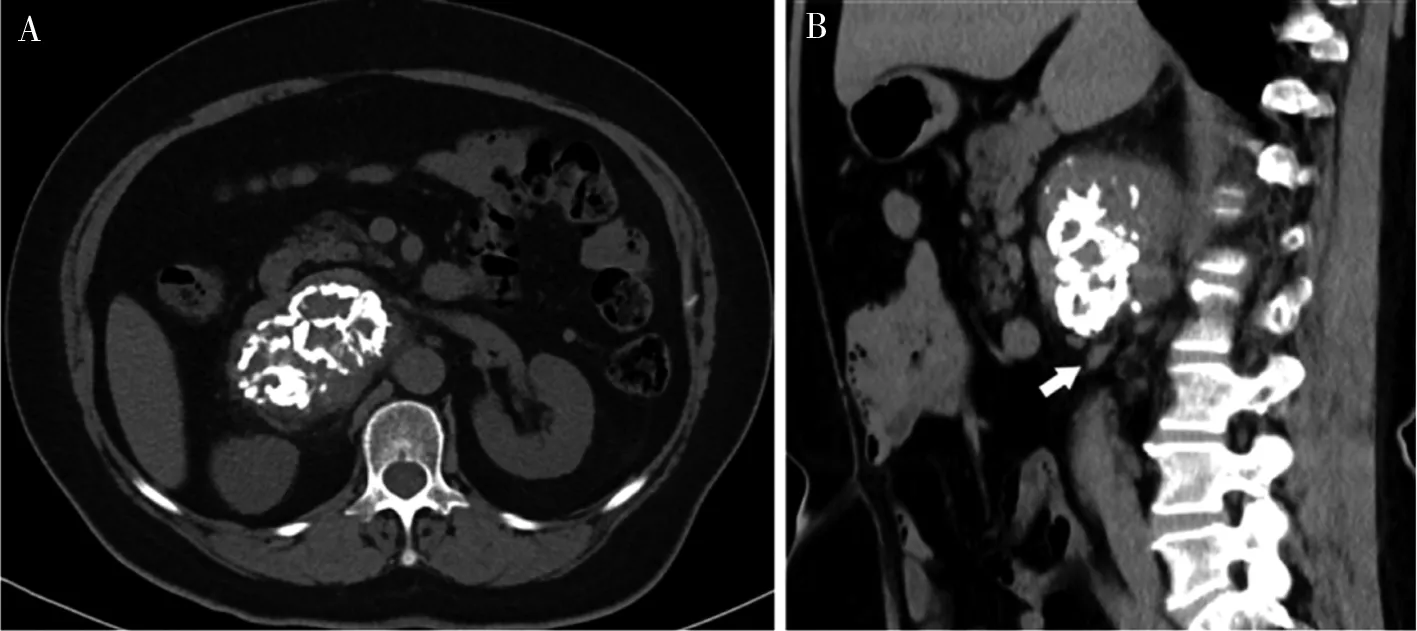
注:患者女,58岁,右侧腹膜后CD;A为MDCT轴位平扫,显示肿块边缘模糊,边界不清楚,内可见特征性的树枝状钙化;B为MDCT矢状位平扫,肿块周围可见多发“卫星”淋巴结(白箭头)。
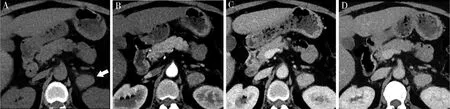
注:患者女,40岁,左侧腹膜后CD;A为MDCT轴位平扫,显示肿块密度均匀,边界不清楚,瘤周可见斑片状渗出(白箭头);B~D分别为MDCT轴位动脉期、静脉期及延迟期,肿块在动脉期呈中度强化,静脉期呈显著强化,延迟期仍呈显著强化但强化程度较静脉期稍减低。
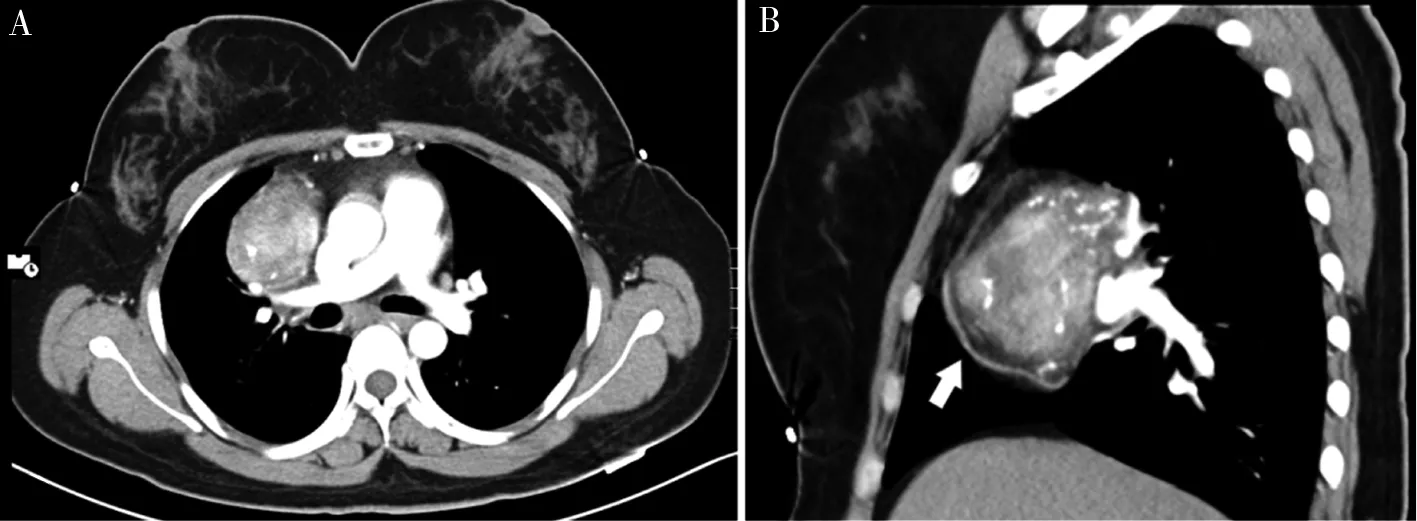
注:患者女,33岁,右侧肺门旁CD;A为MDCT轴位动脉期,显示肿块边界清楚,密度不均质,内部见多发结节状钙化影;B为MDCT矢状位动脉期,显示肿块前下方周围粗大的滋养血管(白箭头)。
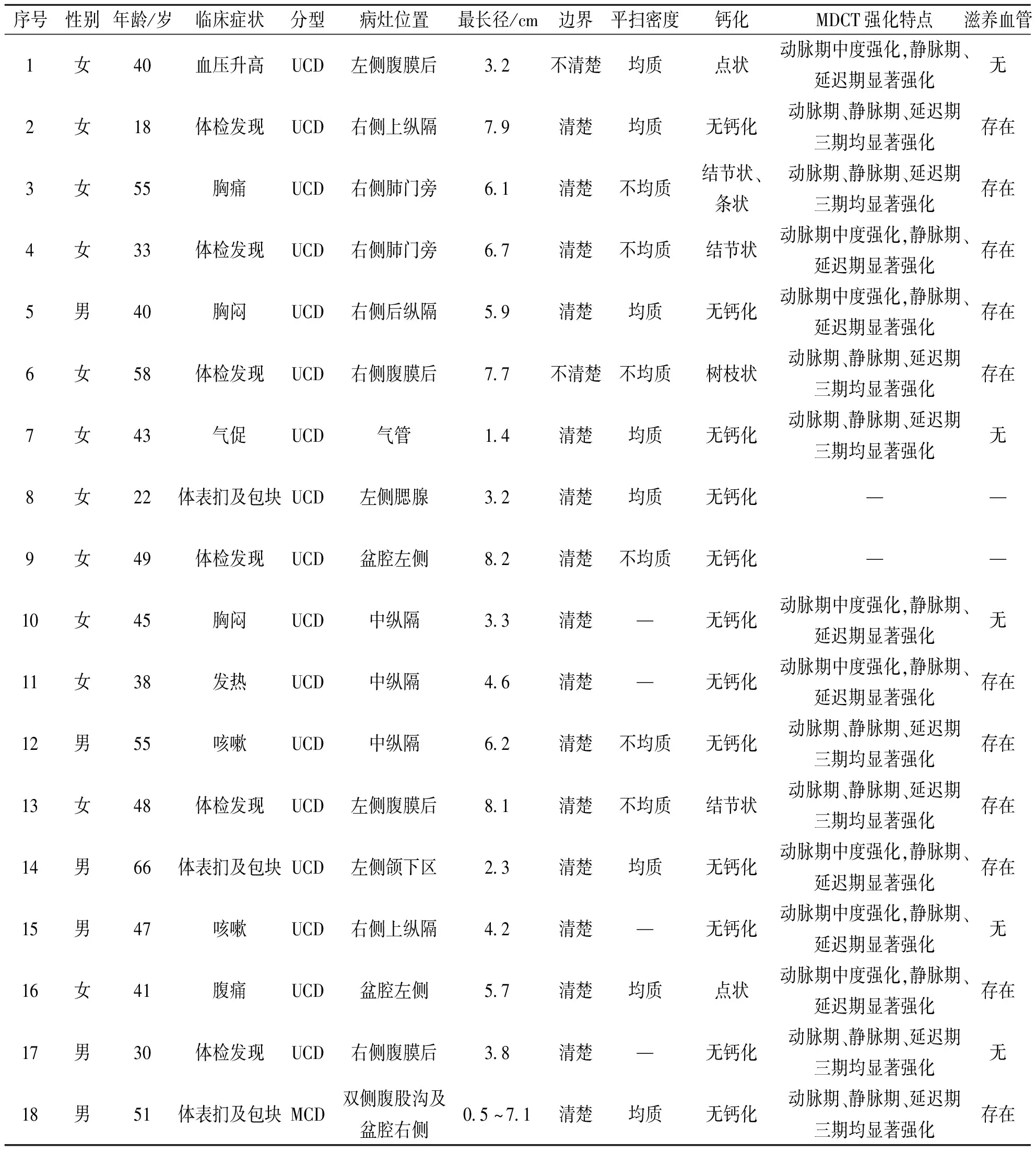
表1 18例CD患者的临床表现和MDCT影像学特征
2.2 病理结果
18例CD经病理证实均为HVV,镜下可见淋巴窦大部分或部分消失,淋巴结内布满均匀一致的小滤泡,滤泡生发中心变小,其内见泡状核的滤泡树突状细胞,有透明变性的小血管穿入生发中心,外套层明显增厚,小淋巴细胞呈同心圆排列,滤泡间区毛细血管增加。见图4。
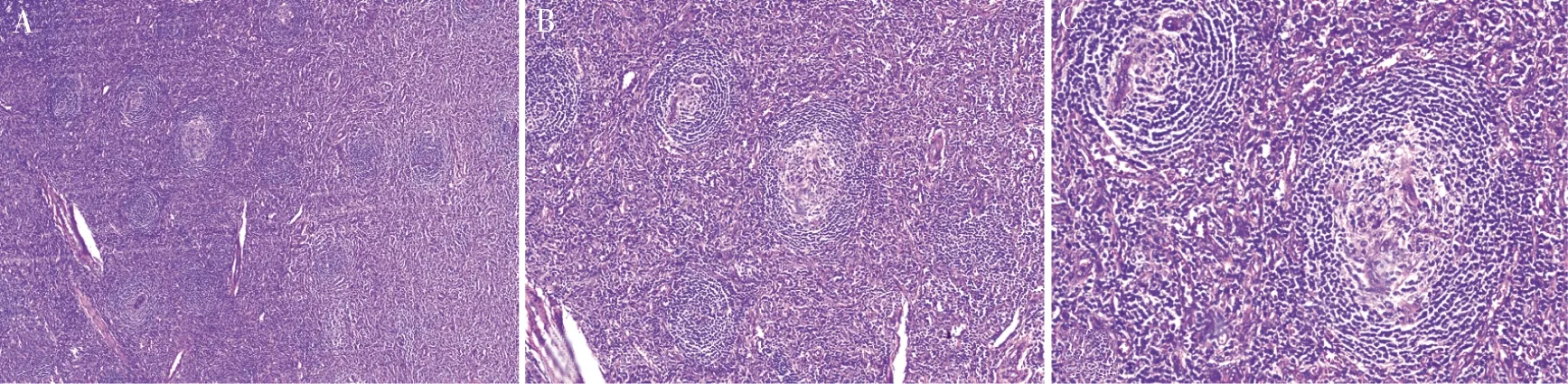
注:患者女,18岁,右侧上纵隔CD;A为镜下显示淋巴结的窦消失,布满大小相近的小滤泡(HE,×5);B为镜下显示滤泡生发中心变小,外套层明显增厚,小淋巴细胞呈同心圆排列(HE,×10);C为镜下显示生发中心可见泡状核的滤泡树突状细胞,有透明变性的小血管穿入,间区毛细血管增加(HE,×20)。
2.3 诊断分析
术前诊断正确4例,术前诊断错误5例,术前不定性诊断9例(诊断为占位)。5例诊断错误的病例中,2例肺门旁肿块误诊为肺癌,1例后纵隔肿块误诊为神经源性肿瘤,1例腹膜后肿块误诊为异位嗜铬细胞瘤,1例腮腺肿块误诊为多形性腺瘤。
3 讨论
CD是一种较为罕见的疾病,男女发病率相当,发病机制目前尚不完全清楚,但白细胞介素-6(IL-6)的过度表达和人类疱疹病毒8型(HHV-8)感染被认为是其重要的致病因素[4-5]。病理学分为HVV和PCV,HVV淋巴窦大部分或部分消失,滤泡生发中心变小并可见小血管穿入,外套层小淋巴细胞呈同心圆排列,滤泡间区毛细血管增加;PCV滤泡间区大量成熟浆细胞增生而血管增生不明显,可见卢梭小体[6-7]。形态学上CD分为UCD和MCD,UCD多发生在20~40岁,其中大部分为HVV,表现为单发类圆形肿块伴或不伴卫星结节,常因体表触及肿物或肿块压迫产生的继发症状等原因就诊,实验室检查多无异常,外科手术常常可以治愈。MCD发病年龄较UCD大,其中大部分为PCV,表现为累及多个解剖学区域多发结节或肿块,常伴有明显的全身症状,例如发热、盗汗、体质量减轻等,实验室检查可见异常,表现为贫血、血沉增快、高球蛋白血症以及低蛋白血症等,需要全身治疗,预后较差,而合并HIV和/或HHV8感染的MCD患者往往症状更为严重,发生淋巴瘤、卡波西肉瘤等恶性肿瘤的概率也更高,预后更差[8-10]。本组18例CD中17例为UCD,1例为MCD,且病理类型均为HVV。
CD可以发生在全身任何部位,但以胸部最为常见(70%),其次是颈部(15%)和腹盆部(15%),其中胸部以纵隔多见,颈部以Ⅱ区和Ⅲ区多见,腹盆部以腹膜后多见[11-13]。虽然CD拥有完整的包膜,但也可因与邻近组织粘连或浸润周围脂肪而边界不清楚,有时由于与邻近器官或血管粘连将导致手术范围扩大。本组CD中有2例位于腹膜后的病灶发现浸润周围脂肪而致边界不清。CD病灶内部如果发生钙化可呈现出多种形态,如点状、结节状或树枝状钙化,其中树枝状钙化被认为最具特征性(图1),而点状钙化最为多见,但是钙化的发生与病灶的大小没有直接联系[14]。在本组CD中有6例发生钙化,以上几种形式的钙化均有出现,在较大或较小的肿块中均有发生。有6例在CT平扫或增强上呈不均质的外观,肿块最长径均>5 cm,考虑是由于局灶性纤维化或者内部坏死而表现为密度不均匀[15]。此外,富血供是CD最重要的一个影像学特征,增强后病灶多呈中度至显著强化[16],也常在病灶周围或者内部看到滋养血管,且MDCT对这些血管的检出率很高[17-19]。本组16例行MDCT增强的CD中除5例体积较小的病灶外,其余11例(包括1例HVV-MCD)均可以在病灶周围发现粗细不等的滋养血管(图3),在较大的病灶周围这些血管显示更加明显,正确地识别这些血管的存在不仅有助于疾病的诊断,还能为外科医生提供有价值的信息,减少术中出血。
由于胸部是CD最为好发的位置,因此UCD常需要与纵隔内异位甲状腺、纵隔内血管瘤、副神经节瘤等富血供病变以及发生于肺门的中央型肺癌进行鉴别。胸内异位甲状腺可合并正常甲状腺的缺如或发育不全,平扫或强化的密度与正常甲状腺相当。纵隔内血管瘤非常少见,CT平扫密度常不均匀,多期增强检查出现特征性的向心性强化有助于鉴别诊断。副神经节瘤与UCD的影像表现较为相似,但副神经节瘤患者常伴有尿儿茶酚胺水平升高,鉴别困难时可行MIBG核素扫描,大多数纵隔副神经节瘤可有摄取。中央型肺癌,好发于中老年男性,致肺门支气管阻塞,肿块强化不如UCD明显,并可以侵犯周围结构。MCD累及多个区域淋巴结且强化多变,因此常需要与淋巴瘤鉴别,但当MCD强化不显著时较难与淋巴瘤鉴别,因为后者强化不明显,淋巴瘤发生钙化罕见可作为重要的鉴别要点。
综上所述,CD中UCD多见,常无明显临床症状,手术常常可以治愈[20-21],在影像上主要表现为孤立、边界清楚、密度均质的软组织密度结节或肿块,MDCT增强呈持续显著强化,结合其它影像表现不难诊断。MCD少见,常伴有明显的全身症状,预后较差,在影像上表现为累及多个解剖学区域的多发结节或肿块,强化程度多变,较难与淋巴瘤鉴别。

