基于EDTA淋洗离心—硫酸盐还原菌固化法去除污泥中重金属镉的研究
陈立航,李顺群,程学磊,申道明,付建宝
(1.天津城建大学 土木工程学院,天津 300384;2.中原工学院 建筑工程学院,河南 郑州 450007;3.新乡学院 土木工程与建筑学院,河南 新乡 453003;4.中交天津港湾工程研究院有限公司中交第一航务工程局有限公司,天津 300222)
1 研究背景
近年来,海河流域经济迅猛发展,同时也带来了大量工业废水和生活污水的排放,造成非常严重的区域环境污染。天津位于海河流域下游,大量重金属Cd及其化合物进入河湖水环境,严重污染了水体与底泥。随着城市污水处理能力不断提高,河湖水污染状况能够得到有效改善,但大量污泥的处理成为新的难题。污泥中含有大量的N、P、K、Ca及有机质,促使污泥资源再利用成为一种广泛的需求[1-2],但污泥中也含有重金属等有害物质。所以污泥处理后应用于城市绿地,从而避免污泥中残余的有毒有害物质危害环境及人类安全,正逐渐成为污泥资源化、安全化和无害化回收利用的重要途径。郭广慧等[3]研究发现,城市污泥中Cd的超标率最高,所以应在资源再利用中优先关注。重金属Cd污染范围广、毒性大,对生态环境危害极大。若土壤、水体的Cd污染直接或间接进入到食物链中,则会损坏人体细胞膜、摧毁细胞功能进而对人体器官及神经中枢造成较大的危害,甚至会造成死亡[4]。
污泥中部分重金属Cd通过溶解、凝聚、沉降等反应存在于污泥胶体的表面以及矿物质颗粒之中,这部分重金属的迁移性和生物可利用性较高,当污泥环境受到物理扰动或者沉积物出现理化性质变化时,会向周围释放并引起二次污染[5]。土壤也存在同样的问题,采取溶剂淋洗萃取方法对土壤进行修复的研究已经非常完善[6],但用于修复污泥尤其是污泥中重金属Cd这方面尚缺少研究。上述土壤修复中所提到的淋洗萃取指的是利用所需提取的特定组分在萃取剂和原溶液中溶解度的差异达到组分迁移的目的。Pan[7]等使用乙醇-水作为污泥液化的溶剂,成功降低了污泥的污染程度和生态风险。污泥重金属淋洗过程中最重要的是淋洗剂的选择,既要保证能够高效地提取重金属,又不破坏污泥的物理、化学和生物结构。本文采用人工合成的络合剂EDTA(ethylene diamine tetraacetic acid)淋洗萃取的方式实现污泥中重金属Cd部分迁移,然后通过离心使淋洗液和污泥两相分离,从而降低污泥中重金属Cd含量。
污泥中重金属Cd一般存在多种形态,其中表面吸附部分的比例是一定的,除此之外还有与污泥中有机质通过物理、化学反应形成的结合体部分,以及与磷酸盐、碳酸盐、氢氧化物等阴离子形成沉淀的部分。对于非表面吸附形态的Cd,EDTA淋洗离心所发挥的去除作用并不明显,因而单一的方法在应用过程中具有较大的局限性。由于重金属污染程度不仅与其含量相关,更取决于其赋存形态[8],不同存在形态的重金属也决定了其在环境中的活性、迁移能力、毒性和危害程度。所以对污泥内部较难去除的Cd,可以采取重金属形态转换的方式,降低其生物利用性以减轻对环境的危害。微生物由于其成本低、环境友好和效果显著等优点在重金属的修复应用中越来越受到关注[9]。硫酸盐还原菌SRB(sulfate-reducing bacteria)是一种常见的应用于生物修复的微生物,通过酸化、吸附、还原沉淀等作用可以转换污泥中重金属的存在形态,从而改变其生物可利用性。Thavamani等[10]发现硫酸盐还原菌在厌氧环境中修复重金属尾矿的效果显著。闫潇等[11]接种硫酸盐还原菌用于铅锌冶炼渣重金属污染修复,降低其生物可利用性,效果显著。但目前将SRB应用于修复污泥中重金属Cd的研究较少。
鉴于此,本文以河湖污染底泥中重金属Cd的去除为研究内容,采取EDTA淋洗离心和SRB固化联合方法以达到更高效的重金属Cd去除效果。研究了EDTA淋洗离心对吸附态重金属Cd的去除效果,探讨了SRB对重金属Cd的固化能力,最后总结了两个方法联合作用的结果,以期为污泥净化、资源利用和环境保护等方面的研究与应用提供参考。
2 材料与方法
2.1 试验材料
试验所用污泥于2019年7月取自天津某河流主要污染河段,样品采集时选用管式泥芯采样器。采样点布置在水流缓慢、沉积稳定和污染严重的区域,在污泥采集区均匀分布的几个采样点采用五点法采集污泥,筛除其中石子及其他杂物后将多点污泥样品混匀为1个样品,通过机械脱水的方式对污泥进行预处理后低温保存运输至实验室。取500 g土样用于测定污泥理化性质,并且根据所测试验不同性质的需求分别以含水污泥和风干污泥两种方式保存[12]。表1为所采集污泥基本物理性质。
由表1可以看出,污泥基本物理性质测定主要包括含水率、密度、容重、孔隙率和pH值这5项指标。其中,污泥pH值以V(土壤)∶V(水)=1∶2.5的体积比通过pH计测定,污泥含水率则是通过电热恒温烘箱在(105±5) ℃的条件下烘干8 h后测定。

表1 试验污泥基本物理性质
2.2 试验方法
2.2.1 EDTA淋洗离心 称取10 g经过2 mm筛选的污泥试样和密度为0.02 mol/L的EDTA溶液100 mL在搅拌机内淋洗混合[6]。淋洗后将混合物装入离心管中进行两相分离,由于污泥黏度较高,在淋洗、离心过程中考虑离心力、淋洗时间、淋洗次数和离心温度等因素对两相分离的影响,通过对比可以得到在不同离心条件下的分离效果,以获得最佳的离心条件。分离后用孔径0.45 μm滤膜过滤分离后的上清液,测定其中Cd浓度。
离心过程所使用的离心管包括管体和管盖两部分。管体底部呈半圆状,设有两块透水石,顶部端口设有外螺纹,管盖设有对应的内螺纹。管体的内部设有网孔直径为25 μm的聚丙烯过滤袋,聚丙烯过滤袋放置于透水石之上。离心过程中由于聚丙烯过滤袋的作用,密度较大的污泥被留在过滤袋内,密度较小的水分则会在离心力的作用下被甩至管壁,然后经透水石流向离心管底部的半圆空间内,实现污泥和水分两相分离。
2.2.2 SRB固化 对淋洗离心后的污泥进行固化。将SRB作为反应菌剂,每个反应试样取污泥150 g,然后各加入15 mL硫酸盐还原菌菌液,在4 000 r/min条件下离心运行5 min,去除上清液后放置于30℃的恒温发酵箱内,保持CO2稳定在5%的条件下厌氧反应30 d[11]。向发酵箱内加入污泥质量5%的稻壳、花生壳[13],经过发酵,稻壳、花生壳会被分解成可被植物吸收利用的有机物[14]。每隔10 d采用pH计测定污泥试样的pH值,同时设置空白对照试样,即无反应菌剂。
2.2.3 重金属Cd含量 试验采用混酸微波消解法测定污泥原样和试样中的Cd含量。称量样品0.2 g,依次加入5 mL HNO3、5 mL HClO4和3 mL H2O2(30%),称取粉碎样品(0.1±0.01) g,加入10 mL硝酸,旋紧罐盖放置过夜。按照微波消解仪设定程序进行消解,待温度冷却压强降低后取出并缓慢打开罐盖排出反应气体。将消解罐放在控温电热板中,于100 ℃加热30 min,冷却后用孔径0.45 μm的滤膜过滤,最后转移到容量瓶中并用蒸馏水定容至50 mL。上述微波消解3个阶段的程序参数分别定为:(1)25 min内升温到185 ℃;(2)185 ℃保持25 min;(3)降温15 min以上,消解液温度降至90 ℃以下[15]。微波消解后通过ICP-MS进行重金属Cd含量的测定。
2.2.4 重金属Cd的存在形态 称取经过200目筛筛后的干污泥试样2 g放入离心管中,按照Tessier法进行连续分级提取。具体操作如下[16]:
(1)关于可交换态部分,取0.5 g经过200目筛筛后的干污泥试样和16 mL浓度为1 mol/L的MgCl2溶液充分混合,在pH值为7、室温条件下震荡1 h,然后在4 000 r/min的条件下离心分离20 min。取上清液用孔径0.45 μm滤膜过滤分离,加入浓度为5%的硝酸定容至25 mL待测。取残余物经去离子水洗涤并离心后保存备用。
(2)关于碳酸盐结合态部分,取第1步残渣和16 mL浓度为1 mol/L的CH3COOH溶液充分混合,在pH值为5、室温条件下震荡6 h,然后在4 000 r/min的条件下离心分离20 min。取上清液用孔径0.45 μm滤膜过滤分离,加入浓度为5%的硝酸定容至25 mL待测。取残余物经去离子水洗涤并离心后保存备用。
(3)关于铁锰氧化物结合态部分,取第2步残渣和16 mL浓度为0.04 mol/L的NH2OH·HCl的25%HAc溶液充分混合,在97 ℃水浴锅中恒温震荡6 h,然后在4 000 r/min的条件下离心分离20 min。取上清液用孔径0.45 μm滤膜过滤分离,加入浓度为5%的硝酸定容至25 mL待测。取残余物经去离子水洗涤并离心后保存备用。
(4)关于有机结合态部分,取第3步残渣和5 mL浓度为0.01 mol/L的HNO3溶液、8 mL浓度为30%的H2O2溶液充分混合。加入HNO3调节pH值为2,在87 ℃水浴条件下震荡2 h,然后加入5 mL H2O2调节至pH值为2,继续振荡2 h后冷却至室温,最后加入5 mL浓度为3.2 mol/L的 NH4Ac的20%HNO3溶液振荡2 h,在转速为4 000 r/min的条件下离心分离20 min。取上清液用孔径为0.45 μm的滤膜过滤分离,再加入浓度为5%的硝酸定容至25 mL待测。取残余物经去离子水洗涤并离心后保存备用。
(5)关于残渣态部分,将第4步中的残余物按2.2.3中所提到的测定重金属含量方法进行检测。
3 结果与分析
3.1 重金属Cd的形态分布
图1为污泥试样中重金属Cd的形态分布。
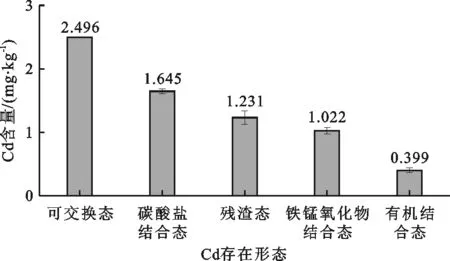
图1 污泥试样中重金属Cd的形态分布
由图1可以看出试验污泥中Cd不同形态的含量依次为:可交换态(36.7%)>碳酸盐结合态(24.2%)>残渣态(18.1%)>铁锰氧化物结合态(15.1%)>有机结合态(5.9%)。上述Cd的存在形态中,可交换态和碳酸盐结合态为生物活性态,因为这两种形态相对比较容易被释放,尤其在强酸性条件下,所以这两种形态具有较大的可移动性,常常表现出较强的潜在生物活性。残渣态则通常被视为稳定态。总的来说降低Cd污染程度的方法是减少其可交换态和碳酸盐结合态的含量,使其稳定。
3.2 离心力对EDTA淋洗离心的作用
试样和淋洗液两相分离的一个外部条件是两者的分离程度,即离心过程中的相对离心力(以离心加速度表征)。按试验要求调整相对离心加速度分别为50g、100g、150g和200g(g为重力加速度,g=9.81 m/s2)进行离心试验。相对离心加速度计算公式如下:
RCF=1.118×10-5×n2×r
(1)
式中:RCF为相对离心加速度,其值为重力加速度g的倍数;n为离心机转速,r/min;r为旋转半径,cm。
图2为污泥试样中重金属Cd含量随离心力大小的变化。

图2 污泥试样中Cd含量随相对离心加速度大小的变化
由图2可以看出,试验组中Cd含量变化明显,随着离心加速度的增加,Cd含量也相应降低。污泥原样中重金属Cd浸出量为2.09 mg/kg,相对离心加速度为100g时,重金属含量降低至0.944 mg/kg,去除率达55%。随着相对离心加速度的增加重金属含量仍有小幅减少,说明离心加速度的增加,可以提升EDTA对Cd的淋洗分离效果。对照组中Cd浸出量无明显变化。
图3为重金属Cd与污泥的两相分离原理图。
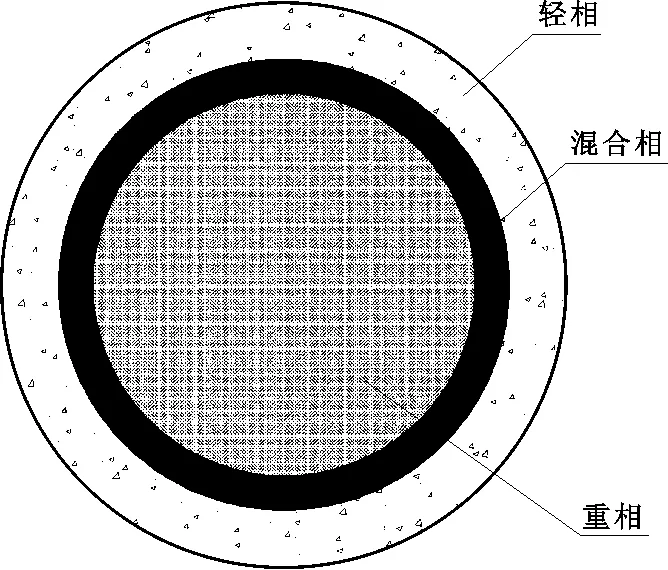
图3 重金属Cd与污泥的两相分离原理图
由图3可以看出在离心过程中,随着离心管的高速转动过滤袋和离心管之间发生相对转动继而产生环隙流场(简称为Taylor-Couctte流动)。这种相对流动会随着两相之间的距离、转速和黏稠度等因素表现出较为不同的流动状态[17]。当相对离心加速度由100g继续增加时,离心管中这种相对流动的规律性减弱,过滤袋和离心管相对转动形成的泰勒涡也随之被破坏。此时管内流动呈现一种较为紊乱的状态,虽然离心加速度不断增加,两相分离效率反而不断下降。所以综合经济因素后认为相对离心加速度为100g较为合适。
3.3 淋洗时间对EDTA淋洗离心的作用
基于3.2所得结论,取RCF=100g进行EDTA淋洗离心试验,每隔3 h对淋洗结果进行检测。图4为污泥试样中重金属Cd含量随淋洗时间的变化。
由图4可知,淋洗时间为3 h时,污泥中Cd的去除率达28.1%,淋洗时间为3~12 h时,EDTA与污泥的混合接触更加均匀,此时段污泥中更多的Cd被去除,重金属Cd含量持续降低,在12 h时降到最低值,此时去除率达52.5%。说明EDTA与污泥中重金属Cd在此阶段已经完成离子交换和络合反应。而当淋洗时间为12~24 h时,此时段Cd的去除率反而逐渐下降。这可能是由于二者形成的不稳定的络合物在持续淋洗搅拌过程中再次分解,并且再次被污泥吸附,从而导致去除率下降。
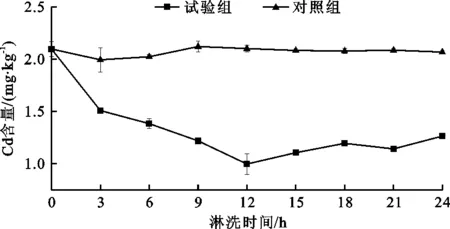
图4 污泥试样中重金属Cd含量随淋洗时间的变化
3.4 淋洗次数对EDTA淋洗离心的作用
基于3.3所得结论,取RCF=100g、淋洗时间为12 h进行EDTA淋洗次数离心试验,图5为污泥试样中Cd含量随淋洗次数的变化。受EDTA吸收能力的制约,单次淋洗的效果有限,当单次EDTA淋洗能力达到饱和时,就无法去除更多的重金属Cd,每增加淋洗次数都是在上一次淋洗的基础上完成。

图5 污泥试样中Cd含量随淋洗次数的变化
由图5可以看出,增加淋洗次数明显提高了重金属Cd去除率,淋洗2次后重金属Cd的去除率与淋洗1次相比由46.0%增加至62.1%,去除率增加了16.1%。而淋洗3次时去除率为66.4%,与淋洗2次相比变化不大,去除率仅增加了4.3%。说明了当淋洗次数增加时去除率也随之提高,而单次去除效率却下降明显,这是由淋洗剂和污泥中Cd的存在形态两个因素所决定的。当淋洗次数由1次增加至2次时,增加了新的淋洗剂,此时所增加的是EDTA的络合能力,所以重金属Cd去除率增加明显。而淋洗次数由2次增加至3次时,由于污泥中重金属的存在形态不同,易被淋洗形态的重金属Cd含量已经大大降低,所以此时的淋洗效果并不明显。总的来说,在重金属Cd淋洗2次后去除率达到相对较高的程度。
3.5 离心温度对EDTA淋洗离心的作用
基于3.4所得结论,取RCF=100g、淋洗时间为12 h、淋洗次数为2次进行不同离心温度的EDTA淋洗离心试验,图6为污泥试样中Cd含量随离心温度的变化。

图6 污泥试样中Cd含量随离心温度的变化
由图6可以看出,随着离心温度的升高,Cd除率不断提高,在离心温度为30 ℃时去除率高达74%。这是因为离心温度升高导致Cd离子在污泥中从固相向液相的扩散速度加快,因此去除率提高较为明显,由此可见在夏季处理污泥比在冬季有更好的效果。
由于试样中重金属Cd可交换态和碳酸盐结合态含量较高,占其总量的60.9%,所以EDTA淋洗离心可以达到较好的去除效果,在优化EDTA淋洗离心各变量因素的条件下,试样中重金属Cd含量降低了1.552 mg/kg,污泥中可交换态及碳酸盐结合态所占比例也随之下降。重金属Cd的生物活性态含量降低,其生物活性和生态危害性也随之降低。
3.6 SRB固化重金属Cd
基于3.5所得结论,将修复后的污泥作为SRB固化试验的试样。图7为未固化污泥试样、固化15 d和固化30 d后污泥试样中重金属Cd各存在形态的含量分布。
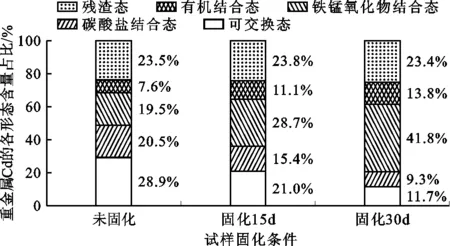
图7 不同固化条件下污泥试样中重金属Cd各存在形态的含量分布
由图7可以看出,在未固化的污泥试样中,重金属Cd可交换态和碳酸盐结合态分别占总量的28.9%和20.5%;铁锰氧化物结合态和残渣态分别占总量的19.5%和23.5%;而有机结合态含量相对较低,占总量的7.6%。
固化15 d后重金属Cd的5种形态发生转化,可交换态和碳酸盐结合态所占比例分别降至21.0%和15.4%。铁锰氧化物结合态和残渣态含量增加,而残渣态基本保持不变。这可能是由于SRB接触污泥后正处于逐步适应环境状态,所以重金属的形态转化并不十分明显。
固化30 d后可交换态和碳酸盐结合态所占的比例明显降低,分别为11.7%和9.3%,远小于未固化污泥样品组的含量。铁锰氧化物结合态和有机结合态所占比例分别升至41.8%和13.8%。残渣态含量基本保持不变。其中不稳定态(主要为可交换态和碳酸盐结合态)的含量由2.589 mg/kg降低至1.103 mg/kg。
在SRB的固化过程中,重金属Cd稳定态(其中包括残渣态、有机结合态和铁锰氧化物结合态)含量逐步提高,未固化污泥样品中稳定态含量为50.6%,固化30 d后稳定态含量增至79.0%。SRB在缺氧条件下对重金属Cd的形态转化起重要作用,主要利用其对重金属的吸附和转化能力,将污泥中溶解态Cd转化成为毒性较低的稳定态。重金属Cd的稳定态含量不断增加说明这种方法固化效果明显,可以有效降低Cd的生物可利用性。其转化作用机制如下:

(2)

(3)
SRB将硫酸盐转化为H2S,H2S与金属发生反应形成金属硫化物沉淀[18]。Cd离子与还原过程中产生的硫化氢反应生成硫化物沉淀,由于硫酸盐还原菌能够在厌氧条件下以SO42-作为末端电子受体将其还原为S2-,进而与重金属离子反应生成不溶解的沉淀物,即CdS。硫酸盐还原菌代谢过程中会产生CO2,重金属Cd可与CO32-反应生成不溶解的碳酸盐[19]。除此之外,SRB细胞膜外存在大量胞外聚合物(EPS),该聚合物中含有羧基、羟基、巯基、氨基、酰胺基和磷酸基等活性基团,这些基团中的N、O、P和S等提供孤对电子与重金属离子结合,从而使水溶态的金属离子被吸附[20]。修复后样品中Cd总量没有发生变化,但其存在形态变化明显。修复后铁锰氧化物结合态成为主要存在形态,Cd的迁移性和生物活性均有明显下降,达到了固化目的。
3.7 SRB固化过程中pH变化
污泥试样在固化过程中由于SRB的还原作用导致污泥溶液中产生较多的S2-,使其pH值发生变化。图8为污泥试样pH值随固化时间的变化。
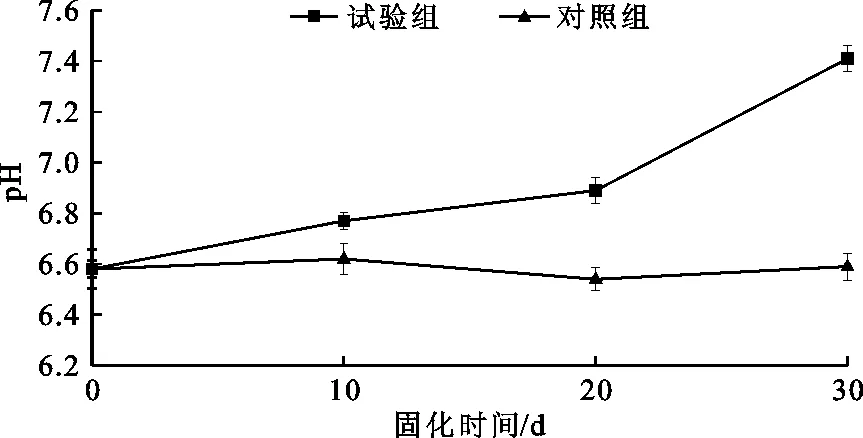
图8 污泥试样固化过程中pH值的值变化
由图8可以看出,污泥初始pH值为6.58,固化过程中试验组pH值从0~20 d内逐渐升高,20~30 d内升高较为显著。这是由于SRB较强的还原作用将SO42-还原生成S2-,S2-与重金属离子形成强碱弱酸盐,导致污泥溶液pH值升高[21]。而对照组pH值则基本保持不变。
4 讨 论
目前国内外学者已经在治理重金属环境污染领域取得了诸多研究成果。但其研究方向多聚焦于重金属总含量,通过物理、化学或生物方法的处理从而达到降低重金属总含量的目的。总体来说由于使用方法较为单一以至所取得的效果极为有限。而污泥中重金属Cd不同存在形态的活性及其所造成环境污染的程度各不相同,与现有方法相比,本研究着眼于重金属Cd的存在形态及其由于环境改变时所引起的形态转化问题,通过物理法和生物法相结合的方式对Cd形态中活性大、污染程度高的部分采取针对性处理,有效降低此部分含量从而达到了减轻污泥中重金属Cd污染程度的目的。
5 结 论
本文提出了EDTA淋洗离心和SRB固化联合作用的方式去除河湖污染底泥中重金属Cd的思路和方法,得出的主要结论如下:
(1)采用EDTA在离心力为100g、淋洗时间为12 h、淋洗次数为2次和离心温度为30 ℃的淋洗离心条件下,污泥中Cd含量由6.793 mg/kg降低至5.241 mg/kg,去除率达22.8%。然后采用SRB对淋洗离心后的污泥进行固化,不稳定态Cd含量由2.589 mg/kg降低至1.103 mg/kg,降低后Cd含量低于《绿化种植土壤》(CJ/T 340-2016)中重金属要求的Ⅳ级标准2 mg/kg。
(2)现阶段对于污泥中重金属去除的研究不应仅局限于追求高去除率,还应将目光放在高稳定性上。基于对重金属形态分布、活性和污染程度的把握,对于不同形态采取针对性方案,通过多种方法相结合的方式降低重金属的危害。若工艺逐步成熟,将可以极大地促进污泥资源再利用,具有极其重要的现实意义。

