气相色谱-质谱法测定食用植物油中短链脂肪酸的测量不确定度评定
徐列兵,郭强,贾煜,朱军,王丹
(河北中石油中心医院,河北廊坊 065000)
测量不确定度是与测量结果关联的一个参数,表明结果的可信赖程度,也是显示测量结果质量的重要指标,尤其是对第三方检验检测机构来讲,当测量结果出现临界值或需要对非标准方法的建立和确认时[1],不确定度评定具有重要意义。
笔者采用的气相色谱-质谱仪测定食用植物油中短链脂肪酸的方法[2]属于实验室自己制定的方法,主要是针对食用植物油品质的研究,食用植物油的品质一直是人们关注的重点,正常食用植物油中应不含有低于16 个碳的脂肪酸酯,但经反复高温加热,会发生氧化、裂解等反应,产生异构体、反式脂肪酸和短链脂肪酸等。因此对食用植物油中短链脂肪酸含量的测定可以作为食用植物油品质鉴别的一种辅助指标。目前,对食用植物油短链脂肪酸的研究报道较少[3-6],也未见其不确定度评定的报道。因此笔者以辛酸的测定为例,根据JJF 1059.1-2012 《测量不确定度评定与表示》以及其它不确定度评定方法[7-15]对测量结果进行不确定度评定,分析其来源,并对不确定度分量进行量化,以获得影响测量结果准确性的因素,并在实验过程中得以关注与控制。
1 实验部分
1.1 原理
正常食用植物油中应不含有低于16 个碳的脂肪酸酯,但经反复高温加热,会发生氧化、裂解等反应,产生异构体、反式脂肪酸和短链脂肪酸等。采用皂化反应原理,在植物油中加入适量NaOH 加热除去长链脂肪酸,再经酸化,用正己烷萃取,可得到游离的短链脂肪酸,用气相色谱-质谱联用仪测定短链脂肪酸的含量。
1.2 主要仪器与试剂
气相色谱-质谱仪:5973i/6890N 型,美国安捷伦科技有限公司。
电子天平:AE240 型,感量为0.1 mg,瑞士梅特勒-托利多公司。
恒温磁力搅拌器:85-2 型,上海司乐仪器有限公司。
正己烷:色谱纯,天津市光复精细化工研究所。
辛酸钠:分析纯,山东西亚化学工业有限公司。
氢氧化钠:分析纯,天津市天大化工实验厂。
浓磷酸:优级纯,国药集团化学试剂有限公司。无水亚硫酸钠:分析纯,天津市佳兴化工有限公司。
样品:食用大豆油。
1.3 仪器工作条件
1.3.1 色谱
色谱柱:HP-5 MS 型色谱柱(30 m×0.32 mm,0.25 μm,美国安捷伦科技有限公司);柱流量:0.5 mL/min;分流比:30∶1;进样口温度:220 ℃;高纯氦气;程序升温:初始柱温80 ℃,保持时间为2 min,以10 ℃/min 升至200 ℃,保持时间为18 min;进样体积:1 μL。
1.3.2 质谱
离子源:EI 源,温度为230 ℃;溶剂延迟:4.00 min;总离子扫描质量范围:40~500 Da;用NIST标准质谱库检索定性;选择离子:m/z60、m/z73。
1.4 实验步骤
1.4.1 样品制备
短链脂肪酸的提取:称取已放置冷却的经100 ℃加热0.5 h 的油样25 g 于圆底烧瓶中,加入3.4 g NaOH,加入适量水(约30 mL)使其溶解,再加入无水亚硫酸钠0.1 g,100 ℃下冷凝回流1 h 后移入分液漏斗,室温静置2 h 使其分层。取水相至锥形瓶,在冰水浴中用浓磷酸调至pH 1,密塞,在冰箱中冷冻0.5 h,取出后,用正己烷萃取两次并定容至10 mL 容量瓶中,经0.45 μm 微孔滤膜(有机相)过滤,得游离的短链脂肪酸,取正己烷层1 μL 进样。
1.4.2 溶液配制
用电子天平准确称取辛酸钠0.011 6 g,用约2 mL 水溶解,以浓H3PO4调pH 1,用辛酸钠酸化后游离出辛酸,然后用5 mL 正己烷萃取,将萃取液置于10 mL 容量瓶中,用正己烷稀释,配制成浓度为1 000 μg/mL 的辛酸标准溶液。
取7 支10 mL 容量瓶,用2 mL 分度吸量管分别量取标准溶液0.5、1、2 mL 置于10 mL 容量瓶中,用正己烷定容,得浓度为50、100、200 μg/mL 辛酸溶液;用5 mL 分度吸量管取50 μg/mL 辛酸溶液5 mL 于10 mL 容量瓶中,定容,得浓度为25 μg/mL 辛酸溶液,再取25 μg/mL 辛酸溶液5 mL 于10 mL 容量瓶中,定容,得浓度为12.5 μg/mL 辛酸溶液;取12.5μ g/mL 辛酸溶液5 mL 于10 mL 容量瓶中,定容,得浓度为6.25 μg/mL 辛酸溶液,最终配制得到辛酸浓度分别为0、6.25、12.5、25、50、100、200 μg/mL 的系列标准工作溶液。按1.3 仪器工作条件进样测定,以色谱峰面积(y)为纵坐标,对应的质量浓度(x,μg/mL)为横坐标进行线性回归,计算得线性方程为y=1.39×104x-1.49×105。
1.4.3 油样中辛酸含量计算
依次测量标准品和样品溶液,样品溶液中辛酸浓度通过线性方程计算得出;油样中辛酸的含量(mg/kg)按式(1)计算。

2 不确定度来源分析
测量不确定度评定分为标准不确定度A 类评定、标准不确定度B 类评定。多次重复测量采用A类评定,其它采用B 类评定,根据以上测定步骤建立的数学模型见式(1)。
测量结果不确定度来源于“人、机、料、法、环、测、抽、样”八个方面。实验人员均具备相应的能力,人员操作的不确定度忽略不计,仅引入人员读数误差导致的不确定度;本实验不涉及抽样,抽样的不确定度可不予考虑;样品及标准溶液的进样均采用自动进样设备,进样体积引入的不确定度可不予考虑。本方法测量结果的不确定度主要来源如下:
(1)样品制备过程:包括25 g 油样单次称量引入的A 类不确定度,天平、样品溶液体积定容引入的B 类不确定度。
(2)标准溶液的制备及标准曲线系列浓度的配制过程:包括标准物质单次称量引入的A 类不确定度,天平、容量瓶、分度吸量管引入的B 类不确定度,人员读数引入的B 类不确定度等。
(3)气相色谱-质谱联用仪引入的B 类不确定度。
(4)在相同条件下,同一样品重复测量(cs)引入的A 类不确定度。
(5)加标回收率(R)引入的A 类不确定度。
(6)环境温度的变化引入体积相对变化的不确定度。
由于各不确定度分量量纲不一致,因此采用相对标准不确定度进行评定。
3 不确定度评定
3.1 样品前处理过程引入的相对标准不确定度
3.1.1 样品称量引入的相对标准不确定度u1,rel


3.2 标准溶液配制引入的相对标准不确定度u3,rel
按照实验方法,此过程引入的不确定度包括标准物质单次称量引入的A 类不确定度和电子天平、2 mL 分度吸量管、5 mL 分度吸量管、10 mL 容量瓶引入的B 类不确定度,因试剂为色谱纯,忽略试剂纯度引入的测量不确定度。
3.2.1 辛酸钠称量引入的相对标准不确定度urel(X)
称 量0.011 6 g 辛 酸 钠(C8H16NaO2),实 际 称量1 次,辛酸钠称量引入的标准不确定度同3.1.1,uc1=0.30 mg,则辛酸钠称量引入的相对标准不确定度urel(X):
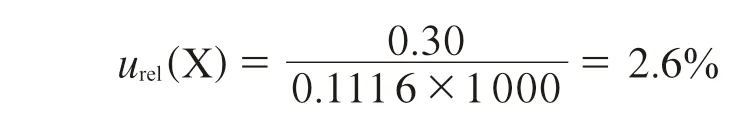
3.2.2 相对分子质量引入的相对标准不确定度
因辛酸标准溶液采用辛酸钠配制,因此存在相对分子量的不确定度,辛酸钠是由C、H、O、Na 四种元素组成,查1993 年国际上公布的元素相对原子质量表,得到C、H、O、Na 四种元素相对原子质量的标准不确定度:u(C)=0.000 8 g,u(H)=0.000 07 g,u(Na)=0.000 002 g,u(O)=0.003 g。

辛酸钠相对分子质量为167.190 41,辛酸钠相对分子质量引入的相对标准不确定度:
urel[M(C8H16NaO2)]=uc2/167.190 41=0.003%
计算结果表明,在进行测量不确定度评定时,相对分子量不准引入的不确定度值较小,可以忽略不计。
3.2.3 计量器具引入的不确定度
本实验方法中,计量器具引入的不确定度来源于2 mL 分度吸量管、5 mL 分度吸量管量、10 mL 容量瓶,此外,还有环境温度变化引入体积相对变化的不确定度和人员读数引入的不确定度。
(1)2 mL 分度吸量管引入的相对标准不确定度urel(2 mL)。
根据《常用玻璃仪器检定规程》[10],2 mL A 级分度吸量管允许误差为±0.012 mL,最小分度值为0.02 mL。按均匀分布考虑,k= 3,2 mL 分度吸量管引入的标准不确定度u(2mL)=0.012/ 3 =0.006 9 mL;假设人员读数误差不超过最小分度值的 1/3,按均匀分布考虑,k= 3,则人员读数引入的标准不确定度u1(e)=0.006 7/ 3 =0.003 9 mL。
合成得2 mL 分度吸量管引入的标准不确定度:


3.3 测量设备引入的不确定度u4,rel
查阅气相色谱质谱校准证书:质谱(MS)灵敏度扩展不确定度U=8%(k=2),测量重复性为3.9%,则质谱灵敏度引入的相对标准不确定度为urel(MS)=U/k=8%/2=4%。计算得气相色谱质谱引入的相对不确定度:
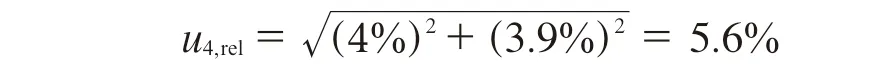
测量设备的不确定度在实验中是无法避免的,因此要使用经过检定合格的或经过校准的测量设备,并且在使用过程中要进行期间核查,确保设备稳定性。
3.4 样品重复测定引入的A 类不确定度u5,rel

3.5 回收率引入的相对标准不确定度u6,rel
平行制备3 份空白样品的加标溶液,辛酸加标浓度为50 μg/mL,测得回收率分别为102%、101%、103%。按照极差法评定回收率引入的不确定度urel(R),极差R=103%-101%=2%,测量次数n=3,查表得极差系数C=1.69,则s(x)=R/C=2%/1.69=1.18%。计算得回收率引入的A 类不确定度:

3.6 不确定度评定结果
以上各个不确定度分量互不相关,则合成相对标准不确定度:
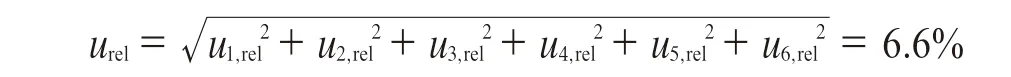
根据数学模型计算得25 g 油样中辛酸含量为13.1 mg/kg,则合成标准不确定度:

取包含因子k=2(近似95%置信区间),则扩展不确定度:U=0.86×2=1.8 mg/kg。
该食用植物油样品中辛酸的含量:(13.1±1.8)mg/kg(k=2)。
4 结语
从实验结果的不确定度评定过程可以看出,标准溶液、标准曲线的配制过程以及测量设备对结果的不确定度影响较大,建议在实验中选用高纯的标准物质或者有证标准物质,尽量减少计量器具使用的次数,使用经检定合格或校准的测量设备。通过不确定度评定,不仅可确定影响测定结果准确性的因素,还对实验方法的建立具有指导意义。

