颈内动脉颅内段慢性闭塞血管内开通术的临床分析
徐耀铭, 杜艳秋, 缪中荣, 高 峰
(1.通辽市医院 神经内科, 内蒙古自治区 通辽 028000;2.首都医科大学附属北京天坛医院 神经介入中心, 北京 100053)
颅内动脉慢性闭塞多数为动脉粥样硬化引起,是缺血性卒中的一个重要原因,以颈内动脉多见,约占全部缺血性脑卒中的10%,其卒中年复发风险为3.6%~22.0%,存在血流动力学障碍的患者年卒中复发风险更高[1]。颈动脉系统中除了神经功能缺损,还可因脑组织长期低灌注而导致认知障碍[2]。因此对于此类患者应给予积极治疗。颈内动脉颅内段慢性闭塞在全部的颅内血管闭塞自然史中约占10.8%[3],目前主要治疗方法仍是药物治疗[4],药物治疗无效的患者可以采取其他治疗方法,包括颅内外搭桥术(extracranial-intracranial bypass surgery, EC-IC)和血管内治疗(endovascular therapy, ET)等。因为颅内外搭桥术存在围手术期高风险及有创性操作的特点不易被患者接受。近年来随着神经介入技术的成熟和介入材料的更新,血管内介入治疗已经成为该领域的研究热点,本研究回顾性收集了颈内动脉颅内段慢性闭塞行血管内再通术患者的临床资料,探讨血管内再通术的安全性及有效性。
1 资料与方法
1.1病例选择 2018年3月至2019年9月北京天坛医院神经介入中心行血管内治疗的症状性颈内动脉颅内段慢性闭塞再通术患者9例,男6例,女3例,年龄46~69岁,平均(52±8)岁。患者有不同程度偏侧肢体无力,认知障碍或短暂性脑缺血发作。从首次发病到介入再通时间21~43天,中位时间29天,既往有高血压病史7例,有糖尿病病史6例,脑卒中病史6例。所有患者均行CT或MR检查,评估梗死部位、范围,排除脑出血及大面积脑梗死患者。所有患者术前均行头颈部血管超声/CTA/MRA检查及多模CT评估病变血管及脑组织灌注及侧支循环等情况。
1.2纳入与排除标准 纳入标准:①年龄>18岁;②症状性:经强化药物治疗4周以上无效仍出现症状的波动、恶化(局灶神经功能缺损的恶化,出现认知障碍等),或美国国立卫生研究院卒中量表(NIHSS)评分增加≥4分或存在血流动力学障碍;③颈内动脉颅内段闭塞被影像学证实,包括TCD/CTA/MRA;④闭塞时间:推测颈内动脉颅内段闭塞时间,患急性脑梗死≥4 w;⑤病因学:颅内大动脉粥样硬化;⑥ASPECTS评分6~10分,经血管影像学检查无前向血流信号(TIMI分级为0);⑦至少有1种脑血管病危险因素(如高血压、糖尿病、高血脂、吸烟等)。排除标准:①无症状性闭塞;②病因学为非动脉粥样硬化性闭塞,如动脉炎、动脉夹层等;③推测闭塞为急性闭塞,时间在24小时内;④经评估闭塞段严重成角;⑤严重血液疾病及心肝肾功能不全;⑥对造影剂、抗血小板聚集药物过敏或不耐受以及消化道溃疡;⑦预期寿命<1年;⑧儿童、孕妇或妊娠期女性;⑨资料不全。
1.3治疗方法
1.3.1围手术管理 包括如下内容:①所有患者均全麻下实施再通手术。②术前服用氯吡格雷联合阿司匹林标准化抗血小板聚集治疗3~5天。③支架首先考虑自膨式支架,其次考虑球扩支架。根据脑梗死溶栓(thrombolysis in cerebral ischemia,TICI)分级,TICI≥2b认为成功再通。④术后严密监控血压;⑤常规服用6个月氯吡格雷联合阿司匹林,根据复查结果调整为单抗治疗。术后严格控制血压、血糖及血脂水平等危险因素。
1.3.2血管内再通术 手术在全身麻醉下进行,全身肝素化,维持活化凝血时间(ACT)在250~300 s,穿刺股动脉成功后置入6 F导管鞘,6 F导引导管送至闭塞血管近端ICA建立路径。造影确认闭塞血管长度、远端血管床,双血管同步路图下Echelon-10微导管(美国ev3公司)和Traxcess-14微导丝(美国MicroVention 公司)相互配合探查通过闭塞段。微导管通过闭塞段后立即撤出微导丝,造影证实微导管头端位于闭塞段远端血管真腔,换用300 cm Transend微导丝(美国Boston 科技公司),头端送至闭塞远端血管床,回撤微导管;根据预估闭塞段血管直径和长度选择合适规格球囊,沿交换导丝将其送至闭塞段进行预扩张,根据预扩张后血管造影、闭塞段近端血管迂曲程度及成角情况选择不同再通策略,如自膨式支架植入、球扩支架植入及单纯球囊扩张。术后即刻造影评估残余狭窄,根据TICI分级评估再通血管远端血流灌注。残余狭窄<30%,且TICI分级≥2b,定义为再通成功。若术后出现美国国立卫生研究院卒中量表(National Institute of Health stroke scale,NIHSS)或改良 Rankin 评分量表(modified Rankin Score,mRS)评分变化,行头部CT、必要时MRI 评价出血或缺血事件,确认终点事件发生(如短暂性脑缺血发作、卒中)。
1.3.3临床随访 分别于术后30、90天进行临床及影像学随访。以后的随访采取电话或门诊随访,临床随访经使用NIHSS评分、mRS评分评估症状改善情况。影像学随访采用颈部血管超声联合经颅多普勒(TCD)/CT血管成像,数字减影血管造影(Digital subtraction angiography,DSA)、CT灌注成像等检查评估患者脑部供血情况。再狭窄定义为支架内再狭窄:经血管造影证实腔内狭窄>50%和较术后原始管腔或支架近段3 mm内的狭窄>20%。临床再狭窄:发生与再狭窄相关责任血管的缺血事件。
2 结 果
2.1手术结果 9例患者全部采用了双路途血管内介入技术,8例患者成功开通成功率89.1%,1例患者因为导丝未通过闭塞段,结束手术,但临床表现同术前比较未出现病情加重。2例自膨式支架,6例球扩式支架。全部8例患者1例出现术后并发症,无死亡病例。出院时8例症状均有所改善,无病情加重病例。

表1 9例颅内动脉闭塞开通患者临床资料
2.2并发症 1例患者术后12小时出现为单眼盲(考虑为视网膜中央动脉栓塞),1个月后好转。无高灌注及脑出血事件发生。
2.3随访结果 30天内无脑血管缺血事件及死亡事件发生。90天时mRS 评分从术前的3.0降到术后的1.0。90天功能独立(mRS:0~2分)比例67%(3/9),中位造影随访11个月,再发狭窄1例,考虑与担心出血而自行停用双抗有关,8例再通术后随访3~12个月,在此期间无缺血事件。6个月时发现支架内狭窄1例,狭窄率为30%(考虑与患者双抗3个月后自行改为单抗有关),此例为无症状性狭窄。
2.4典型病例 男性,54岁。主诉“右侧肢体活动无力2年,加重伴发作性言语笨拙及多睡2个月”。既往高血压病史9年,2年前患脑梗死经住院常规抗栓治疗好转,遗留右侧肢体活动力弱,但可自行行走;吸烟史20年。2个月前患者逐渐出现右侧肢体无力加重,同时伴有吐字欠清晰及反应迟钝,查头MRI提示急性脑梗死(图a ~ c),头CTA提示LC7段闭塞(图d)。NIHSS评分8分。服用阿司匹林、氯吡格雷及阿托伐他汀等药物2个月无效来诊,完善检查确定LC7闭塞,HR-MRI提示闭塞段存在不稳定斑块(图e、f),CT灌注成像见左侧大脑半球灌注减低(图g)。于2018年11月3日入院,全麻下行闭塞血管再通术治疗(图h~n),球扩后植入winspan支架1枚,TICI分级为3级(图m,n)手术顺利,术后3天NIHSS评分降为4分。90天复查时病情稳定,认知障碍恢复,CTA提示血管通畅(图o),CTP提示脑灌注正常(图p),mRS评分2分。
3 讨 论
颈内动脉颅内段慢性闭塞是缺血性脑卒中主要原因之一,与无症状的闭塞相比症状性的年复发风险为5%~6%[5],伴有显著的血流动力学障碍者复发风险更高[6]。引发脑卒中的病因中脉粥样硬化是最常见的病因,约占70%[7],常见于老年和男性。在年轻患者中颈动脉夹层是较常见的病因[8];其他少见病因包括肿瘤、脑动脉瘤、垂体卒中、动脉炎、Moyamoya综合征、外伤、放射和颈动脉部位手术等[9]。导致脑卒中的病因包括动脉粥样硬化斑块或碎片脱落导致的栓塞,占卒中的2/3;还有脑灌注降低导致的缺血事件。根据脑组织血供的不同代偿、动脉闭塞的不同部位,颅内动脉闭塞可能无症状或症状较轻,而难以准确判定血管的闭塞时间。多个研究结果提示闭塞位于颈段的技术成功率高于远端闭塞者[10-11]。目前认为闭塞至床突段及以上者,其血管内介入再通成功率低、风险大、远期效果不佳,手术带来的益处不多,需要谨慎选择合适的患者。另外还需要考虑的因素是闭塞时间,既往研究显示闭塞时间越长开通成功率越低,准确的血管闭塞时间往往难以判断,临床多根据临床症状及影像学检查去推测,随着血管闭塞时间延长,血栓可能随之延续、血管内血流减少后血管壁塌陷、闭塞段纤维化,从而导致术中导丝通过时更难找到真腔以及容易出现夹层。近年来,随着介入技术的成熟和材料的发展,经强化药物治疗无效的症状性颈内动脉颅内段慢性闭塞患者,血管内介入再通术是另一个可行的选择。
本研究纳入9例颈动脉颅内段慢性闭塞行血管内治疗,开通率为89.1%(8/9),术后并发症发生率及再狭窄率分别为11%。1例术后12小时出现了突发左眼视力丧失,原因为术中微栓子栓塞了视网膜中央动脉所致,当时未给予溶栓治疗,30天后电话随访时视力完全恢复。1例患者半年时随访行头CTA提示支架内轻度再狭窄,无神经功能缺损的症状和体征,考虑与患者术后3个月未遵医嘱自行改为单抗药物有关,嘱患者重新服用双抗治疗并适当延长双抗用药时间。
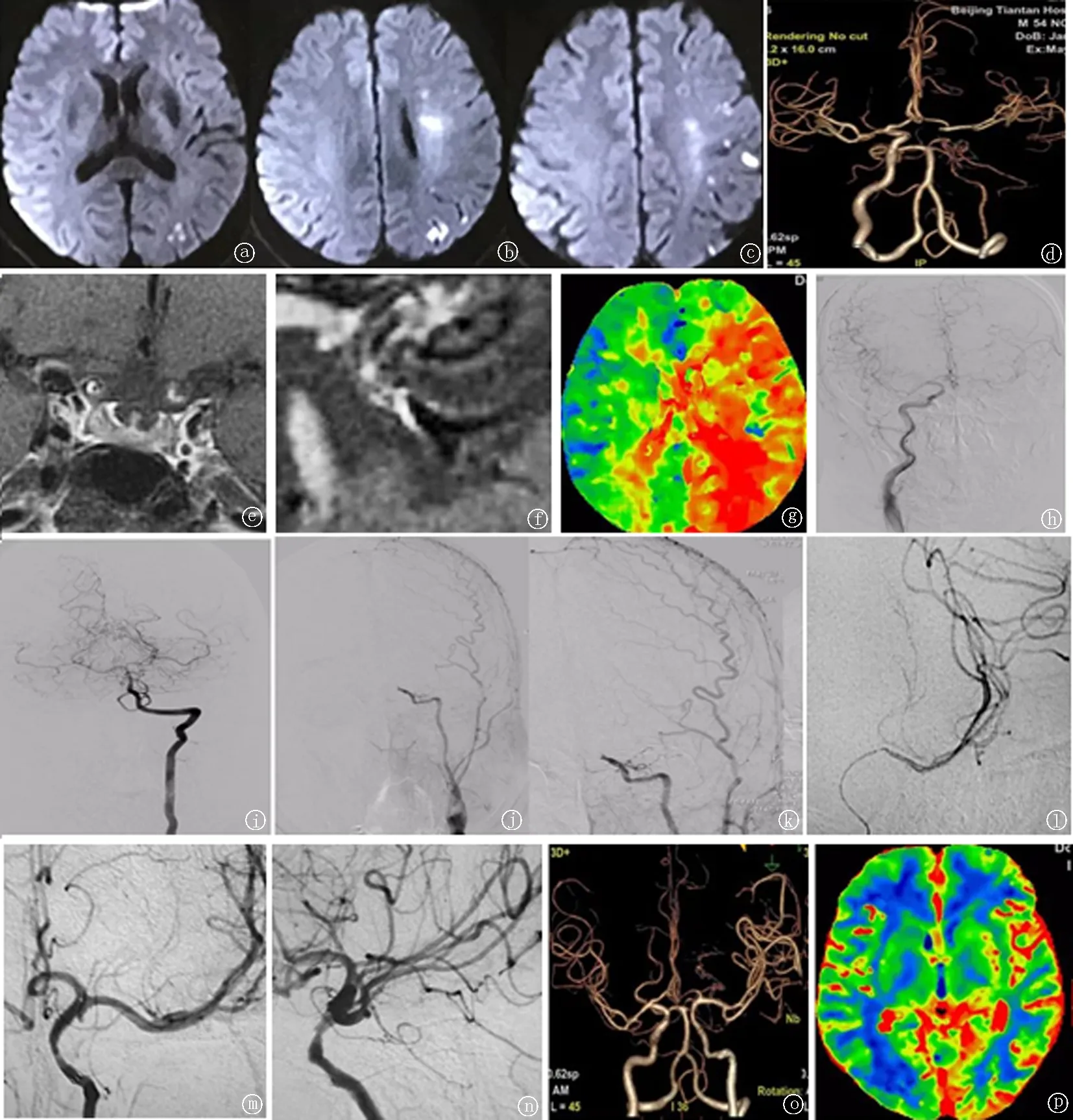
图1 典型病例血管再通术前后影像学资料 a~c:为患者发病时头MRI影像见左侧大脑半球散在点片状高信号影;d:为发病时头CTA见左侧颈内动脉C7段闭塞;e,f:为颈内动脉闭塞段高清核磁可见闭塞段流空影消失,不均质混杂影像提示为不稳定斑块(箭头所示);g:为头CT灌注可见左侧大脑中动脉支配区低灌注;h~k:为术前DSA提示前交通开放及软脑膜动脉部分代偿,灌注延迟表现;i:微导丝穿过闭塞段,经微导管超选造影证实在真腔内;m、n:支架植入后造影,血管通畅血流TICI分级3级;o:术后90天复查头CTA提示血管通畅未见狭窄;p:为CT灌注提示左侧大脑半球灌注正常
血管再通的关键因素是微导丝可否顺利穿过闭塞段进入血管真腔。本组病例中有1例患者术中反复尝试微导丝通过,仍不能穿过闭塞段而放弃手术,考虑与血管闭塞时间较长导致其远端血管内血栓机化有关。根据冠脉慢性闭塞再通的经验在急性闭塞后3个月内实行再通成功率高[12],说明病变血管远近段血管条件是决定介入再通率的重要因素,慢性闭塞使闭塞远端血管内血栓形成和机化会使再通率下降。本组患者从急性缺血事件到开通时间均未超过3个月,这也许是本组病例再通率较高的原因之一。
目前颈动脉颅内段慢性闭塞患者,血管内再通治疗的适应证尚未明确,结合本组病例数据,推荐如下参考: ①患者颈动脉远端闭塞的时间最好在3个月以内; ②术前需要充分评估血流动力学参数变化,确定脑组织的损伤程度;③患者明确存在与闭塞血管相关的临床症状; ④闭塞节段局限(<15 mm),长段病变要谨慎开通,术中操作应该更谨慎,对于反复尝试失败的及时终止开通。除此之外,还应该全面分析影响患者获益的其他因素,如血管通路条件、残端形态、闭塞段血管的成角、血栓钙化程度、以及开通策略等。以前的血管再通研究中,因缺乏全面的影像评估,微导丝误操作可造成动脉夹层、蛛网膜下腔出血和脑实质出血的案例并不少见[13]。本组严格筛选患者和充分影像判断,通过术前评估技术指导再通过程和尽可能规避风险。
目前颅内动脉慢性闭塞血管内开通治疗仍处于探索阶段,技术操作仍缺乏统一的规范化指南或共识的指导。本研究结果提示颈内动脉颅内段慢性闭塞血管内开通术安全可行,可以在临床推广,但鉴于此结果为本中心的临床观察,结果需要谨慎看待。其局限性在于本研究为单中心回顾性研究,病例数较少,可能会存在偏移,此外对患者远期预后缺乏长期的随访。因此有待于多中心大样本随机对照试验以进一步验证。

