微波消解-微分脉冲阳极溶出伏安法测定茶叶中铅
朱小亮,吴到懋,樊冬玲*,孙步旭,王辉,司波
1. 江苏省宿迁环境监测中心(宿迁 223800);2. 宿迁市产品质量监督检验所(宿迁 223800)
铅是一种常见重金属,在人体内不易排出,对人体器官具有致命损伤[1-2]。由于工业快速发展,土壤被重金属污染加剧,茶叶中重金属含量有上升趋势[3-4]。测定铅比较常见的方法有电感耦合等离子体光谱(ICPAES)法[5]、原子吸收光谱法[6~7]、分光光度法[8]、电感耦合等离子体-质谱(ICP-MS)法[9-11]等。但方法检测仪器昂贵,测试成本高。阳极溶出伏安法[12-13]是一种操作简单、稳定好、灵敏度高且成本低的检测方法,获得广泛应用[14-15]。
干法消化和湿法消化是目前样品前处理重要的2种方法[16]。但干法消化耗时较长,元素易损失;湿法消化样品容易被污染,影响检测结果准确性,同时试验过程产生消化酸雾,危害分析人员健康和环境。微波消解可以优先降低试剂用量,减少环境污染[17-18]。微波消解得到广泛应用。
结合微波脉冲阳极伏安技术和微波消解优点,测定茶叶中铅,并与ICP-MS法比对,结果一致。表明检测方法准确可靠,同时检测方法不需除氧、干扰少、灵敏度高,应用于实际样品分析,能取得满意结果。
1 材料与方法
1.1 材料与仪器
RST5200F型电化学分析仪(深圳世瑞思科技有限公司);三电极系统(辅助电极为铂电极,工作电极为银基汞膜电极,参比电极为Ag/AgCl电极);Agilent 7900型电感耦合等离子体-质谱仪(美国安捷伦科技有限公司);MASTER 40A型微波快速消解仪(上海新仪微波科技有限公司);铅标准溶液(质量浓度1 000 μg/mL有证标准物质,国家标准物质研究所);试剂均为分析纯以上;用水为自制高纯水。
1.2 试验方法
将50 mL浓度0.6 mol/L HCl溶液倒入100 mL烧杯,放入搅拌子充分搅拌,放入三电极系统,设置微分脉冲伏安溶出电化学最佳条件,从-0.1 V起负向扫描至-1.0 V,记录在-0.4 V(vs. Ag/AgCl)处的溶出峰电流,做空白试验;按照同样的条件,配制不同浓度铅标准溶液,测定-0.4 V(vs. Ag/AgCl)峰电流,实际样品经微波消解后按照此方法测定。
2 结果与分析
2.1 支持电解质溶液的选择
为考察不同底液对铅离子(2.0 μg/L)峰电流影响,分别以0.5 mol/L HAc-NaAc(pH 5.0),0.5 mol/L KCl,0.5 mol/L NH3-NH4Cl(pH 4~5),0.5 mol/L PBS缓冲液,0.5 mol/L (NH4)2SO4,0.5 mol/L H2SO4,0.5 mol/L HCl和0.5 mol/L NaNO3底液进行试验。结果表明,以HCl为底液时,基线平稳,同时以不同浓度HCl(0.1,0.2,0.6,0.8和1.0 mol/L)作为电解质溶液测定,对比发现0.6 mol/L HCl基线平稳、峰电流最大,峰形对称,重现性好。故选择0.6 mol/L HCl为测定底液。
2.2 铅阳极溶出伏安图
由图1可知,铅在工作电极溶出峰电位-0.40 V(vs. Ag/AgCl),峰电流峰形较好,电流强度随铅离子浓度增大而增大,峰肩基本对称,底液无干扰峰,基线平稳,可用于铅离子定量分析。
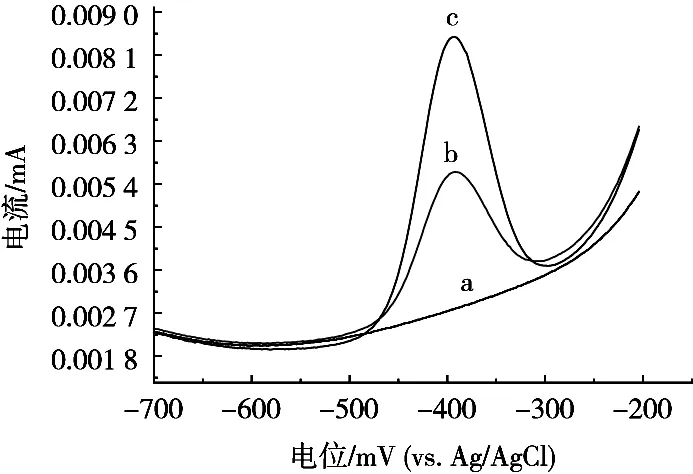
图1 铅离子阳极溶出伏安图
2.3 富集电位对峰电流影响
在底液浓度0.6 mol/L HCl、铅浓度2.0 μg/L体系中,在-1.0~-0.1 V范围内改变富集电位,考察富集电位对峰电流影响。由图2可知,铅离子的溶出峰电流随着富集电位的负移而迅速增大,富集电位过-0.9 V后,峰电流增加缓慢,峰电流过-1.0 V后,峰电流明显减小;富集电位超过-1.0 V继续负移时,在汞膜电极周围有明显气泡产生,发生析氢现象。故选择富集电位-0.9 V。
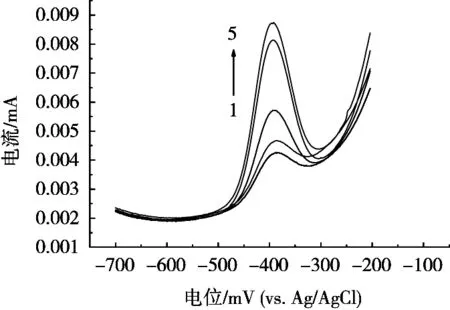
图2 富集电位对溶出峰电流的影晌
2.4 振幅、周期选择
在底液浓度0.6 mol/L HCl、铅离子质量浓度2.0 μg/L、富集电位-0.9 V体系中,在20~110 mV范围内改变微分脉冲振幅,考察微分脉冲振幅对峰电流影响。由图3可知,铅离子的溶出峰电流随着振幅增大而增大,同时溶出峰电位发生负向移动;但振幅大于80 mV时,峰的形状发生突变,峰肩变宽,峰发生拖尾,灵敏度较差,对铅离子浓度的测定产生干扰,检测重现性较差,不利于铅的定量分析。故选择微分脉冲振幅80 mV。由图4可知,随着微分脉冲周期增大,铅离子的溶出峰电流先增大后减小,脉冲周期0.1 s时峰电流最大,峰形较好,满足铅检测要求,因此选择微分脉冲周期0.1 s。
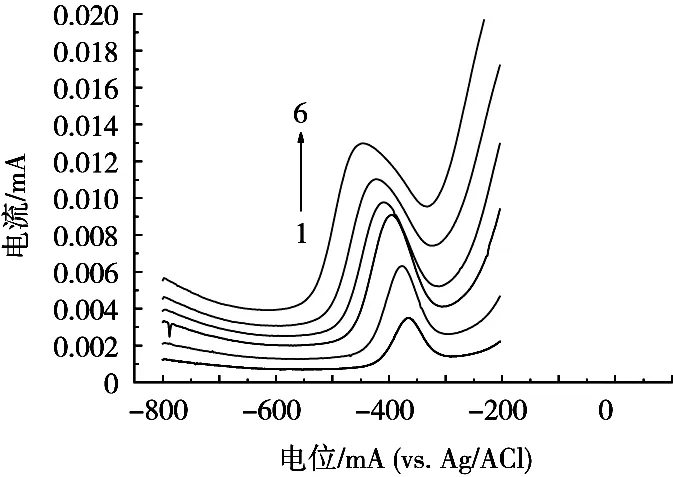
图3 微分脉冲振幅对溶出峰电流的影响
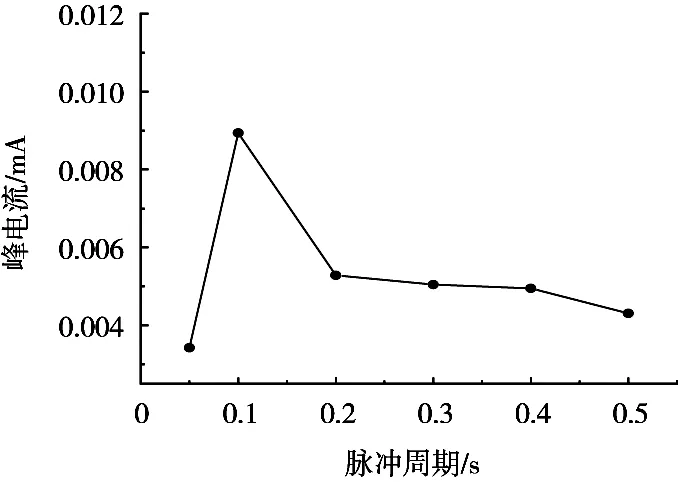
图4 峰电流与脉冲周期的关系
2.5 富集时间的选择
在支持电解质浓度0.6 mol/L HCl、铅离子质量浓度2.0 μg/L、电位-0.9 V、振幅80 mV体系中,考察微分脉冲富集时间对峰电流影响,见图5。富集时间在100~500 s逐渐增大时,溶出峰电流随之增大,峰形对称,溶出峰电流稳定。随着富集时间增加,峰电流增加缓慢,但背景溶出峰电流增加较快,不利于铅离子的测定。缩短铅离子的富集时间,有利于铅扩大铅离子测定范围。420 s时,铅离子的溶出峰电流较大,峰形对称,满足测定,故选择富集时间420 s。
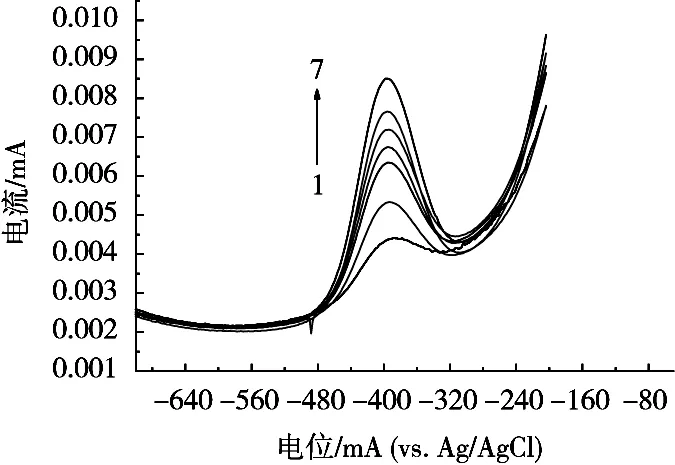
图5 富集时间与峰电流关系
2.6 溶解氧对峰电流的影响
为考察溶解氧对测定体系的影响,在测试中通入高纯氮气进行测定,另一组在实验室开放的体系中测定,2种体系中测得峰电流强度基本一致,表明铅的溶出是通过电位转正实现的,因此测定铅离子浓度不需要除氧,可在实验室开放的空间进行,且操作简单。
2.7 干扰离子对检测体系影响
按照最佳检测条件,铅溶液标准质量浓度10 μg/L进行测定,测定相对误差±5时,500倍的Mn2+、Zn2+、Fe3+、Al3+、Co2+,100倍的Bi3+,50倍的Ca2+,Sn2+,20倍的Ni2+均无干扰,大量对铅离子检测均无干扰。
2.8 标准工作曲线及检出限
在最佳试验条件下,按照逐级稀释的方式,配制不同浓度的铅标准溶液,测定微分脉冲阳极溶出峰电流。结果表明,铅的质量浓度在0~14 μg/L范围内,铅离子浓度与峰电流呈线性关系,如图6所示,线性方程为i(mA)=0.001 21+3.819 3×10-4ρ(μg/L),相关系数为0.999 8,以3倍信噪比作为仪器的检出限,其检出限为0.1 μg/L。
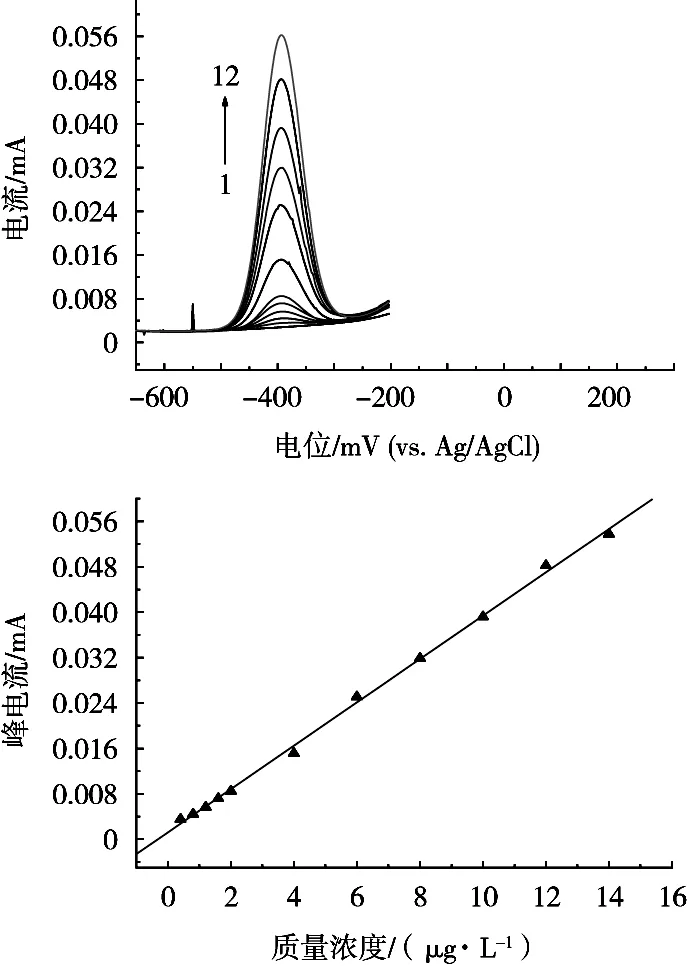
图6 铅离子质量浓度与溶出峰电流线性关系
2.9 精密度和准确度试验
配制一定浓度铅标准溶液,在最佳试验条件下,考察方法的准确度及回收率,结果见表1。方法相对标准偏差1.74%~3.69%,平均值3.11%,回收率91.4%~103%,平均回收率96.8%。试验表明方法精密度及准确度较高,可用于茶叶中铅测定。
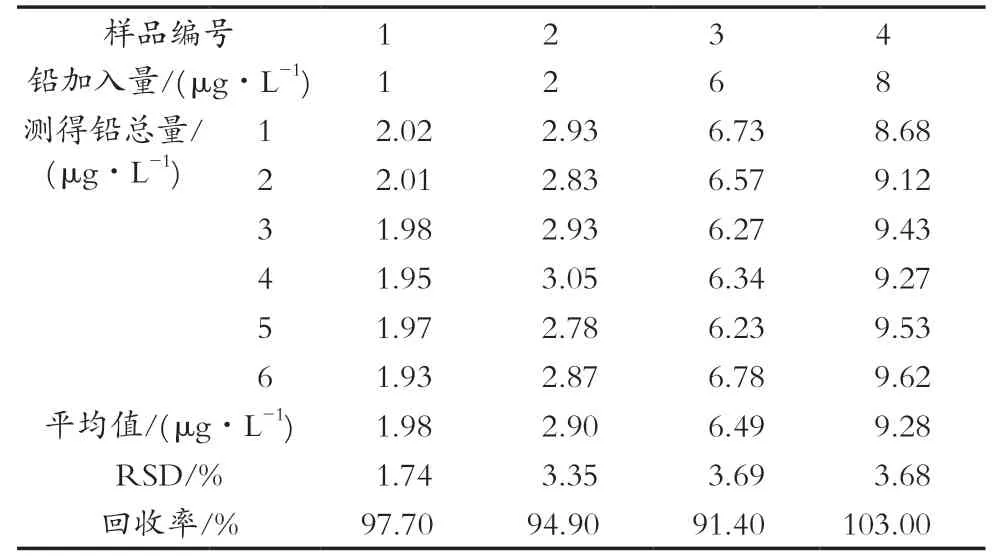
表1 精密度及回收率试验
2.10 样品分析
2.10.1 样品微波消解处理
用电子天平称取1.000 g干燥茶叶于消解罐中,并加入5.0~6.0 mL浓硝酸和1~2 mL过氧化氢,静置10 min,待剧烈反应后,把消解罐拧好,放于微波消解仪中消解,消解仪程序见表2。消解完成后,冷却室温后打开消解罐,并用稀盐酸洗涤消解罐,消解液在电热板上蒸干,移入50 mL容量瓶中,用0.6 mol/L HCl盐酸溶液定容,按试验最佳条件进行分析,同时做试剂空白试验。

表2 微波消解仪的消解程序
2.10.2 实际样品分析
采购市场上4种不同茶叶,按照微波消解方法消解样品,采用微分脉冲阳极溶出法进行测定,将测定结果与ICP-MS法测定结果进行对比分析,结果见表3。结果显示,2种方法测定结果一致,表明方法测定可靠,可用于茶叶中铅的测定。
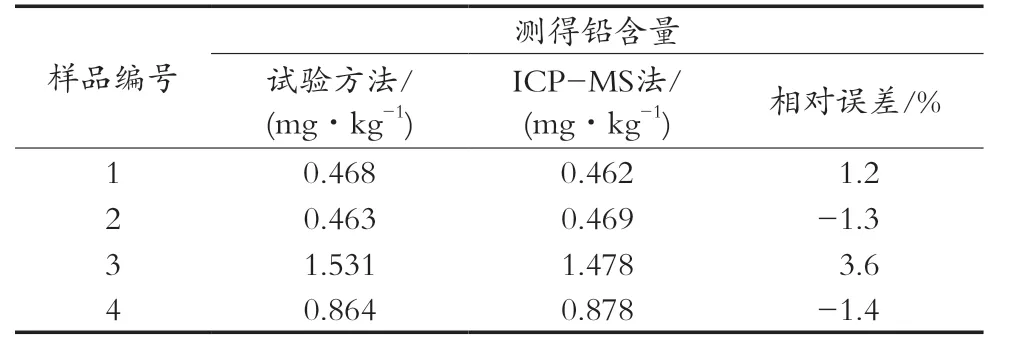
表3 茶叶中铅测定结果比较(n=6)
3 结论
在0.6 mol/L HCl底液中,优化电化学条件:富集电位-0.9 V、时间420 s、振幅80 mV、周期0.1 s时,铅在工作电极上于-0.4 V(vs. Ag/AgCl)出现一个灵敏的微分脉冲阳极溶出伏安峰,峰电流与铅离子质量浓度在0~14 μg/L范围内呈良好的线性关系,线性方程为i(mA)=0.001 21+3.819 3×10-4ρ(μg/L),相关系数为0.999 8,方法的检出限为0.005 mg/kg。方法把微波消解与阳极溶出优点融合,无污染,试剂用量少,铅不易损失,检测结果准确,是一种实用铅的测定方法。

