趋化素及可溶性ST2对阵发性心房颤动射频消融术后复发的预测价值
杨华 孟利民 信栓力 常超 刘吉祥 赵秀峰 王霞 王雅男 张仁杰 申晨
056002 邯郸市第一医院心内一科
心房颤动(atrial fibrillation,AF)是临床上最常见的心律失常之一,发病率呈上升趋势,其致死率高、致残率高和复发率高[1],AF使患者卒中发生风险升高5倍,心力衰竭风险升高3倍。近年来,导管射频消融术成为治疗AF安全有效的方法,但术后高复发率限制了其广泛应用。目前尚无方法或药物能完全预防射频消融术后AF的复发,故识别AF复发的预测因子,降低复发率至关重要。研究表明,AF复发可能与炎症和心房纤维化有关[2],炎症可进一步加重心房肌细胞的损伤、坏死、凋亡和纤维化,导致心房的结构重构和电重构,促进AF的发生和维持。趋化素(chemerin)与炎症、脂肪生成、脂质稳态及动脉粥样硬化有关[3],在很多炎性和代谢性疾病中都有所增高,但尚未研究其与AF射频消融术后复发的关系。可溶性ST2(soluble ST2,sST2)水平升高是促进心肌纤维化的重要因素[4]。也有学者研究发现AF患者sST2水平升高,但其对射频消融术后复发的影响尚不清楚[5]。因此,本研究通过对行导管射频消融治疗的AF患者进行研究,探讨趋化素及sST2对AF患者术后复发的预测价值,评估患者复发的风险,为进行个体化治疗提供依据。
1 对象和方法
1.1 研究对象
选择2015年11月至2018年11月于邯郸市第一医院心内科首次接受三维电解剖标测系统(3-dimensional electroanatomic mapping system,CARTO)指导下环肺静脉电隔离射频消融治疗的非瓣膜性阵发性AF患者100例,男性49例,女性51例,平均年龄(56.1±10.5)岁。所有纳入的患者均完成术后12个月的随访,阵发性AF射频消融术后的复发率为27%(27/100)。根据AF复发情况将患者分为复发组(27例)和未复发组(73例)。纳入标准:入院时行标准12导联心电图诊断为心房颤动。7 d内自行或药物或电复律转为窦性心律的患者视为阵发性AF。排除标准:急性或终末期肝病、严重慢性阻塞性肺病、急性冠状动脉综合征、恶性肿瘤、过去2周内出现的活动性感染、血红蛋白<8 g/dl、严重主动脉瓣和二尖瓣病变、左房(left atrial),LA直径>55 mm、左室射血分数(left ventricular ejection fraction,LVEF)<45%,经食道超声心动图发现云雾状影(自发显影现象)。本研究符合医学伦理学要求,研究方案经邯郸市第一医院伦理委员会批准(伦理号:2015-23),所有入选患者签署知情同意书。
1.2 方法
入院后详细记录患者的各项临床资料,包括年龄、性别、体重、身高、当前吸烟状况、心血管危险因素(高血压、糖尿病、高脂血症)、心脏病家族史和药物使用情况,包括血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂(angiotensin-converting enzyme inhibitors/angiotensin receptor blocker,ACEI/ARB)、β受体阻滞剂、胺碘酮及口服抗凝药物等,全面的体格检查(血压、心率、心肺查体情况等)。使用CHA2DS2-VASc评分评估卒中风险,HAS-BLED评分评估出血风险。
术前所有患者均行标准12导联心电图、24 h动态心电图、常规术前实验室检查(血常规、血脂、肾功能、甲状腺功能等)、N末端B型利钠肽原(N-terminal pro brain natriuretic peptide,NT-proBNP)、胸部X线、经胸和经食道超声心动图检查。术前停止口服抗凝剂,用依诺肝素桥接术前间期。术前均停用抗心律失常药物5个半衰期以上。
1.3 趋化素和sST2水平的检测
所有患者射频消融术前取静脉血样,于禁食8 h后,静坐30 min后采集,混匀,立即离心,并在-80℃下储存,待标本全部收集完毕后1次测定。采用酶联免疫吸附法的双抗体夹心法测定血清趋化素(ng/mL,试剂盒由上海西唐生物科技有限公司提供)和血清sST2水平(测量范围为3.1~200 ng/ml)(Presage ST2试剂盒,美国Critical diagnostics公司)。为减小AF对趋化素及sST2的影响,术前均于窦性心律下留取标本。
1.4 超声心动图评估
采用飞利浦公司的超声心动图机,探头频率为2.5~3.5 MHz。方法:以声学成像模式取心律稳定的连续3个心动周期的胸骨旁长轴、心尖四腔和心尖二腔二维灰阶动态图像。测量LA舒张末期前后径大小,心尖四腔切面测量LA舒张末期上下和左右径大小,采用双平面面积长度法计算LA容积,使用LA容积和患者体表面积计算LA容积指数;测量左室舒张末期横径、左室舒张末期内径(心电图Q波开始),采用改良Simpson’s双平面法测量并计算LVEF;同时评价室壁运动异常、室壁厚度和心脏瓣膜等。
1.5 射频消融方法
按照2007年ACC/AHA/ESC的AF指南中的环肺静脉隔离导管消融原则及方法,在CARTO系统指引下,进行左房三维结构建壳和环肺静脉电隔离。在整个手术过程中持续监测有创动脉血压、血氧饱和度和心电图。消融终点为肺静脉电位处于完全电隔离状态。AF消融时,若有典型右房三尖瓣峡部依赖的房扑的依据,则在连接三尖瓣环和下腔静脉口之间的峡部进行连续线性消融,以达到三尖瓣峡部双向阻滞。
1.6 术后管理及随访
术后6 h开始口服抗凝剂,新型抗凝药物或华法林(使国际标准化比值维持在2~3),术后至少持续3个月;根据CHA2DS2-VASC评分,3个月后评估是否继续口服抗凝剂;抗凝药物未起效前给予低分子量肝素皮下注射。抗心律失常药物治疗持续3个月。术后1个月内口服质子泵抑制剂。术后3个月内饮食避免坚硬、带刺、刺激性及难消化的食物。
嘱患者于术后第3、6和12个月门诊随访,行12导联心电图和24 h动态心电图监测,评估AF复发情况,若12个月内患者出现心悸胸闷症状的患者,即刻就诊并行心电图记录是否复发,尽早行动态心电图检查。AF复发定义为消融术3个月后,经心电图或24 h动态心电图证实快速房性心律失常的发作持续时间≥30 s。
1.7 统计学方法
2 结果
2.1 两组患者的一般临床资料比较
复发组的年龄、体重、吸烟、糖尿病史、高血压病史、ACEI、ARB药物使用情况、CHA2DS2-VASc和HAS-BLED评分均显著高于未复发组(均为P<0.05),而两组患者的其它临床资料相似(均为P>0.05),见表1。
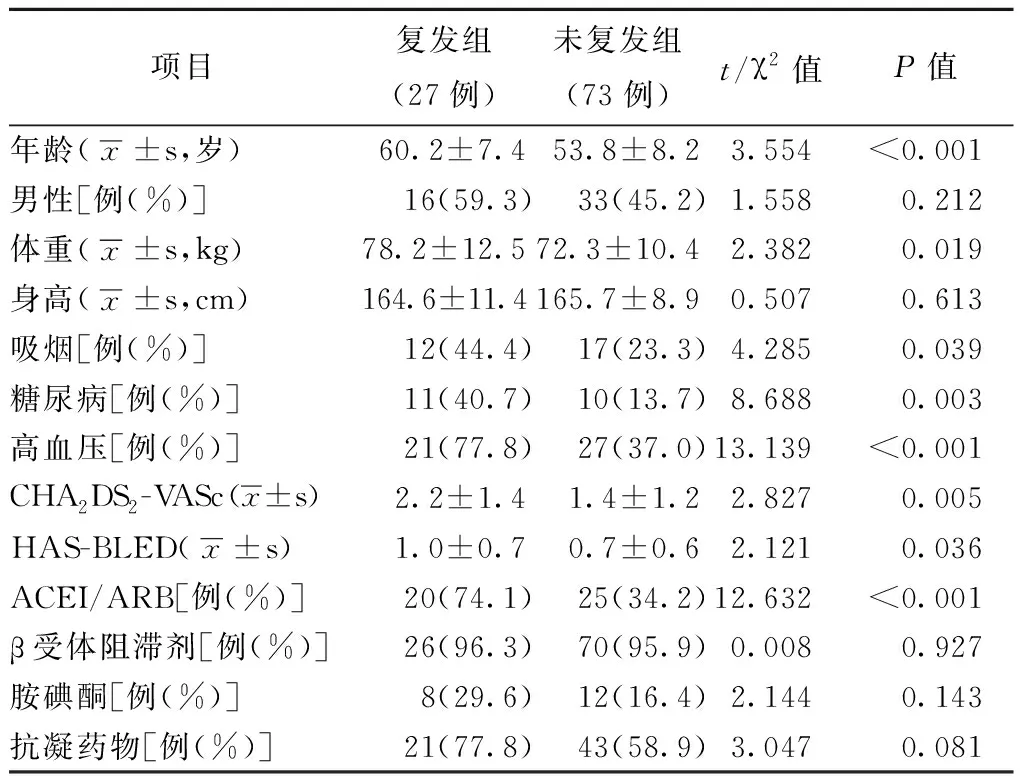
表1 两组患者的一般临床资料比较
2.2 两组患者的实验室检查指标比较
与未复发组患者相比,复发组的血清趋化素[(162.7±24.2) ng/ml比(132.7±22.7)ng/ml,P<0.01]和sST2水平显著升高[(35.7±8.3)ng/ml比(15.2±6.9) ng/ml,均为P<0.01];而其他实验室检查结果则无明显差异(均为P>0.05)。
2.3 两组患者的超声心动图参数的比较
与未复发组患者相比,复发组患者LA舒张末期直径[(39.8±5.1)mm比(34.8±6.2)mm]、LA容积[(62.1±10.4)ml比(46.3±12.7)ml]和LA容积指数[(34.5±6.4)ml/m2比(25.1±7.3)ml/m2]均显著增高,差异具有统计学意义(均为P<0.01)。
2.4 影响AF消融术后复发因素的logistic回归分析
对患者的年龄、体重、吸烟史、糖尿病史、高血压病史、ACEI/ARB药物应用、血清趋化素及sST2水平、LA舒张末期直径和LA容积指数等变量进行多因素logistic回归分析,结果显示趋化素(OR=1.055,95%CI:1.030~1.081,P<0.001)和sST2(OR=1.552,95%CI:1.235~1.951,P<0.001)是阵发性AF射频消融术后复发的独立预测因素。
3 讨论
本研究的主要发现是趋化素及sST2对AF射频消融术后复发有一定的预测价值。 以肺静脉隔离为主要方式的导管射频消融术已成为症状性和药物难治性AF患者的一种有效和安全的治疗策略。既往研究表明,AF射频消融术的平均年成功率为60%~70%[6]。复发率较高,如何预测AF患者射频消融术后复发的风险尤为重要。
趋化素是最近被发现的脂肪因子,与脂肪细胞分化、成熟及代谢、体重指数、胰岛素抵抗等代谢性疾病及心血管疾病相关,可促进免疫反应及炎症的级联反应[7]。sST2与炎症、纤维化和心脏功能相关[8]。但是趋化素及sST2是否能预测AF复发仍未见报道。
本研究中表明趋化素和sST2水平高的AF患者射频消融术后复发率更高,提示这些患者从射频消融中获益较少,趋化素和sST2水平可能有助于导管消融术后AF复发的预测。研究表明,炎症、氧化应激、纤维化参与AF的发生和维持,但AF的发生是否直接启动炎症和氧化应激途径,或是否存在已有的系统性炎症或促氧化条件导致了AF的发生仍不明确[9]。但是,AF发生后会出现恶性循环,炎症和氧化应激途径的激活会导致钙通道的增加和钠通道的减少,即电重构,进而导致LA纤维化,即结构重构,包括成纤维细胞增殖、炎症和凋亡[10]。另外,炎症反应可以通过调节成纤维细胞活性和影响基质金属蛋白酶/基质金属蛋白酶抑制剂的系统平衡,促进AF基质的形成,增加AF易感性[11]。研究证实,趋化素由成纤维细胞释放,通过促进巨噬细胞向脂肪组织迁移来调节炎症反应[12],并且可通过减少蛋白激酶B磷酸化,增加半胱氨酸蛋白酶裂解诱导心肌细胞凋亡[13],趋化素通过激活丝裂原活化蛋白激酶信号通路刺激血管平滑肌细胞增殖,可能导致血管炎症和重构[14]。因此,我们推测趋化素可能通过促炎、促凋亡及促纤维化的作用来发挥其促AF的效应。
本研究提示高水平的趋化素及sST2是AF射频术后复发的独立预测因素,可能成为AF治疗的潜在靶点,二者有可能成为检测LA严重纤维化、LA重构的指标,因此,射频消融术前测定趋化素和sST2水平可评估术后复发风险,从而识别高危人群,采取相关预防措施,提高手术成功率。
我们的研究不包括非阵发性AF、睡眠呼吸暂停、慢性阻塞性肺病或心力衰竭患者,且入选患者的平均LA直径相对较低,且动态心电图监测只进行了24 h,因此,这些因素对AF复发的预测价值无法评估。此外,AF在1年后复发率较高,因此随访2~3年可能更合适。我们的研究为单中心研究且样本量相对较小,趋化素及sST2水平升高是否可作为LA结构重构的标志,以及鉴别AF复发是由于肺静脉电位的重新连接还是存在非肺静脉触发灶,仍需更多研究去进一步证实。
利益冲突:无