基于营养评估的吞咽功能训练对脑卒中后吞咽功能障碍患者的影响
林燕琼 郭艳霞 郭演云
脑卒中是一种常发于中老年人的脑血管性疾病,致死率和致残率均较高,临床症状一般表现为神经功能缺失、神经系统严重受创、脑部血液循环障碍等。吞咽功能障碍是脑卒中患者常见并发症之一,其发生率约为脑卒中患者的37%~74%[1]。有报道表明[2],脑卒中后吞咽功能障碍主要临床表现为发音困难、饮水或进食呛咳,需小口多次吞咽、进食困难等。易因水、电解质紊乱、营养不良、误吸导致肺部感染等并发症,是影响脑卒中预后的独立危险因素之一。因此,科学、及时治疗脑卒中后吞咽功能障碍,对提升脑卒中治疗效果、降低病死率、改善预后尤为重要。既往一般使用常规肠内营养支持,效果不佳。基于营养评估的吞咽功能训练是一种新型的治疗方式,但相关报道较少[3]。本研究探讨基于营养评估的吞咽功能训练对脑卒中后吞咽功能障碍患者的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取本院2016年1月至2018年12月收治的脑卒中后吞咽功能障碍患者110例。纳入标准:经MRI、CT、实验室检查均符合脑卒中诊断标准[4],符合吞咽功能障碍诊断标准[5],并通过才藤氏吞咽障碍7级评分法诊断,所有患者均为中重度吞咽功能障碍;生命体征、神经学体征稳定,依从性强,可配合完成本次研究;对本次研究知情并签署知情同意书;无咽喉器官或口腔占位病变。排除标准:合并有小脑及脑干梗死、短暂性脑缺血发作、可逆性缺血性神经功能缺失;近期使用过肌松剂、利尿剂、镇静剂等对吞咽功能有影响的药物;合并有意识障碍、精神类疾病者及病程为3 d内死亡;合并有严重免疫系统、造血系统疾病及心、肝、肾等疾病。将患者等分为对照组和观察组,对照组中男25例,女30例;年龄51~69岁,平均(60.38±3.24)岁;病程3~59 d,平均(31.45±3.26)d。观察组中男26例,女29例;年龄50~69岁,平均(60.19±3.51)岁;病程4~60 d,平均(31.27±3.81)d。本研究经医学伦理委员会批准,两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组患者入院后,均采取常规综合治疗,出血性脑卒中使用脱水、系统脑细胞活化剂、对症支持治疗等,缺血性脑卒中采用脑细胞活化剂、抗凝、动静脉溶栓降纤、改善循环、抗血小板聚集等治疗。
1.2.1 对照组 给予常规肠内营养支持,治疗时间为4周。于患者入院3 d内通过鼻胃十二指肠管,按照35 kcal/kg的供给量给予肠内营养混悬液。当患者可进食时,家属遵医嘱准备食物,先小口缓慢喂食,逐渐加量。
1.2.2 观察组 给予基于营养评估的吞咽功能训练,治疗时间为4周。吞咽功能训练方法:(1)指导患者每天面对镜子进行口唇闭锁训练(张口-闭口-微笑-鼓腮-吐气),若无法自主完成则由护理人员辅助完成。(2)指导患者每天进行下颌运动,将口最大程度张开后松弛,接着由下颌向两侧运动;对于无法完成下颌运动者,先对痉挛肌肉进行冷刺激或按摩,促使咬肌放松,然后再开始训练。(3)指导患者进行舌运动训练,将舌头最大程度向前或向两侧伸出,若无法自行完成舌运动训练者,由护理人员辅助进行,用纱布将患者舌尖包裹,进行轻缓牵拉,接着叮嘱患者用力缩舌,使之能够前后运动,并嘱患者可通过舌尖对口唇周围进行舔吮,以促进舌头的灵活性。(4)冷刺激锻炼。使用冰冻过的棉棒蘸取冰水对腭弓、软腭、咽后壁及舌根进行刺激,嘱患者进行吞咽动作锻炼,每天3次,每次10 min。(5)通过对患者进行洼田饮水试验,对患者吞咽功能进行判断,确认吞咽功能有所提高后,将直接进食训练与以上训练相结合,先通过半固形食物进行直接进食训练,逐渐过渡到固形食物。训练方式:患者先充分休息30 min后,在安静环境下,取坐位或半坐位,头稍偏向健侧方向,可自主进食者则自主进行;若无法自主进食者,由护理人员辅助进食,先小口缓慢摄入,食物不超过1勺,待患者完全咽下后,再摄入下一口。(6)营养评估支持。根据患者吞咽功能恢复情况及训练进展,给予现用现配的全营养性商用营养制剂,由低稠度逐渐增加为高稠度,每天进食次数为5~6次,每天进食总热量根据患者体质量进行计算,总热量=25 cal/kg×标准体质量(kg)。(7)营养制剂稠度判断标准。通过下端有孔径为3.5 mm小孔的岩田黏度计(容积:50 ml)测量营养制剂的稠度,在岩田黏度计中装入不同稠度的营养制剂,然后将小孔放开,以营养制剂完全从岩田黏度计中流出的时间作为稠度判断标准,总共分为4级,级数越高,营养制剂越为浓稠。其中4级稠度为160~200 s,呈果蓉状;3级稠度为110~120 s,呈奶昔状;2级稠度为60~70 s,呈核桃露状;1级稠度为8~12 s,呈粥水状。
1.3 观察指标
比较两组患者以下指标:(1)治疗前后电视透视吞咽功能检查评分(VFSS)、Burke吞咽障碍筛查量表(Burke)评分情况。VFSS评分[6]:对患者吞咽功能进行评价,总分为10分,分数越高表示患者吞咽功能越好。Burke评分[7]:通过Burke吞咽障碍筛查量表评分对患者吞咽障碍情况进行评价,总分为7分,分数越高,表示患者吞咽障碍越为严重。(2)比较两组患者营养指标(Hb、ALB、TP)水平情况。(3)身体指数中上臂肌围、肱三头肌皮褶厚度以及体质量指数变化情况。体质量指数:通过Body质量Mass Index(BMI指数)对患者身体质量指数进行计算。(4)治疗后并发症发生情况,包括压力性损伤、泌尿系统感染、消化不良、呼吸不畅。
1.4 统计学处理
采用SPSS 17.0统计学软件,进行数据处理,计量资料比较采用t或t’检验,计数资料比较采用χ2检验。检验水准α=0.05。
2 结 果
2.1 治疗前后两组患者VFSS,Burke评分比较
观察组患者治疗后VFSS评分明显高于对照组,Burke评分均明显低于对照组,差异有统计学意义(P<0.05),见表1。

表1 治疗前后两组患者VFSS,Burke评分比较(分,
2.2 治疗前后两组患者营养指标比较
观察组患者治疗后营养指标Hb、ALB、TP水平均明显高于对照组,差异有统计学意义(P<0.05),见表2。
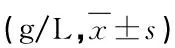
表2 治疗前后两组患者营养指标比较
2.3 两组患者治疗前后体格指标比较
两组患者治疗前上臂肌围、肱三头肌皮褶厚度以及体质量指数比较差异无统计学意义(P>0.05);治疗后,观察组上臂肌围、肱三头肌皮褶厚度以及体质量指数均明显高于对照组,差异有统计学意义(P<0.05),见表3。

表3 治疗前后两组患者体格指标比较
2.4 两组患者治疗后并发症发生率比较
观察组患者并发症发生率明显低于对照组,差异有统计学意义(P<0.05),见表4。

表4 两组患者治疗后并发症发生率比较 例(%)
3 讨 论
吞咽功能障碍是脑卒中患者最为常见的并发症,也是导致脑卒中患者并发肺部感染的独立危险因素之一,会导致抑郁症、脱水、营养不良发生,对患者生命安全和预后均有严重影响。目前对于脑卒中后吞咽障碍发生机制尚未完全明确,有报道指出[8],脑卒中后吞咽障碍是因为脑卒中患者因双侧皮质脑干束损害或者延髓麻痹所导致的假性延髓麻痹,从而对吞咽中枢造成损害,进而降低了与吞咽相关的肌肉运动协调性。既往临床对于脑卒中后吞咽功能障碍患者治疗方法较多,可通过康复治疗、替代进食、药物治疗等,但疗效不佳,一般通过常规肠内营养支持进行营养补给,患者营养摄入也不甚理想[9]。有报道表示[10],基于营养评估的吞咽功能训练对脑卒中后吞咽功能障碍患者临床疗效显著,可促进患者功能恢复,改善营养指标和预后。
吞咽功能训练是临床常用的吞咽功能障碍治疗方法,参照神经元再塑原理与神经促通技术,在患者发生吞咽功能障碍初期,通过对食管肌肉、咽、口部的被动与主动控制训练,以达到恢复肌肉协调性和灵活性的目的,从而提升构音和吞咽器官的血液循环,再与冷刺激相结合,以此提升中枢神经系统对患者吞咽功能的敏感性,强化吞咽反射[11]。但由于吞咽功能训练持续时间较长,在对患者吞咽功能障碍进行治疗期间,对进食有一定影响,且脑卒中后患者机体内蛋白质呈高分解代谢状态,机体容易处于应激状态,会增加能量消耗,导致营养不良[12]。有报道表明[13],脑卒中后吞咽功能障碍患者在住院1周后,约有一半发生营养不良,会促进感染等并发症的发生,延长康复时间。基于营养评估的吞咽功能训练是一种新型的治疗方式,通过吞咽功能训练与营养评估支持相结合,从而促进患者功能恢复,充分补充营养[14]。VFSS评分是临床评价吞咽功能常用的量表,Burke评分常用于吞咽障碍情况评价。本研究结果表明,观察组患者VFSS评分明显高于对照组,Burke评分明显低于对照组。证实基于营养评估的吞咽功能训练对脑卒中后吞咽功能障碍功能恢复效果显著,可提高患者吞咽能力。
营养不良是脑卒中后吞咽功能障碍患者常见的并发症之一,Hb、ALB、TP是临床评价营养状况较为常用的指标[15-17];观察组患者营养指标Hb、ALB、TP水平均明显高于对照组(P<0.05);观察组患者上臂肌围、肱三头肌皮褶厚度以及体质量指数均明显高于对照组(P<0.05);观察组患者并发症发生率显著少于对照组(P<0.05),提示基于营养评估的吞咽功能训练可提升脑卒中后吞咽功能障碍患者营养状况,改善体格指标,提升免疫力,促进恢复。压力性损伤、泌尿道感染、呼吸不畅等是脑卒中后吞咽功能障碍患者常见的并发症[18]。分析其原因,患者对鼻胃管接受程度不高,且当患者可自行进食时,吞咽功能未完全恢复,易出现呛咳等症状,患者进食较少,从而降低营养状况,促进营养不良的发生。而基于营养评估的吞咽功能训练是将营养评估支持和吞咽功能相结合,根据患者恢复情况给予不同稠度营养制剂进行进食,且每日进食经过热量计算,可完全达到机体营养需求,以此提升营养状况,改善体格指标[19-20]。
综上所述,基于营养评估的吞咽功能训练对脑卒中后吞咽功能障碍患者吞咽功能改善效果明显,可促进营养的吸收,改善营养状况,降低并发症发生率,安全可靠,值得临床推广应用。

