微波辅助无催化剂高效串联环化合成吡啶[2,3-d]嘧啶衍生物
林俊洁,王 爽,李伟强,崔 鑫,黄 超
(云南民族大学化学与环境学院,昆明650503)
吡啶[2,3-d]嘧啶类化合物是一种含氮杂环化合物(结构见图1),具有独特的结构和功能,在有机化学中占有非常重要的地位[1~4].吡啶[2,3-d]嘧啶衍生物具有抗菌[5,6]、抗癌[7,8]、抗炎[9]、抗糖尿病[10]和抗病毒[11]等生物活性,其合成备受关注.
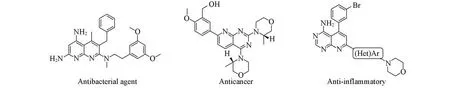
Fig.1 Structures of bioactive pyridine[2,3-d]pyrimidines
基于吡啶[2,3-d]嘧啶类化合物在生物活性和有机合成中的重要作用,其化合物骨架分子主要利用酸、碱或离子液体进行催化合成.Wawzonek[12]在酸或碱催化下通过缩合反应17 h制备了吡啶[2,3-d]嘧啶-2,4-二酮类化合物,化合物的收率低于20%;Zhang等[13]利用固体酸催化以2,6-二氨基嘧啶-4(3H)-1酮、硝基烯烃和醛为原料的多米诺环化反应8 h,合成了吡啶[2,3-d]嘧啶衍生物;Shi等[14]利用6-氨基嘧啶-2,4-二酮与α,β-不饱和酮化合物的离子液体反应5 h,合成了吡啶[2,3-d]嘧啶衍生物.这些方法存在反应时间长及后处理复杂等缺陷,限制了其进一步应用,因此在吡啶[2,3-d]嘧啶衍生物合成上仍存在优化提升空间.近年来,化学家们改进了吡啶[2,3-d]嘧啶类化合物的合成方法,主要是针对催化剂进行了优化,包括酸催化法、纳米材料法和电化学催化法等(Scheme 1)[15~20].但这些方法通常需要剧烈的反应条件,反应步骤多,条件复杂,反应时间较长,产率不高或难以工业化;在某些情况下,所使用的催化剂对环境有害,不能重复使用.因此,有必要继续探究新的合成吡啶[2,3-d]嘧啶衍生物的方法.
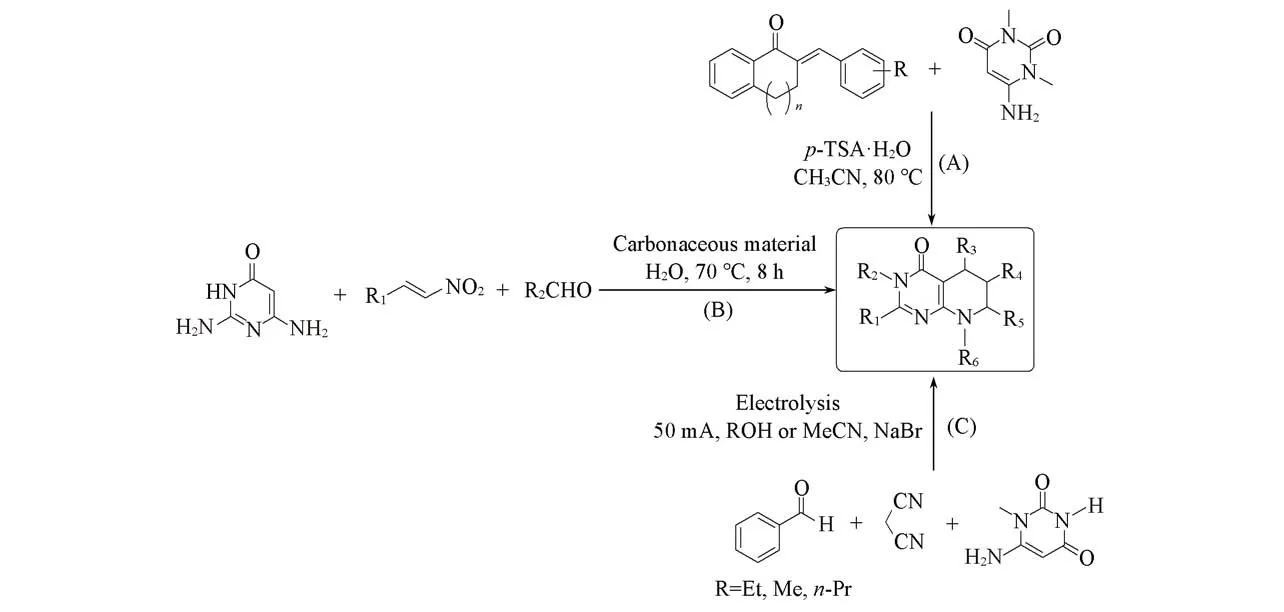
Scheme 1 Synthesis of pyridine[2,3-d]pyrimidinone compounds by acid catalysis(A),carbonaceous material(B)and electrochemical catalysis(C)
微波技术的引入为有机合成提供了一个高效且绿色的合成过程,与传统合成方法相比,微波技术具有操作简单、反应时间短、效率高及能耗低等优点,是绿色化学的一个重要组成部分[21~23].微波技术的应用为杂环化合物的合成开辟了新途径[24~26],为越来越多的化合物合成提供了更大的可能性,如缩短反应时间[27]及减少副产物的生成[28].通过高效、绿色且简便的合成方法制备具有分子多样性的吡啶[2,3-d]嘧啶衍生物,对于增加其生物活性多样性以及其它功能化应用具有意义.
本文在微波辐射合成多样性取代2-吡啶酮衍生物及吡咯衍生物研究的基础上[29~31],利用微波技术在反应时间及催化方式上进行优化,最终在微波辐射条件下,以α,β-不饱和酮类化合物和1,3-二甲基-6-氨基脲嘧啶为原料,无催化剂高效串联环化合成了含吡啶[2,3-d]嘧啶骨架分子的衍生物,经过简单的重结晶即可得到纯净化合物.该方法具有成键效率高、反应时间短、收率良好及后处理简单等特点.
1 实验部分
1.1 试剂与仪器
乙腈(纯度99%)、二甲基亚砜(DMSO,纯度99%)、乙醇(纯度99%)、丙酮(纯度99%)、异丙醇(i-PrOH,纯度99%)、甲苯(纯度99%)和N,N-二甲基甲酰胺(DMF,纯度99%)购自天津市致远化学试剂有限公司;碘(Iodine,纯度99%)、1,3-二甲基-6-氨基脲嘧啶(纯度99%)、苯乙酮类化合物(纯度99%)和苯甲醛类化合物(纯度99%)购自上海泰坦科技股份有限公司;所用试剂均为化学纯或分析纯;GF-254高效薄层色谱硅胶板(TLC)购自山东青岛海洋化工厂.
Discover(单模)型微波合成仪,美国CEM公司;Bruker AvanceⅢc-400 MHz核磁共振波谱(NMR)仪,德国Bruker公司,以CDCl3或DMSO-d6为溶剂进行测试,TMS为内标;X-5 LED型显微熔点测定仪(控温型),北京泰克仪器有限公司;Nicolet iS10型傅里叶变换红外光谱(FTIR)仪,KBr压片,美国Thermo Fisher Scientific公司.
1.2 实验过程
目标化合物的合成路线如Scheme 2所示.
参照文献[32]方法合成查尔酮类化合物以及α,β-不饱和酮类化合物.
将0.5 mmol查尔酮1a、0.5 mmol 1,3-二甲基-6-氨基脲嘧啶和1.5 mL二甲基亚砜依次加入10 mL干燥的微波反应试管中;置于微波合成仪中预搅拌30 s,于210℃搅拌反应10 min,用TLC监测至反应完成;加入5 mL乙醇,冷却至室温,待产物析出后,减压抽滤,用乙醇和乙腈各10 mL洗涤,重结晶后于40℃真空干燥12 h,得到吡啶[2,3-d]嘧啶类化合物3a.采用相同方法合成其它吡啶[2,3-d]嘧啶类化合物3b~3x.化合物3a~3x的理化数据和核磁共振波谱数据分别列于表1和表2.核磁共振波谱图见图S1~图S48(见本文支持信息).
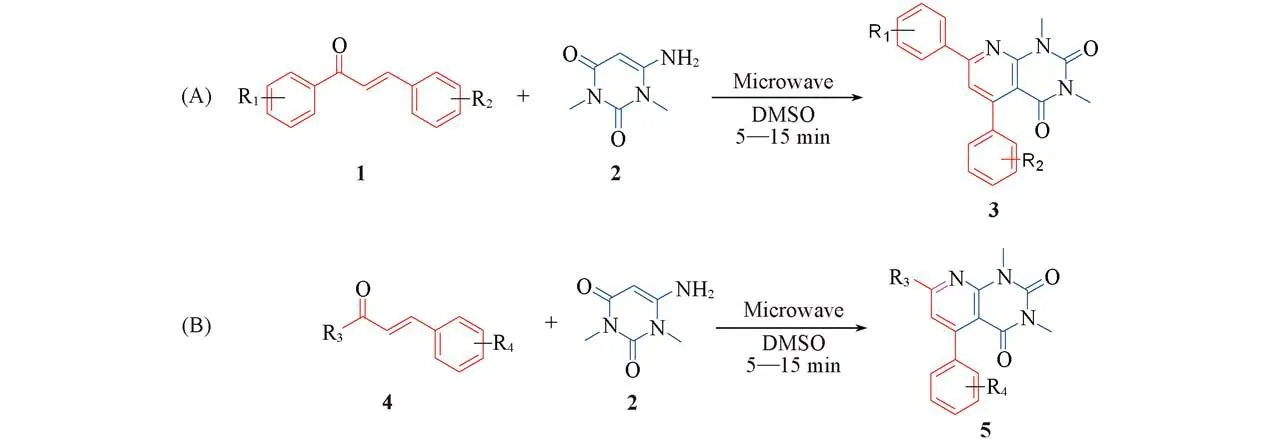
Scheme 2 Synthetic routes of target compounds 3(A)and 5(B)
将0.5 mmolα,β-不饱和酮4a、0.5 mmol 1,3-二甲基-6-氨基脲嘧啶和1.5 mL二甲基亚砜依次加入10 mL干燥的微波反应试管中;置于微波合成仪中预搅拌30 s,于210℃搅拌反应5 min,用TLC监测至反应完成;加入5 mL乙醇,冷却至室温,待产物析出后,减压抽滤,用乙醇和乙腈各10 mL洗涤,重结晶后于40℃真空干燥12 h,得到吡啶[2,3-d]嘧啶类化合物5a.采用相同方法合成其它吡啶[2,3-d]嘧啶类化合物5b~5d.化合物5a~5d的理化数据和核磁共振波谱数据分别列于表1和表2.核磁共振谱图见图S49~图S56(见本文支持信息).

Table 2 1H NMR and 13C NMR data for compounds 3a—3x and 5a—5d*
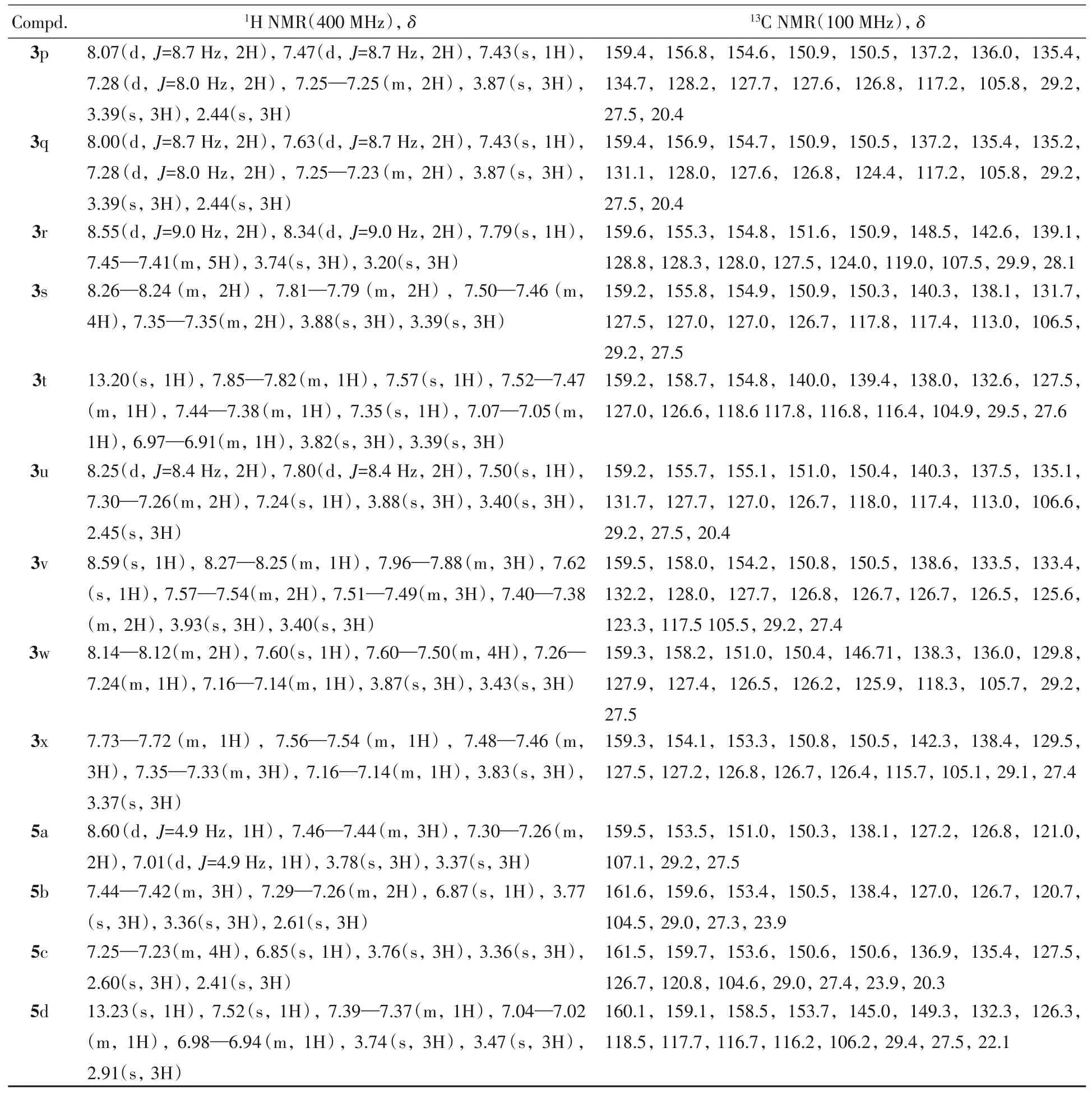
Continued
2 结果与讨论
2.1 合成吡啶[2,3-d]嘧啶反应的条件优化
以查尔酮(1a)和1,3-二甲基-6-氨基脲嘧啶(2)为模型反应底物,考察了催化剂、溶剂和温度等因素对产率的影响,反应条件优化结果见表3.
首先,以碘为催化剂,乙腈为溶剂,分别在无微波辐射和微波辐射条件下对模型反应进行了探索(表3中Entries 1~4).在相同的反应温度下,反应时间从8 h缩短到1.5 h,表明微波辐射可以促进该反应的进行.在微波辐射下,随着反应温度的升高,反应时间缩短至1 h,化合物3a的收率从80%增加到85%(表3中Entries 4~6),表明温度对反应有较大影响.随后,考察了无催化剂条件下的反应情况,保持反应温度为130℃,延长反应时间,发现化合物3a的收率并未显著提高(表3中Entries 7~9).实验中根据该反应情况尝试更换溶剂,以寻找合适的反应溶剂.在相同的反应温度及时间条件下,分别使用乙腈、乙醇、异丙醇、甲苯、N,N-二甲基甲酰胺和二甲基亚砜等作溶剂,在微波辐射条件下研究了合成目标化合物3a的反应情况(表3中Entries 7和10~14),发现化合物3a的收率从30%增加至71%,因此确定最佳反应溶剂为二甲基亚砜.对反应温度进行了探索,在相同反应时间下,以二甲基亚砜为溶剂,反应温度从180℃升高到210℃,目标化合物3a的收率从77%增加至82%(表3中Entries 15~18),说明温度对该反应有较大影响,因此确定最佳反应温度为210℃.对反应时间进行了筛选(表3中Entries 18~20),通过对比发现最佳反应时间为10 min.此外,将该反应置于无微波辐射189℃条件下反应10 min,仅以36%的收率得到化合物3a(表3中Entry 21),表明除了温度对该反应具有较大影响外,微波辐射对该反应也具有重要的促进作用.通过对模型反应各种影响因素的优化和筛选,确定了如下的反应最佳条件:以1.5 mL二甲基亚砜为溶剂,在反应温度为210℃,微波功率为48 W及无催化剂存在条件下,用0.5 mmol化合物1a与0.5 mmol化合物2反应10 min,以88%的收率得到目标化合物3a(表3中Entry 20).
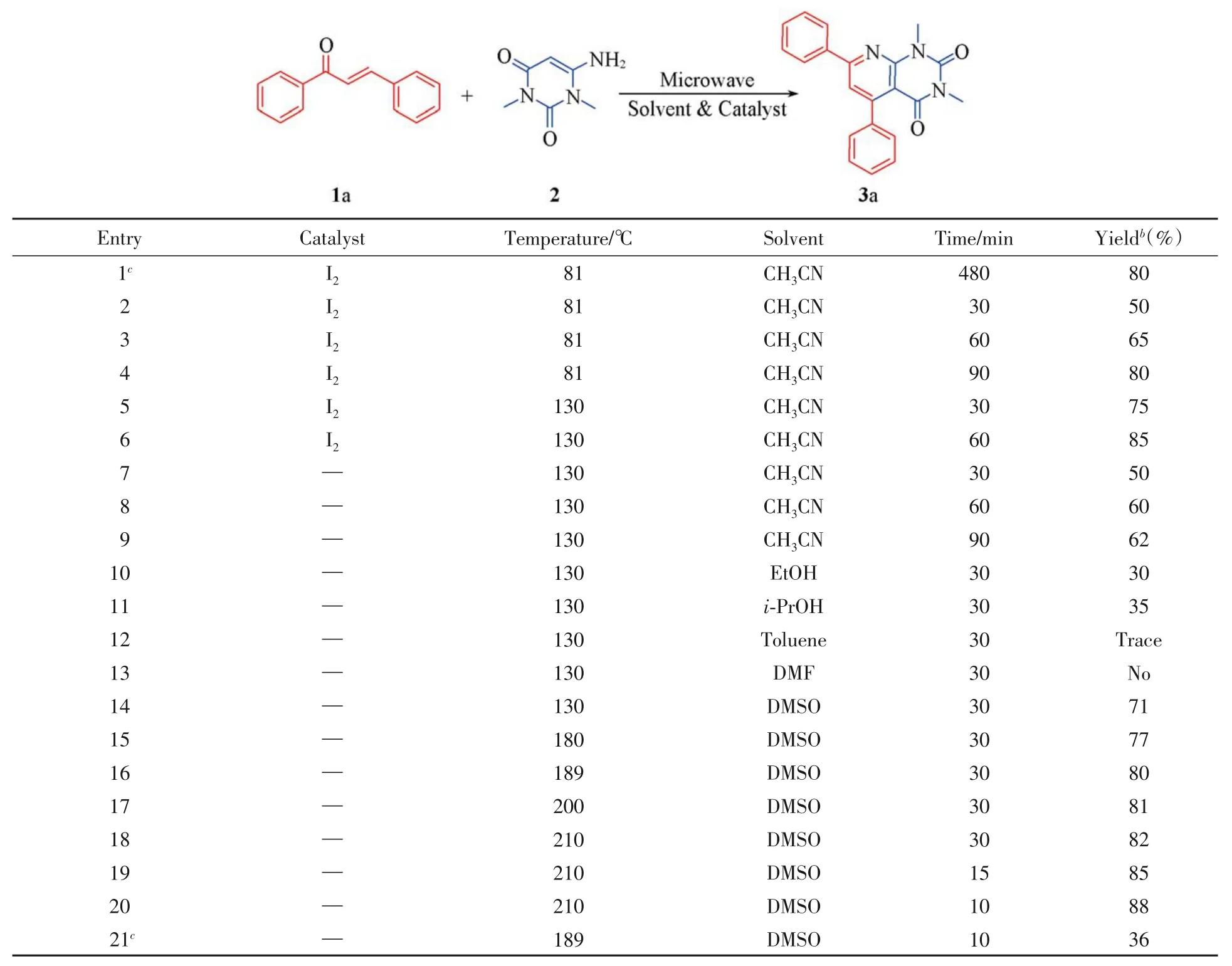
Table 3 Optimization of the reaction conditionsa
2.2 吡啶[2,3-d]嘧啶衍生物的合成
在最佳反应条件下,对反应底物的适用范围进行了研究(表4),在模型反应中,以88%的良好收率得到吡啶[2,3-d]嘧啶化合物3a.利用此方法对不同取代基的α,β-不饱和酮类化合物进行了底物扩展.结果显示,以含有供电子取代基的查尔酮为底物能够得到理想的产物3b~3k,产率最低可达78%;以卤素取代的查尔酮为底物得到吡啶[2,3-d]嘧啶化合物3l~3q,产率最低可达81%;以含有吸电子取代基的查尔酮为底物也能以良好的产率得到了理想的产物3r~3u,说明空间位阻对反应无太大影响.用稠杂环查尔酮与1,3-二甲基-6-氨基脲嘧啶反应以中等至良好的产率得到产物3v~3x,证明该反应具有良好的普适性.所有化合物均不需要经过柱层析,只需经过简单的过滤、洗涤和重结晶即可得到纯净化合物.
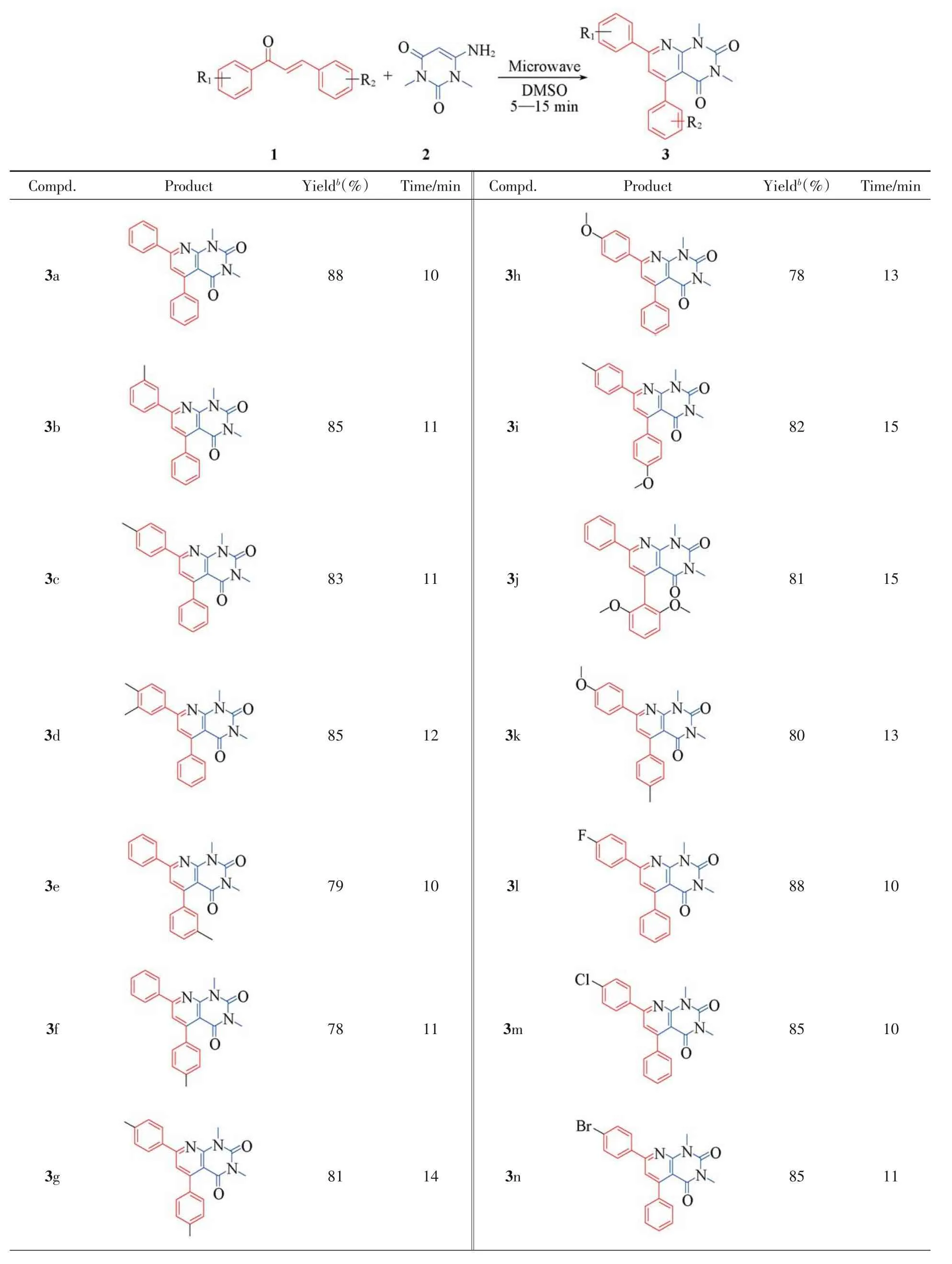
Table 4 Synthesis of pyridine[2,3-d]pyrimidinone derivatives from chalconesa
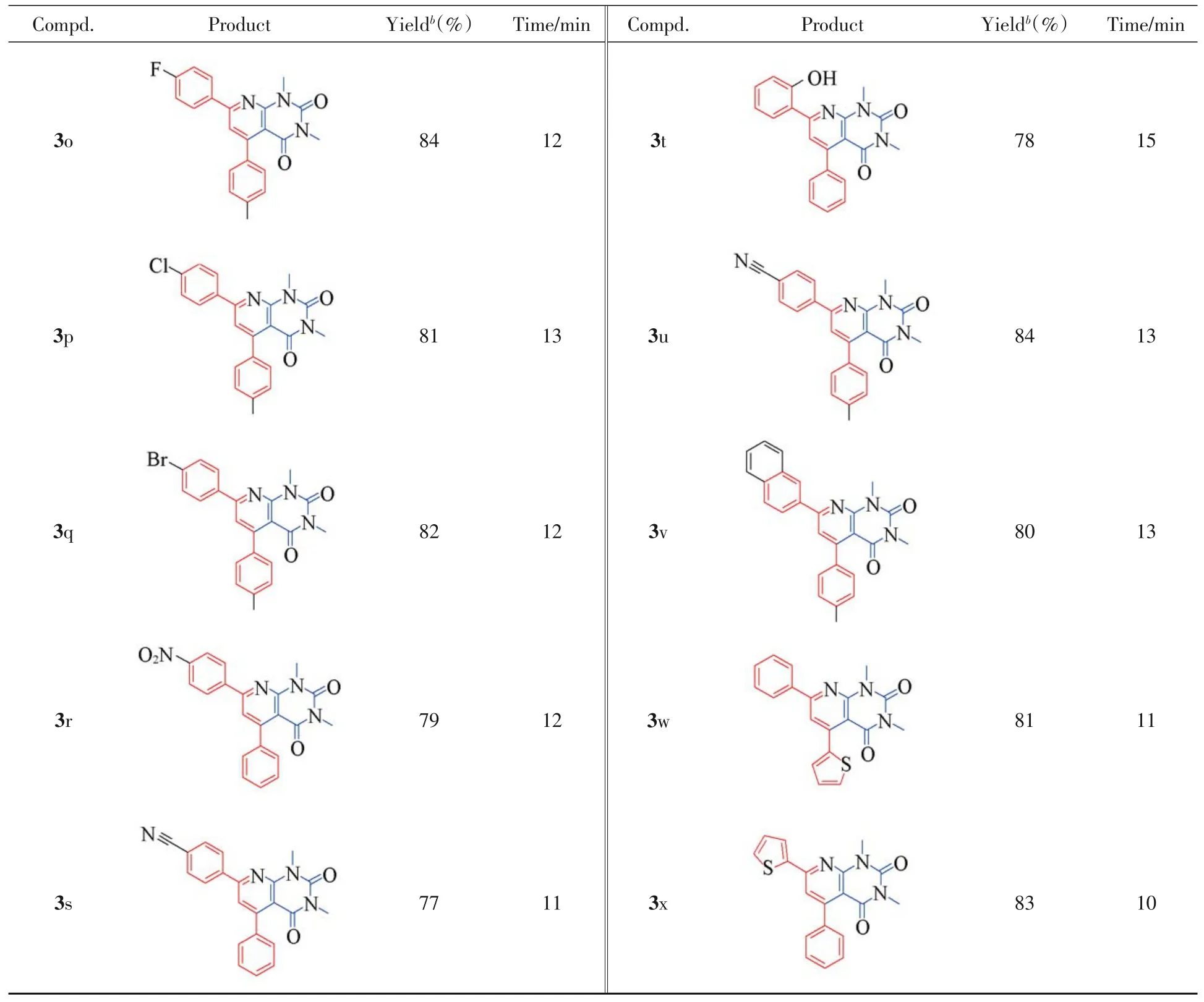
Continued
为了进一步扩大底物的普适性,将底物1简化为底物4,发现产率并未明显降低,以最低70%的产率得到化合物5a~5d(表5),证明该反应具有良好的普适性,并增加了分子多样性.
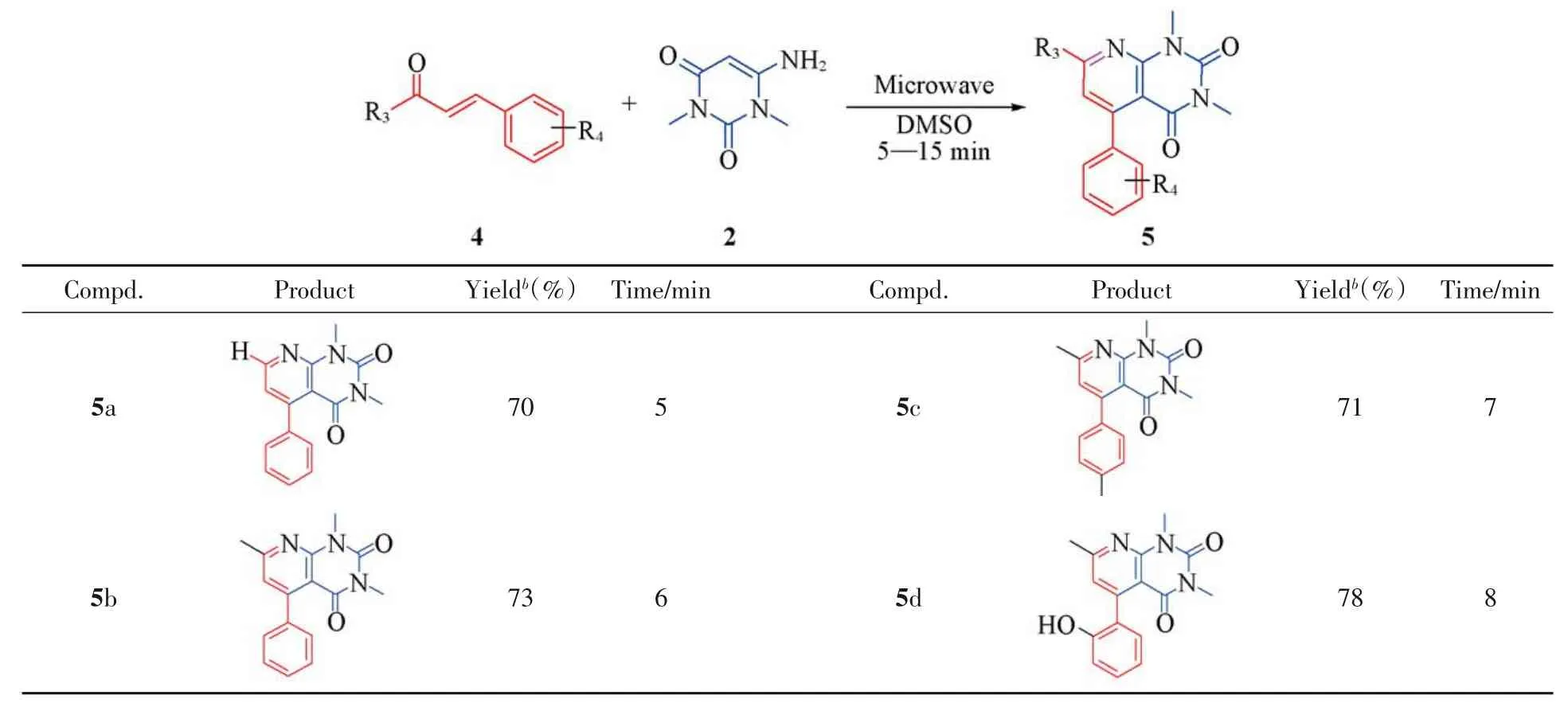
Table 5 Synthesis of pyridine[2,3-d]pyrimidinone derivatives fromα,β-unsaturated ketonesa
2.3 反应机理探讨
基于上述结果和文献[12,34]报道,提出了该反应的反应机理(Scheme 3).首先,查尔酮(1a)与1,3-二甲基-6-氨基脲嘧啶(2)发生Michael加成反应;通过互变异构将含有亚胺结构的中间体A转变为含有烯胺结构中间体B;氨基与羰基发生加成反应成环得到中间体C;再经脱水和芳构化得到1,3-二甲基-5,7-二苯基吡啶[2,3-d]嘧啶-2,4(1H,3H)-二酮(3a).
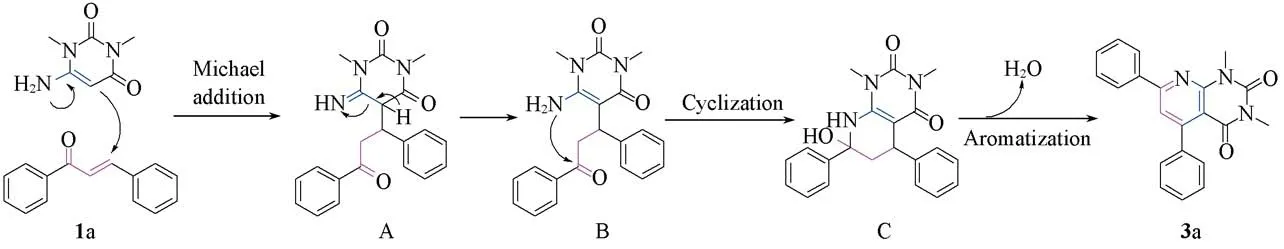
Scheme 3 Possible mechanism of pyridine[2,3-d]pyrimidine synthesis
3 结 论
以α,β-不饱和酮类化合物和1,3-二甲基-6-氨基脲嘧啶为原料,在微波辐射及无催化剂条件下,经高效串联环化反应5~15 min合成了28个具有分子多样性的吡啶[2,3-d]嘧啶系列化合物,其中有21个未见文献报道.该方法具有成键效率高、反应时间短、操作简单及收率良好等特点,通过简单的抽滤、洗涤和重结晶即可得到纯净的化合物.该方法利用微波辅助合成,具有高效、绿色及操作简便等优点,拓展了微波技术在有机合成中的应用.该方法为更多化合物的合成提供了方法参考,特别是为吡啶[2,3-d]嘧啶类衍生物的工业化生产提供了借鉴意义.鉴于吡啶[2,3-d]嘧啶类衍生物具有的生物活性,该方法可为寻找新的活性化合物提供参考.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200563.

