TiO2 /Ni-Fe水滑石复合光电极的制备及催化性能
陈代梅,伍承林,李金洪,梁 勇,王 杰
(中国地质大学(北京)a.材料科学与工程学院;b.实验室与设备管理处;c.财经处,北京 100083)
0 引言
随着世界人口的快速增长和工业的迅速发展,环境问题尤其是水污染问题逐渐成为当今世界所面临的一大难题[1-2]。光催化技术被认为是最具有发展潜力解决环境污染问题的绿色新技术。光催化技术就是利用太阳能,催化剂在光激发下产生电子和空穴对,化学反应产生的强氧化性活性物种具有极强氧化性,可以把有机污染物完全降解为二氧化碳和水[3-4]。但光催化技术存在电子-空穴分离效率低、催化剂难以和溶液分离等问题限制了其实际应用。研究人员又将催化剂材料负载在一定的导电基体上,同时利用外加电压辅助电子-空穴的分离传输并抑制其复合,形成一种新的催化技术——在电化学辅助下的光电协同催化技术(光电催化)。
光电催化技术是在光催化反应系统中引入了外加偏压形成的内置电场,可以加速电子-空穴的分离,电子会从半导体的导带迁移到外电路,同时,空穴会在催化剂表面积累,参与氧化降解有机污染物反应或者参与水氧化产氧的反应[5-7]。常用的半导体光电极材料主要有TiO2、ZnO、WO3、Fe3O4、CdS或ZnS等氧化物和硫化物半导体[8-12]。其中TiO2光电极因其无毒无害、化学性质稳定、成本低、催化活性高、氧化能力强等优点[13-14],在光电催化技术中得到了广泛的应用。与一般的TiO2粉体相比,纳米管状的TiO2因其具有更大的比表面积和更强的吸附能力,表现出更高的光催化活性和光电转换效率,能极大地改善TiO2的光电催化性能。但是,TiO2禁带宽度较宽,只能被紫外光激发,且光生电子空穴复合率高,使得其光电催化活性不高。因此,采用半导体复合法对TiO2光电极进行改性修饰,以提高其可将光利用率,降低电子-空穴复合率等。
水滑石类层状化合物(LDHs)是一类具有广阔应用前景的阴离子型层状化合物,层间具有可交换的阴离子。水滑石由于其具有可调变的组成和离子交换等优异的性能,尤其是含有Fe,Ni,Co 等金属离子的水滑石,用来复合光阳极半导体材料,可以提高材料的光电氧化活性[15]。基于此,本实验采用水热合成结合电沉积方法制得TiO2/Ni-F 水滑石(TiO2/NiFe-LDH)复合光电极材料。实验表明,TiO2/NiFe-LDH 复合光电极的光电催化降解活性远高于单一TiO2光电极材料,这是由于NiFe-LDH 纳米片较高的可见光吸收能力,可以提高TiO2光电极的可见光吸收范围,同时NiFe-LDH纳米片作为助催化剂可以提高光生电子的空穴分离效率,大大提高了TiO2光电催化活性。
1 实验试剂与仪器
试剂:钛酸丁酯、浓盐酸、六水合硝酸镍、七水合硫酸亚铁、无水乙醇(均为分析纯且无提纯处理,购于国药集团试剂有限公司)。实验用水为自制二次去离子水。
设备:电子天平(BSA124S,赛多利斯仪器系统有限公司);多头磁力搅拌器(HJ-6A,江苏科析仪器有限公司);紫外可见分光光度计(U-3900,日立(中国)有限公司);电化学工作站(CHI760E,上海辰华仪器有限公司);场发射扫描电子显微镜(ZEISS-SUPRASS,卡尔蔡司有限公司)。
2 实验方法
2.1 样品制备
(1)氟掺杂锡氧化物(FTO)玻璃预处理。首先将玻璃片置于丙酮中超声清洗30 min,取出后用去离子水反复冲洗,再置于无水乙醇中超声清洗30 min,取出后用去离子水反复冲洗,最后再用去离子水超声清洗30 min,放入100 ℃烘箱中烘2 h,冷却至室温后取出,用保鲜膜密封于玻璃培养皿中备用。
(2)TiO2纳米棒阵列的制备。量取一定量(12~15 mL)的去离子水与一定量(12~15 mL)的浓盐酸(质量分数37%)于100 mL 小烧杯中,混合搅拌10 min;然后在连续搅拌下逐滴加入0.35~0.50 mL钛酸四丁酯。随后用保鲜膜密封住烧杯,继续搅拌混合液直到溶液变清澈透明。将所得到的溶液转移至100 mL规格的聚四氟乙烯反应釜内衬中,将清洁好的FTO玻璃以导电侧面朝上的方式与反应釜内衬壁成一定角度放置。将反应釜拧紧后放入烘箱中,150 ℃下恒温15 h。冷却至室温后,取出FTO玻璃用去离子水反复冲洗,在60 ℃烘箱中干燥2 h。由此得到生长在FTO玻璃表面呈白色膜状的TiO2纳米棒阵列。
(3)TiO2/Ni-Fe 水滑石(TiO2/NiFe-LDH)复合光电极的制备。实验采用电沉积方法在TiO2/FTO 上负载NiFe-LDH。将0.015 mol 的Ni(NO3)2·6H2O 和0.015 mol的FeSO4·6H2O 溶于100 mL 的去离子水中,搅拌30 min配成电解质溶液。以生长有TiO2纳米棒阵列的FTO 玻璃为工作电极,铂丝作对电极,饱和甘汞电极(SCE)作参比电极,在电化学工作站上电沉积Ni-Fe水滑石。沉积电压为-1.0 V vs.SCE。电沉积时间分别为30、60 和100 s。电沉积完成后将FTO玻璃取出并用去离子水冲洗,然后置于空气中以使Fe2+自氧化为Fe3+。最后得到TiO2/NiFe-LDH 复合光电极。
2.2 样品表征
以X射线衍射(XRD,D8-Advance,德国布鲁克公司)表征复合光电极的晶体结构;场发射扫描电子显微镜(FESEM,ZEISS-SUPRASS55,蔡司公司)表征复合光电极材料形貌。以紫外-可见漫反射光谱(UV-vis DRS,U-3900,日本电子)来表征材料的光吸收。
2.3 光电性能测试
采用上海辰华仪器有限公司的CHI760e 型电化学工作站测量光电极的光电流、电化学阻抗谱等光电化学性能。采用三电极体系,样品电极为工作电极,饱和甘汞电极为参比电极,铂电极为对电极;测量介质为0.1 mol/L 的Na2SO4溶液,照射光源为100 W 的氙灯。将生长有样品的FTO 玻璃用黑色胶带遮住一部分,留出2 cm×2 cm的有效面积,放入石英池中,调整石英池的高度与光源的高度一致,FTO 玻璃片与光源的距离为8 cm。分别采用线性扫描伏安法和计时光照法测量光电极的光电流,其中线性扫描的速率为10 mV/s,扫描范围为-1.0~1.0 V;计时间隔为30 s,总测量时长为300 s。无光照条件下,在-1.0~0.2 V范围内以1 kHz 的频率测量光电极的莫特-肖特基曲线。光照条件下,在-0.4 V 下0.01 Hz~100 kHz范围内测量电化学阻抗谱(EIS)。
2.4 光电催化性能测试
以亚甲基蓝以及甲基橙(MO)降解为模型体系,评价所制备出的光电极在可见光下的光电催化降解性能。降解实验仍然在CHI760e 型电化学工作站上进行。底物浓度均为10 ×10-6,300 W 氙灯光源。具体操作是:将100 mL的待降解溶液倒入石英池中,放入对电极和参比电极,将生长有样品的FTO玻璃用黑色胶带遮住一部分,留出2 cm ×2 cm 的有效面积,放入石英池中。FTO 玻璃片与光源的距离为10 cm,向待降解物溶液中放入磁子搅拌,搅拌达吸附平衡。每隔一段时间(30 min)取样3 mL待降解溶液,用紫外可见分光光度计测定其在最大吸收波长光照下的吸光度变化,计算降解效率。其中:C为待降解物经过一定时间的光电催化降解后的浓度;C0为待降解物在暗反应一段时间后达到吸附-脱附平衡后的浓度;C/C0表示光电催化降解的效率。
3 结果与讨论
3.1 结构和形貌表征
由图1 可见,3 种光电极在27.6°、33.7°、52.1°、62.8°及66.2°处都出现明显衍射峰,这是FTO玻璃片的特征峰。TiO2光电极的XRD 图中,27.6°、36.1°、54.5°、62.8°、64.1°、68.5°和70.1°处出现明显的特征峰,根据标准卡片JCPDS No.88-1172,这些特征峰分别对应于金红石相TiO2的(110)、(101)、(211)、(002)、(310)、(301)和(112)晶面,说明水热合成的TiO2纳米棒阵列为金红石相。NiFe-LDH的XRD谱图中只出现了FTO玻璃片的特征峰,没有发现水滑石的衍射峰,这可能是电沉积制备水滑石的结晶度很差。TiO2/NiFe-LDH的XRD图谱和TiO2光电极的XRD图完全一致,只观察到金红石相TiO2和FTO 的特征峰,观察不到水滑石的特征峰。
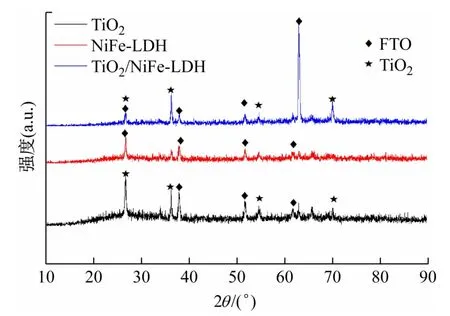
图1 TiO2、NiFe-LDH、TiO2/NiFe-LDH光电极的XRD图
图2 是水热合成TiO2纳米棒阵列和不同电沉积时间的TiO2/NiFe-LDH 复合光电极的SEM 图。由图可以看到,TiO2的微观形貌为纳米棒阵列,均匀分布在FTO表面。纳米棒顶端呈规整的四方形。图2(b)~(d)分别为水滑石电沉积时间为30、60 和100 s 的复合光电极的形貌图。当电沉积时间30 s时,TiO2纳米棒阵列表面只沉积了少量NiFe水滑石纳米片,尺寸约为1 μm;随着沉积时间增加60 s和100 s,TiO2纳米棒阵列表面负载NiFe水滑石的量增加,尺寸也逐渐增大为2 μm左右。对于电沉积100 s的样品,由于表面沉积了过多的镍铁水滑石,水滑石纳米片之间相互团聚在一起,完全盖住了二氧化钛纳米棒。从电镜图可以预测一定量镍铁水滑石的负载,其层状结构有利于光生空穴的传出,可以促进光生电荷分离,提高光电活性;但过多的水滑石纳米片团聚,完全覆盖二氧化钛纳米棒阵列,可能会堵住了光生电荷和空穴分离的通道,不利于光电催化活性的提高,这一点在后面的光电催化降解实验得到证实。

图2 复合光电极的SEM图
3.2 光吸收性能
由图3 可见,TiO2纳米棒阵列在紫外光区域表现出很强的吸收,其吸收边在410 nm 处,但是对可见光基本没有吸收。而镍铁水滑石在400~800 nm的可见光区域有较强的吸收。当两者形成复合物后,由于镍铁水滑石的可见光吸收较高,导致复合电极在可见光区域的吸收有一定增加。这就大大增加了复合光电极的可见光吸收范围,从而最终提高可见光的光电催化活性。

图3 TiO2、NiFe-LDH、TiO2/NiFe-LDH的紫外可见漫反射光谱
3.3 光电化学性能测试
3.3.1 光电流
光电流密度是衡量光电极性能的重要参数之一,它反映了在一定强度光照下,迁移出光电极表面的电子密度。本文利用CHI760e 型电化学工作站对TiO2、NiFe-LDH、TiO2/NiFe-LDH 3 种光电极的光电流进行了测量。在将生长有样品的FTO 玻璃用黑色胶带遮住一部分,留出2 cm ×2 cm 的有效面积,放入石英池中,调整石英池的高度与光源的高度一致,FTO玻璃片与光源的距离为8 cm,施加的电压为0.6 V。测量结果如图4 所示。NiFe-LDH光电极的光电流密度最低,仅有0.2 mA/cm2;从紫外可见漫反射光谱可知,虽然NiFe-LDH能实现较广范围内的光吸收,但较好的光吸收并不意味着较大的光电流密度。说明NiFe-LDH 的光生电荷的复合率很高,这是导致其光电活性低的直接原因。TiO2/NiFe-LDH复合光电极具有最高的光电流密度(1.56 mA/cm2),是TiO2光电极的1.7 倍,NiFe-LDH 的7.8 倍。这归功于两者复合后,NiFe-LDH层状结构可促进TiO2光生空穴的导出,提高TiO2电子-空穴的分离效率。

图4 TiO2、NiFe-LDH、TiO2/NiFe-LDH的光电流曲线
3.3.2 电化学阻抗谱
在电化学阻抗谱图(EIS)中,弯曲曲线的半径越小说明样品的电化学阻抗越小,即表明光生电子在转移过程中受到的阻力越小,电荷传导效率越好。由图5 可见,TiO2/NiFe-LDH 复合光电极具有最小的曲线半径,其次依次是TiO2和NiFe-LDH,这个结果和光电流的结果一致的。

图5 TiO2、NiFe-LDH、TiO2/NiFe-LDH的电化学阻抗谱图
3.4 光电催化活性测试
采用亚甲基蓝和甲基橙两种染料为模型体型,考察TiO2、NiFe-LDH、TiO2/NiFe-LDH 3 种光电极的光电催化活性。图6(a)给出了3 种光电极的光电催化降解亚甲基蓝的降解率。NiFe-LDH 光电极的降解效果最差,3 h 对亚甲基蓝的降解效率不足20%,而TiO2纳米棒阵列光电极3 h 的降解率能达到70%,TiO2/NiFe-LDH复合光电极的光电催化活性最好,降解率可以达到95%。在相同实验条件下,对3 种光电极进行了光电催化降解甲基橙的实验比较,结果如图6(b)所示。NiFe-LDH光电极对甲基橙几乎没有降解效果;TiO2光电极有一定降解效果,3 h 内降解了65%的甲基橙;而TiO2/NiFe-LDH复合光电极的降解效果最好,3 h内能降解率可以达到92%。光电催化降解实验说明形成的复合光电极光电降解活性优于单一的TiO2纳米棒阵列光电极和NiFe-LDH光电极。
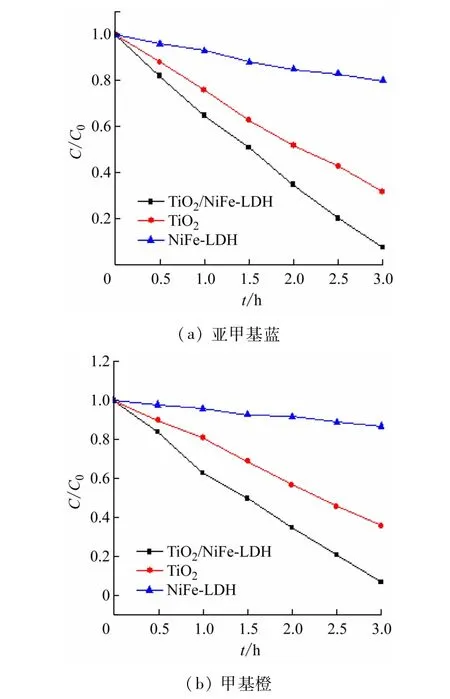
图6 TiO2、NiFe-LDH、TiO2/NiFe-LDH的光电催化降解曲线
图7 为不同水滑石电沉积时间得到的TiO2/NiFe-LDH复合电极的光电催化降解曲线。电沉积时间30 s的复合电极的亚甲基蓝的降解率是69%。当电沉积时间增加到60 s,复合电极样品的降解率提高95%。然而,继续增加电沉积时间到100 s,得到的复合电极光电催化反而有所降低。这是由于过长时间的电沉积会导致镍铁水滑石纳米片在TiO2纳米棒负载量过大,水滑石团聚。由于水滑石完全覆盖住了TiO2纳米棒阵列,不仅影响了TiO2对光照的吸收,且不利于TiO2光生载流子迁移到电极表面,导致光生电子-空穴的复合率增加,最终使得光电催化降解效率反而变差。

图7 不同水滑石电沉积时间下TiO2/NiFe-LDH的亚甲基蓝降解曲线
3.5 复合光电极活性提高的机理探讨
具体的光电催化机理如图8 所示。TiO2和NiFe-LDH两种半导体可以吸收光能量,产生光生电子-空穴对。负载在TiO2纳米棒阵列的NiFe-LDH纳米片作为助催化剂可以促进TiO2的光生空穴出,迁移到催化剂表面,和表面吸附的反应物发生氧化反应,最终生成CO2和H2O。或是和表面吸附的水生成羟基自由基(·OH),·OH 具有极强的氧化活性,可以彻底降解水中的有机污染物。另一方面,NiFe-LDH纳米片产生的光生电子跃迁到的TiO2导带位置上,施加的外加偏压形成了内建电场给电子一个驱动力,使电子经FTO玻璃转移到Pt 电极上,进一步加速电子-空穴分离和传输。Pt电极上面蓄积的大量光生电子和表面吸附氧分子反应产生超氧自由基(·O-2)活性物种,也可以降解有机污染物。因此,可以看出复合光电极活性提高的原因是NiFe-LDH纳米片较高的可见光吸收能力,可以提高TiO2光电极的可见光范围,同时NiFe-LDH纳米片作为助催化剂可以提高光生电子的空穴分离效率,从而大大提高了TiO2光电催化活性。

图8 TiO2/NiFe-LDH复合光电极的光电降解机理
4 教学要求
4.1 实验目的
本文立足于本科生综合性实验的教学中,该实验项目设定是围绕着科研中研究热点问题,光电催化在环境污染的应用。该实验项目具有一定的理论深度,又有一定的实际应用价值。通过完成该综合性实验,既可以锻炼学生的动手能力,又可以进一步拓展学生的实验思维和科研兴趣,具体实验目的如下:
(1)让学生深入了解光电催化的基本理论。掌握光电极的制备方法。
(2)了解半导体的一些基础概念如半导体的能带特性、光吸收特性及其发生氧化还原反应的反应过程。
(3)学习纳米半导体材料的表征方法,掌握材料光电化学性质的测试手段和分析方法。
(4)学习和掌握半导体光电极材料的光电催化活性的实验评价方法,并可以简单分析其中的机理过程。
4.2 思考和讨论
(1)纳米光电极材料的表征方法还有哪些?
(2)电极材料的制备手段有哪些?光电材料的电化学测试手段有哪些?
(3)光电催化降解污染物的机理和途径有哪些?
(4)半导体材料的禁带宽度和光吸收的关系?光吸收,电子空穴分离效率和光电催化活性之间的关系?
5 结论
本文通过水热合成法结合电化学沉积制备了TiO2纳米棒阵列、NiFe-LDH、TiO2/NiFe-LDH3 种光电极材料。通过XRD、SEM 和UV-vis DRS 对光电极材料的晶体结构,形貌和光吸收进行表征,采用电化学手段测试了光电极材料的光电流和交流阻抗数据。采用亚甲基蓝和甲基橙为有机污染的模型体系,考察了3种光电极材料的光电降解活性。实验发现,TiO2/NiFe-LDH复合光电极具有比单一TiO2纳米棒阵列和NiFe-LDH更高的光电降解活性。活性提高的原因是NiFe-LDH纳米片较高的可见光吸收能力,可以提高TiO2光电极的可见光范围,同时NiFe-LDH 纳米片作为助催化剂可以提高光生电子的空穴分离效率,最终提高光电催化活性。
本实验是一个综合实验设计项目,融合了化学、材料、环境、电化学、光电化学的相关理论知识。实验设定围绕目前研究的科研热点和社会实际问题。要求学生在查阅大量文献的基础上,运用各个学科所学理论知识,应用在实践环节。实验包括材料制备、表征和材料性能评价,大型设备的操作和分析等方面的知识点。通过该综合实验,提高了学生的动手能力和解决问题能力,同时也激发了学生的科研热情,培养学生的科学研究素养。

