CRRT联合超声引导下PTGD在治疗重症急性胆源性胰腺炎中的临床评价
张 潇
(绵阳市中心医院 四川 绵阳 621000)
重症急性胰腺炎(SAP)在临床上发作率与病死率极高。在目前的国内临床进展中,大多数的胆源性胰腺炎均为急性胰腺炎。目前,对于此类疾病的诊治方法是通过内镜鼻胆管引流术(ERCP)与胰胆管括约肌切开术联合应用治疗此项疾病[1]。重症急性胰腺炎患者发病时常伴随休克、ARDS以及术后麻醉风险等不良症状。为了找出一项对患者伤害小、操作便捷以及经济适用的治疗方法,从解除胆道梗阻、充分引流胆汁的方向出发,目的是胆道减压,对此类疾病的救治十分重要。在临床上应用肝胆囊穿刺置管引流手术(PTGD)对重症胆源性胰腺炎及逆行治疗能够更好的清除炎性介质,保护脏器器官功能不受损,超声下经皮经肝胆穿刺支管引流手术完成对胆道的检验,可缓解患者的临床症状,改善临床病症带来的影响,其主要内容为。
1 资料与方法
1.1 一般资料
遴选我院2019年6月—2020年5月重症医学科收容的66例重症急性胆源性胰腺炎患者,采用红蓝球法无差异的将其分为常规组(CRRT治疗,33例)与观察组(CRRT+PTGD治疗,33例),以上患者接受临床诊断与观察后均符合重症急性胆源性胰腺炎的标准。其中男性约为39例,女性27例;Oddi括约肌狭窄8例(12.12%),胆石症55例(83.33%);人群年龄均在22到80岁,年龄均数(47.97±8.97)岁,对比以上患者年龄、性别以及并发症等状况,差异较低(P>0.05),符合统计学描述。
1.2 研究方法
1.2.1 治疗方法 以上患者均在遵从医嘱的情况下禁饮禁食、纠正吸氧、胃肠道减压、提供营养以及舒缓疼痛,改善身体内的酸碱平衡,减低胃酸的分泌,削减胰腺分泌。在患病初期可通过适当的光谱抗生素对其进行抗感染治疗;积极对并发症予以救治,发生休克后要及时抢救,迅速通过抗休克治疗改善患者临床症状,而心衰患者则可进行强心治疗治愈心衰的发生。ARDS患者可通过机械通气维持患者的临床症状平稳[2]。常规组确诊后即开始CRRT治疗,而观察组可在常规组治疗方式的基础上开展经皮经肝胆微创胆囊穿刺置管引流手术。
1.2.2 CRRT治疗 通过连续静脉-静脉的输液滤过模式(CVVH),利用Seldinger技术穿刺股静脉与右侧颈内静脉后置针双腔导管形成临时血管通道。血滤机(参数:表面积1.8~2.1m²,滤器:HFl200,每4~12h更换)通过前稀释将血液输入,保持24h不断流,血流量可维持在200~300mL/min,与患者的实际情况结合后可对电解质成分和酸碱平衡进行纠正。超滤量可参考全天的补液量与生理基本需要。注入普通肝素使其泵入完成血液抗凝,而胰岛素则可通过持续泵入控制血液中的血糖值,根据APTT、血糖检测值等对肝素和胰岛素的泵入量进行调节。根据患者的实际病情状况适当停止CRRT。
1.2.3 PTGD微创穿刺置管 利用彩色多普勒超声诊断仪以PTGD对患者行超声检查,充分了解胆囊大小、分布状况以及周围组织器官形态。指导患者采取仰卧位,于右侧腋前线或者腋中线第8、9肋间为本次穿刺的穿刺点,予以常规消毒与铺巾,抽取2%利多卡因对穿刺区域进行局部麻醉,CDFI经引导后与肝脏中较大的血管、肾脏等避过,于超声引导采用穿刺针经皮经肝胆在胆囊床位点刺入胆囊,见胆汁后,植入导丝,拔针后完成穿刺,皮肤扩张后沿导丝置入引流导管,将导丝拔除固定导管,接入引流袋,取胆汁液于细菌学培养,采用生理盐水将其冲洗,便于引流。非胆囊炎患者,等到临床症状完全消失后,在超声提示下胆囊的形态变化与大小均恢复正常,窦道形成后将导管夹闭2d,若患者无禁忌症则可将引流管拔出[3]。
1.3 观察指标
对患者心跳、心率、呼吸、血压等临床指征(腹痛缓解时长、腹胀减弱时长、ICU住院时长以及机械通气治疗时长)进行测量,对患者病死率进行计算。
1.4 统计学分析
数据采用SPSS19.0统计学软件分析处理,计数资料采用率(%)表示,行χ2检验,计量资料用均数±标准差()表示,行t检验,P<0.05为差异有统计学意义。
2 结果
2组患者入院后的未治疗期间,临床指标的比较差异性较低(P>0.05),无统计学意义。较常规组而言,观察组患者的腹痛缓解时长、腹胀减弱时长、ICU住院时长以及机械通气治疗时长等均低于常规组,差异较大(χ2=0.569,P=0.451<0.05),符合统计学描述。见表1。
表1 2组患者临床指征变化()
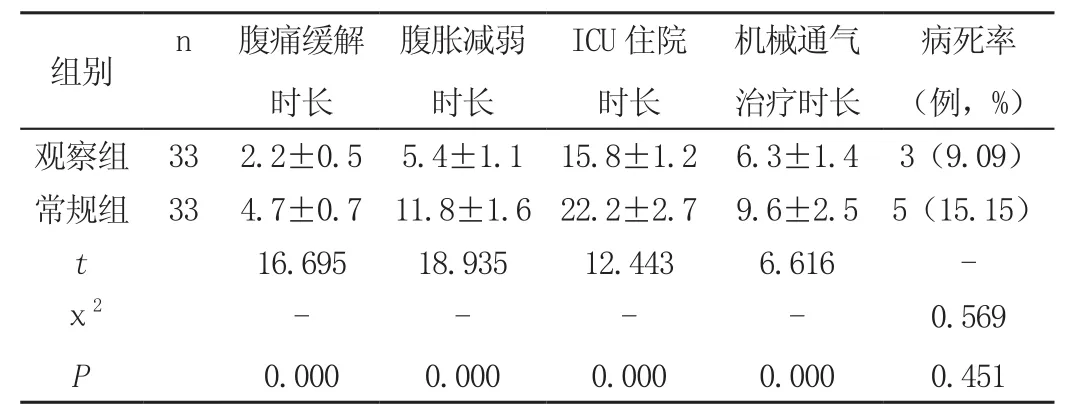
表1 2组患者临床指征变化()
病死率(例,%)组别 n 腹痛缓解时长腹胀减弱时长ICU住院时长机械通气治疗时长观察组 33 2.2±0.5 5.4±1.1 15.8±1.2 6.3±1.4 3(9.09)常规组 33 4.7±0.7 11.8±1.6 22.2±2.7 9.6±2.5 5(15.15)t 16.695 18.935 12.443 6.616 -χ2 - - - - 0.569 P 0.000 0.000 0.000 0.000 0.451
3 讨论
近年来临床上针对重症胰腺炎的治疗有了一定程度的进步,但病死率仍居高不下。重症胆源性胰腺炎(SAP)的发病初期由于免疫因子的大量释放导致机体出现全身炎性反应综合征(SIRS),在重要器官炎性浸润后发生组织功能与器官水肿诱发了多器官功能障碍综合征(MODS)。持续肾脏治疗CRRT在近年来的医学发展中,在急性肾功能衰竭、MODS、以及脓毒症等重症疾病中起到了一定的临床应用效果,其主要治疗机制是清除SAP炎性反应产生的炎性因子,从中间过程切断SIRS的病理变化,改善机体症状[4]。
胆源性胰腺炎主要是由于胆结石与胆管、胆囊炎发生炎性反应累及十二指肠发生梗阻,致使胰液无法排除,激活了胰酶的自身消化能力,诱发急性胰腺炎[5]。因此主要治疗方向为解除胆道梗阻、消减胰胆管压力。在外科领域的不断进步下。ERCP与乳头括约肌切开术的联合对于此类疾病的病理表现具有十分明显治疗作用,但具有一定的限制。PTGD作为新兴的微创导流胆汁、消减胰胆管压力的治疗方法,可对胰腺炎进行治疗。临床采用CRRT联合PTGD应用效果显著,在本文中,治疗前,2组患者的临床指征比较不明显(P>0.05),治疗干预后观察组的临床指征表现均小于常规组,而病死率观察组(9.09%)小于常规组(15.15%),差异较为明显,可比较(P<0.05)。说明了CRRT+PTGD在临床应用中,用时更短,效果更好,可降低病死率。
综上所述,本文中将PTGD与CRRT联合应用于重症急性胆源性胰腺炎中,其临床治疗效果得到了明显的对比且效果良好,在实际临床引用中对既往的治疗方法有更多的优势,如微创、减低患者的住院费用以及减轻病死率等。因此,于重症急性胆源性胰腺炎患者应用此类治疗方式,能显著提高治疗效果,为临床治愈提供参考,值得推广。

