过程分析技术(PAT)在原料药生产中的应用
刘 伟,何 勇,3*,吴 斌,2,蒋轲磊,2
(1.点睛数据科技(杭州)有限责任公司,浙江 杭州 310027;2.浙江大学-点睛数据 智能制药- 在线分析及监控技术联合实验室,浙江 杭州 310027;3.Camo Anlytics公司,挪威 奥斯陆)
由于产品的质量与患者的利益息息相关,制药行业制造生产的过程需经过严格的确认。为保证药品的安全性和有效性,美国食品药品监督管理局(FDA)、欧洲药监局(EMA)和中国国家药品监督管理局(NMPA)等药监部门通过《药品生产质量规范》对药品生产和质量管理进行严格的监管,但这也造成了药品生产企业在面对一些新技术时踌躇不前的局面。华尔街日报曾评论“制药行业在用3西格玛的工艺生产6西格玛的产品”。而其它行业由于新技术的应用,产品品质和生产效率均得到大幅提升。为改变制药行业这一现状,FDA在2002年发布了《面向21世纪的基于科学知识和风险管理的良好生产规范》,并指出制药行业可以通过过程分析技术来促进医药制造的现代化[1]。为推动过程分析技术在制药行业的应用,FDA、EMA相继发布了以近红外为例的过程分析技术在医药行业应用的指南[2-3]。过程分析技术在人用药物注册技术要求国际协调会(ICH)的质量指南Q8(R2)中被定义为:一种设计、分析和控制生产的系统,该系统通过实时测量原材料、生产中的物料,及工艺流程中的关键质量和性能属性,从而保证最终产品的质量[4]。过程分析技术的应用,将使药品的实时测试放行成为可能。
目前先进的跨国药企,如礼来、强生[5]、辉瑞已运用过程分析技术实现了药品的连续制造,并获得了FDA的批文。另外,诺华、葛兰素史克、龙沙以及国内的天津天士力、华润江中等药企也通过过程分析技术实现了产品的中控放行。过程分析技术在医药行业的应用也受到了国内许多专家和学者的关注[6-7]。原料药的质量将直接影响制剂的质量,比如原料药的晶型对制剂的功效,颗粒度分布对溶出的影响[8]。但目前为止国内尚未见在企业现场通过过程分析技术来提升制剂中活性药物成分-原料药质量控制水平的研究报道。
本文所述项目在原料药生产过程中的重结晶工艺中实施,项目采用近红外光谱分析技术实时检测原料药精制过程中溶解液中的原料药浓度和水含量(质量分数),指导补加溶剂(甲醇/水),将原料药浓度、水含量和甲醇/水比例调至工艺要求内,并实现浓度调节的中控放行,进入到下一工艺环节——降温结晶。整个过程分析技术项目包括系统软硬件的3Q确认:安装确认(IQ)、运行确认(OQ)和性能确认(PQ)。安装确认主要是确认硬件系统——光谱仪主机、光纤附件、流通池探头能正常安装,软件系统——收集光谱、建模和在线软件能正常安装;运行确认和性能确认主要是证明安装好的光谱仪硬件系统能够正常运行且光谱仪采集的标准样品的吸光度、位置、波长重复性等指标能够满足药典要求,软件系统能够正常建模并运行在线控制,且满足权限控制的要求——分级管理。以此证明整个系统能够用于现场数据采集,进而进入到分析方法(模型)的开发和验证,最后进行系统的性能确认。采用在线近红外替代传统质量控制部门检测调控结晶前的原料药浓度、水含量和甲醇/水比例,可以降低偏差发生的概率,提升工艺控制水平,结合降温结晶过程可以实现过程分析技术对结晶颗粒度的控制,提升产品的批间一致性。
1 过程分析技术(PAT)
如上文ICH Q8(R2)中给出的定义,过程分析技术专注于工艺理解、过程控制以及基于科学和风险的决策,可以促进对关键工艺参数和关键物料属性的理解,确定这两者与产品关键质量属性之间的相互作用关系,从而保证最终产品的质量。一个完整的过程分析技术系统通常包含收集光谱的光谱仪、建立模型的多变量数据分析、在线显示和控制系统。
1.1 实验设计
实验设计可通过有组织地设计所需要的样品,以最经济的方式最大化地获得样品信息。常用实验设计方法包括因子设计、响应面设计、混料设计。本实验采用混料设计,通过有目的的改变各混合成分的比例,以利用最少的实验样品获得工艺过程最大的变异,节约建模成本。
1.2 光谱仪
光谱仪是过程分析技术系统的前端,主要负责采集过程数据。目前在过程分析技术应用中,光谱仪主要包括近红外、中红外、拉曼光谱仪[9-12]。这些光谱仪测量得到的样品光谱包含物质的分子振动和转动信息,结合化学计量学模型,可以预测得到物质的理化信息(如浓度)。本实验采用近红外光谱仪结合化学计量学模型预测原料药溶解液中的原料药浓度和水含量。
1.3 多变量数据分析
多变量数据分析软件通过偏最小二乘算法建立光谱仪收集的光谱数据与产品关键质量属性之间的数学模型。建模时,首先找到校正样品光谱的权函数(Weight loading),并利用校正样品光谱矩阵点乘权函数得到校正样品的得分(Score),再基于降维后的得分与参考值采用最小二乘进行回归。得分是校正样品光谱在权函数方向上的“投影”,因此偏最小二乘算法也叫“隐结构投影法”[13-14]。
在建模的过程中,采用影响力图-霍特林T2vs.F残差(Hottling T2vs.F Residual)来筛选异常样品(离群样品)。Hottling T2统计量计算每个样品光谱提取出来的得分与总体样品的比值,F Residual统计量计算每个样品光谱提取后的剩余信息占总体剩余信息的比值,剩余信息由原始光谱减去光谱得分点乘载荷得到还原光谱。在一定的显著性水平(通常为0.01)下,可以得到这两个统计量的阈值限。当一个样品光谱的这两个统计量都超出限度时,可以判断为异常值或离群值。
1.4 在线显示与控制工具
加载有模型的在线显示软件从光谱仪实时获取数据,对数据实时显示和预测,并将预测结果通过通讯协议输出给集散控制系统(DCS)或数据采集和监视控制系统(SCADA)。控制系统根据预测结果采用PID(比例、微分和积分)模型进行生产工艺参数的控制,从而实现整个过程分析技术系统的闭环控制。
2 过程分析技术(PAT)项目实施过程
2.1 建模样品参数范围确定

图1 实验样品组分浓度分布图Fig.1 Component concentration distribution diagram of experiment samples
建模样品均来自车间商业化生产现场,车间现场的样品包含预测时所有的变异信息,可提高模型的稳健性。采样时,罐内原料药溶解液温度按照生产要求控制在(70±2) ℃。基于原料药在甲醇/水中溶解度和实际生产的需要,实验设计应满足以下条件:原料药在甲醇/水中溶解度为30%,且投料时水含量最低为6.5%;浓度调节工艺要求:原料药含量调至19.5%~22.5%,水含量调至22.5%~24.5%,甲醇/水比例调至28~32∶72~68。在以上条件下,实验设计确定的样品各组分分布如图1所示。由于采用商业化生产的样品进行实验,受每个批次投料的影响,实际生产过程中的样品浓度分布与实验设计略有出入。
2.2 光谱仪参数及软件信息
采用布鲁克傅里叶变换近红外光谱仪(型号:Matrix-F),波数范围:4 000~12 500 cm-1。光源为气体冷却的卤钨灯,功率为20 W。干涉仪为永久校准的迈克尔逊干涉仪。检测器采用铟镓砷检测器。光谱仪分辨率设置为 8 cm-1,扫描次数为32,流通池光程为2 mm,32次平均结果得到光谱。
光谱仪控制软件为OPUS 7.5,建模及优化采用 Camo公司的Unscrambler X 10.5,在线显示采用Unscrambler Process Pulse Ⅱ 5.54。
2.3 样品光谱及参考值收集
原料药粗品投入甲醇/水溶剂中,经升温溶解和活性炭脱色后转移至结晶罐中,加热至工艺要求温度范围:(70±2)℃。保温一段时间后,进入浓度调节工艺。开启循环取样系统(循环取样系统安装有加热盘管以防止通过流通池的原料药溶解液结晶附着在流通池内),使罐内的原料药溶解液通过安装在循环取样系统上的流通池,并通过视盅查看及确认通过流通池的原料药溶解液无气泡。开启近红外光谱仪,收集流过流通池的原料药溶解液光谱。收集完样品光谱后,立即通过循环取样系统取出两个平行样品,并送至质量控制实验室采用高效液相色谱法检测原料药浓度[13],卡尔费休滴定方法检测水含量,采用企业内部标准检测,取两次检测结果平均值作为参考值。
2.4 模型评估
建模采用偏最小二乘回归算法中的标准算法——非线性迭代偏最小二乘(NIPALS)[14-15]算法,通过校正均方根误差(RMSEC)、交叉检验均方根误差(RMSECV)和预测均方根误差(RMSEP)以及对应的决定系数(R2)来评估模型的性能。分析方法验证中主要比较预测标准偏差(SEP)和参考方法的实验室标准误差(SEL)。
2.5 在线预测及控制
建立好的模型在通过验证后导入到Unscrambler Process Pulse软件对实时采集的近红外光谱进行在线预测和显示,预测结果通过OPC(OLE for process control)协议输送给集散控制系统,控制系统根据预测结果进行补加溶剂的判断计算,并控制智能阀门和流量计补加溶剂。
3 结果与讨论
3.1 光谱波段与预处理
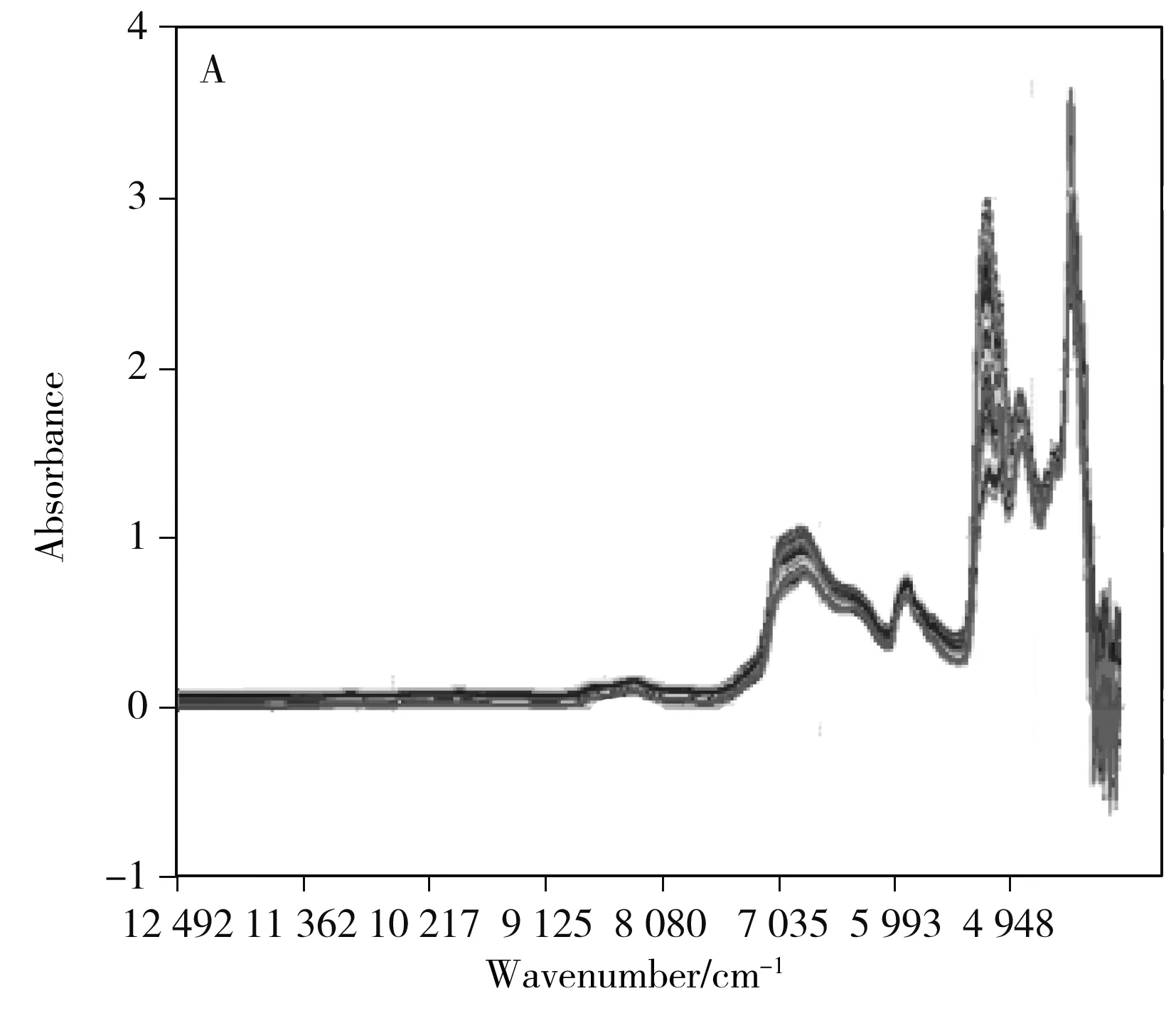
图2A为流通池探头采集到的原料药溶液的原始光谱图,总共118个。波数4 400~4 000 cm-1范围内主要为噪声。波数12 500~9 000 cm-1范围内出现的明显的基线横漂现象可采用一阶导数预处理进行消除。在波数5 090、6 900 cm-1附近主要为水的合频和一倍频峰,在这两个波数附近,吸光度随水含量的提升而增加[12]。其他位置为原料药、甲醇和水吸收的重叠峰。由于水在5 090、6 900 cm-1附近对光的吸收太强,建模时舍去这一部分。综上,选取6 200~5 600 cm-1段光谱并采用Savitzky-Golay(SG) 算法[16]求一阶导数(平滑点数为7点,拟合多项式级数为2)作为建模光谱,预处理后的光谱如图2B所示。
3.2 校正模型与测试验证模型
3.2.1 校正集建模结果将118个样品分为两个部分:校正集(100)和独立测试集(18),校正集样品光谱经过预处理,结合参考值利用偏最小二乘算法建模。建模范围:原料药含量 19%~30%,H2O含量 8%~25%。图3为原料药的模型结果图,其中图3A为得分图,图中为99%置信度下的霍特林置信椭圆。图3B为载荷图,图中蓝/红/绿色线分别为第1、2、3载荷。在偏最小二乘算法中,载荷也代表数据降维的方向,第1载荷方向上数据变异最大,第2次之。载荷是得分空间和光谱空间之间的“桥梁”。图3C为解释图,代表因子个数(潜变量数)对响应矩阵(向量)的解释。图3D为参考值和预测值的对比图,从图中可知使用3个因子数模型的校正性能:RMSEC=0.384,R2=0.982;20折交叉检验性能:RMSECV=0.405,R2=0.981;两者数据接近,说明模型稳健。水分模型结果:RMSEC=0.481,R2=0.991;20折交叉检验性能:RMSECV=0.506,R2=0.982(未给出水分模型结果图)。
3.2.2 测试集验证结果模型建立后采用18个独立样品测试模型性能,样品原料药含量范围为20%~30%,水为10%~25%。图4A为原料药的预测结果:RMSEP=0.270,R2=0.993,预测误差RMSEP小于校正误差RMSEC(0.384),说明模型的预测性能良好;图4B为水的预测结果:RMSEP=0.893,R2=0.967,预测误差RMSEP大于校正误差RMSEC(0.481),这是由有1个样品的预测误差超出两倍的模型校正误差所致。图5A为样品的得分分布,其中蓝颜色代表校正集样品得分,红颜色代表测试集样品得分,椭圆为99%置信度下的霍特林置信椭圆。图5B为测试集样品的影响力图,其中两条红色线分别为99%置信度下霍特林和F残差统计量阈值线,无测试集样品落于阈值线外,即无异常值。表1统计了样品的建模信息和内部验证信息。



表1 模型参数及预测结果Table 1 Parameters and prediction result of models
3.3 模型分析方法验证与系统性能验证
为保证模型在车间现场使用时的准确性和稳健性,需对模型的性能进行分析方法验证。定量模型验证内容包括以下5个方面:线性和范围、准确性、精密度(重复性)、专属性、稳健性[3,17-18]。验证结果如表2所示。
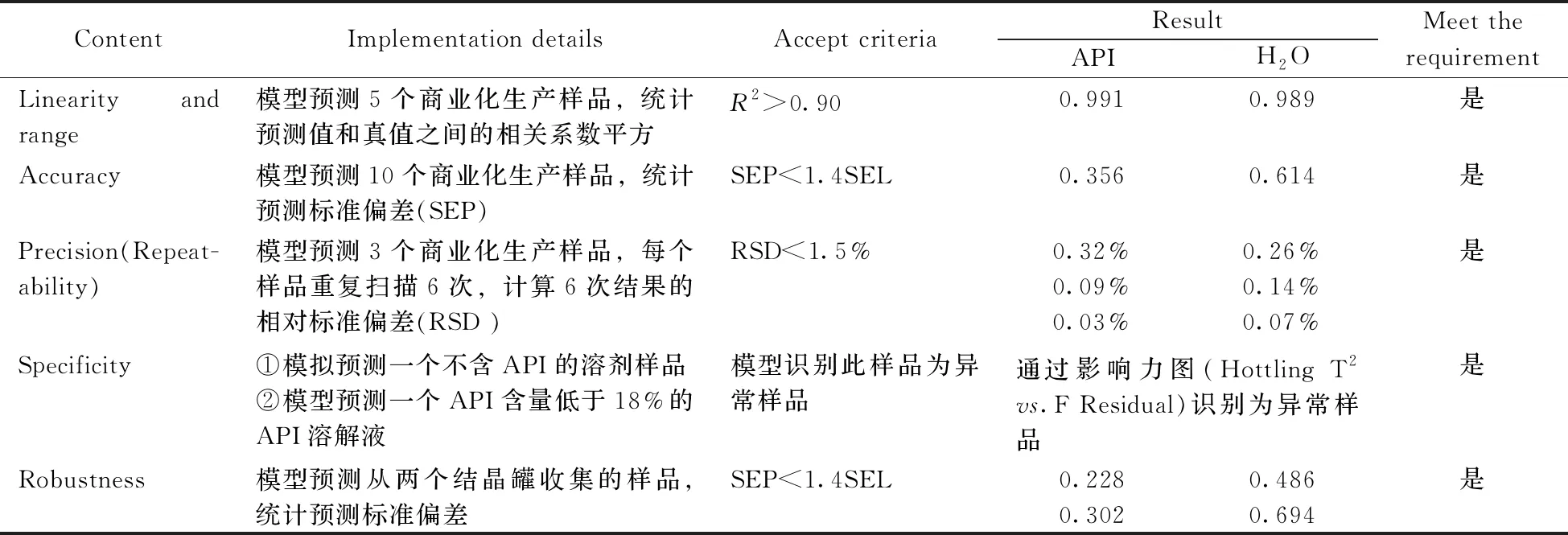
表2 模型分析方法验证结果Table 2 Validation results of analytical method for models
模型通过分析方法验证后,还需采用3个商业化批次进行系统性能确认,通过后检测系统方能投入到正式的商业化运行。篇幅所限,此处不做详细展开。
3.4 商业化批次原料药溶液浓度调节过程
图6为Unscrambler Process Pulse 导入上文建立的原料药和水分预测模型后进行一个商业化批次浓度调节的实时监控结果。如图6A所示,粉色线为结晶罐内原料药浓度变化曲线,绿色线为结晶罐内水含量变化曲线。在原料药浓度调节过程中,控制系统根据实时检测结果逐步向结晶罐内补加溶剂(甲醇/水),原料药浓度分步从24.6%调节至目标值21%,水含量则从20.2%逐步升高到23.4%。图6B为实时样品溶液的光谱图。图6C为预测样品的得分图,图中灰色点代表校正样品在得分空间中的分布,绿色点代表在线预测的样品在得分空间中的分布。图6D为影响力图,影响力图的横坐标为Hottling T2,纵坐标为F Residual,通过影响力图可以判断预测的光谱是否属于异常值。当样品落于影响力图的右上角时,即样品的Hottling T2和F Residual都超出99%置信度下的阈值线,则判断为异常值。当原料药浓度和水含量调整至工艺要求范围内,且光谱的霍特林和F残差值均落于影响力图的阈值线内时,可以关闭光谱仪,并将调节结果打印作为中控放行证据黏贴在生产批记录上,结晶工艺进入下一个工艺步骤——降温结晶。
3.5 实施成效
在本项目模型校正集的RMSEC、RMSECV和测试集的RMSEP非常接近,通过分析方法验证对模型性能进行了确认;最后通过3个商业批次确认整个在线监控系统能够满足预期性能要求,监控系统得以进入商业化运行阶段。通过在降温结晶前的浓度调节工艺中采用在线近红外监控调节原料药浓度、水含量和甲醇/水比例,可将原有通过质量控制部门调节工艺的时间6~8 h缩短至1 h,减少保温时间,节约蒸汽能耗费用,缩短批次时间,提高生产效益(6.67%),每月批次可从30批增加到32批。另外每年可以节省约30万检测费用和约50万蒸汽费用。因此在线近红外监控原料药降温结晶前的浓度调节工艺不仅可以提升工艺控制水平,保证生产过程中间产品质量的稳定性和一致性,还可以为企业创造巨大的经济效益。

图6 一个商业化批次浓度调节监控过程Fig.6 Monitoring process of concentration adjustment for a commercial batch A.real-time API and H2O predicted values;B.real-time raw NIR spectra;C.real-time scores;D.real-time influence
4 结 论
本文详细介绍了在良好质量规范条件下实施过程分析技术项目的完整流程。该项目采用在线近红外光谱分析技术监控原料药精制环节中的浓度调节过程,并实现了产品的中控放行。本方法也可应用于其它场景,如原料药生产过程中监控危险反应、溶剂回收、干燥水分。在制剂中,过程分析技术可用来监控造粒过程、混和均匀度、包衣过程等。另外,在中药和生物制药行业,过程分析技术也有广泛的应用。
采用过程分析技术替代传统的质量控制实验室检测,不仅可以提高生产效率,降低质量控制实验室检测费用和检测过程中产生的废液,实现绿色生产;还可以提升产品批次间的一致性。目前各国监管机构也都鼓励制药企业在生产过程中采用过程分析技术。相信在监管部门和药企的共同努力下,中国会有越来越多的过程分析技术项目应用于生产过程的实时监控,并最终实现整个制药行业的智能制造和连续制造。
——多功能光谱仪

